Содержание
ПРЕВРАЩЕНИЯ ВЕЩЕСТВ | Энциклопедия Кругосвет
Содержание статьи
ПРЕВРАЩЕНИЯ ВЕЩЕСТВ. Вещества могут претерпевать два типа превращений: физические и химические.
Физические превращения.
Когда с веществом происходит физическое изменение, состав его молекул остается прежним, т.е. вещество сохраняет свою химическую индивидуальность. Существует три типа основных физических превращений – плавление, испарение и замерзание. Лед – твердое вещество – при плавлении превращается в воду – жидкость, которая при замерзании снова становится льдом. Молекулы льда и воды состоят из одних и тех же элементов (H и O), находящихся в одинаковых пропорциях. Когда лед тает, никаких химических реакций не происходит. Другой тип физических превращений – изменение формы вещества, например при его резании, шлифовании, измельчении, растворении, эмульгировании и т.д. Еще один тип физического превращения – сублимация (возгонка), переход твердого вещества непосредственно в газообразное. Именно это превращение имеет место, когда мокрое белье сохнет на морозе.
Именно это превращение имеет место, когда мокрое белье сохнет на морозе.
Химические превращения
происходят постоянно и повсюду; при этом изменяется химическая индивидуальность веществ, одни вещества превращаются в другие с иными свойствами. Так, при ржавлении железа образуется новое вещество – ржавчина (оксид железа). Химические превращения могут сопровождаться физическими изменениями. При горении древесины (твердое вещество) образуются диоксид углерода (газ), вода (жидкость) и углерод (твердое вещество). Химические превращения чрезвычайно многообразны, их изучением и классификацией занимается наука химия. Вот некоторые типы превращений, принятые в химии.
Реакции присоединения.
Объединение молекул двух или нескольких веществ с образованием молекулы одного нового вещества. Примером служит горение магния на воздухе: 2Mg + O2® 2MgO.
В органической химии этим термином часто пользуются для обозначения таких реакций, как взаимодействие этилена С2H4 с бромом с образованием дибромэтана:
C2H4 + Br2 ® C2H4Br2
Реакции разложения.

Распад исходного вещества на два или более простых. Так, при разложении оксида ртути образуются элементная ртуть и кислород: 2HgO ® 2Hg + O2.
Реакции замещения.
Замена атомов в молекулах сложного вещества атомами простого вещества. Например, железо замещает медь в растворе сульфата меди:
Fe + CuSO4® FeSO4 + Cu
Реакции обмена.
Образование двух новых веществ при взаимодействии двух исходных. Например, иодид натрия NaI и нитрат свинца Pb(NO3)2 обмениваются своими составными частями с образованием иодида свинца и нитрата натрия:
2NaI + Pb(NO3)2® PbI2 + 2NaNO3
Атом хлора обменивается с одним или более атомами водорода в молекуле углеводорода, например метана СН4, следующим образом:
CH4 + Cl2® CH2Cl + HCl
Реакция гидролиза.
Гидролиз (расщепление с участием воды) – это реакция двойного разложения, когда одним из исходных компонентов является вода. При гидролизе хлорида аммония NH4Cl образуется гидроксид аммония NH4OH и соляная кислота HCl:
При гидролизе хлорида аммония NH4Cl образуется гидроксид аммония NH4OH и соляная кислота HCl:
NH4Cl + H2O ® NH4OH + HCl
Реакция нейтрализации.
Особый случай реакции обмена – взаимодействие кислоты с эквивалентным количеством основания с образованием соли и воды. Соляная кислота HCl и гидроксид натрия NaOH нейтрализуют друг друга с образованием хлорида натрия NaCl и воды:
HCl + NaOH ® NaCl + H2O
Проверь себя!
Ответь на вопросы викторины «Физика»
Что такое изотоп, чему равно число Авогадро и что изучает наука реология?
Превращения химические — Справочник химика 21
Превращение химической энергии в электрическую возможно при помощи электрохимического (гальванического) элемента, примером которого может служить элемент Якоби — Даниэля, состоящий из цинкового и медного электродов, опущенных соответственно в растворы сульфатов цинка и меди, разделенные пористой диафрагмой во избежание их перемешивания (см. рис. 75). Схема электрохимической цепи элемента Якоби —Даниэля записывается следующим образом [c.269]
рис. 75). Схема электрохимической цепи элемента Якоби —Даниэля записывается следующим образом [c.269]
Гальванический элемент — простое устройство для превращения химической энергии в электрическую в небольшом удобном контейнере. При изготовлении коммерческих элементов химики используют самые разнообразные комбинации металлов и ионов. В простейшем сухом элементе (рис. Vni.lO) — называемом часто батарейкой — в качестве анода используется цинк, а в качестве катода — диоксид марганца (МпОг). Раствор в большинстве сухих элементов содержит ионы аммония и хлорид цинка. В щелочных батарейках раствор содержит гидроксид калия (КОН). [c.529]
ПРЕВРАЩЕНИЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ РАДИОАКТИВНОЕ ПРЕВРАЩЕНИЕ [c.14]
Химическое превращение — это качественный скачок, при котором исчезают одни вещества и образуются другие. Происходящая при этом перестройка электронных структур атомов, ионов и молекул сопровождается выделением или поглощением теплоты, света, электричества и т. п. — превращением химической энергии в другой вид энергии. [c.158]
п. — превращением химической энергии в другой вид энергии. [c.158]
Изучение закономерностей ядерных реакций позволяет создать теорию происхождения химических элементов и их распространенности в природе. Согласно данным ядерной физики и астрофизики синтез и превращение химических элементов происходят в процессе развития звезд. Образование атомных ядер осуществляется либо за счет термоядерных реакций, либо — реакций поглощения ядрами нейтронов. [c.16]
В связи с открытием все новых и новых сфер проявления электрохимических закономерностей представляется целесообразным и современным несколько видоизменить определение электрохимии как науки, изучающей взаимное превращение химической и электрической энергии. [c.9]
Взаимное превращение химической и электрической форм энергии совершается только в электрохимических системах, поэтому их изучение составляет предмет электрохимии. [c.12]
Разряд аккумулятора сопровождается превращением химической энергии в электрическую, причем активные вещества переходят в продукты разряда заряд аккумулятора, наоборот, превращает электрическую энергию в химическую, а продукты разряда — в первоначальные активные вещества. [c.865]
[c.865]
Химическое превращение, химическая реакция есть главный предмет химии. Изучение различных свойств элементов и молекул дает в сущности для химии вспомогательный материал, облегчающий главную задачу, задачу рационального управления химическим превращением… [c.158]
Раздел V ПРЕВРАЩЕНИЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ [c.657]
Раздел V. Превращение химических элементов [c.658]
Горение — сложный, быстро протекающий химический процесс взаимодействия горючего и окислителя, сопровождающийся появлением пламени, излучающего энергию в виде тепла и света. Этот процесс лежит в основе превращения химической энергии топлива в механическую в тепловых двигателях. [c.112]
Комбинация двух электрохимических электродов предназначен для превращения химической энергии в электрическую, в Элемент медь/цинк гп/гп +//Си +/Си (+) [c.92]
Теоретически эффективность превращения химической энергии в электрическую через теплоту очень мала, поэтому, уже [c. 602]
602]
В качестве критериев эффективности ХТС используют как экономические критерии в виде различных технико-экономических показателей (средняя величина прибыли, приведенный доход, себестоимость, приведенные затраты и т. д.), так и технологические критерии (производительность, мощность, качество выпускаемой продукции расходные нормы сырья и энергии для ХТС в целом для отдельных элементов ХТС или ХТП — к. п. д. ХТП, которые представляют собой, например, для процессов химического превращения — степени превращения химических компонентов, а для процессов межфазной массопередачи — степени межфазного перехода, или коэффициенты извлечения термодинамический или эксергетический к. п. д. элементов и т. д.) [1, 2, 4, 49]. [c.34]
Сгорание является важнейшим процессом, обусловливающим полезную работу двигателя, так как при этом происходит превращение химической энергии топлива в тепловую и далее в механическую. Процесс сгорания определяет мощностные и экономические показатели двигателя, а характер его протекания существенно влияет на надежность и долговечность двигателя [16]. [c.50]
[c.50]
Удельная теплота (фазового превращения химической реакции) джоуль на килограмм [c.7]
Это классическое определение, берущее начало от В. А. Кистя-ковского и отвечающее принципам классификации наук, сформулированным Ф. Энгельсом, сохраняется как основа нового определения. Оно дополняется, однако, характеристикой признаков, присущих электрохимическим явлениям электрохимия изучает взаимное превращение химической и электрической форм энергии, системы, в которых это превращение соверш.ается (в равновесии и в динамике), а также все гетерогенные явления и процессы, равновесие и скорость которых определяются скачком потенциала между граничащими фазами и связаны с переносом зарядов через границы фаз в виде расчлененных актов окисления и восстановления. [c.9]
Основные показатели эффективности функционирования элементов ХТС выражают в виде коэффициентов полезного действия (к. п. д.) элементов или величин, характеризующих фактический выход химического продукта из элемента ХТС, которые для технологических процессов собственно химического превращения представляют собой степени превращения химических компонентов, а для технологических процессов межфаз-ной массопередачи — степени межфазного перехода (степени разделения) или коэффициенты извлечения. К. п. д. элементов показывают степень приближения технологического процесса к равновесию. Расчеты к. п. д. требуют знания равновесных соотношений, хотя эти величины определяются в основном кинетикой процесса фактическое число компонентов, вступивших в химическую реакцию, или количество поглощаемого компонента зависит соответственно от скорости химического превращения или от скорости массопередачи. [c.15]
К. п. д. элементов показывают степень приближения технологического процесса к равновесию. Расчеты к. п. д. требуют знания равновесных соотношений, хотя эти величины определяются в основном кинетикой процесса фактическое число компонентов, вступивших в химическую реакцию, или количество поглощаемого компонента зависит соответственно от скорости химического превращения или от скорости массопередачи. [c.15]
Трудности при моделировании такого рода ФХС обусловлены не только их сложностью, но и тем, что до недавнего времени были недостаточно разработаны соответствующие разделы теоретической механики неоднородных сред. Так, отсутствовали общие уравнения движения многофазных сред, которые учитывали бы многокомпонентный массо- и теплоперенос, фазовые превращения, химические реакции, неравномерность распределения частиц дисперсной фазы по размерам. Поэтому моделирование процессов массовой кристаллизации из растворов сводилось либо к решению уравнения баланса размеров кристаллов вне связи с силовыми и энергетическими взаимодействиями фаз, либо к оперированию алгебраическими (при анализе установившихся режимов) уравнениями баланса массы и тепла для аппарата в целом как для объекта с сосредоточенными параметрами. [c.4]
[c.4]
Как показывает опыт и как можно обосновать теоретически, при равномерном охлаждении системы, в которой не происходит фазовых превращений (химические реакции считаем исключенными), изменение температуры происходит тоже равномерно. [c.351]
Полимераналогичные превращения — химические реакции боковых групп или атомов основной цепи с низкомолекулярными соединениями, протекающие без разрыва химических связей между звеньями макромолекулы и не приводящие к изменению строения ее скелета. Принимается, что степень полимеризации при этом остается постоянной. [c.403]
Понятие о химическом элементе. Ядерная модель атома. Протоны, нейтроны, электроны. Дефект массы. Магические ядра. Космическая распространенность химических элементов. Химические элементы в земной коре. Радиоактивность. Превращение химических элементов. Ядерная химия. Ядерные реакции. Синтез химических элементов. Ядерные реакции в природе. Происхождение химических элементов. [c.7]
[c.7]
Внутримолекулярные превращения — химические реакции, обусловленные внутримолекулярными перегруппировками или взаимодействиями между собой атомов или функциональных групп одной макромолекулы, изменяющие первичную структуру полимерной цепи, но не приводящие к существенному изменению степени полимеризации исходного полимера. [c.397]
ЛИЧНЫМИ соединениями. Химические реакции, в результате проведения которых длина и форма цепи макромолекул заметно не изменяются, носят название полимера н алогичных превращений. Химические превращения в звеньях макромолекул полимеров затруднены вследствие малой подвижности цепей и возможности деструкции полимера в условиях реакции. [c.15]
Электрохимия занимается изучением г акономерностей, связанных с взаимным превращением химической н электрической форм энергии. Химические реакции сопровождаются обычно поглощением или выделением теплоты (тепловым эффектом реакции), а не электрической энергии. В электрохимии рассматриваются реакции, или протекающие за счет подведенной извне электрической энергии, или же, наоборот, служащие источником ее получения такие реакции называются электрохимическими. Следовательно, электрохимические реакции с энергетической точки зрения не идентичны химическим, и в этом одна из причин, по которым электрохимия должна рассматриваться как самостоятельная наука. [c.9]
В электрохимии рассматриваются реакции, или протекающие за счет подведенной извне электрической энергии, или же, наоборот, служащие источником ее получения такие реакции называются электрохимическими. Следовательно, электрохимические реакции с энергетической точки зрения не идентичны химическим, и в этом одна из причин, по которым электрохимия должна рассматриваться как самостоятельная наука. [c.9]
Два злектронопроводящих тела, контактирующие с электролитом и обеспечивающие обмен зарядами с участниками электрохимической реакции, а также передачу электронов во внешнюю цепь (см. ниже) пли получение их из 1знешней цепи они называются электродами. На электродах — на границе раздела двух различно проводящих фаз — происходит перенос заряда, т. е. протекают электрохимические реакции, иными словами, именно здесь локализовано взаимное превращение химической и электрической форм [c.12]
Аналогичные результаты были получены при изучении реакции электровосстановления кислорода.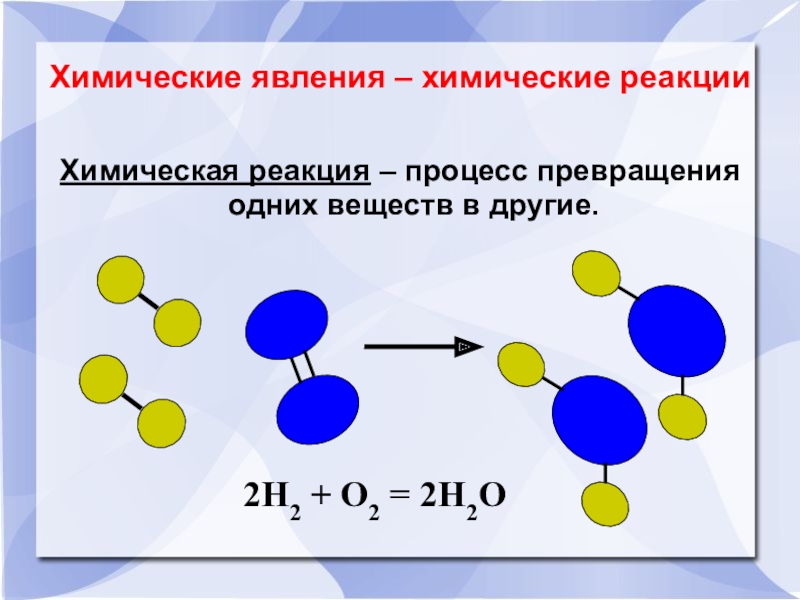 Эта реакция играет важную роль в процессах коррозии металлов и при работе элементов с воздушной деполяризацией. Интерес к ней особенно возрос в последние годы в связи с проблемой нелосредствениого превращения химической энергии в электрическую при помощи топливных элементов. В настоящее время выяснены основные кинетические особенности реакции восстановления кислорода в кислых и щелочных средах (Н. Д. Томашев, А. И. Красильщиков, 3. А. Иофа, В. С. Багоцкий и др.). Так, электровосстановление кислорода на ртути, серебре и золоте оказалось возможным описать следующими уравнениями [c.441]
Эта реакция играет важную роль в процессах коррозии металлов и при работе элементов с воздушной деполяризацией. Интерес к ней особенно возрос в последние годы в связи с проблемой нелосредствениого превращения химической энергии в электрическую при помощи топливных элементов. В настоящее время выяснены основные кинетические особенности реакции восстановления кислорода в кислых и щелочных средах (Н. Д. Томашев, А. И. Красильщиков, 3. А. Иофа, В. С. Багоцкий и др.). Так, электровосстановление кислорода на ртути, серебре и золоте оказалось возможным описать следующими уравнениями [c.441]
Химический процесс сопровождается изменением состава веществ, их структуры и обязательно энергетическими изменениями в реаги- )ующей системе. При химическом процессе происходит перегрупии-ровка атомов, сопровождающаяся разрывом химических связей в исходных веществах и образованием химических связей в продуктах 1)еакции. Вследствие взаимосвязанности форм движения материи и их 1 заимоиревращаемости при химических реакциях происходит превращение химической энергии в теплоту, свет и пр. [c.6]
[c.6]
В последние 10ды у нас и за рубежом проводились комплексные исследования более детального химизма нефтеобразования в условиях, максимально моделирующих природный нефтесинтез (за исключением продолжительности опытов по причине отсутствия у исследователей времени продолжительностью в миллион лет). В результате установлены общие закономерности образования основных классов углеводородов нефти из отдельных групповых компонентов растений и животных организмов, а также продуктов их первичных превращений (химический аргумент). [c.54]
В пламенах происходит также образование заряженных ча стиц — ионов, ион-радикалов. Присутствие заряженных частиц в пламени было установлено еще в 1600 г., когда Гильберт показал, что пламя разряжает электроскоп. За последние 10— 15 лет внимание к исследованию ионизации в пламенах возро ело главным образом в связи с разработкой магнито-гидроди намического способа превращения химической энергии топлива в электрическую. [c.115]
[c.115]
Известно, что все химические реакции сопровождаются определенным энергетическим эффектом, т, е. выделением или поглощением эпергпп в том илн ипом виде. Чаще всего наблюдается при химических реакциях выделение или поглощение теплоты. Количественно ьнергетический эффект выражается посредством записи в уравнении реакции значения выделенной или поглощенной энергии. Так как в уравнении реакции формула каждого вещества символизирует его количество, равное одному молю, а коэффициент при формуле—число молей этого вещества, то значение энергии, записапное в уравнении, относят к обозначенным в уравнении количествам исходных и получившихся веществ. Значение выделенной эиергии записывают обычно в правой части уравнения со знаком плюс, а поглощенной — со знаком минус. В первом случае реакцию называют экзотермической, во втором — эндотермической. Уравнения, отражающие ие только сохранение массы, но и сохранение энергии при химических реакциях, называются тер.но.химическими. Термохимия — это раздел науки, изучающий взаимные превращения химической и тепловой энергии. Термохимические уравнения обладают всеми свойствами алгебраических равенств и, таким образом, с ними можно совершать и алгебраические операции, [c.76]
Термохимия — это раздел науки, изучающий взаимные превращения химической и тепловой энергии. Термохимические уравнения обладают всеми свойствами алгебраических равенств и, таким образом, с ними можно совершать и алгебраические операции, [c.76]
Химическими источниками тока (ХИТ) называются устрейства, посредством которых свободная энергия пространственно разделенных окислнтельно-юсстановительных процессов превращается в электрическую энергию. Процесс превращения химической энергии в элеК трическую в химическом источнике тока называется разрядом. [c.865]
Начало XX века ознаменовалось, после открытия Ромбергом свободного трифенилметильного радикала, возрождением представления о свободных радикалах как реально существующих осколках молекул. До этого времени на протяжении-40 лет идея о реальности радикалов была изгнана из химии. В радикалах видели только удобный символический прием изображения строения органических соединений. После экспериментального подтверждения реальности радикалов с новой силой ожил интерес исследователей к радикалам, к изучению той роли, которую они могут играть в реакциях. Эту роль еще в середине XIX века предвидели А. М. Бутлеров и другие исследователи, полагавшие, что радикалы реально существуют. Новый мир радикалов как частиц с весьма своеобразными свойствами, необычайно активных относительно реакций, в которые они могут вступать, прёдстал перед взором исследователей. Возникла новая область науки — химия радикалов, тесно связанная с учением о скоростях превращений — химической кинетикой. Неудивительно-поэтому, что в первой четверти XX века появляются работы, в которых настойчиво проводится мысль о значении радикалов в процессе пиролиза органических веществ [Ц —13]. Встречающиеся в этих работах данные о влиянии температуры и давления на быстроту крекинга и выход продуктов но-13 [c.18]
Эту роль еще в середине XIX века предвидели А. М. Бутлеров и другие исследователи, полагавшие, что радикалы реально существуют. Новый мир радикалов как частиц с весьма своеобразными свойствами, необычайно активных относительно реакций, в которые они могут вступать, прёдстал перед взором исследователей. Возникла новая область науки — химия радикалов, тесно связанная с учением о скоростях превращений — химической кинетикой. Неудивительно-поэтому, что в первой четверти XX века появляются работы, в которых настойчиво проводится мысль о значении радикалов в процессе пиролиза органических веществ [Ц —13]. Встречающиеся в этих работах данные о влиянии температуры и давления на быстроту крекинга и выход продуктов но-13 [c.18]
С общекинетической точки зрения большой интерес представляет исследование кинетического изотопного эффекта при высокотемпературном крекинге меченых этапов [1221 (С Нз — С Нз и С Нз — С Нз). Явление кинетическога изотопического эффекта состоит в изменении скорости превращения химических соединений вследствие изменения их изотопического состава. Изучение этого эффекта дает возможность сделать существенные выводы относцтельно закономерностей элементарных химических реакций и механизма суммарных реакций. Так, исследование кинетического изотопического эффекта при высокотемпературном крекинге меченых атомов в смеси с обычным этаном позволило по измерениям радиоактивности образующегося в процессе крекинга метана установить, что скорость разрыва связи С — С меньше таковой для связи С — С на 11 +2%, что значительно превышает величину 3 /о, находимую из формул для теории изотопического эффекта (121, 124]. Вероятность раз- [c.60]
Изучение этого эффекта дает возможность сделать существенные выводы относцтельно закономерностей элементарных химических реакций и механизма суммарных реакций. Так, исследование кинетического изотопического эффекта при высокотемпературном крекинге меченых атомов в смеси с обычным этаном позволило по измерениям радиоактивности образующегося в процессе крекинга метана установить, что скорость разрыва связи С — С меньше таковой для связи С — С на 11 +2%, что значительно превышает величину 3 /о, находимую из формул для теории изотопического эффекта (121, 124]. Вероятность раз- [c.60]
Основы общей химии (1988) — [
c.29
]
Общая химия (1979) — [
c.20
,
c.21
]
Кинетика гетерогенных процессов (1976) — [
c.87
]
Введение в физическую химию и кристаллохимию полупроводников Издание 2 (1973) — [
c. 228
228
]
Сочинения Теоретические и экспериментальные работы по химии Том 1 (1953) — [
c.37
]
Сочинения Научно-популярные, исторические, критико-библиографические и другие работы по химии Том 3 (1958) — [
c.49
,
c.207
,
c.210
,
c.222
,
c.241
,
c.256
,
c.274
,
c.275
]
ПРЕВРАЩЕНИЯ ВЕЩЕСТВ — это… Что такое ПРЕВРАЩЕНИЯ ВЕЩЕСТВ?
- ПРЕВРАЩЕНИЯ ВЕЩЕСТВ
- Вещества могут претерпевать два типа превращений: физические и химические.
Физические превращения. Когда с веществом происходит физическое изменение, состав его молекул остается прежним, т.е. вещество сохраняет свою химическую индивидуальность. Существует три типа основных физических превращений — плавление, испарение и замерзание. Лед — твердое вещество — при плавлении превращается в воду — жидкость, которая при замерзании снова становится льдом. Молекулы льда и воды состоят из одних и тех же элементов (H и O), находящихся в одинаковых пропорциях. Когда лед тает, никаких химических реакций не происходит. Другой тип физических превращений — изменение формы вещества, например при его резании, шлифовании, измельчении, растворении, эмульгировании и т.д. Еще один тип физического превращения — сублимация (возгонка), переход твердого вещества непосредственно в газообразное. Именно это превращение имеет место, когда мокрое белье сохнет на морозе.
Когда с веществом происходит физическое изменение, состав его молекул остается прежним, т.е. вещество сохраняет свою химическую индивидуальность. Существует три типа основных физических превращений — плавление, испарение и замерзание. Лед — твердое вещество — при плавлении превращается в воду — жидкость, которая при замерзании снова становится льдом. Молекулы льда и воды состоят из одних и тех же элементов (H и O), находящихся в одинаковых пропорциях. Когда лед тает, никаких химических реакций не происходит. Другой тип физических превращений — изменение формы вещества, например при его резании, шлифовании, измельчении, растворении, эмульгировании и т.д. Еще один тип физического превращения — сублимация (возгонка), переход твердого вещества непосредственно в газообразное. Именно это превращение имеет место, когда мокрое белье сохнет на морозе.
Химические превращения происходят постоянно и повсюду; при этом изменяется химическая индивидуальность веществ, одни вещества превращаются в другие с иными свойствами.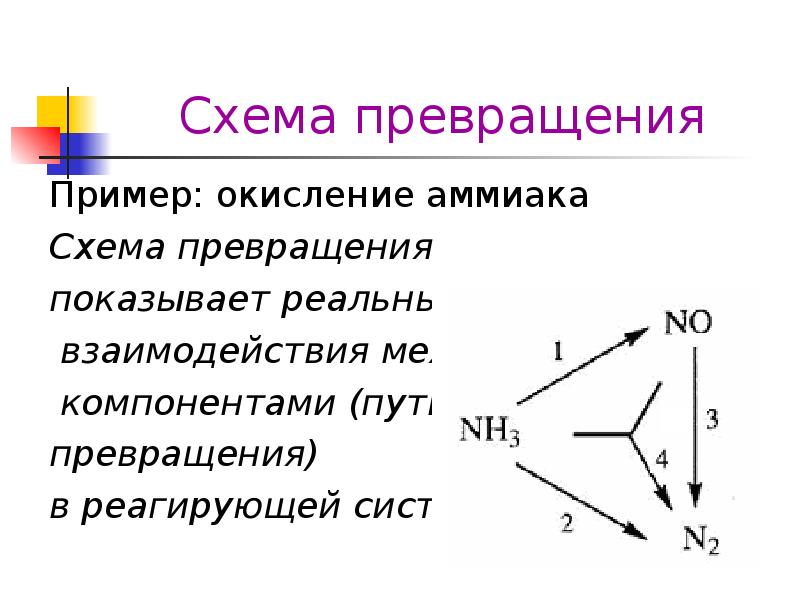 Так, при ржавлении железа образуется новое вещество — ржавчина (оксид железа). Химические превращения могут сопровождаться физическими изменениями. При горении древесины (твердое вещество) образуются диоксид углерода (газ), вода (жидкость) и углерод (твердое вещество). Химические превращения чрезвычайно многообразны, их изучением и классификацией занимается наука химия. Вот некоторые типы превращений, принятые в химии.
Так, при ржавлении железа образуется новое вещество — ржавчина (оксид железа). Химические превращения могут сопровождаться физическими изменениями. При горении древесины (твердое вещество) образуются диоксид углерода (газ), вода (жидкость) и углерод (твердое вещество). Химические превращения чрезвычайно многообразны, их изучением и классификацией занимается наука химия. Вот некоторые типы превращений, принятые в химии.
Реакции присоединения. Объединение молекул двух или нескольких веществ с образованием молекулы одного нового вещества. Примером служит горение магния на воздухе: 2Mg + O2 -> 2MgO. В органической химии этим термином часто пользуются для обозначения таких реакций, как взаимодействие этилена С2h5 с бромом с образованием дибромэтана: C2h5 + Br2 -> C2h5Br2
Реакции разложения. Распад исходного вещества на два или более простых. Так, при разложении оксида ртути образуются элементная ртуть и кислород:
2HgO -> 2Hg + O2. Реакции замещения. Замена атомов в молекулах сложного вещества атомами простого вещества. Например, железо замещает медь в растворе сульфата меди: Fe + CuSO4 -> FeSO4 + Cu
Замена атомов в молекулах сложного вещества атомами простого вещества. Например, железо замещает медь в растворе сульфата меди: Fe + CuSO4 -> FeSO4 + Cu
Реакции обмена. Образование двух новых веществ при взаимодействии двух исходных. Например, иодид натрия NaI и нитрат свинца Pb(NO3)2 обмениваются своими составными частями с образованием иодида свинца и нитрата натрия: 2NaI + Pb(NO3)2 -> PbI2 + 2NaNO3 Атом хлора обменивается с одним или более атомами водорода в молекуле углеводорода, например метана СН4, следующим образом: Ch5 + Cl2 -> Ch3Cl + HCl
Реакция гидролиза. Гидролиз (расщепление с участием воды) — это реакция двойного разложения, когда одним из исходных компонентов является вода. При гидролизе хлорида аммония Nh5Cl образуется гидроксид аммония Nh5OH и соляная кислота HCl: Nh5Cl + h3O -> Nh5OH + HCl
Реакция нейтрализации. Особый случай реакции обмена — взаимодействие кислоты с эквивалентным количеством основания с образованием соли и воды.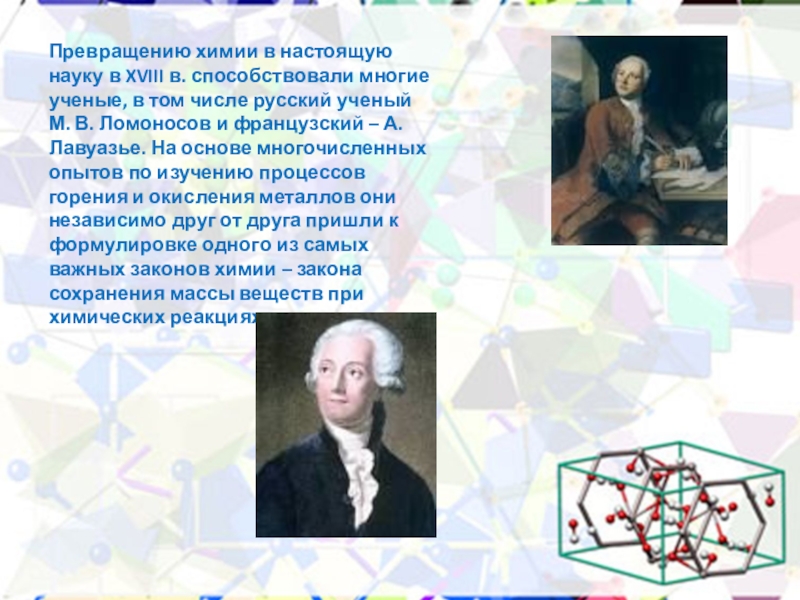 Соляная кислота HCl и гидроксид натрия NaOH нейтрализуют друг друга с образованием хлорида натрия NaCl и воды: HCl + NaOH -> NaCl + h3O
Соляная кислота HCl и гидроксид натрия NaOH нейтрализуют друг друга с образованием хлорида натрия NaCl и воды: HCl + NaOH -> NaCl + h3O
ЛИТЕРАТУРА
Ма Ш. Современная теория критических явлений. М., 1980 Дикерсон Р. и др. Основные законы химии. М., 1982
Энциклопедия Кольера. — Открытое общество.
2000.
- ХИМИЯ КОЛЛОИДНАЯ
- ЭКВИВАЛЕНТНАЯ МАССА
Смотреть что такое «ПРЕВРАЩЕНИЯ ВЕЩЕСТВ» в других словарях:
Обмен веществ — или метаболизм, лежащий в основе жизни закономерный порядок превращения веществ и энергии в живых системах, направленный на их сохранение и самовоспроизведение; совокупность всех химических реакций, протекающих в организме. Ф. Энгельс,… … Большая советская энциклопедия
Обмен веществ и энергии — (у микробов) одно из кардинальных св в у всех организмов, выражающееся в совокупности процессов превращения веществ и энергии, направленных на сохранение и воспроизведение жизни.
О. в. э. у микробов принципиально сходен с таковым у высших… … Словарь микробиологии
Обмен веществ — см. Метаболизм. Экологический энциклопедический словарь. Кишинев: Главная редакция Молдавской советской энциклопедии. И.И. Дедю. 1989. Обмен веществ превращения веществ (и энергии) в организмах, обеспечивающие их жизнеспособнос … Экологический словарь
обмен веществ и энергии — (син. метаболизм) совокупность процессов превращения веществ и энергии в живом организме и обмена организма веществами и энергией с окружающей средой … Большой медицинский словарь
Обмен веществ — и энергии – совокупность процессов превращения веществ и энергии в животном организме и их обмена с окружающей средой; рассматривается по составляющим компонентам: белковый, липидный, углеводный, энергетический, водно солевой, витаминный … Словарь терминов по физиологии сельскохозяйственных животных
Круговорот веществ — на Земле, повторяющиеся процессы превращения и перемещения вещества в природе, имеющие более или менее выраженный циклический характер.
 Эти процессы имеют определённое поступательное движение, т. к. при так называемых циклических… … Большая советская энциклопедия
Эти процессы имеют определённое поступательное движение, т. к. при так называемых циклических… … Большая советская энциклопедияОБМЕН ВЕЩЕСТВ — метаболизм, совокупность протекающих в живых организмах химич. превращений, обеспечивающих их рост, жизнедеятельность, воспроизведение, постоянный контакт и обмен с окружающей средой. Благодаря О. в. происходит расщепление и синтез молекул,… … Биологический энциклопедический словарь
Обмен веществ в растении — Этим выражением (представляющим перевод немецкого термина Stoffwechsel английские физиологи заменяют его термином метаболизм) обозначают совокупность превращений вещества, обуславливающих жизненную деятельность организма. Следует, прежде всего,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
круговорот веществ — на Земле, повторяющиеся процессы превращения и перемещения вещества в природе, имеющие более или менее циклический характер.
 Общий круговорот веществ складывается из отдельных процессов (круговорот воды, газов, химических элементов), которые не… … Энциклопедический словарь
Общий круговорот веществ складывается из отдельных процессов (круговорот воды, газов, химических элементов), которые не… … Энциклопедический словарьКРУГОВОРОТ ВЕЩЕСТВ — в природе, относительно повторяющиеся взаимосвязанные физические, химические и биологические процессы превращения и перемещения вещества в природе. До создания В. И. Вернадским биогеохимии и учения о биосфере в науке бытовало представление о… … Биологический энциклопедический словарь
Книги
- Межфазные превращения и формирование поверхности многокомпонентных полупроводников в жидких средах. Учебное пособие, Мокроусов Геннадий Михайлович, Зарубина Оксана Николаевна, Бекезина Татьяна Петровна. В пособии на примере полупроводников типа А`Bv и A`BVI рассмотрены, типичные межфазные превращения (потенциалопределяющие реакции), протекающие в системах многокомпонентное соединение-вода… Подробнее Купить за 987 грн (только Украина)
- Межфазные превращения и формирование поверхности многокомпонентных полупроводников в жидких средах Учебное пособие, Мокроусов Г.
 , Зарубина О., Бекезина Т.. В пособии на примере полупроводников типа АШВУ и AnBVI рассмотрены типичные межфазные превращения (потенциалопределяющие реакции), протекающие в системах многокомпонентное соединение-вода… Подробнее Купить за 867 руб
, Зарубина О., Бекезина Т.. В пособии на примере полупроводников типа АШВУ и AnBVI рассмотрены типичные межфазные превращения (потенциалопределяющие реакции), протекающие в системах многокомпонентное соединение-вода… Подробнее Купить за 867 руб - Межфазные превращения и формирование поверхности многокомпонентных полупроводников в жидких средах. Учебное пособие, Г. М. Мокроусов, О. Н. Зарубина, Т. П. Бекезина. В пособии на примере полупроводников типа AIIIBV и AIIBVI рассмотрены типичные межфазные превращения (потенциалопределяющие реакции), протекающие в системах многокомпонентное соединение -… Подробнее Купить за 858 руб
Другие книги по запросу «ПРЕВРАЩЕНИЯ ВЕЩЕСТВ» >>
Превращения веществ. Роль химии в нашей жизни
Превращения веществ. Роль химии в нашей жизни
Автор: edu2
Методическая копилка —
Химия
МБОУ «СОШ №2 г. Щигры Курской области»
Щигры Курской области»
Урок химии
8 класс
«Превращения веществ.
Роль химии в нашей жизни»
Подготовила:
Ерохина Елена Николаевна
учитель химии высшей
квалификационной категории
ПЛАНИРОВАНИЕ ТЕМЫ «ВВЕДЕНИЕ»
1 урок. Предмет химии. Вещества.
2 урок. Превращение веществ. Роль химии в нашей жизни.
3 урок П.р. №1. Приемы обращения с лабораторным оборудованием.
4 урок. Краткие сведения по истории химии. Основоположники
отечественной химии.
5 урок. Знаки химических элементов. Периодическая таблица
химических элементов Д.И.Менделеева.
6 урок. Химические формулы. Относительные атомная и
молекулярные массы.
Урок «Превращение веществ. Роль химии в нашей жизни» — это второй урок в теме «Ведение», изучается в 8 классе. Учебник: Химия. 8 класс. Учебник для общеобразовательных учебных учреждений, автор Габриелян О.С.
Литература для учителя:
- Химия. 8 класс: учебник для общеобразовательных учреждений/ О.С. Габриелян.- 2-е издание., стереотип.- М.: Дрофа, 2013 г.
- Химия. 8 класс: рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 8 класс»/ О.С. Габриелян, С.А. Сладков.- М.: Дрофа, 2013 г.
- Леенсон И.А., 100 вопросов и ответов по химии. Материалы для школьных рефератов, факультативных занятий и семинаров. – М.:АСТ –Астрель, 2002.
- Большая Серия Знаний. Химия. Коллектив авторов. – М.: ООО «ТД «Издательство Мир книги». «Русское энциклопедическое товарищество», 2006.
- Курмашева К.К., Химия в таблицах и схемах.- М.: «Лист Нью», 2003.
- Ковалевская Н.Б., Химия.8 класс. В таблицах и схемах., М.: «Издат – Школа XXI век», 2003.

5. Катаева Л.Г., Толкачёва Т.К., Химия: Карточки – задания по неорганической химии. 8 класс. Книга для учителя. – М., Просвещение. 1998.
Литература для обучающихся:
- Химия. 8 класс: учебник для общеобразовательных учреждений/ О.С. Габриелян.- 2-е издание., стереотип.- М.: Дрофа, 2013 г.
- Химия. 8 класс: рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 8 класс»/ О.С. Габриелян, С.А. Сладков.- М.: Дрофа, 2013 г.
- Леенсон И.А., 100 вопросов и ответов по химии. Материалы для школьных рефератов, факультативных занятий и семинаров. – М.:АСТ –Астрель, 2002.
- Большая Серия Знаний. Химия. Коллектив авторов. – М.: ООО «ТД «Издательство Мир книги». «Русское энциклопедическое товарищество», 2006.
ТЕМА: ПРЕВРАЩЕНИЯ ВЕЩЕСТВ. РОЛЬ ХИМИИ В НАШЕЙ ЖИЗНИ.
Цели и задачи урока
Образовательные:
сформировать у обучающихся знания:
о физических и химических явлениях;
о различии этих явлений;
сформировать первоначальное понятие о химической реакции;
об условиях протекания химических реакций;
о признаках химических реакций.
Развивающие:
продолжить работу над формированием у обучающихся:
навыков частично – поисковой деятельности;
умения работать в должном темпе;
умение пользоваться справочными материалами;
умения описывать физические свойства веществ;
умения различать понятия «тело» и «вещество».
Воспитательные:
воспитывать уважение к интеллектуальному труду;
формировать умение вести диалог, дискутировать, выслушивать друг друга.
План урока:
- Проверка домашнего задания. Полётное повторение.
- Изучение нового материала. Физические и химические явления.
- Презентации подготовленные обучающимися о положительном и отрицательном значении химии в жизни человека.
- Закрепление полученных знаний.
- Задание на дом.
- Рефлексия
Начальная подготовка обучающихся:
Обучающиеся знакомы к этому уроку с понятиями тело и вещество, с изменением веществ из курсов природоведения и физики.
Форма урока:
Комбинированный урок.
Оборудование урока:
- Компьютер, мультимедийный проектор, экран.
- Презентации.
- Пробирки, спиртовка, спички, ступка, пестик, пробиркодержатель; реактивы: растворы CuSO4, BaCl2, NaOH, HCl; сахароза, мел.
- Инструктивные карты
Ход урока
- Организационный этап (1мин.)
- Этап проверки знаний.
|
Деятельность учителя
|
Деятельность обучающихся
|
Время
|
|
Задаёт короткие устные вопросы, которые дублируются в инструктивной карте, в очень быстром темпе и при правильном ответе разрешает ученику сесть.
|
Работают по заданию 1 инструктивной карты
№1. Дайте понятия: предмет химии, тело, вещество, атом, химический элемент, формы существования химического элемента, вещества простые и сложные, свойства веществ.
|
3 мин.
|
|
Даёт задания по вариантам для самостоятельной работы
|
Выполняют самостоятельно задания №2,3 инструктивной карты.
|
4 мин.
|
- Мотивационный этап.
|
Деятельность учителя
|
Деятельность обучающихся
|
Время
|
|
Создание проблемной ситуации.
Демонстрация слайдов.
Посмотрите внимательно на слайды. Что происходит с веществами? Сформулируйте тему урока.
А как вы считаете, каковы цели данного урока?
|
Формулируют тему и цели урока.
Тему урока записывают в тетрадь
|
3 мин.
|
- Операционно-исполнительский этап.
|
Деятельность учителя
|
Деятельность обучающихся
|
Время
|
|
Человеку постоянно приходится сталкиваться с теми или иными явлениями. Одни из них являются физическими, другие – химическими.
Разберёмся, что обозначают данные понятия. На ваших столах лежат инструктивные карты, где описаны лабораторные опыты, которые вам предстоит выполнить.
По результатам лаб. Опытов проводит обсуждение.
|
Выполняют лабораторные опыты.
Лабораторный опыт №1.
На фильтровальную бумагу капните на значительном расстоянии друг от друга по 1 капле воды и этилового спирта. Какая из капель высыхает быстрее? Какие явления – физические или химические — происходят при этом?
Лабораторный опыт №2.
Возьмите лист бумаги и сверните его. Что изменилось? Какое явление – физическое или химическое — наблюдается при этом?
|
5 мин.
|
|
Проводит демонстрации явлений.
Д.1. Измельчение кусочков мела.
Д.2. Действие на мел кислотой.
Д.3. Взаимодействие CuSO4 с NaOH.
Д.4. Взаимодействие BaCl2 с Н2SO4.
Д.5. Горение спички, спиртовки.
Д.6. Обугливание сахарозы.
|
Наблюдают за происходящими явлениями. Готовят ответ на вопрос: Какие явления – физические или химические — происходят при этом? Каковы их признаки?
|
10 мин.
|
|
В ваших инструктивных картах в задании 3 даны определения двух понятий. Ваша задача установить, какое из определений соответствует понятию «физическое явление», а какое – «химическому явлению».
Проводит фронтальный опрос обучающихся по результатам проделанной работы.
Записывает в тетради признаки химических явлений.
|
Заканчивают определения, записывают их в тетрадь, приводят примеры.
Явления, при которых одни вещества превращаются в другие, называются…………………
Например, ………………………….
Явления, при которых изменяются форма, размеры тел или агрегатное состояние веществ, а состав их остается постоянным, называются ……………………………………………
Например, ………………………….., ………………………………………….., ………………………………
Записывают в тетрадь признаки химических явлений: изменение окраски, выделение газа, выпадение осадка, появление запаха, выделение или поглощение света и тепла.
|
6 мин.
|
|
Рассматривает вопрос по теме «Роль химии в жизни человека».
Как вы думаете, какова роль химии в жизни человека?
|
Выступают 2 обучающихся с презентациями по темам: «Положительное значение химии», «Отрицательное значение химии».
Обучающиеся приходят к мысли, что без химии немыслима жизнь современного человека. В тоже время, они отмечают, что неразумное, неконтролируемое применение химических веществ приводит к пагубным последствиям.
|
5 мин.
|
5. Рефлексивно-оценочный этап.
|
Деятельность учителя
|
Деятельность обучающихся
|
Время
|
|
Предлагает выполнить задания в РТ.
|
Выполняют задание в рабочей тетради по вариантам: №1 с.12 (1 вариант) и №2 с.13 (2 вариант).
|
3 мин.
|
|
Запишите домашнее задание.
|
Записывают в дневник Д/З из инструктивной карты.
|
1 мин.
|
|
А сейчас я прошу вас оценить урок, работая с инструктивной картой.
Выставление оценок обучающимся за работу на уроке.
|
Самоанализ (нужное подчеркивают)
1. Своей работой на уроке я
— Доволен
— Недоволен
2. Урок мне показался
— Интересным
— Неинтересным
3. Материал урока был
— Понятен — Непонятен
|
3 мин.
|
|
Спасибо. Урок окончен. До свидания.
|
Прощаются.
Сдают учителю на проверку инструктивные карты.
|
1 мин.
|
химическое превращение
Химические превращения в растворе электролита за счет внешней электрической энергии происходят в электролизерах или электролитических ваннах (см. рис. 1.1). В таких системах часть раствора электролита, находящаяся у анода, называется анолитом, находящаяся у катода — католитом.[ …]
Химическая технология — естественная, прикладная наука о способах и процессах производства продуктов (предметов потребления и средств производства), осуществляемых с участием химических превращений технически, экономически и социально целесообразным путем.[ …]
Химическое производство — совокупность процессов и операций, осуществляемых в машинах и аппаратах и предназначенных для переработки сырья путем химических превращений в необходимые продукты. [ …]
[ …]
Химическая промышленность потребляет довольно много энергии, чтобы обеспечить переработку сырья в продукты, -около 15% всех энергоресурсов расходуется в этой области техники. Энергия не столько потребляется непосредственно для получения продукта, сколько обеспечивает условия его производства. Кроме того, нередко химические превращения сопровождаются выделением энергии (экзотермические реакции). Поэтому энергетическая система должна обеспечивать не только распределение энергии по стадиям производства, но и по возможности возвращение ее после использования в переработке сырья.[ …]
Химический реактор — устройство, аппарат для проведения химических превращений (химических реакций).[ …]
Химическое действие, вызванное первичным поглощением рентгеновского или у излучения, очень мало; измеримые химические изменения обусловлены рядом последовательных вторичных ионизационных процессов, протекающих под действием выбитых электронов ¡[2а, 18]. Этим объясняется сходство химических превращений в целлюлозе под действием уоблучения и облучения частицами высокой энергии, такими, как электроны. [ …]
[ …]
Химические превращения в атмосфере инициируются, главным образом, продуктами фотолиза озона, кислорода, воды, оксидов азота.[ …]
Химические превращения являются источником необходимой для микроорганизмов энергии. Живые организмы способны использовать только связанную химическую энергию. Универсальным переносчиком энергии в клетке является аденозинтрифосфорная кислота (АТФ).[ …]
В химических производствах протекают разнообразные процессы, связанные или с выделением энергии, или с ее затратой, или со взаимными превращениями и переходами. Энергия затрачивается на подготовку сырья, осуществление химических превращений, выделение продуктов, транспортировку материалов, сжатие газа и т. д. Потребление разных видов энергии в стоимостном выражении распределяется между процессами химического производства следующим образом: в химических реакциях — 5-40%, в массообменных процессах — 30-80%, в теплообменных процессах — 60-90%.[ …]
В химическом производстве элементы — это машины, аппараты и другие устройства, связи — это материальные трубопроводы, паропроводы и проч. , которые соединяют машины, аппараты, устройства. В элементах происходит превращение потоков (изменение их состояния — разделение, смешение, сжатие, нагрев, химические превращения и т.д.). По связям потоки (материальные, тепловые, энергетические) передаются из одного элемента в другой. Это позволяет представить химическое производство как химико-технологическую систему.[ …]
, которые соединяют машины, аппараты, устройства. В элементах происходит превращение потоков (изменение их состояния — разделение, смешение, сжатие, нагрев, химические превращения и т.д.). По связям потоки (материальные, тепловые, энергетические) передаются из одного элемента в другой. Это позволяет представить химическое производство как химико-технологическую систему.[ …]
Ряд химических превращений требует инициирования, чтобы превращения могли протекать с заметной скоростью. Таким инициатором могут быть химические вещества — катализаторы. Химические процессы с их участием называются каталитическими.[ …]
Физико-химические свойства смол: среднечисловая молекулярная масса смол, определенная криоскопией в нафталине, колеблется от 600 до 800 ед. Кроме того, возможно применение АСВ для производства пеков, ингибиторов радикальных процессов окислительной деструкции полимеров, ингибиторов коррозии и т. д. В связи с проблемой рационального использования АСВ, определенную перспективу приобретает направление — получение концентратов АСВ путем глубокой деасфальтизации нефтяных остатков бензином (Добен-процесс). Продукты Добен-процесса могут быть использованы как стабилизаторы полимеров, сырье для углеродистых и композиционных материалов и т. д.[ …]
Продукты Добен-процесса могут быть использованы как стабилизаторы полимеров, сырье для углеродистых и композиционных материалов и т. д.[ …]
Выше были даны основы химической технологии как науки и как способа производства. Многообразие химических превращений и многостадийность протекающих процессов обусловливают большое разнообразие технологических и конструктивных решений в различных производствах. Тем не менее можно выделить основные направления в химической технологии, которые в настоящее время являются перспективными для ее дальнейшего развития.[ …]
АЗОТФИКСАЦИЯ — процесс химического превращения атмосферного газообразного азота (Ну) в нитраты (Л/0з») или аммиак (Л/Нз), которые могут использоваться растениями для синтеза аминокислот и других азотсодержащих органических молекул.[ …]
Для обеспечения полноты химических превращений необходимо перемешивание шихты. Другим условием для нормального течения процесса является достаточное содержание серы в огарке — для перевода всего NaCl) в. Na;iS04. В случае недостатка серы к огарку добавляют свежий колчедан. Для того чтобы хлорирующий обжиг начался и затем шел автотермично, достаточно смесь подогреть до 200—300 °С. Обжиг сопровождается выделением S02) S03, HCl. Кислые газы обжига поглощают водой с получением смеси кислот (НС1 и h3SO+), которую используют для выщелачивания меди.[ …]
Если в результате развития химических превращений горючей смеси скорость выделения тепла превысит скорость отвода тепла в окружающую среду с учетом всех форм энергетического обмена с ней, или скорость зарождения активных центров реакции превысит скорость их гибели, то при определенном значении температуры или концентрации активных продуктов начнется прогрессивное самоускорение реакции до взрывной — воспламенение.[ …]
Под действием потока электронов химические превращения в газах значительно ускоряются. Этот метод пригоден преимущественно для очистки дымовых газов ТЭС от N0 и 802. Сначала поток дымовых газов очищают от золы. Затем подают аммиак, и газовую смесь подвергают облучению. В результате из аммиака, оксидов азота и серы образуется сухой порошок — смесь солей Н4)2804 и (МН4)2804 2(ГШ4)2803. После отделения солей (например на электрофильтре или рукавном фильтре) газ выбрасывают через дымовую трубу, а смесь солей используют в качестве удобрения. Основными достоинствами метода являются его простота и отсутствие вторичных загрязнителей, включая сточные воды. Обычно достигается степень очистки от N0 70-90 %. Разрабатываются различные модификации метода: с рециклом очищенного газа, с облучением газа в две стадии, когда большая часть дозы поглощается на первом этапе. Основным недостатком метода считаются значительные энергетические затраты.[ …]
В результате из аммиака, оксидов азота и серы образуется сухой порошок — смесь солей Н4)2804 и (МН4)2804 2(ГШ4)2803. После отделения солей (например на электрофильтре или рукавном фильтре) газ выбрасывают через дымовую трубу, а смесь солей используют в качестве удобрения. Основными достоинствами метода являются его простота и отсутствие вторичных загрязнителей, включая сточные воды. Обычно достигается степень очистки от N0 70-90 %. Разрабатываются различные модификации метода: с рециклом очищенного газа, с облучением газа в две стадии, когда большая часть дозы поглощается на первом этапе. Основным недостатком метода считаются значительные энергетические затраты.[ …]
Обмен веществ и энергии. Совокупность химических превращений, протекающих в клетке или организме, связанных между собой и сопровождающихся превращением энергии, называется обменом веществ и энергии.[ …]
Это объясняется тем, что в комплексе различных химических превращений одной из основных является реакция окисления компонентов горючего кислородом воздуха, а в процессах коагуляции частиц формирования отложений и загрязнений велика роль поверхностно-активных веществ. [ …]
[ …]
Цепное воспламенение. Подавляющее большинство химических реакций, в том числе химические превращения при воспламенении и горении, являются сложными. В таких реакциях исходные вещества превращаются в конечные продукты с образованием ряда промежуточных соединений, которые восстанавливаются в ходе химических превращений. Ведущую роль в развитии цепных реакций играют активные части, легко вступающие в реакции с исходными или промежуточными продуктами.[ …]
Окислительно-восстановительная функция заключается в химическом превращении веществ, которые содержат атомы с переменной степенью окисления (это в основном соединения железа, марганца и др.). В результате происходят превращения большинства химических соединений, при этом преобладают биогенные процессы окисления и восстановления.[ …]
Такое сильное уменьшение энергии активации показывает, что химическое превращение карбоксильной группы Аэр-52 в —СНгОН-группу приводит к потере ферментативной активности [202].[ … ]
]
При составлении материального баланса обычно задаются степени превращения исходных веществ в стехиометрических уравнениях как результат химического превращения в реакционном элементе. Этим однозначно определяются количества выходящих из элемента всех компонентов и далее можно определить другие показатели процесса (селективность, выход продукта) и параметры потока (его количество, концентрации). Но могут быть заданы и другие показатели химического превращения — количество продуктов, концентрации компонентов или их выход, селективности. По (3.11) — (3.15) их можно пересчитать в степени превращения и затем рассчитывать материальный баланс. Таких данных должно быть столько, сколько есть независимых стехиометрических уравнений.[ …]
Более всего склонны к окислению жидкие нефтепродукты; если они не содержат химически нестабильных веществ, то продукты окисления практически не влияют на общий баланс загрязненности жидкости, составляя в нем незначительную часть. Однако в бензинах, а также в некоторых дизельных топливах содержится значительное количество непредельных углеводородов, которые склонны к химическим превращениям при хранении и транспортировании. В бензинах, полученных методом термического крекинга, содержание непредельных углеводородов может составлять 30—45% от общего количества продукта, а в дизельных топливах, полученных методом каталитического крекинга, достигает 7% [13]. Непредельные углеводороды способствуют интенсивному осмолению горючего и образованию в нём твердого осадка — асфальто-смолис-тых соединений.[ …]
В бензинах, полученных методом термического крекинга, содержание непредельных углеводородов может составлять 30—45% от общего количества продукта, а в дизельных топливах, полученных методом каталитического крекинга, достигает 7% [13]. Непредельные углеводороды способствуют интенсивному осмолению горючего и образованию в нём твердого осадка — асфальто-смолис-тых соединений.[ …]
Генерация электрической энергии за счет протекающих в растворе электролита химических превращений происходит в гальванических элементах или химических источниках тока (рис. 1.2). Здесь электрод, направляющий электроны во внешнюю цепь, называется отрицательным полюсом элемента, принимающий электроны из внешней цепи — положительным.[ …]
Температура потоков в элементах ХТС изменяется за счет внутренних источников ((?ист), один из которых — химические превращения. Теплота реакции др равна изменению энтальпии вследствие изменения химического состава реакционной среды ([ …]
Чтобы биосфера продолжала существовать и на Земле не прекращалось развитие жизни, постоянно должны происходить непрерывные химические превращения ее живого вещества. Иными словами, вещества после использования одними организмами должны переходить в усвояемую для других организмов форму. Такая циклическая миграция веществ и химических элементов может осуществляться только при определенных затратах энергии, источником которой является Солнце. Академик В.Р. Вильямс указывал, что единственный способ придать чему-то конечному свойства бесконечного — это заставить конечное вращаться по замкнутой кривой, то есть вовлечь его в круговорот.[ …]
Иными словами, вещества после использования одними организмами должны переходить в усвояемую для других организмов форму. Такая циклическая миграция веществ и химических элементов может осуществляться только при определенных затратах энергии, источником которой является Солнце. Академик В.Р. Вильямс указывал, что единственный способ придать чему-то конечному свойства бесконечного — это заставить конечное вращаться по замкнутой кривой, то есть вовлечь его в круговорот.[ …]
Подавляющее большинство процессов в клетке — ферментативные. Жизнь протекает при «низких» температурах, и без участия катализаторов химические превращения просто не могут происходить со скоростями, необходимыми для осуществления сложных реакций, с разрывом прочных ковалентных связей. Регуляция мощного каталитического потенциала клетки достигается двумя принципиально разными путями: изменением количества ферментов и активности последних. На активность фермента влияет количество доступного субстрата, физико-химические параметры среды и взаимодействие с особыми метаболитами, называемыми модуляторами. Ферменты, активность которых зависит от модуляторов, называют регуляторными. Они имеют для связывания субстрата центр, где протекает акт катализа, и еще один участок, называемый аллостерическим, для присоединения регулятора. Аллостерический путь регулирования обеспечивает «тонкую» настройку метаболизма в соответствии с изменяющимися условиями среды, и она осуществляется почти «мгновенно».[ …]
Ферменты, активность которых зависит от модуляторов, называют регуляторными. Они имеют для связывания субстрата центр, где протекает акт катализа, и еще один участок, называемый аллостерическим, для присоединения регулятора. Аллостерический путь регулирования обеспечивает «тонкую» настройку метаболизма в соответствии с изменяющимися условиями среды, и она осуществляется почти «мгновенно».[ …]
Данный метод получил наибольшее распространение в мире из всех циклических (сухих и мокрых) процессов, благодаря хорошей изученности химических превращений и большому практическому опыту, а также доступности исходного хемосорбента — соды и целесообразности применения метода для широкого диапазона концентраций извлекаемого SO2.[ …]
Современными исследованиями установлено, что лишь незначительная часть масла в процессе его эксплуатации претерпевает существенные химические превращения (срабатываются присадки, окисляются тяжелые углеводороды, адсорби руется сажа). Удалив из отработанного масла продукты окисления, механические примеси, топливные, фракции, воду, эти масла можно использовать вторично. [ …]
[ …]
Комплексы между ферментом и продуктом для алкогольде-гидрогеназы дрожжей диссоциируют довольно быстро, так что лимитирующими являются стадии химического превращения [20]. Это позволяет измерить кинетические изотопные эффекты для указанных стадий с помощью стационарной кинетики. Установлено, что окисление дейтерированных спиртов RCD2OH и восстановление бензальдегидов дейтерированным NADH (т. е. NADD) протекают значительно медленнее соответствующих реакций с участием немеченых соединений ( h/ d = 3—5) [14, 20]. Это показывает, что перенос гидрид-иона (или дейтерид-иона) осуществляется в ходе лимитирующей стадии реакции. Измерение константы скорости переноса гидрид-иона в случае алкогольдегидрогеназы печени лошади с помощью предстацио-нарной кинетики выявило наличие аналогичных изотопных эффектов [21, 22].[ …]
Под устойчивостью геосистем к техногенному воздействию понимают их способность к самоочищению от продуктов техногенеза, зависящую от скорости химических превращений и интенсивности выноса этих продуктов из геосистем. [ …]
[ …]
Одной из особенностей молекулы ФАД является наличие двух циклов, соединенных достаточно гибкой пирофосфор-ной связью. Поэтому существенное значение для химических превращений и особенно для понимания механизма катализируемых с участием флавинов ферментативных реакций имеет вопрос о конформации молекулы ФАД.[ …]
Химия древесины и полимеров как наука изучает: 1) основы физики и химии высокомолекулярных соединений, в том числе способы получения полимеров, особенности химического строения их молекул, физической структуры, химических превращений и поведения в растворах; 2) основные классы синтетических полимеров, в том числе способы получения, свойства и применение основных их представителей; 3) строение и свойства основных компонентов древесины на основе общих закономерностей химии полимеров; 4) сущность процессов химической переработки древесины и ее отдельных компонентов.[ …]
Детали механизма действия большинства этих ферментов более или менее известны. Установлено, например, наличие и положение каталитических групп и последовательность химических превращений в ходе реакции (хотя и не для всех случаев). Лучше всего изучены реакции, протекающие с образованием промежуточных соединений, которые можно выделить и охарактеризовать. Это не только дает представление о механизме химических превращений, но и позволяет сразу получить важную информацию о положении субстрата относительно каталитических групп фермента.[ …]
Лучше всего изучены реакции, протекающие с образованием промежуточных соединений, которые можно выделить и охарактеризовать. Это не только дает представление о механизме химических превращений, но и позволяет сразу получить важную информацию о положении субстрата относительно каталитических групп фермента.[ …]
Интенсивность процесса гетерогенного катализа на пористых катализаторах определяется соотношением скоростей транспорта (переноса) реактантов в порах катализатора и химического превращения реагирующих веществ на поверхности пор.[ …]
Главное отличие от анодирования в механизме формирования оксидного слоя при микродуговом оксидировании связано с газоразрядными процессами в микропорах. Высокотемпературные химические превращения и транспорт вещества электролита в зону электрического разряда приводят к специфическим изменениям по сравнению с анодированием в фазовом составе и строении оксидного слоя. Сформированный оксидный слой состоит из технологического, основного (рабочего) и переходного слоев, плавно переходящих друг в друга. В рабочем слое основной фазой может быть а-А1203, а в технологическом и переходном преобладают алюмосиликаты.[ …]
В рабочем слое основной фазой может быть а-А1203, а в технологическом и переходном преобладают алюмосиликаты.[ …]
Распределение времени пребывания реакционной смеси всегда имеет место в реакторах с перемешиванием (рис. 2.58,а). Какая-то часть входящего потока быстро достигает выхода. Время для превращения веществ будет небольшим. Другая часть потока долго находится в реакционной зоне. На выходе все части потока перемешиваются. Если за время пребывания каждой порции реакционной смеси акт химического превращения (т. е. превращения молекулы исходного вещества в продукт) заканчивается, то распределение времени пребывания не скажется на общем превращении. Но возможны длительные, многоэтапные превращения. Полимеризация — последовательное присоединение молекул мономера к растущей цепочке образующегося продукта. Длина полимерной цепи зависит от времени проведения реакции. В проточном реакторе с перемешиванием из-за различного времени пребывания отдельных частей потока в нем на выходе будем иметь смесь полимерных молекул с различной длиной цепи, или с различной молекулярной массой. Неоднородность молекулярно-массового состава продукта сказывается на его качестве.[ …]
Неоднородность молекулярно-массового состава продукта сказывается на его качестве.[ …]
По происхождению ВМС подразделяются на природные, выделенные из природных материалов; к ним относятся природный каучук, белки, сложные углеводы (полисахариды) и др., искусственные, полученные в результате химических превращений природных полимеров, и синтетические, полученные синтезом из низкомолекулярных соединений (мономеров) .[ …]
Так, при выбросе двуокиси серы и соединений ртути из достаточно высоких источников (высокие трубы) концентрации этих ингредиентов путем рассеяния быстро достигают в приземном слое воздуха существующих допустимых норм. Однако в дальнейшем в результате химических превращений и накопления (после осаждения на растительность, почву или вымывания в реки и озера) их относительная токсичность и потенциальная опасность для многих организмов и человека возрастают.[ …]
Удаление из газов тех или иных газообразных вредностей осуществляется взаимодействием последних с жидкими, твердыми или газообразными веществами. Как следствие, примеси связываются или нейтрализуются, превращаясь в соединения любого агрегатного состояния. Взаимодействие может иметь физико-химический, химический или биохимический характер. Так, твердые вещества поглощают газообразные примеси физадсорбцией или хемосорбцией, при химическом взаимодействии. Жидкие вещества растворяют их без химического (абсорбция) и с химическим взаимодействием, при которюм примесь превращается в нейтральное вещество, остающееся в растворе или в Другом агрегатном состоянии выделяющееся из жидкого поглотителя. Взаимодействие примеси с газообразным компонентом носит только химический характер, когда вредность либо нейтрализуется, оставаясь газовой, либо образует аэрозоль (пыль, туман), улавливаемый известными способами. Среди реакций в газовой фазе ведущее место занимают термические процессы (пиролиз, дожигание и др.). Для ускорения обезвреживания загрязнителей во всех типах химических превращений могут быть использованы катализаторы.[ …]
Как следствие, примеси связываются или нейтрализуются, превращаясь в соединения любого агрегатного состояния. Взаимодействие может иметь физико-химический, химический или биохимический характер. Так, твердые вещества поглощают газообразные примеси физадсорбцией или хемосорбцией, при химическом взаимодействии. Жидкие вещества растворяют их без химического (абсорбция) и с химическим взаимодействием, при которюм примесь превращается в нейтральное вещество, остающееся в растворе или в Другом агрегатном состоянии выделяющееся из жидкого поглотителя. Взаимодействие примеси с газообразным компонентом носит только химический характер, когда вредность либо нейтрализуется, оставаясь газовой, либо образует аэрозоль (пыль, туман), улавливаемый известными способами. Среди реакций в газовой фазе ведущее место занимают термические процессы (пиролиз, дожигание и др.). Для ускорения обезвреживания загрязнителей во всех типах химических превращений могут быть использованы катализаторы.[ …]
За этим последовали дополнительные испытания, обсуждение полученных результатов, изучение возможности решения проблем, связанных с высокими значениями pH, концентрацией солей и присутствием других организмов, отличных от бактерий, таких, как грибки, рассмотрение возможности применения различных физических и химических методов обработки, обсуждение самых различных вопросов, начиная от биологических методов обработки и кончая оценкой методов разделения и использования химического превращения в процессе обработки. [ …]
[ …]
При действии гидролизующих агентов, в особенности кислот и ферментов, но также и щелочей, они расщепляются на исходные составные части.[ …]
Для извлечения сорбированных веществ могут быть использованы. экстрагирование органическим растворителем, изменение степени дис-социации слабого электролита в равновесном растворе, отгонка адсорбированного вещества с водяным паром, испарение адсорбированного вещества током инертного газообразного теплоносителя. В отдельных случаях осуществляют химические превращения сорбированных веществ с последующей десорбцией.[ …]
Полученные результаты авторы исследования объясняют возможностью химических превращений препаратов после их адсорбции на угле.[ …]
Почти все производственные объекты нефтяной и газовой промышленности при соответствующих условиях загрязняют окружающую среду множеством опасных вредных веществ разной экологической значимости. Помимо собственых природных углеводородов, их спутников, продуктов переработки, в составе загрязнителей содержатся многочисленные реагенты, катализаторы, ПАВ, ингибиторы, щелочи, кислоты, вещества, образующиеся при горении, химическом превращении и т. д. Основные из них рассматриваются подробнее /20, 21/.[ …]
д. Основные из них рассматриваются подробнее /20, 21/.[ …]
Галогенсодержащие органические соединения, многие-из которых являются канцерогенными веществами [311], относятся к наиболее распространенным загрязнителям атмосферного воздуха. При этом в последние годы опасность загрязнения окружающей среды этими веществами постоянно увеличивается в связи со все возрастающими масштабами развития производства этих соединений в виде пестицидов, винилхлорида, поливинилхлорида, фтор-углеродсодержащих хладагентов (фреонов), ракетного топлива и хлорсодержащих растворителей (трихлорэтилен, дихлорэтан, хлороформ и др.). Мировое производство хлорфторуглеводородов (в основном это хлорфторметаны, ССЬР и СС12Рг, на долю которых приходится около 90% всех фреонов) составляет несколько миллионов тонн в-год, причем две трети этого количества применяют в качестве носителей в различных бытовых аэрозолях [312], Основным источником поступления этих соединений в атмосферу являются рефрижераторные установки и всевозможные бытовые аэрозоли. В 1975 г. 85% хлорфторметанов было выброшено в атмосферу и лишь остальные 15% использовали в холодильных установках и кондиционерах [312]. Вследствие высокой химической инертности и малой растворимости в воде СР2С1г и СРС1з способны долгое время находиться в атмосфере без изменений. Наиболее важным химическим превращением этих веществ является их фотодиссоциация под действием УФ-радиации солнца (длина волны 200 нм), сопровождающаяся образованием атомов хлора и потреблением атмосферного озона [313]. Поскольку содержание хлорфторметанов в тропосфере и стратосфере постоянно возрастает, эти фотохимические реакции могут привести к нарушению равновесного содержания озона и к уменьшению его количества в стратосфере, что приведет к существенному изменению климата нашей планеты [314].[ …]
В 1975 г. 85% хлорфторметанов было выброшено в атмосферу и лишь остальные 15% использовали в холодильных установках и кондиционерах [312]. Вследствие высокой химической инертности и малой растворимости в воде СР2С1г и СРС1з способны долгое время находиться в атмосфере без изменений. Наиболее важным химическим превращением этих веществ является их фотодиссоциация под действием УФ-радиации солнца (длина волны 200 нм), сопровождающаяся образованием атомов хлора и потреблением атмосферного озона [313]. Поскольку содержание хлорфторметанов в тропосфере и стратосфере постоянно возрастает, эти фотохимические реакции могут привести к нарушению равновесного содержания озона и к уменьшению его количества в стратосфере, что приведет к существенному изменению климата нашей планеты [314].[ …]
Химические превращения основных компонентов в древесине в процессах О-алкилирования и этерификации Текст научной статьи по специальности «Химические науки»
Химия растительного сырья. 2001. №2. С. 47-55.
УДК 634.G.B13.11:661.71B.1
ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ ОСНОВНЫХ КОМПОНЕНТОВ В ДРЕВЕСИНЕ В ПРОЦЕССАХ О-АЛКИЛИРОВАНИЯ И ЭТЕРИФИКАЦИИ
© Н.Г. Базарнова
Алтайский государственный университет, Димитрова, вв, Барнаул,
656099 (Россия) e-mail: [email protected]
В работе представлены экспериментальные данные по изучению химических превращений древесины и основных компонентов (лигнин, целлюлоза, гемицеллюлозы) в ее составе, без предварительного разделения в реакциях О-алкилирования и этерификации. Показано, что в химическое взаимодействие вступают все компоненты древесины. Введение новых функциальных групп в результате химических превращений позволяет получать новые полимерные композиции, которые могут найти большое практическое применение.
Введение
Целесообразность химической переработки древесины без разделения ее на компоненты очевидна с экономической и экологической точек зрения.
Химическая переработка древесины в высокомолекулярные композиции, содержащие в своем составе производные целлюлозы, лигнина, гемицеллюлоз — новое направление в химии древесины, которое развивается на кафедре органической химии Алтайского госуниверситета и сформулировано в [1]. Исследования в этом направлении интенсивно ведутся во всем мире в последние 10-15 лет, однако они носят в основном прикладной характер и связаны с получением различных материалов с полезными потребительскими свойствами [2-9]. Для успешного, прорывного развития данного направления требуется проведение фундаментальных исследований, связанных с разработкой теоретических основ процессов химической переработки древесины без разделения ее на компоненты. Одной из основных задач является оценка реакционной способности и свойств компонентов в процессах превращения их непосредственно в древесине, поиск методов исследования таких процессов и продуктов.
Одной из основных задач является оценка реакционной способности и свойств компонентов в процессах превращения их непосредственно в древесине, поиск методов исследования таких процессов и продуктов.
В данной работе представлены результаты исследований химических превращений компонентов древесины в реакциях О-алкилирования и этерификации ее без разделения на компоненты.
Химические превращения древесины
С целью установления состава и закономерностей превращений отдельных компонентов непосредственно в древесине нами была разработана схема выделения их из О-алкилированной или этерифицированной древесины:
ИК- и ЯМР-спектры компонентов, выделенных по предложенной схеме, соответствуют спектрам соответствующих производных, полученных из изолированных компонентов.
ИК-спектры продуктов О-алкилирования и этерификации отличаются от ИК-спектра исходной древесины осины и соответствующих компонентов во всем интервале исследуемых частот 4000-400 см-1. В спектрах сохраняется полоса поглощения в области ~3430-3450 см-1, ответственная за колебания ОН-групп с ослабленными Н-связями, что свидетельствует об их неполном замещении.
В спектрах сохраняется полоса поглощения в области ~3430-3450 см-1, ответственная за колебания ОН-групп с ослабленными Н-связями, что свидетельствует об их неполном замещении.
Продукты карбоксиметилирования содержат в своем составе -СН2СООН — группу, связанную простой эфирной связью. Валентным колебаниям карбоксилат-иона- в ИК-спектрах соответствуют полосы поглощения при 1600, 1425 и 1380 см-1. В спектрах производных древесины и лигнина полоса в области 1600 см-1 перекрывается с характеристичной полосой ароматического кольца в области 1595 см-1. Спектры этерифицированных производных отличаются интенсивной полосой поглощения при ~1740 см-1. В области 2920 см-1 увеличивается интенсивность полос поглощения валентных колебаний групп СН3-, -СН2-. В ИК-спектрах продуктов бензилирования происходят изменения как в области 36003200 см-1, так и в области 1800-1650 см-1 и 750-670 см-1. Происходит уменьшение валентных колебаний ОН-групп и появление валентных колебаний САг-Н-связи (триплет 3090, 3060, 3030 см-1). Появление полос при 736 и 695 см-1 в спектрах бензилированных целлюлозы, ксилана и увеличение их интенсивности в спектрах бензилированных лигнина и древесины характерны для деформационных колебаний САг-Н-связи.
Появление полос при 736 и 695 см-1 в спектрах бензилированных целлюлозы, ксилана и увеличение их интенсивности в спектрах бензилированных лигнина и древесины характерны для деформационных колебаний САг-Н-связи.
Спектральные исследования позволяют полагать, что производные древесины, полученные в различных реакциях, содержат в своем составе замещенные целлюлозу, лигнин, гемицеллюлозы. Замещение осуществляется неравномерно.
Установленное распределение алкильных или ацильных групп между отдельными компонентами модифицированной древесины подтверждает предположения, сделанные на основе анализа спектральных данных: О-алкилированию и этерификации по ОН-группам в составе древесины подвергаются все основные компоненты (табл. 1-4). Высокомолекулярные компоненты, находясь непосредственно в клеточной стенке древесины, в найденных нами условиях, вступают во взаимодействие с образованием простых или сложных эфиров как в кислой, так и в щелочной средах.
Превращения целлюлозы
Во всех изучаемых реакциях целлюлоза подвергается замещению в меньшей степени, чем лигнин и гемицеллюлозы. В КМЦ, выделенной из КМД, полученной как твердофазным, так и суспензионным способами, содержится небольшое количество КМГ, что соответствует степени замещения порядка 80.
Сравнительный анализ карбоксиметилхолоцеллюлозы и целлюлозы показывает, что КМГ распределены между ними примерно одинаково. Это обусловлено тем, что реакция протекает, в первую очередь, в термодинамически совместимых областях и распределение КМГ между ОН-группами целлюлозы и гемицеллюлоз определяется соотношением компонентов в этой области (50 : 50). Сравнительный анализ ИК- и ЯМР-спектров бензилированной целлюлозы (БЦ), выделенной из бензилдревесины и полученной из изолированной целлюлозы, свидетельствует об идентичности этих продуктов. Бензилирование изолированной целлюлозы протекает более глубоко, чем непосредственно в древесине, и заканчивается через 2 ч от начала реакции. Соотношение количества бензильных групп у первичного и вторичных атомов углерода элементарного звена макромолекулы БЦ составляет ~1 .8 : 1 . Продукты бензилирования, полученные с использованием механохимической активации, более неоднородны по сравнению с бензилпроизводными, полученными в избытке реагентов, и содержат в своем составе фрагменты незамещенных макромолекул целлюлозы и лигнина, которые были выделены методами Кюршнера и Комарова.
Бензилирование изолированной целлюлозы протекает более глубоко, чем непосредственно в древесине, и заканчивается через 2 ч от начала реакции. Соотношение количества бензильных групп у первичного и вторичных атомов углерода элементарного звена макромолекулы БЦ составляет ~1 .8 : 1 . Продукты бензилирования, полученные с использованием механохимической активации, более неоднородны по сравнению с бензилпроизводными, полученными в избытке реагентов, и содержат в своем составе фрагменты незамещенных макромолекул целлюлозы и лигнина, которые были выделены методами Кюршнера и Комарова.
Таблица 1. Содержание карбоксиметильных групп (%) в карбоксиметилдревесине, холоцеллюлозе, целлюлозе, выделенных из нее (суспензионный способ)
Растворитель Древесина ХолЦ Ц (НУК) Ц (К)
Пропанол-2 25.0 14.7 6.3 6.8
н-гексан 13. 9 14.8 6.9 6.4
9 14.8 6.9 6.4
Бензол 12.9 13.4 6.4 6.0
Этилацетат 20.0 12.4 7.3 6.8
Диметилсульфоксид 23.9 — — 7.2
Примечание: НУК — надуксусная кислота, К — метод Кюршнера: способы выделения.
Таблица 2. Содержание карбоксиметильных групп (%) в карбоксиметилдревесине, холоцеллюлозе, целлюлозе, выделенных из нее (твердофазный способ)
Условия карбоксиметилирования ВЦМ (шары) ВЦМ (цилиндры)
ОНдрев : ЫаОН: Ыа-МХУК (моль) 1:1:1 1:1:05 1:1:1 1:1:0.5
Продолжительность реакции, мин 8 10 15 15
Карбоксиметилированная древесина 17. 4 18.6 19.9 15.2
4 18.6 19.9 15.2
Карбоксиметилированная холоцеллюлоза 12.4 11.0 15.8 8.2
Карбоксиметилированная целлюлоза 6.2 6.2 7.0 4.7
Таблица 3. Содержание бензильных групп (%) в бензилированных при 110°С древесине и компонентах, выделенных из нее
Продолжительность Бензилдревесина Бензилцеллюлоза Бензиллигнин
бензилирования, ч
2 24.3 17.8 22.5
6 31.5 29.0 24.8
Таблица 4. Свойства ацетатов бутиратов древесины и компонентов, выделенных из нее (условия синтеза: ОН(древ) : УА : КК= 1 : 1 : 1 моль, 100°С, 6 ч)
Сложный эфир Содержание лигнина по Комарову, % Содержание связанных кислот, %
уксусная масляная
Древесины 19. 6 43.6 13.2
6 43.6 13.2
Целлюлозы 1.3 22.4 3.8
Лигнина 95.3 22.6 5.8
Ксилана 2.9 9.8 4.3
Этерификация как изолированной целлюлозы, так и непосредственно в древесине протекает с более низкими степенями превращения, чем для гемицеллюлоз и лигнина. В смешанных сложных эфирах целлюлозы содержится меньшее количество остатков пропионовой, масляной или валериановой кислот, чем в эфирах холоцеллюлозы и гемицеллюлоз. Высококристалличные микрофибриллы целлюлозы покрыты слоями гемицеллюлоз, поэтому ее ОН-группы стерически менее доступны для больших по объему молекул карбоновых кислот (рис. 1).
Превращения гемицеллюлоз
Из смешанных сложных эфиров древесины выделены ацетаты бутираты 4-О-метилглюкуроноксилана (в дальнейшем по тексту ксилан) и определена степень этерификации его из расчета, что максимальное теоретическое содержание ацетильных групп — 38.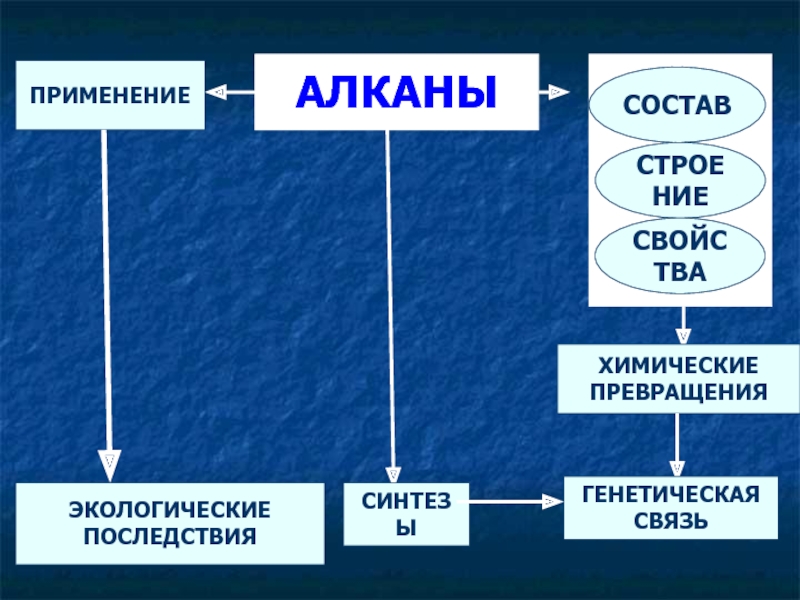 9%, а бутирильных — 52.2%. Степень превращения ксилана при соотношении реагентов 1 : 1 : 1 моль через 8 ч от начала реакции составляет 29, 33, 37% по ацетильным и 8, 11, 12% по бутирильным группам при температурах синтеза 80, 100, 120°С соответственно (рис. 2). Максимальная степень превращения, рассчитанная в целом по ацильным группам, составляет 49% при 120°С.
9%, а бутирильных — 52.2%. Степень превращения ксилана при соотношении реагентов 1 : 1 : 1 моль через 8 ч от начала реакции составляет 29, 33, 37% по ацетильным и 8, 11, 12% по бутирильным группам при температурах синтеза 80, 100, 120°С соответственно (рис. 2). Максимальная степень превращения, рассчитанная в целом по ацильным группам, составляет 49% при 120°С.
Превращения гемицеллюлоз в бензиловые и карбоксиметиловые эфиры оценивали по разности между количеством замещенных и незамещенных моносахаридов, в пересчете на древесину. В образцах древесины, бензилированной в течение 1 ч, обнаружены следы таких незамещенных моносахаридов, как глюкоза, арабиноза, рамноза, галактоза. С увеличением продолжительности бензилирования в продуктах гидролиза найдена только ксилоза.
Степень превращения ксилана в бензиловые эфиры непосредственно в древесине через 6 ч от начала реакции составляет 75, 84, 91% при температурах реакции 90, 100, 110°С соответственно.
На примере бензилирования ксилана, предварительно выделенного из древесины, установлено, что преимущественно образуется 2-О-бензилглюкуроноксилан. Степень бензилирования в пересчете на ксилозу составляет 80 (максимальная — 200), т.е. образуется монозамещенный продукт, что следует из данных ЯМР- и ИК-спектроскопии (индекс симметрии полосы ИК-поглощения валентных колебаний ОН-групп ~1).
Неоднородность замещения в элементарных звеньях макромолекул гемицеллюлоз показана на примерах бензилирования и карбоксиметилирования и подтверждается наличием незамещенных моносахаридов, которые количественно были определены в гидролизатах карбоксиметилированной (табл. 5) и бензилированной древесины. Степень превращения гемицеллюлоз при карбоксиметилировании и бензилировании сравнима и составляет 70-80%.
Рис. 1. Степень превращения целлюлозы (а) в зависимости от продолжительности (т, ч) температуры реакции (°С)
Рис. 2. Степень превращения ксилана (а) в зависимости от продолжительности (т, ч) и температуры реакции (°С)
Превращения лигнина
Лигнины, модифицированные в составе древесины осины, выделены по Комарову из бензил- и карбоксиметил- и по Каллоу из этерифицированных производных. Содержание кислотонерастворимого лигнина: в карбоксиметилдревесине составляет 8-16.6% и зависит от природы растворителя, использованного в синтезе; в бензилдревесине -15-16%. В исходной древесине найдено 22% лигнина по Комарову. В продуктах алкилирования, таким образом, содержится 36-75% лигнина от его количества в исходной древесине. Сложные эфиры лигнинов выделены с выходами 16-18%. Модифицированные в одинаковых условиях лигнины в составе древесины, диоксан-лигнины, лигнины Фрейденберга имеют сходные ИК- и ЯМР -спектры.
При карбоксиметилировании древесины осины в среде пропанола-2 и воды были исследованы превращения лигнина на примере диоксанлигнина (ДЛ):
С9Н6!1О1!62(ОСН3)и8(ОНфен)0,25(ОНперв)0,55(ОНВТОр)0,42(ОНСсюН)0,05, который карбоксиметилировали (40°С, 1 ч), варьируя продолжительность (1-3 ч) и температуру (40, 60, 80°С) щелочной обработки, с увеличением которых возрастают количество карбоксильных групп за счет введенных КМГ и массовая доля углерода, уменьшается массовая доля водорода.
Таблица 5. Содержание незамещенных моноз в древесине осины, карбоксиметилированной при
соотношениях реагентов ОН(древ) : С1СН2СОО№ : №ОН = 1 : 1 : 1
т, мин Глюкоза, % Арабиноза, % Ксилоза, %
0 8.45 5.25 17.50
2 4.79 (5.15)* 5.03 (5.13) 9.13 (16.73)
5 2.30 (3.70) 4.10 (4.62) 8.00 (14.10)
8 2.02 (2.97) 2.83 (3.88) 3.00 (8.64)
10 (2.27) (3.17) (6.15)
Примечание: соотношение реагентов 1 : 1 : 0.5 моль.
Максимальное содержание введенных карбоксиметильных групп (КМГ, %) должно составлять 7.3%, если исходить из количества фенольных ОН-групп (2.1%) в исходном ДЛ. Однако максимальное содержание введенных КМГ составляет 19.7%. Очевидно, что в реакцию карбоксиметилирования вступают не только фенольные, но и некоторые алифатические ОН-группы. Методом фталирования установлено, что количество первичных и вторичных алифатических ОН-групп в
карбоксиметилированном диоксанлигнине меньше, чем в исходном.
Более резкое уменьшение количества вторичных ОН-групп связано с их реакцией с С1СН2СОО№ с образованием карбоксиметилового эфира, так как они проявляют более высокую реакционную способность при О-алкилировании.
При карбоксиметилировании в реакцию в основном вступают фенольные и вторичные алифатические ОН-группы.
В лигнине, находящемся непосредственно в древесине, в реакцию карбоксиметилирования в первую очередь также вступают фенольные и частично вторичные алифатические ОН-группы.
Превращение лигнина в процессе карбоксиметилирования в водно-спиртовой (жидкостный модуль = 13) и водной (жидкостный модуль = 0.3, интенсивное перемешивание) средах было изучено на примере медно-аммиачных лигнинов (лигнин Фрейденберга). Полученные продукты хуже растворяются в воде, чем соответствующие продукты карбоксиметилирования древесины. Сопоставление содержания метоксильных, карбоксильных групп и элементного состава О-алкилированного продукта с теоретическим расчетом по формуле строения выделенных лигнинов Фрейденберга указывает на алкилирование более половины всех ОН-групп.
В бензилированных ДЛ и лигнине, выделенном из БД, через 6 ч от начала реакции содержится 20.9 и 24.8% (110°С) БГ соответственно, что составляет примерно половину от прореагировавших кислых ОН-групп. В продуктах бензилирования древесины и лигнинов, полоса, ответственная за ИК-колебания фенольных ОН-групп в области 1270 см-1 не проявляется. Кроме того, в ЯМР спектрах 13С отсутствует сигнал Саром-ОНфен, а в ПМР-спектрах не фиксируется ОНфен.
Таким образом, обнаружена более высокая способность кислых ОН-групп вступать в реакции О-алкилирования как для лигнинов находящихся непосредственно в древесине, так и для изолированных лигнинов.
Превращения лигнина в процессе этерификации изучены на примере лигнинов Фрейденберга и выделенного из этерифицированной древесины (табл. 6). Данные по накоплению содержания ацильных групп в лигнине (в составе древесины) показывают, что за 8-10 ч лигнин этерифицирован на 75-90%, причем количество введенных ацетильных групп больше, чем бутирильных.
Количество не прореагировавших ОН-групп, по истечении 8-10 ч реакции, становится постоянным и равным количеству фенольных ОН-групп, определяемых хемосорбционным методом. Так, в этерифицированных лигнинах Фрейденберга и выделенных из этерифицированной древесины содержится по 3.0 и 2.4% фенольных ОН-групп, и по 4.3 и 3.4% непрореагировавших ОН-групп соответственно. В образцах лигнина Фрейденберга, ацетилированного в течение различного времени, хемосорбционным способом найдены следующие количества ОНфен: 3.3% (2 ч), 3.2% (4 ч), 2.9% (6 ч), 2.6% (8 ч). В исходном препарате содержится 3.5% фенольных ОН-групп.
Таблица 6. Влияние мольного соотношения реагентов в реакции этерификации на количество связанных кислот в продуктах реакции
Сложный эфир Мольные соотношения реагентов Содержание связанных кислот, %
уксусной масляной
Древесины осины 1 : 1 : 1 44.6 13.2
1 : 3 : 3 43.8 16.2
1 : 10 : 10 39.7 18.9
Лигнина, выделенного 1 : 1 : 1 22.6 5.8
из этерифицированной 1 : 3 : 3 25.7 10.1
древесины 1 : 10 : 10 22.4 13.8
Лигнина Фрейденберга 1 : 1 : 1 19.4 8.3
из древесины осины 1 : 3 : 3 24.8 9.8
1 : 10 : 10 21.7 13.6
Реакционная способность ОН-групп лигнина при этерификации уменьшается в ряду: первичные > вторичные > фенольные, что подтверждено также экспериментальными данными по ацетилированию купроксамлигнина с защищенными ОН-группами. Константа скорости этерификации исходного купроксамлигнина составляет 3.6 мин-1, для лигнина с блокированными ОН первичными (фталированием в бензоле) — 1.5 мин-1, а для лигнина с блокированными ОН алифатическими (фталированием в пиридине) К = 0.9 мин-1.
Химические реакции полиоз и лигнина с участием ОН-групп — кислотно-основные взаимодействия и непосредственно образование эфиров, можно отнести к типу полимераналогичных при условии сохранения высокомолекулярного характера компонентов.
Реакции полиоз и лигнина как полимерных цепей в кислой (при этерификации) и щелочной (при О-алкилировании) средах подразделяются на две группы: реакции фрагментации, способствуют деградации полиоз («пилинг» и статистическая деструкция) и лигнина; реакции конденсации, в основном характерные только для лигнина.
Реакции лигнина как в кислой, так и в щелочной средах сопровождаются образованием хинонметидных структур, которые в дальнейшем подвергаются различным превращениям [13, 14]. Более реакционно-способные фенолят-ионы хинонметидных структур алкилируются с образованием карбоксиметиловых или бензиловых эфиров. Фрагменты макромолекул, с защищенными таким образом фенольными ОН-группами в реакции конденсации или полимеризации не вступают. Таким образом, процессы деструкции преобладают над процессами конденсации. Подтверждением вышесказанному является 100%-ная растворимость бензилированного диоксанлигнина в хлороформе, продуктов карбоксиметилирования — в воде. Одним из показателей, по которому судят о протекании конденсационных процессов в лигнине, является количество протонов, связанных с ароматическим кольцом. В ПМР-спектрах исходного диоксанлигнина отношение интенсивностей сигналов 1Н ароматических колец и алифатических 1Н составляет 1.73. В карбоксиметилированных лигнинах это соотношение изменяется в пределах 1.7-2.0, т.е. конденсация по ароматическим кольцам практически не протекает. Об этом также свидетельствует и светлая окраска продуктов бензилирования и карбоксиметилирования.
Продукты этерификации древесины и лигнина имеют темную окраску, что указывает на протекание процессов конденсации в лигнине. Нами найдено, что в первую очередь в реакцию вступают более реакционно-способные первичные, а затем вторичные ОН-группы. Фенольные ОН-группы этерифицируются незначительно. Это и способствует протеканию конденсационных процессов в лигнине. По результатам элементного анализа этерифицированных лигнина в составе древесины осины и купроксамлигнина установлено, что процесс этерификации в кислой среде сопровождается их некоторой конденсацией. Так, в ПМР-спектрах лигнинов, выделенных из этерифицированной древесины, наблюдается очень низкая интенсивность от сигналов 1H, связанных с ароматическим кольцом, что также свидетельствует о протекании процессов конденсации.
Воздействие щелочных или кислых растворов на полиозы в основном сопровождается процессами статистической деструкции их макромолекул. В промывных водах продуктов модифицирования не обнаружено моносахаридов.
Заключение
Реакционная способность высокомолекулярных компонентов, составляющих древесную матрицу, определяется ее строением. Лигнин и гемицеллюлозы, сосредоточенные большей частью в межклеточном веществе и поверхностных слоях клеточной стенки, образующих лигноуглеводную матрицу, являются наиболее доступными для реагентов в известных процессах химической переработки древесины (процессы делигнификации, гидролиза). При обработке древесины реакционной смесью кислотного или щелочного характеров в найденных нами условиях протекают три параллельных процесса: разрушение структуры клеточной стенки, сопровождающееся освобождением ОН — групп из морфологических и надмолекулярных образований, деструкция макромолекул на более низкомолекулярные фрагменты и непосредственно алкилирование или ацилирование освобождающихся ОН — групп целлюлозы, лигнина, гемицеллюлоз.
Как показано нами в данной работе, О-алкилированию и этерификации по ОН-группам в составе древесины подвергаются все ее основные компоненты: целлюлоза, лигнин, гемицеллюлозы.
Введение новых функциональных групп в макромолекулы целлюлозы, гемицеллюлоз, лигнина при сохранении их относительно высокой молекулярной массы позволяет отнести все исследованные нами процессы к полимераналогичным превращениям. Введение одной и той же функциональной группы в лигнин и полиозы позволяет получать разнообразные полимерные материалы с заданными ценными потребительскими свойствами [І0-І2].
Список литературы
1. Базарнова Н.Г. Химические превращения древесины в реакциях О-алкилирования и этерификации: Дис. … докт. хим. наук. Красноярск. 1 999. 380 c.
2. Kishi H, Shiraishi N. Wood-Phenol Adhesives Prepared from Carboxymethylated Wood. (1 ) // J. Appl. Polymer Sci. 1986. Vol. 32. №1. P. 3189-3209.
3. Honma S., Nakano T. Carboxymethylation of Wood in Organic Solvent-Water Reaction Media // J. Jpn. Wood Res. Soc. 1991. Vol. 37. №7. P. 625-630.
4. Tan X., Yu, Q. Study on Carboxymethylating Modification of Wood and Its Solubility // Chemistry and Industry of Forest Products. 1997. 17. №3. P. 33-39.
5. Honma S.O., Kouichi X.M. Mechanical and thermal properties of benzylated wood // FRI Bull. 1992. V. 176. P. 140146.
6. Cai Hongbin, Yu Quanying Studies on preparation and thermoplasticity of benzylated wood. Linchan Huaxue Yu Gongye // Chemistry and Industry of Forest Products. 1997. Vol. 18. №1. P. 23-29.
7. Hon D. And Chao W.Y. Composites from benzylated wood and polystyrenes: Their Processability and viscoelastic properties // Journal of Applied Polymer Sciense. 1993. Vol. 50. P. 7-11.
8. Hon D. and San Luis J.M. Thermoplasticization of Wood. 11. Cyanoethylation // Journal of Polymer Sciense: Polymer Chemistry Part A. 1989. Vol. 27. P. 4143-4160.
9. Nakano T. Mechanism of thermoplasticity for chemically — modified wood // Holzforschung. 1994. 48. №4. S. 318-324.
10. Карбоксиметилированный лигноуглеводный химический реагент для буровых промывочных жидкостей / Базарнова Н.Г., Галочкин А.И., Маркин В.И., Токарева И.В. и др. / Патент России №2127294 от 10.03.1999 на заявку №97117265/03 от 28.10.97.
11. Лыкасов А.В., Катраков И.Б., Базарнова Н.Г., Галочкин А.И. Изучение процессов глубокой химической переработки растительного сырья. Бензилированная древесина — термопластичное связующее // Известия вузов. Химия и химическая технология. 1997. Т. 40. Вып. 6. С. 96-99.
12. Базарнова Н.Г., Чубик П.С., Хмельницкий А.Г., Галочкин А.И., Маркин В.И. Карбоксиметилированная древесина — химический реагент для приготовления буровых растворов // Журнал прикладной химии. 2001. Т. 74. С. 660-666.
13. Зарубин М.Я. Реакции лигнина при сольволизе растворами кислот и оснований: Дис… докт хим. наук. Л., 1976. 429 c.
14. Резников В.М. Реакционная способность лигнина и его превращения в процессе делигнификации древесины // Химия древесины. 1977. №3. С. 3-23.
Поступило в редакцию 3 марта 2001 г.
|
4 Химические и физические превращения | За пределами молекулярных границ: проблемы химии и химической инженерии
мер, суспензий, композитов), подтвержденные частично механическими измерениями отдельных молекул, будут иметь решающее значение для роста в этой области.
ВЫЗОВЫ И ВОЗМОЖНОСТИ НА БУДУЩЕЕ
Как мы можем получить прямую информацию о молекулярных деталях пути реакции и использовать ее для разработки новых процессов? В то время как фемтосекундная спектроскопия позволила наблюдать реакции в коротком временном масштабе, основной проблемой является разработка сверхбыстрых методов, таких как сверхбыстрая дифракция электронов, которые позволят наблюдать фактическую молекулярную структуру переходного состояния, а не только скорость его изменения. проход.В качестве общей цели мы хотим иметь возможность создавать подвижные картины самих реакций, наблюдая за всеми промежуточными состояниями и скоростью их взаимопревращения. Такие движущиеся картинки могут быть созданы уже сейчас с помощью компьютерного моделирования реакции; проблема в том, чтобы определить, верны ли эти изображения. Таким образом, вторая задача состоит в том, чтобы взаимодействовать с теоретической химией для получения наилучших возможных расчетов, а затем разработать экспериментальную проверку основных теоретических предсказаний, чтобы увидеть, подтверждают ли эксперименты правильность расчетов.
Большинство механистических работ посвящено химическим реакциям в растворе или чрезвычайно простым процессам в газовой фазе. Возрастает интерес к реакциям в твердых телах или на твердых поверхностях, таких как поверхности твердых катализаторов, контактирующих с реагирующими газами. Некоторые такие катализаторы действуют внутри пор определенного размера, например, в порах цеолитов. В этих случаях только определенные молекулы могут проникать в поры, чтобы добраться до реакционной поверхности, и они удерживаются в определенных положениях, когда реагируют.Фактически, процесс превращения метанола в бензин Mobil зависит от реакций, катализируемых цеолитами.
Также растет интерес к реакциям с участием металлоорганических соединений на границе между органической и неорганической химией. Многие такие реакции полезны в синтезе, где металлоорганические реагенты могут иметь важные свойства в качестве катализаторов. Многие детали механизмов реакций в металлоорганической химии пока неясны; понимание этих механизмов позволит разработать улучшенные катализаторы.
Была проделана большая работа, чтобы помочь понять, как ионы металлов реагируют или катализируют реакции в растворе. Многие ферменты также используют связанные ионы металлов для катализирования своих реакций, и все еще необходимо понимать, как они работают. Когда мы действительно разберемся с ними в деталях, мы сможем производить биомиметические катализаторы для полезных производственных процессов.
Когда молекулы реагируют термически, при комнатной температуре или при нагревании, они находятся в низшем электронном состоянии. Однако, когда реакции происходят при облучении молекул видимым или ультрафиолетовым светом, в процессах участвуют частицы, находящиеся в электронных возбужденных состояниях.Некоторые детали таких процессов известны, но многое еще предстоит сделать. Поскольку фотовозбуждение важно во многих областях — фотосинтезе, фотографии, электронных дисплеях, солнечных элементах, вызывающей рак ul-
Химическая трансформация — обзор
7.17.3.1 Принцип
Химическая трансформация, катализируемая ферментом, также дает возможность изучать катализ на уровне одной молекулы. Если это химическое преобразование дает флуоресцентный продукт (т.е.е. флуорогенная реакция), мониторинг флуоресценции продукта может непосредственно исследовать катализ. Этот подход флуорогенной реакции, возможно, наиболее популярен при изучении ферментов на уровне одной молекулы. Сообщалось о двух экспериментальных схемах применения этого подхода для анализа активности одного фермента: один для обнаружения генерации каждой молекулы продукта в режиме реального времени одним ферментом с разрешением одного оборота, 21–23,54–56,65–67 , а другой — для мониторинга накопления всех молекул продукта с течением времени, производимых одним ферментом, заключенным в ограниченный объем. 68–75
Используя схему однооборотного детектирования в реальном времени, Риглер и его коллеги сначала исследовали активность пероксидазы хрена на уровне одной молекулы, 22,54 , которая была дополнительно изучена Энгелькампом и соавторами. 66 Velonia et al., 23 Flomenbom et al., 55 и Carette et al. 62 использовали этот подход для изучения катализа липазы. Xie et al. 21 и Moerner et al. 56 изучил β -галактозидазу, излюбленную систему в исследованиях в области одномолекулярной энзимологии. Хофкенс и его коллеги также использовали это для изучения химотрипсина. 65 Напротив, используя инкапсуляцию в ограниченном объеме, Yeung et al. 68 изучали лактатдегидрогеназу, а Dovichi et al. 69 изучали щелочную фосфатазу путем улавливания отдельных ферментов в капиллярных трубках.Noji и соавторы 70 и Collier и соавторы 75 использовали микрокамеры, сформированные из полидиметилсилоксановых (PDMS) штампов, а Уолт и соавторы 71,72 использовали микрокамеры, сформированные на концах оптических волокон, для улавливания отдельных молекул β -галактозидазы. для анализов активности. Липосомы 74 и эмульсии вода-в-масле 73 также использовали для инкапсулирования индивидуальных ферментов щелочной фосфатазы 74 и химотрипсина 73 для анализа активности с флуорогенными реакциями.
Здесь исследования Се и соавторов 21 и Ноджи с соавторами 70 с использованием подхода флуорогенной реакции используются для иллюстрации этих двух экспериментальных схем, оба из которых изучали β -галактозидазу в качестве модельного фермента.
Химическая трансформация — обзор
2 Что такое механизм в органической химии?
Химики-органики используют термин «механизм» в двух разных смыслах, которые играют разные роли в том, как эти химики понимают химические превращения.Механизм в широком смысле — это, грубо говоря, полная характеристика динамического процесса преобразования набора молекул реагентов в набор молекул продукта. 3 Такая характеристика отслеживает, как непрерывный путь, движения атомных ядер и — в некоторой форме — регистрирует зависящую от времени эволюцию электронов, которая совпадает с ядерными движениями. Следовательно, механизмы в этом широком смысле — это что-то вроде кинофильмов химического превращения. С другой стороны, механизмы в тонком смысле представляют собой дискретные характеристики преобразования как последовательности шагов.Начиная с реагентов (или, по крайней мере, некоторых из них), эти стадии описывают превращение одной важной структуры 4 по пути превращения в следующую важную структуру по пути. Иногда, отслеживая движение электронов стрелками, также предоставляется указание на то, как достигается преобразование между этими важными промежуточными соединениями. Таким образом, механизмы в этом тонком смысле похожи на серию тщательно отобранных и последовательно упорядоченных снимков химического превращения.Эти разные способы представления химического превращения в виде непрерывного процесса или дискретной последовательности шагов вписываются в теоретический аппарат органической химии в разных местах. Толстая концепция механизма реакции лежит в основе теоретических моделей химического превращения, взятых из термодинамики (таких как теория равновесия и спонтанности и теория переходного состояния). Тонкая концепция механизма связывает преобразование с классической структурной теорией органической химии, которая пытается объяснить характеристики химических превращений с точки зрения особенностей структур (или структурных формул) реагирующих частиц.Поскольку понятие механизма имеет эти два разных смысла, но при этом считается изображающим (в любом смысле) один и тот же процесс, оно служит концептуальным мостом, связывающим классическую структурную теорию органической химии с более абстрактными моделями преобразований. .
Когда авторы учебников по органической химии от среднего до продвинутого дают характеристику понятия механизма, они часто начинают с некоторой версии толстой концепции. Гулд в своей классической книге «Механизм и структура в органической химии» описывает механизм реакции как: «гипотетическую картину поведения участвующих атомов.Такая картина, по-видимому, начнется незадолго до того, как реагирующие частицы приблизятся друг к другу, а затем продолжит регистрацию непрерывного пути атомов (и их электронов) во время реакции »[Gould, 1959, p. 127]. Миллер предлагает расплывчатую, но похожую характеристику: «Механизм химической реакции состоит из всего, что происходит, когда исходные материалы реакции превращаются в продукты» [Miller, 2004, p. 1]. Обе эти характеристики предполагают, что механизмы представляют собой или являются отображением непрерывного процесса преобразования между реагентами и продуктами.После введения этого толстого понятия механизма эти авторы сразу же отступают, заявляя, что химики, как правило, не способны предоставить и не нуждаются в таких полных и непрерывных характеристиках механизма. Вместо этого, самое большее, что химики могут установить или к чему они должны апеллировать, — это тонкое, дискретное понятие механизма. 5 Затем учебники переходят к описанию механизмов множества различных химических реакций, причем все в тонком смысле.Учитывая, что именно механизмы в тонком смысле слова занимают центральное место в изложении теории органической химии, стоит задуматься о том, почему толстая концепция механизма продолжает играть важную роль в первоначальных характеристиках механизмов реакции химиками.
Один из очевидных способов объяснить непреходящую важность толстой концепции механизма состоит в том, что она представляет собой регулирующий идеал, к которому стремятся химики, но которого они не могут достичь.Если бы это объяснение было правильным — а это, по общему признанию, то, что часто предлагается в учебниках, — можно было бы ожидать, что можно будет идентифицировать то, что дополнительная информация, теоретически содержащаяся в подробном описании механизма, позволила бы химику-органику объяснить или предсказать или дизайн, который он или она не может сделать с помощью простой тонкой характеристики механизма. Такое прагматическое следствие возможности дать подробное описание механизма придало бы некоторый реальный вес идее о том, что толстые описания — это то, к чему должен стремиться химик-органик.Хотя есть некоторые правдоподобные примеры, когда подробное описание механизма может оказаться важным для понимания (в смысле химиков-органиков) результата химической реакции, 6 обычно не так. Только в исключительных обстоятельствах для химика-органика имело бы практический смысл продолжить исследование механизма реакции после того, как он разработал убедительные аргументы в пользу тонкого описания механизма реакции.Это говорит о том, что, по крайней мере в практическом смысле, причина того, что химики-органики продолжают характеризовать механизмы в широком смысле, не в том, что они каким-то образом являются конечной целью механистических исследований. Вместо этого я думаю, что толстая концепция механизма играет более абстрактную, концептуальную роль, потому что она естественным образом вписывается в теоретические модели, которые химики используют для представления химических превращений.
Самый фундаментальный способ, которым химики-органики представляют химические превращения, — это пути вдоль поверхностей потенциальной энергии.В своей самой богатой версии поверхность потенциальной энергии отображает потенциальную энергию (или иногда свободную энергию) системы взаимодействующих молекул в зависимости от изменений относительного положения составляющих их атомов. Путь на этой поверхности от расположения атомов, соответствующих разделенным реагентам, к расположению атомов, соответствующих разделенным продуктам, будет записывать энергию химической системы, которая претерпевает непрерывное превращение из реагентов в продукты. Изменения положения атомов (и распределения электронов) вдоль пути с наименьшей энергией такого рода примерно соответствовали бы механизму реакции в широком смысле.Механизмы в этом широком смысле, следовательно, переводятся в математическое представление химического превращения в рамках фундаментальной структуры, которую используют химики-органики для размышлений о химических превращениях. Когда химические реакции рассматриваются как пути вдоль поверхности потенциальной энергии, появляется возможность использовать термодинамику и статистическую механику для разработки моделей, которые связывают скорости и распределения продуктов химического превращения, которые являются основными экспериментальными фактами, доступными химикам-органикам, с относительные разности энергии, представленные на поверхности потенциальной энергии.Таким образом, размышляя о механизмах химических реакций в этом широком смысле, химики-органики могут установить взаимосвязь между экспериментальными фактами, которые они измеряют в лаборатории (скорости и распределения продуктов), и абстрактными математическими моделями химических превращений. Наблюдаемые особенности реакций накладывают ограничения на то, какой должна быть поверхность потенциальной энергии, соответствующая превращению, и наоборот. И объяснение, и предсказание результатов химических реакций, и экспериментальное определение механизмов зависят, таким образом, от использования этих взаимных ограничений.
Учитывая, что фундаментальные модели химических реакций рассматривают их как непрерывные превращения, тесно связанные с механизмами в широком смысле слова, может возникнуть недоумение, как химикам-органикам удается обходиться почти исключительно тонкими характеристиками механизмов реакций. В следующем разделе я представлю пример того, как такой механизм развивается и развивается перед лицом дополнительных экспериментальных данных, но можно сказать что-то о том, как это делается заранее.Основная идея состоит в том, что для объяснений и предсказаний, которыми в первую очередь занимаются химики-органики, необходимо знать лишь кое-что об относительных энергиях нескольких выбранных структур на непрерывном пути превращения реагентов в продукты. Пока описание механизма позволяет сделать вывод об этих важных структурах (обычно о переходном состоянии и стабильных промежуточных звеньях), оно будет поддерживать виды выводов, необходимых для предсказания и объяснения.Точно так же виды экспериментальных результатов, к которым обычно обращаются химики для установления механизма реакции, позволяют только сделать какие-то выводы об этих важных моментах на непрерывном пути превращения. Поэтому именно потому, что виды объяснений и предсказаний, произведенные химиками-органиками, требуют только энергетической информации о нескольких избранных структурах на пути трансформации, тонкие характеристики способны играть центральную роль в теории органической химии (см. [ Goodwin, 2003; 2007] для более подробных примеров того, как механизмы используются в такого рода объяснениях).
Учебники по органической химии обычно подчеркивают две вещи при описании (тонких) механизмов, которые фактически будут занимать их в большей части их текстов. Во-первых, механизмы реакции указывают или позволяют сделать вывод о структурах важных промежуточных структур на пути от реагентов к продуктам. Гулд, например, характеризует механизм в тонком смысле как «изображение участвующих видов в один или несколько критических моментов в ходе реакции» [Gould, 1959, p.127]. Это то, чего можно было ожидать, учитывая приведенное выше объяснение того, почему тонких механизмов достаточно для понимания органической химии. Во-вторых, эти механизмы разбивают химическую реакцию на последовательность этапов. Например, Лоури и Ричардсон говорят: «Механизм реакции — это спецификация посредством последовательности элементарных химических стадий подробного процесса, посредством которого происходит химическое изменение» [Lowry and Richardson, 1987, p. 190]. Эти две особенности механизмов связаны, и обе они важны для роли механизмов в понимании химических реакций.
Предоставление информации о важных промежуточных структурах в превращении, таких как переходное состояние или стабильные промежуточные соединения, позволяет химикам-органикам выполнять структурный анализ относительных энергий этих промежуточных продуктов. Структурный анализ, в свою очередь, позволяет предсказывать или объяснять относительные энергетические различия между структурами на основе небольшого набора надежно применимых и легко распознаваемых структурных особенностей. Эти относительные разности энергий затем можно использовать с помощью стандартных теоретических моделей химических переходов для вывода важных эмпирически измеряемых характеристик химических реакций, таких как относительные скорости или распределения продуктов. 7 Таким образом, структурный анализ относительной разницы энергий между важными промежуточными соединениями в ходе химического превращения является современной реализацией цели Бутлерова объяснить все химические свойства веществ на основе их химической структуры. 8 Именно эта особенность механизмов облегчает применение классической структурной теории и ее современных потомков к современному пониманию химических реакций.
Разделение реакции на шаги имеет несколько важных функций.Он разбивает то, что может быть сложным структурным изменением, на последовательность стандартных небольших изменений. Это позволяет во многих случаях идентифицировать или указывать, какое из этих стандартных изменений действует как «узкое место» (или, говоря химическим языком, «этап определения скорости») для развития реакции. Именно структура переходного состояния этого узкого места является наиболее важной для объяснения или предсказания наблюдаемых особенностей химических реакций. Кроме того, такое разложение может сделать очевидным, где альтернативные пути есть, а где нет.Например, реакция, которая протекает через стабильный промежуточный продукт, может быть предметом множества перегруппировок или побочных реакций. Кроме того, поскольку отдельные стадии разложения стандартизированы, они позволяют сделать вывод о структурах важных промежуточных продуктов в конкретной реакции, механизм которой предлагается. Это означает, что разделение реакции на этапы может помочь с первой необходимой характеристикой механизма — позволяя сделать вывод о структурах в «критические моменты» трансформации.Один из способов сделать это — определить, какой из этапов механизма является «узким местом», а затем охарактеризовать этот этап как стандартный. Когда есть общая информация о геометрии переходного состояния этого стандартного типа стадии реакции, эта информация может быть применена к конкретному случаю, чтобы произвести правдоподобные предсказания геометрии соответствующего переходного состояния. Например, если механизм реакции включал стадию согласованного нуклеофильного замещения, то можно было бы правдоподобно сделать вывод, что переходное состояние будет включать приближение нуклеофила и уходящую группу, выходящую с противоположных сторон примерно тригонального плоского центрального атома.Учитывая эту приблизительную геометрию, химик-органик сразу же знает некоторые структурные особенности, которые будут иметь важное влияние на наблюдаемые особенности реакции, такие как — в данном случае — стерические затруднения приближающегося нуклеофила и т. Д. Стандартизованное ступенчатое разложение химического превращения, таким образом, значительно облегчает объяснения и предсказания, которые обычно делают химики-органики. Во многих случаях тонкой характеристики механизма реакции такого рода достаточно, чтобы объяснить все относящиеся к делу экспериментальные факты или провести различие между конкурирующими объяснениями механизма реакции.
Некоторое подтверждение идеи о том, что разложение химической реакции на стандартизованные стадии передает большую часть информации о механизме реакции, которая важна для химиков-органиков, можно найти, рассматривая системы номенклатуры, которые были разработаны химиками-органиками для описания механизмов реакции. Ингольд был источником первой такой системы (см. [Ingold, 1953, главы 7 и 8]), целью которой было различать различные виды реакций замещения и элиминирования.Последующие химики расширили и улучшили исходную систему Ингольда. Текущая система, рекомендованная ИЮПАК (руководящим органом химической номенклатуры), направлена на то, чтобы назвать механизмы в соответствии с «основной валютой молекулярных изменений: образование и разрыв связей» [Guthrie, 1989, p, 25]. Для того чтобы различать механизмы в этих терминах, необходимо передать три характеристики механизма по его названию:
- 1.
Число шагов реакции.
- 2.
Последовательность шагов.
- 3.
Природа этих шагов, включая значительные диффузионные шаги.
[Guthrie, 1989, p, 25]
Стандартные устройства используются для разделения отдельных шагов механизма и записи их порядка (поэтому отдельные шаги разделяются знаком «+» и пишутся слева по верно). Характер шагов передается путем следования серии правил, которые используют ранее существовавшие схемы для классификации реакций и агентов, участвующих в них.Например, стадии классифицируются как замены, добавления, исключения или перегруппировки, а агенты классифицируются как нуклеофилы или электрофилы. Шаг называется, указывая, сколько связей с центральным атомом (ами) образовано и разорвано, и являются ли эти изменения связей нуклеофильными или электрофильными процессами. Электрофильное присоединение к двойной связи с последующим образованием связи между карбокатионом и нуклеофилом будет обозначено: A E + A N .Это название указывает на то, что реакция представляет собой двухэтапный процесс, в котором образуются две связи. Первая связь образуется между одним из стержневых атомов и электрофилом, а следующая связь формируется на отдельном этапе между оставшимся стержневым атомом и нуклеофилом. Конечно, для более сложных реакций должны использоваться дополнительные устройства, но: «даже такие сложные механизмы можно рассматривать как последовательности легко символизируемых компонентных процессов» [Guthrie, 1989, p. 25]. Теперь я представлю пример того, как механизм химической реакции или класс химических реакций развивается на основе экспериментальных данных.
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с вашим системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Преобразование энергии: определение, типы и примеры — научный класс [видео 2021]
Различные типы преобразований энергии
Химическая энергия — это энергия, хранимая в веществе через связи химических соединений. Энергия, хранящаяся в этих химических связях, может высвобождаться и преобразовываться во время любой химической реакции.
Подумайте, когда вы голодны. Когда вы съедаете кусок хлеба, чтобы утолить голод, ваше тело разрушает химические связи хлеба и использует его для снабжения организма энергией.В этом процессе химическая энергия преобразуется в механическую энергию, которую вы используете для движения, и о которой мы поговорим более подробно чуть позже. Он также преобразует его в тепловую энергию , которая создается в процессе метаболизма в вашем теле для выработки тепла. В большинстве случаев химическая энергия выделяется в виде тепла, и это преобразование химической энергии в тепло, или тепловую энергию, называется экзотермической реакцией .
Далее, есть два основных типа механической энергии : кинетическая энергия и потенциальная энергия. Кинетическая энергия — это энергия, связанная с движением объекта. Следовательно, любой движущийся объект обладает кинетической энергией. Точно так же существует два типа потенциальной энергии : гравитационная потенциальная энергия и упругая потенциальная энергия. Гравитационная потенциальная энергия связана с энергией, запасаемой объектом из-за его расположения над землей. Упругая потенциальная энергия — это энергия, запасенная любым объектом, который может растягиваться или сжиматься.Потенциальная энергия может быть преобразована в кинетическую энергию и наоборот.
Например, когда вы совершаете смертельный прыжок с тарзанки с моста, вы выполняете различные преобразования энергии. Во-первых, когда вы готовитесь к прыжку, у вас есть гравитационная потенциальная энергия — эластичный шнур ослаблен, поэтому нет упругой потенциальной энергии. Когда вы прыгаете, вы преобразуете эту потенциальную гравитационную энергию в кинетическую при падении. При этом эластичный шнур начинает растягиваться.По мере того как шнур растягивается, он начинает накапливать упругую потенциальную энергию. Когда шнур полностью вытянут, вы останавливаетесь в самом низу, так что в этот момент у вас есть упругая потенциальная энергия. Затем шнур отбрасывает вас назад, тем самым преобразуя накопленную упругую потенциальную энергию в кинетическую энергию и гравитационную потенциальную энергию. Затем процесс повторяется.
Электрическая энергия — это энергия, переносимая заряженными частицами при их движении вокруг проводника. Прекрасный пример высвобождения электрической энергии — во время грозы.Удар молнии по дереву — это пример преобразования электрической энергии в тепло или тепловую энергию. Дерево нагревается и может даже загореться в результате электрического разряда.
Химическая энергия также может быть преобразована в электрическую. Например, химическая энергия в батарее преобразуется в электрическую. Электрическая энергия, которая включает в себя движение электрических зарядов или токов, может использоваться для питания повседневных устройств, таких как компьютеры и фонарики.
Механическая энергия также может быть преобразована в электрическую. Например, гидроэлектростанция использует механическую энергию проточной воды для выработки электроэнергии. Энергия ветра — это еще одно преобразование механической энергии в электрическую. Механическая энергия ветра преобразуется в электрическую, которая затем может быть преобразована в другие виды энергии.
Наконец, ядерная энергия — это энергия, запасенная в ядре атома.Эта энергия может проявляться двумя разными способами. Во-первых, это процесс деления. При делении ядер нестабильное ядро распадается и при этом выделяет огромное количество энергии. Атомная бомба является примером процесса деления. Короче говоря, энергия, выделяющаяся при разрушении крошечного атомного ядра, может высвободить достаточно энергии, чтобы разрушить один или два города. Энергия ядерного деления может быть преобразована в электрическую, тепловую и механическую энергию.
Другой процесс ядерной энергии на самом деле противоположен делению. Ядерный синтез — это процесс слияния двух разных ядер для создания другого большего ядра. Этот процесс также высвобождает огромное количество энергии. Из двух типов ядерной энергии термоядерный синтез является наиболее желательным из-за отсутствия ядерных отходов. Процессы деления оставляют остаточные эффекты, такие как радиация, а синтез — нет. В настоящее время у нас есть только атомные электростанции деления, но исследования по использованию энергии ядерного синтеза продолжаются.
Существуют и другие вторичные типы энергии, но это всего лишь вариации энергии, описанной выше. Например, лучистая энергия и солнечная энергия являются результатом электрической и ядерной энергии. Солнце выделяет энергию в процессе синтеза, объединяя атомы водорода в атомы гелия. Результатом является высвобождение световой энергии и солнечной энергии, которая также называется электромагнитным излучением . Другой вид энергии — это звуковая энергия. Звуковая энергия — это энергия, переносимая звуковыми волнами.Однако звук должен создаваться механическим или электрическим процессом, поэтому мы можем классифицировать его как механический или электрический тип энергии.
Как видите, большинство видов энергии можно преобразовать в другие виды энергии. Это основная концепция преобразования энергии. Странно то, что тепловая энергия обычно является конечным продуктом преобразования, а не причиной преобразования. Большинство процессов преобразования энергии заканчиваются производством тепловой энергии.При этом одним из основных примеров преобразования тепловой энергии в другой вид энергии является двигатель. Разница температур в двигателе — это то, что позволяет двигателю работать и производить механическую энергию, которая приводит в движение автомобиль. Однако этот процесс также производит тепловую энергию в качестве побочного продукта.
Резюме урока
Принцип сохранения энергии гласит, что энергия не может быть ни разрушена, ни создана. Напротив, энергия преобразуется из одной формы в другую.Многие из этих преобразований энергии могут быть полезны. Например, преобразование механической энергии водопада в электрическую энергию или преобразование ядерной энергии в электрическую для обеспечения энергией города очень полезно. Однако некоторые из них могут быть вредными, например, выброс ядерной энергии для разрушения небольшого города. Но главный вывод из этого урока заключается в том, что для любого типа процесса, который вы можете придумать, вероятно, присутствует трансформация энергии. Попробуйте думать о повседневных процессах и искать в них преобразования энергии.
Результаты обучения
Используйте то, что вы узнали во время этого урока, для достижения следующих целей:
- Укажите принцип энергосбережения
- Перечислите несколько форм энергии, способных к преобразованию
- Обсудить различные типы преобразований энергии
- Приведите примеры полезных или вредных преобразований энергии
(PDF) Химия как наука о превращении веществ
———.2005. Лавуазье и Менделеев о стихиях. Основы химии 7: 31-48.
———. 2006a. Элементы, соединения и другие химические виды. Философия науки 73: 864-875.
———. 2006b. Существенная путаница. Исследования по истории и философии науки 37: 322-336.
———. 2008. Микроструктурализм: проблемы и перспективы. В материале: Природа химических веществ, под редакцией
К. Рутенберг и Дж. Ван Бракель. Вюрцбург: Кенигсхаузен и Нойман.
Гербштейн, Франк Х. 2005. Кристаллические молекулярные комплексы и соединения: структуры и принципы.
Оксфорд: Издательство Оксфордского университета.
Hunger, J. 2006. Как классические модели терпят неудачу. В «Бостонских исследованиях философии науки» под редакцией Д. Бэрда,
Э. Скерри и Л. Макинтайр. Берлин: Springer.
Изуми, Тошико и Донна Г. Блэкмонд. 2009. Правило двойной растворимости выполняется для рацемизирующихся энантиомеров.
Химия. Европейский журнал 15: 3065-3068.
Янич Петр. 1994. Protochemie: Programm einer konstruktiven Chemiebegründung. Общий журнал
Философия науки 22: 71-87.
Джонс, Дж. С. 2008. Приложение: Применение правила фаз к гидратам природного газа. Международный журнал
Машиностроительное образование 36 (2): 182.
Халдояниди, К.А. 2003. Структурные особенности твердых фаз и топология фазовых диаграмм. Журнал
Структурная химия 44: 116-129.
Ким, Джэгвон. 1990. Супервентность как философское понятие. Метафилософия 21: 1-27.
Кьельман, Томас и Ивар Олавссон. 1972. Исследования водородных связей. LVIII. Кристаллические структуры нормального тетрагидрата
и дейтерированной серной кислоты, (H5O2 +) 2SO4- и (D5O2 +) 2SO4
2- Acta Crystallographica
B28: 1692-1697.
Кляйн, Урсула. 2008. Историческая онтология материальных субстанций: c. 1700-1830. In Stuff: The Nature of
Chemical Substances, под редакцией К.Рутенберг и Дж. Ван Бракель. Вюрцбург: Königshausen &
Neumann.
Koningsveld, R., W.H. Штокмайер, Э. Нис. 2001. Фазовые диаграммы полимеров: Учебник. Оксфорд: Oxford
University Press.
Косуге, Кодзи. 1993. Химия нестехиометрических соединений. Оксфорд: Издательство Оксфордского университета.
Крипке, Саул. 1980. Именование и необходимость. Оксфорд: Блэквелл.
Курнаков Н.С. 1914. Verbindung und chemisches Individual. Zeitschrift für anorganische Chemie 88: 109-
127.
Ледимэн, Джеймс и Дон Росс. 2007. Все должно уйти. Оксфорд: Издательство Оксфордского университета.
ЛаПорте, Джозеф. 2004. Естественные виды и концептуальные изменения. Кембридж: Издательство Кембриджского университета.
Ле Пойдевен, Роберт. 2000. Космос и хиральная молекула. In Of Mind and Molecules: New Philosophical
Perspectives in Chemistry, под редакцией Н. Бхушана и С. Розенфельда. Нью-Йорк: Oxford University
Press.
Лен, Жан-Мари. 1995 г.Супрамолекулярная химия: концепции и перспективы. Вайнхайм: ВЧ.
Ли, Дунцин. 1994. Влияние кривизны на правило фаз. Равновесия жидкой фазы 98: 13-34.
Лю, X.R., и S.M. Hong. 2007. Доказательства индуцированного давлением фазового перехода аморфного состояния в аморфное
в двух объемных металлических стеклах на основе лантаноидов. Письма по прикладной физике 90: 251903.
Левдин, Пер-Олов. 1991. О движении ядра и определении молекулярной структуры. Журнал молекулярной структуры
(Теохимия) 230: 13-15.
Ландегаард, Ларс Ф., Гуннар Век, Малкольм И. МакМахон, Серж Дегренье и Поль Лубейр. 2006.
Наблюдение молекулярной решетки O8 в эпсилон-фазе твердого кислорода. Природа 443: 201-204.
Майнцер, Клаус. 1998. Вычислительные и математические модели в химии: эпистемологические основы и новые
перспективы исследований. В Автономии химии: 3-й Эрленмейер-коллоквиум по философии
химии, под редакцией П. Яниха и Н.Псаррос. Вюрцбург: Кенигсхаузен и Нойман.
Mandelcorn, L., ed. 1964. Нестехиометрические соединения. Нью-Йорк и Лондон: Academic Press.
Младек, Бьянка М., Патрик Шарбонно и Даан Френкель. 2007. Сосуществование фаз кластерных кристаллов:
За пределами правила фаз Гиббса. Physical Review Letters 99: 235702.
Нидхэм, Пол. 2002. Открытие, что вода — это h3O. Международные исследования в философии науки
16: 205-226.
———.2006. Теория химических реакций и химических веществ Аристотеля. В «Бостонских исследованиях в философии науки
» под редакцией Д. Бэрда, Э. Скерри и Л. Макинтайра. Берлин: Springer.
———. 2007. Макроскопические смеси. Журнал философии 104: 26-52.
———. 2008a. Вода — это смесь? Преодоление различий между физическими и химическими свойствами. Исследования
по истории и философии науки 39: 66-77.
———. 2008b. Критика концепции воды Крипке / Патнэма.In Stuff: The Nature of Chemical
Substances, под редакцией К. Рутенберга и Дж. Ван Бракеля. Вюрцбург: Кенигсхаузен и Нойман.
———. 2009. Микроэссенциализм: каков аргумент? Ноус: четвертый.
———. далееc. б. Редукция и появление: критика Кима. Философские исследования.
Цифровая трансформация: готовы ли химические предприятия?
Катализатор инноваций
В последние годы возросшая конкуренция, меняющиеся потребности клиентов, развивающаяся нормативно-правовая среда и динамические уравнения затрат серьезно сказались на химических предприятиях, создав все более сложную среду.В результате многие химические предприятия сосредоточены на переосмыслении своих бизнес-моделей и операционных моделей с помощью трансформационных тенденций, исходящих из других отраслей. Поскольку многие глобальные отрасли и секторы охватывают дигитализацию в самых разных областях, от бизнес-процессов до управления взаимоотношениями с клиентами, цифровая трансформация становится важной бизнес-целью, выходящей за рамки простого улучшения сути бизнеса. Глобальная химическая промышленность может выиграть от такой трансформации, которая может стать катализатором для открытия бизнес-инноваций в масштабах всего предприятия.
Настоящая цель цифровых технологий — помочь преобразовать всю организацию путем определения эффективной дорожной карты преобразования бизнеса с использованием цифровых технологий в масштабах всего предприятия, включая:
a) Оценка зрелости с точки зрения бизнес-инноваций и внедрения цифровых (и экспоненциальных технологий)
b) Обеспечение более тесного сотрудничества, внутреннего и внешнего, между организационными функциями
c) Понимание ценности, создаваемой трансформацией бизнеса
И при этом химические предприятия, вероятно, осознают, что цифровые технологии могут служить уникальным катализатором для сплочения всей организации вокруг непрерывных инноваций и создания ценности.Ожидается, что цифровые технологии не только раскроют инновационный потенциал химических предприятий, но и повысят весь спектр акционерной стоимости (рост выручки, операционная маржа, эффективность активов, а также другие сильные стороны компании, такие как устойчивость и безопасность).
Приближаясь к цифровой трансформации
В мировой химической промышленности проводится множество специальных подходов и экспериментов с цифровыми и экспоненциальными технологиями. Тем не менее, многие химические предприятия не уверены в преимуществах, которые может дать цифровая революция, и осторожно относятся к цифровому преобразованию в масштабах всего предприятия.
Вызовы, стоящие перед химическими предприятиями, которые могут ограничить их достижение цифрового превосходства, включают:
- Текущие цифровые обязанности неуместны
- Управление изменениями для облегчения принятия персоналом цифровой повестки дня отсутствует
- Критическая роль кибербезопасности, управления талантами и стратегических союзов не была полностью признана
- В краткосрочной перспективе больше всего ожидаются цифровые возможности в бизнес-операциях, продажах и маркетинге
Тем не менее, значительная часть химических предприятий в глобальном исследовании цифровой химии Deloitte Global 2016 осознает растущую важность цифровых инициатив в повышении их инновационного потенциала, но подавляющее большинство сосредоточено на аспекте данных.Высшее руководство химических предприятий имеет возможность активно развивать цифровую культуру, которая, вероятно, поможет химическим организациям внедрять инновации и, в конечном итоге, обеспечит полную трансформацию, ориентированную на рост бизнеса и операции.
Определены пять факторов, способствующих расширению цифровых инициатив
Следующие рекомендации, основанные на результатах глобального исследования цифровой химии Deloitte Global 2016 и отраслевых наблюдений, могут помочь химическим предприятиям усовершенствовать свои цифровые стратегии:
- Создание надежного процесса трансформации, начиная с четкой стратегии цифрового предприятия
- Обеспечьте масштабируемость цифровых технологий в масштабах всего предприятия за счет разработки устойчивой стратегии, основанной на глубоком понимании, которая создает и укрепляет внутренние возможности
- Создать структурированный подход для выявления рисков в сложных и динамичных экосистемах
- Создание гибких операционных моделей, которые могут задействовать новые приоритетные ресурсы для планирования, выполнения и управления цифровой деятельностью
- Внедряйте непрерывные инновации в культуру, которая поддерживает новые идеи и поощряет обучение
.




 ., ………………………………………….., ………………………………
., ………………………………………….., ……………………………… Это и загрязнение окружающей среды, плохое качество продуктов питания, ухудшение здоровья человека. Только грамотное применение достижений химии приносит пользу человечеству.
Это и загрязнение окружающей среды, плохое качество продуктов питания, ухудшение здоровья человека. Только грамотное применение достижений химии приносит пользу человечеству.
