Содержание
Как добывается соляная кислота? | Минералтрейд
Многим известно, соляная кислота, в промышленности используемая достаточно широко, может иметь природное происхождение. Ее можно встретить в некоторых гейзерах и других местах выхода на поверхность термальных вод. Если говорить отдельно о хлороводороде, то он является частью таких минералов, как бишофит, сильвин и галит.
Что это такое?
- Галит — обыкновенная соль, которую все мы используем в пище. Другими словами — это NaCl.
- Сильвин — хлорид калия. Кристаллы минерала по форме выглядят как кубики.
- Бишофит — хлорид калия, который можно встретить на территории Поволжья.
Узнав больше о реакции этот минералов, можно ответить на вопрос, как получить концентрированную HCl в промышленных масштабах.
Как синтезируют вещество?
- Наиболее востребованная технология производства соляной кислоты в промышленности подразумевает использование хлорида натрия. Она образуется, когда на поваренную соль влияют h3SO4 определенной концентрации.
 Суть такого способа состоит в растворении в воде газообразного хлористого водорода. С его помощью кислота в промышленности добывается еще двумя способами:
Суть такого способа состоит в растворении в воде газообразного хлористого водорода. С его помощью кислота в промышленности добывается еще двумя способами: - Синтетический. Чтобы узнать, как получить концентрированную соляную кислоту, ученые сожгли водород в хлоре.
- Попутный. Здесь применяется хлороводород, получаемый в процессе взаимодействия с органическими веществами. В частности, с углеводами. Абгазный хлороводород формируется в процессе дегидрохлорировании и хлорирования органики. Вещество синтезируется при пиролизе отходов хлорорганики. Пиролизом является процесс разложения углеводородов при фактическом отсутствии кислорода.
Попутное вещество для кислоты может образовываться из неорганических веществ. Например, из хлоридов некоторых металлов. Сильвин используется в процессе изготовления удобрений для повышения урожайности (K). Магний также необходим большинству растений, поэтому остается востребованным и бишофит. Из них производятся как подкормки, так и полноценная соляная кислота.
Абгазная технология производства соляной кислоты — наиболее популярная сегодня. Подобная индустрия используется в 90% случаях при создании реагента.
: Технологии и медиа :: РБК
«Мы начали регистрировать хлороводород в северном и южном полушариях только после начала глобальной пылевой бури, — рассказал член-корреспондент РАН и научный руководитель эксперимента ACS Олег Кораблев. — Скорее всего, он уже был в атмосфере, и его постепенно «разносила» атмосферная циркуляция. Позже, во время спада глобальной бури, мы также наблюдали HCl, в том числе в средних широтах».
После окончания второй пылевой бури концентрация HCl начала постепенно снижаться. В «Роскосмосе» отметили, что появление хлороводорода соответствует прохождению Марсом перигелия — ближайшей к Солнцу точки орбиты.
Читайте на РБК Pro
«Это первый случай регистрации галогенового газа в атмосфере Марса, и он — свидетель совершенно нового химического цикла, который нам предстоит понять», — пояснил профессор Оксфордского университета Кевин Олсен, участвующий в исследованиях.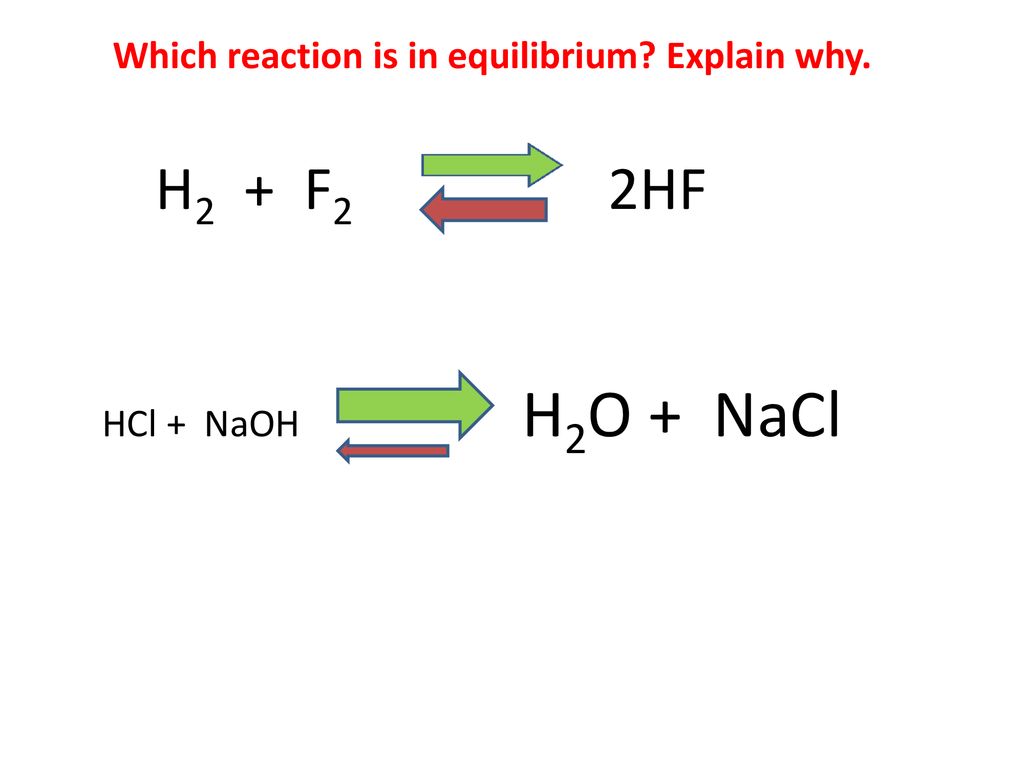
Сейчас ученым предстоит понять, откуда берется хлороводород и куда он исчезает после пылевых бурь. В качестве гипотезы появления вещества выдвигаются вулканические процессы, однако пока что не удалось найти связь между всплесками появления HCl и сейсмоактивностью на Марсе. Кроме того, ученые не исключают, что ответ на вопрос в буквальном смысле «лежит на поверхности» планеты, поскольку хлороводород появляется только в период пылевых бурь.
«Это очень малая примесь, но она помогает исследовать эволюцию атмосферы, как она себя ведет, какими источниками она пользуется. В то же время это очень точно показывает уровень нашей космической техники: Институт космических исследований сделал прекрасный инфракрасный спектрометр, который позволяет очень малые примеси в атмосферах планет определять», — сказал РБК научный сотрудник Астрономического института им. Штернберга Владимир Сурдин.
«Это нестабильный продукт жизнедеятельности, поэтому одна из возможностей — это биогенное происхождение, но это бабушка надвое сказала, надо разбираться, там и метан обнаруживали. Вообще, хлороводород обнаруживается во многих атмосферах планет. Вот недавно была история с атмосферой Венеры — там действительно было серьезное открытие. Есть на Юпитере и Сатурне, и вообще не факт, что он не связан с биогенной деятельностью на Юпитере и Сатурне, потому что там есть места, где комнатная температура и жидкая вода», — сказал РБК доктор физико-математических наук, ведущий научный сотрудник НИИЯФ МГУ Александр Панов.
Вообще, хлороводород обнаруживается во многих атмосферах планет. Вот недавно была история с атмосферой Венеры — там действительно было серьезное открытие. Есть на Юпитере и Сатурне, и вообще не факт, что он не связан с биогенной деятельностью на Юпитере и Сатурне, потому что там есть места, где комнатная температура и жидкая вода», — сказал РБК доктор физико-математических наук, ведущий научный сотрудник НИИЯФ МГУ Александр Панов.
В ноябре прошлого года американские ученые связали пылевые бури с исчезновением воды на Марсе. Они пришли к выводу, что бури буквально выдувают воду с поверхности планеты в верхние слои атмосферы, после чего она уходит в космос.
Ингибированная соляная кислота НАПОР-HCl
ПродукцияИнгибированная соляная кислота НАПОР-HCl
Ингибированная соляная кислота НАПОР-HCl по составу представляет смесь соляной кислоты с массовой долей хлористого водорода 20-24% (синтетической, технической или являющейся полупродуктом химических производств) и ингибитора кислотной коррозии НАПОР КБ. Предназначена для кислотной обработки и подавления сульфатвосстанавливающих бактерий призабойной зоны нефтяных скважин, для травления черных металлов и изделий из них, а также для химической очистки котлов и аппаратов.
Предназначена для кислотной обработки и подавления сульфатвосстанавливающих бактерий призабойной зоны нефтяных скважин, для травления черных металлов и изделий из них, а также для химической очистки котлов и аппаратов.
Ингибированная соляная кислота
Ингибированная соляная кислота – это едкая, негорючая жидкость, растворяющая большинство металлов и оксидов. Однако, к ней устойчив фарфор, керамика, стекло, гранит. Кислота хорошо смешивается с водой, эфиром и бензолом.
Ингибированная соляная кислота способна разлагать любые отложения, в частности и карбонатные, при этом, не оказывая существенных негативных воздействий на металл. Данное свойство возможно благодаря растворенному в кислоте ингибитору.
Способность ингибированной соляной кислоты растворять карбонатные отложения нашла широкое применение в нефтяной промышленности. Ее широко применяют для воздействия на пласты при нефтеразработках. Данная кислота предназначена для кислотной обработки скважин, а также, применяется для подавления сульфатвосстанавливающих бактерий.
Так как пласты, богатые нефтью, зачастую далеки от идеального для начала добычи нефти состояния, одним из важнейших этапов нефтеразработки является подготовительный. От того, насколько качественно он будет завершен, зависит качество нефти и нефтерподуктов, а так же их цена. Слишком грязная нефть, в которой присутствует много примесей, требует качественной очистки, дорогостоящих реагентов. Поэтому, при добыче важно учесть все возможные вложения, связанные с улучшением качеств нефтяных пластов. Одной из распространенных проблем являются коррозии различного типа, которые действуют как на нефтепромысловое оборудование, так и на сам продукт. Для улучшения состояния пород, сложенных из известняка, пород-доломитов, а также, загрязненных карбонатными отложениями, применяют ингибированную соляную кислоту. Она улучшает сообщаемость скважин с пластом, расширяет и очищает трещины и поры в породе от отложений, микроорганизмов.
Кислотная обработка скважин — эффективный метод очистки продуктивного пласта от продуктов загрязнения, попавших или образовавшихся в призабойной зоне в процессе вскрытия бурением, цементажа обсадной колонны или при эксплуатации скважины.
Дебит скважины во многом зависит от проницаемости продуктивного пласта (главным образом его призабойной зоны – ПЗП), которая всегда меняется в процессе заканчивания и эксплуатации скважины. Коллекторские свойства неизбежно ухудшаются вследствие набухания глин, выпадения солей из пластовых вод, образования стойких эмульсий, отложения смол, парафинов и продуктов коррозии в фильтровой части ствола, гидратации пород, размножения сульфатвосстанавливающих бактерий.
Кроме применения в нефтедобывающей отрасли, ингибированная соляная кислота используется для травления и очистки окисленных слоев черных и цветных металлов, а также, для химической очистки от неорганических отложений, накипи котлов или аппаратов.
Преимуществом соляной кислоты ингибированной является то, что она сохраняет антикоррозийную стабильность в течение всего срока хранения. При этом на покрытие цистерн она не действует отрицательно, а также, не влияет на качество нефти и на процесс нефтепереработки.
АО «НАПОР» предлагает соляную ингибированную кислоту НАПОР-HCl для кислотной обработки и подавления сульфатвосстанавливающих бактерий (СВБ) призабойной зоны нефтяных скважин, с целью улучшения сообщаемости пластов и скважин между собой, а также, очистки и расширения пор и трещин. Также, применяют соляную ингибированную кислоту НАПОР-HCl для того, чтобы снять фильтрационное сопротивление коллекторов, которые сложены из карбонатных пород (доломитов и известняков) или загрязненных карбонатными отложениями.
Также, применяют соляную ингибированную кислоту НАПОР-HCl для того, чтобы снять фильтрационное сопротивление коллекторов, которые сложены из карбонатных пород (доломитов и известняков) или загрязненных карбонатными отложениями.
Компания HCL запускает платформу обмена цифровыми услугами — Пресс-релизы
НОИДА, Индия, 25 сентября 2015 г./PRNewswire/ — Компания HCL Technologies (HCL), ведущий глобальный поставщик ИТ-услуг, сегодня объявила о запуске новой платформы обмена цифровыми услугами на основе программного обеспечения ServiceNow. Эта платформа дает предприятиям возможности интеграции услуг и управления услугами (SIAM), позволяя им эффективно запрашивать и получить бизнес-услуги в рамках своих организаций.
На платформе обмена цифровыми услугами осуществляется формирование запросов услуг, например запросов содержимого, от различных подразделений, а также предоставление предприятию, ИТ-специалистам и пользователям стандартного каталога услуг с определенной сервисной утилитой и гарантией, которые затем могут использоваться через различные каналы доступа.
Это предложение сочетает ведущую отраслевую платформу управления услугами ServiceNow с опытом компании HCL в областях разработки корпоративных процессов управления услугами, интеграции процессов и технологий и организационных изменений, обеспечивающих единую среду услуг. Примеры услуг на цифровой платформе обмена: Smart Content-as-a-Service (интеллектуальное содержимое как услуга), Smart Analytics-as-a-Service (интеллектуальная аналитика как услуга), Smart Commerce-as-a-Service (интеллектуальная коммерция как услуга) и Smart Asset Services (интеллектуальные услуги управления активами).
«Большинство организаций перегружены чрезмерным объемом электронной почты и администрирования, и им требуется автоматизация бизнес-процессов, — сказал Том Мур, вице-президент по глобальным поставщикам и интеграторам услуг, компания ServiceNow. — За счет трансформации модели управления услугами компания HCL помогает клиентам избежать путаницы в электронной почте, автоматизировать управление задачами и повысить показатели бизнеса».
«Предприятиям 21-го века потребуется чрезвычайная гибкость для обеспечения лучшей в классе единой среды для своих пользователей. Поэтому предприятиям необходим доступ по запросу к динамически настраиваемому набору интеллектуальных бизнес-услуг, — сказал Калиан Кумар, старший вице-президент и главный технолог — ITO, HCL Technologies. — В платформе обмена цифровыми услугами используется уникальная концепция координации DryIce компании HCL, объединяющая бизнес-услуги, такие как содержимое и аналитика, для предоставления результатов на основе модели «все как услуга» (XaaS)».
«Платформа обмена цифровыми услугами компании HCL обладает настраиваемым и интуитивно понятным, основанным на ролях интерфейсом пользователя с интегрированным масштабированием и гибкостью, которые обеспечивают простоту использования и развертывания для предприятий разных отраслей, — сказал Жако ван Эден, исполнительный вице-президент и глобальный руководитель подразделения по вопросам, выходящим за рамки цифрового бизнеса, HCL Technologies.
Сегодня более 100 клиентов по всему миру пользуются предложениями компании HCL на платформе ServiceNow, и сертифицированные компанией HCL профессионалы по платформе ServiceNow управляют с ее помощью более чем миллионом активов.
http://www.hcltech.com/press-releases/it-infrastructure-management/hcl-launches-digital-service-exchange-platform
Кунал Такалкар (Kunal Takalkar)
Отдел корпоративных связей
[email protected]
+91 981077 3217
Источник: HCL Technologies Ltd
Динамическое освещение Human centric lighting | Биологическое и эмоционально-эффективное освещение
Что такое Human Centric Lighting?
Human Centric Lighting (с англ. «освещение, ориентированное на человека») – это концепция в организации автоматизированного динамического освещения помещений, согласно которой работа искусственных источников света строится с учетом воздействия на активность, самочувствие и настроение человека.
Компания «Световые Технологии» является разработчиком уникального на отечественном рынке решения по организации динамического освещения согласно концепции Human Centric Lighting — светодиодных светильников серии Color Fusion (CH CF). Эта система освещения позволяет воздействовать на человека, подстраиваясь под его биологические ритмы с помощью изменения цветовой температуры (Тцв).
Влияние биоритмов на активность и настроение человека
В течение дня мы ощущаем различные периоды активности, что во многом обусловлено воздействием света на наш организм. Так, например, при дневном свете человек более активен, чем при искусственном освещении. А в яркий солнечный день мы чувствуем себя лучше, нежели чем в плохую погоду. Наш организм реагирует на изменение света, его цвета, количества, времени дня, сезона и погодных условий.
Как динамическое биоосвещение может воздействовать на организм человека в течение дня
Взаимосвязь цветовой температуры света и суточных ритмов привела к идее о том, что можно оказывать существенное влияние на периоды активности человека с помощью искусственного динамического освещения путем вариации цветовой температуры в течение рабочего дня. Так родилась концепция под названием Сircadian Lighting.
Так родилась концепция под названием Сircadian Lighting.
Смысл концепции биоосвещения сводится к тому что активность человека значительно увеличивается при Тцв = 4000-6000 К и снижается при Тцв = 2700-3500 К. Работать в течение всего дня при высоких цветовых температурах (Тцв ~ 6000 К) – вредно, поскольку уровень вырабатываемого мелатонина может не достичь нормального показателя, что собьет суточный ритм и может привести к перенапряжению, бессоннице. При низких цветовых температурах может произойти обратное, и человек рано почувствует усталость, не будет продуктивен на работе и т.д. Решением проблемы ориентированного на человека освещения стало создание систем с источниками света, цветовая температура в которых может меняться по заранее заданному сценарию или с помощью непосредственного управления человеком.
Система управления освещение HCL от компании «Световые Технологии»
Работа систему управления реализована на последней редакции протокола DALI стандарта EN62386 Part 209 в плане управления цветовой температурой DALI Device Type 8 (DALI DT8). Это позволяет нам предлагать удобные в эксплуатации и внедрении полнофункциональные автоматизированные системы управления светильниками с изменяемой цветовой температурой.
Это позволяет нам предлагать удобные в эксплуатации и внедрении полнофункциональные автоматизированные системы управления светильниками с изменяемой цветовой температурой.
По вопросам подбора оборудования HCL вы можете воспользоваться нашим бесплатным сервисом
Области применения систем Human Centric Lighting
Светильники модификации CH CF с поддержкой автоматизированного изменения цветовой температуры, приближенной к дневному солнечному циклу, находит свое применение на объектах:
-
Офисные, бизнес центры
-
VIP кабинеты
-
Переговорные
-
Подземные сооружения без доступа естественно солнечного света
-
Различные объекты северных регионов страны
-
Учебные и медицинские учреждения
-
Прочие объекты, где создается среда с акцентом на продуктивность и комфорт человека
Умный свет или биодинамическое освещение.
 Что такое технология HCL?
Что такое технология HCL?
Мы проводим примерно 70% времени в закрытых пространствах с недостаточным количеством дневного света. И более половины от этого времени мы проводим на работе, подвергая свое зрение нагрузкам при недостаточном искусственном свете.Что с течением времени приводит к потере концентрации, переутомлению, мигрени, бессоннице и проблемам со зрением.
Современные технологии помогли справится с такими недостатками искусственного света как неравномерное или избыточное освещение и пульсация. Но технологии не стоят на месте, как и потребности человека, поэтому на рынке начали появляться автоматизированные системы управления светом HCL, которая помогла не только сделать свет комфортным для глаз человека, но и решить ряд таких проблем как: снижение нагрузки на сеть и оборудование, что позволило повысить энергоэффективность систем и снизить расходы на электроэнергию.
Научное обоснование
В основе системы управления светом HCL лежит концепция Circadian Lighting. Суть концепции заключается в том, чтобы с помощью искусственного динамического освещения, изменяя цветовую температуру в течении дня оказать влияние на периоды активности человека.
Суть концепции заключается в том, чтобы с помощью искусственного динамического освещения, изменяя цветовую температуру в течении дня оказать влияние на периоды активности человека.
К примеру, активность человека увеличивается при свете с цветовой температурой 4000-6000 K и снижается при 2700-3500 K. Длительное освещение светом с температурой 6000 K может вызвать у сотрудника перенапряжение и бессонницу. Низкие же цветовые температуры наоборот могут оказать негативное воздействие: человек будет малоэффективен и быстро почувствует усталость.
Идеальным для человека будет то освещение, которое копирует дневной свет местности постоянного проживания. Поэтому главной задачей HCL является искусственное дневное освещение, которое выстраивает управление цветовой температурой согласно движению солнца в определенной местности.
Human Centric Lighting (HCL)
Современное биодинамическое освещение — это комплекс источников света, управляемых с помощью обучаемого искусственного интеллекта. Такой симбиоз позволяет создать комфортные условия для работы и отдыха человека, меняя в течении дня цвет и яркость освещения, снизить утомляемость глаз и повысить работоспособность.
Такой симбиоз позволяет создать комфортные условия для работы и отдыха человека, меняя в течении дня цвет и яркость освещения, снизить утомляемость глаз и повысить работоспособность.
Наши новые светильники системы HCL созданы на базе обычных офисных светильников типа Armstrong и Грильято. В этих светильниках установлены несколько светодиодных модулей с разными цветовыми температурами. Дополнительно, с помощью двух драйверов регулируется интенсивность излучения каждого модуля.
Такое решение было установлено и в линейку наших офисных светильников “Панель” с интегрированным бактерицидным УФ-очистителем воздуха. Что достаточно актуально во время пандемии и позволяет полностью автоматизировать процесс эффективной очистки воздуха от вирусов и бактерий.
Вся система управления светильниками осуществляется по протоколу DALI, с помощью контроллера и одного двухканального драйвера. Выбор запрограммированного сценария производится или с помощью ПДУ (телефона, планшета, ПК) или можно настроить режим работы светильника вручную.
Основные преимущества HCL перед обычными, галогенными или другими источниками света
-
Глаза в течении рабочего дня не устают за счет света приближенного к дневному. Сотрудник чувствует себя комфортнее и становится более продуктивен. -
Широкий спектр использования: от офисных и производственных помещений до домашних условий. Иными словами используется в тех условиях, где создается среда нацеленная на продуктивность и комфортные условия труда и отдыха человека. -
Автоматизированный выбор цветовой температуры и интенсивности освещения в зависимости от времени суток и года. -
Экономия электроэнергии. Так как в качестве источников света используются высококачественные светодиоды, способные менять температуру света, то это позволяет обеспечить экономию электроэнергии до 75% в сравнении с традиционным освещением. Также снижается нагрузка на электросеть и оборудование, тем самым повышается энергоэффективность и снижаются затраты на электроэнергию.
Также снижается нагрузка на электросеть и оборудование, тем самым повышается энергоэффективность и снижаются затраты на электроэнергию.
-
Простой монтаж. В зависимости от пожеланий заказчика можно установить один светильник, а можно создать целый единый комплекс из множества источников света. Дополнительно, стоит отметить возможность интеграции такого оборудования в систему “умный дом”.
Применение технологии Human Centric Lighting (HCL)
Освещение торговых помещений
В торговле освещение должно создавать комфортные условия для покупателей и помогать продавать товар. Уже научно доказано, что значение цветовой температуры в продажах очень велико и имеет ряд нюансов, которые нужно учитывать при составлении проекта по освещению торговых площадей. К примеру, освещение светом.
2500-3200 K придаст свежести овощам и фруктам, а теплые тона сделают придадут сырам и выпечке насыщенный желтый оттенок. В ювелирных салонах изделия из платины, серебра и золота наиболее выигрышно смотрятся при цветовой температуре 4000 K и интенсивности излучения 1000 лк и даже выше. И в тоже время драгоценные камни в этом случае смотрятся тускло. Поэтому в ювелирных магазинах применяется система из общего света интенсивностью не более 500-750 лк и акцентных светильников, благодаря которым драгоценные камни начинают сиять и привлекать к себе внимание.
В ювелирных салонах изделия из платины, серебра и золота наиболее выигрышно смотрятся при цветовой температуре 4000 K и интенсивности излучения 1000 лк и даже выше. И в тоже время драгоценные камни в этом случае смотрятся тускло. Поэтому в ювелирных магазинах применяется система из общего света интенсивностью не более 500-750 лк и акцентных светильников, благодаря которым драгоценные камни начинают сиять и привлекать к себе внимание.
Офисное освещение
Это основное направление в применении HCL, которое направлено на создание комфортных условий труда человека, снижению утомляемости и усталости глаз и повышению рабочей эффективности за счет воспроизведения циркадного ритма, к которому человек привык. Так как наши светильники изготовлены по форм-фактору классических офисных светильников типа Армстронг и Грильято, то монтаж не составит никакого труда и не потребует дополнительных расходов. А в будущем позволит сократить расходы на электроэнергию и нагрузку на электросеть.
Стоит отметить также нашу актуальную в нынешнее время линейку светильников типа Армстронг, но с интегрированным рециркулятором. Помимо автоматизации интенсивности освещения и смены цветовой температуры в течении дня, этот тип светильников будет очищать воздух от вирусов и бактерий, периодически включаясь на 1 час в 2 часа в течении рабочего времени и перед началом рабочего дня.
Освещение для животноводства и птицефабрик
Ранее мы писали о том какую важную роль играет правильно подобранная цветовая температура и интенсивность на удой, рост и яйценоскость популяции животных и птиц. Циркадный ритм имеет большое значение не только для человека, но и для животных. И очень важно, чтобы в этом ритме были постепенные переходы от одной цветовой температуры к другой, так называемые искусственные закаты и рассветы. Плавный переход снизит риск стрессового состояния у животных. Использование систем HLC в агропромышленности может полностью заменить естественный световой день, что очень актуально в областях, где световой день ввиду погодных и географических условий короткий.
Перечень нашей продукции, которая адаптирована под технологию HCL
Остались вопросы?
Узнать подробности или получить подробную консультацию по нашим светильникам и технологии HCL вы можете позвонив по телефону:
8 800 550-10-78
8 812 309-16-08
Правила подготовки к сдачи анализа крови на иммунологические исследования
Перед сдачей иммунологических тестов необходмо подготовить себя к этому исследованию следующим образом: воздержаться от физических нагрузок, приема лекарств и алкоголя, изменений в питании в течение 24 часов до взятия крови. Накануне исследования исключить психологические и другие виды стрессов. Вам не следует принимать пищу после ужина, лечь спать нужно накануне в обычное для Вас время и встать не позднее чем за час до взятия крови. Утром после подьема воздержитесь от курения. Если вы испытываете трудности с отменой лекарств, то обязательно сообщите об этом лечащему врачу.
Если вы испытываете трудности с отменой лекарств, то обязательно сообщите об этом лечащему врачу.
Очень важно, чтобы Вы точно следовали указанным рекомендациям, так как только в этом случае будут получены ценные результаты исследования крови или другого биологического материала.
Иммунологическое исследование суточной мочи на метанефрин, норметанефрин, свободный кортизол.
Вы должны подготовить себя к этому исследованию следующим образом: накануне сбора суточной мочи исключить из пищи шоколад, кофе, бананы, ананасы, сыр, цитрусовые, крепкий чай, свеклу. Если возможно, то прекратить за неделю до сбора мочи прием всех лекарственных препаратов. Исключите прием алкоголя. Сбор мочи осуществляйте до проведения рентгенологических исследований, выполнения физиотерапевтических процедур, хирургических вмешательств, обследований и инфузий.
В лаборатории получают консервант — 10 мл. 6N HCL. Мочу собирайте в широкогорлый сосуд с консервантом (HCL— это соляная кислота, обращайтесь с раствором очень аккуратно, не допускайте попадания кислоты на кожу или одежду). Во время сбора мочу охлаждайте до 4-8ºС. Измерте объем суточной мочи и сообщите в лабораторию (очень важно как можно точнее измерить объем, это влияет на результат исследования!). В лабораторию принесите небольшое количество мочи (5 мл.), предварительно перемешав ее.
Во время сбора мочу охлаждайте до 4-8ºС. Измерте объем суточной мочи и сообщите в лабораторию (очень важно как можно точнее измерить объем, это влияет на результат исследования!). В лабораторию принесите небольшое количество мочи (5 мл.), предварительно перемешав ее.
Очень важно, чтобы Вы точно следовали указанным рекомендациям, так как только в этом случае будут получены ценные результаты исследования суточной мочи.
Иммунологические исследования гормонов: ЛГ, ФСГ, Тs.
Гонадотропины гипофиза лютеинизирующий гормон — ЛГ, фолликулостимулирующий гормон – ФСГ и основной андроген тестостерон – Тs имеют эпизодическую природу секреции. Для получения надежных результатов необходимо определение этих гормонов в смешанных пробах крови. Для этого забор крови у Вас будет производен трижды с интервалом 20 минут (т.е.Вам необходим 1 час времени!). В пуле проб исследуют уровень ЛГ, ФСГ, Тs.
Иммунологическое исследование — CrossLaps мочи (маркер резорбции кости).

Вам необходимо собрать вторую порцию утренней мочи (5 мл.) и принести в лабораторию. Таже в этой порции мочи необходимо определить уровень креатинина (биохимическая лаборатория).
Иммунологическое исследование — определение альдостерона в крови.
Для получения надежных результатов Вам необходимо за 2 недели до исследования исключить безсолевую диету (если таковая соблюдалась ранее). Исследование не должно производиться во время острых заболеваний, т. к. уровень альдостерона может падать. Лечащий врач должен решить вопрос об отмене перед исследованием лекарственных препаратов, которые могут повлиять на результат исследования (мочегонные, α- и β-адреноблокаторы). Забор крови производится сидя, при этом Вы должны находиться в этом положении не менее 2 часов (т.е. Вам необходимо 2 часа времени!).
Иммунологическое исследование — определение адренокортикотропного гормона (АКТГ) и кортизола (кровь).

Накануне исследования Вам необходимо исключить физические нагрузки (в т.ч. спортивные тренировки) и прием алкоголя. В течение часа перед сдачей крови предпочтительно воздержаться от курения. Сдавать кровь на исследование необходимо
до 9-00 часов утра, если нет особых указаний Вашего лечащего врача.
Иммунологическое исследование — определение ренина.
За 2 недели до исследования, по согласованию с лечащим врачом, Вам следует отменить прием препаратов, которые могут повлиять на результаты исследований (диуретики, гипотензивные препараты, оральные контрацептивы, препараты солодки). Забор крови производится стоя, при этом Вы должны находиться в положении стоя не менее 1 часа (т.е. Вам необходим 1 час времени!).
Соляная кислота
2
Соляная кислота повышает активность катализатора
25 августа 2020 г. — Исследовательская группа разработала процесс синтеза, который резко увеличивает активность катализаторов обессеривания сырой нефти. Возможно, новый процесс можно было бы использовать и для катализаторов …
— Исследовательская группа разработала процесс синтеза, который резко увеличивает активность катализаторов обессеривания сырой нефти. Возможно, новый процесс можно было бы использовать и для катализаторов …
Секреты жуткой фотографической техники
Октябрь30, 2019 — В 1960-х годах французский художник по имени Жан-Пьер Судр начал экспериментировать с малоизвестным фотографическим процессом XIX века, создавая драматические черно-белые фотографии с неземной вуалью …
Расшифровка механизма: как органические кислоты образуются в атмосфере
12 мая 2021 года — кислотность атмосферы все больше определяется углекислым газом и органическими кислотами, такими как муравьиная кислота. Второе из них влияет на рост облаков и pH дождевой воды.Но химический …
Включение и выключение цвета пористого материала с помощью кислоты
8 февраля 2019 г. — Стабильный, меняющий цвет состав демонстрирует потенциал для электроники, датчиков и газа . ..
..
«Терминаторский» жидкий металл движется и растягивается в трехмерном пространстве
20 марта 2019 г. — Во франшизе блокбастера «Терминатор» злой робот трансформируется в различные человеческие формы и объекты и просачивается сквозь узкие отверстия благодаря своему «жидкому металлу»…
Пористые материалы проливают свет на очистку окружающей среды
5 июля 2018 г. — Ученые разработали стабильные монокристаллические пористые органические каркасы с водородными связями, которые термически и химически стойкие, обладают большой площадью поверхности и флуоресцентными свойствами. …
LED-Ing the Way: чистый и удобный метод окисления пластиковых поверхностей для промышленности
11 июня 2019 г. — Исследовательская группа использовала диоксид хлора для окисления полипропилена.Под действием светодиодного излучения радикалы ClO2 * атакуют метильные группы полипропилена, превращая их в карбоновую кислоту. C-H …
Предотвращение разрушения бетонных мостов
19 декабря 2018 г. — В новом исследовании изучается неблагоприятное воздействие адсорбции компонентов природного газа, обнаруженных в нашей окружающей среде, и смесей нескольких таких газов одним из материалов, из которых состоит …
— В новом исследовании изучается неблагоприятное воздействие адсорбции компонентов природного газа, обнаруженных в нашей окружающей среде, и смесей нескольких таких газов одним из материалов, из которых состоит …
Доставка грузов полимерами
Янв.22 февраля 2021 г. — Разлагаемые полимеры на биологической основе предлагают варианты химической переработки и могут быть инструментом для хранения и высвобождения полезных молекул. Ученые разработали класс полимеров на основе сахара, которые …
Реактор
превращает парниковый газ в чистое жидкое топливо
3 сентября 2019 г. — Реактор электрокатализа, построенный в Университете Райса, перерабатывает диоксид углерода для производства чистых растворов жидкого топлива с использованием электричества. Ученые, стоящие за изобретением, надеются, что оно станет…
Хлороводород
Хлороводород — это газ при комнатной температуре. Растворы хлористого водорода в воде известны как соляная кислота. Хлористый водород широко используется в химической промышленности в качестве реагента при производстве других химикатов. Большая его часть образуется как побочный продукт реакций с участием хлора.
Хлористый водород широко используется в химической промышленности в качестве реагента при производстве других химикатов. Большая его часть образуется как побочный продукт реакций с участием хлора.
Использование хлористого водорода
Хлористый водород используется в различных областях химической промышленности:
№
- при производстве 1,2-дихлорэтана (этилендихлорид) и хлорэтилена (винилхлорида), используемых, в свою очередь, для производства поли (хлорэтилена) (ПВХ).
- в производстве фторуглеродов (например, тетрафторэтена, мономера для поли (тетрафторэтилена).
- в производстве хлора. По сути, это рециркуляция, поскольку большая часть хлористого водорода образуется в качестве побочного продукта, когда хлор вступает в реакцию с реагентом, например, при производстве хлорэтилена (винилхлорида) с образованием ПВХ. Кислота, превышающая потребность (см. Ниже), может быть подвергнута электролизу с образованием водорода и хлора. Особым достижением этого электролиза, который используется компанией Bayer в Китае, является процесс ODC (катод, истощающий кислород).
- для очистки поверхности стали («травление»), поскольку она оставляет поверхность стали в лучшем состоянии для дальнейшей обработки, такой как покрытие и гальваника. Другие кислоты иногда используются для травления нержавеющей стали.
- при производстве титана и магния.
- для регенерации ионообменных смол.
- для производства неорганических хлоридов (например, хлорида алюминия).
- для регулирования pH в самых разных производственных процессах, включая производство питьевой воды и пищевых продуктов.
- при производстве некоторых красителей.
Производство хлористого водорода
Подавляющее большинство хлористого водорода / соляной кислоты образуется как побочный продукт. В США, например, хлористый водород / соляная кислота в качестве побочного продукта составляет около 90% от общего объема производства, большая часть этого приходится на производство хлорэтилена через 1,2-дихлорэтан для производства поли (хлорэтен), ПВХ. Затем он используется для производства большего количества 1,2-дихлорэтана и, таким образом, недоступен для других процессов.
Затем он используется для производства большего количества 1,2-дихлорэтана и, таким образом, недоступен для других процессов.
При производстве магния электролизом хлорида магния также производится кислота, но ее снова рециркулируют.
Среди других процессов, которые производят хлористый водород / соляную кислоту, — хлорирование углеводородов, например хлорирование метана с образованием хлорметана, этана в хлорэтан и бензола в хлорбензол.
Другие процессы производства хлористого водорода / соляной кислоты включают производство изоцианатов, используемых для производства полиуретанов и фторуглеродов.
Некоторые заводы, на которых вырабатывается хлористый водород / соляная кислота, были построены рядом с заводами, которые используют эту кислоту. Например, хлористый водород / хлористоводородная кислота, полученные при производстве изоцианатов, затем направляются по трубопроводу на завод по производству ПВХ для производства 1,2-дихлорэтана.
Кислота также производится при производстве сульфата калия (используется в качестве специального удобрения, например, для цитрусовых и винограда) из хлорида калия и серной кислоты.
Небольшое количество кислоты образуется при сжигании хлора в водороде. Оба реагента получают в результате электролиза водных растворов хлорида натрия (рассола). Реагенты нагревают вместе. Реакция является сильно экзотермической, и большое внимание уделяется контролю реакции, главным образом, за счет управления расходами двух газов.
И водород, и хлор очень чистые, если их получить электролизом рассола. Образующийся хлористый водород используется либо в виде газа, либо поглощается водой в специальных сосудах, обычно сделанных из графита.Он хранится в виде концентрированного раствора (около 30% HCl) и является самой чистой производимой соляной кислотой.
Дата последнего изменения: 15 февраля 2017 г.
соляная кислота — полное руководство
Определение
Соляная кислота — это коррозионно-активная кислота, образующаяся при растворении хлористого водорода (HCl) в воде, поэтому она представляет собой водный раствор галогенида водорода. Соляная кислота используется в различных отраслях промышленности в качестве очищающего, травильного или регулирующего pH раствора, а также в разбавленной форме содержится в желудочном соке.Хлористый водород иногда называют соляной кислотой, хлоридом гидроксония, хлораном, уайт-спиритом или солевым кислотным раствором.
Соляная кислота используется в различных отраслях промышленности в качестве очищающего, травильного или регулирующего pH раствора, а также в разбавленной форме содержится в желудочном соке.Хлористый водород иногда называют соляной кислотой, хлоридом гидроксония, хлораном, уайт-спиритом или солевым кислотным раствором.
соляная кислота (HCl)
Соляная кислота использует
Соляная кислота имеет диапазон применения от физиологического до промышленного. В промышленности сильные коррозионные свойства HCl и то, что она является простейшей кислотой на основе хлора, делают ее дешевым и эффективным, хотя и опасным и разрушительным соединением. Водный раствор должен находиться под давлением или охлаждаться. , иначе он превратится в ядовитый газ, если компоненты воды испарятся и составят менее 60% от общего раствора.Хотя полный список использования соляной кислоты занял бы много страниц, наиболее распространенные применения обсуждаются более подробно ниже.
В промышленности
Промышленная соляная кислота используется в самых разных секторах. Это важный ингредиент в готовых промышленных товарах, таких как поливинилкарбонат (ПВХ), бисфенол А (BPA) и этилендихлорид (EDC). BPA используется в производстве поликарбонатных пластиков и эпоксидных смол, но он опасен для здоровья из-за канцерогенных эффектов.По этой причине многие пластмассы в настоящее время производятся и рекламируются как продукты, не содержащие бисфенол А. Все эти органические соединения используются в производстве пластмасс и в качестве лабораторных растворителей, но могут быть очень канцерогенными.
Подготовка металла к дальнейшему производству включает один из двух аналогичных процессов: травление и пассивацию. В то время как пассивация обеспечивает более легкий эффект, с использованием слабокоррозионных кислот для удаления примесей, оставшихся во время производства металла, защиты металла от загрязняющих веществ, сглаживания поверхности и повышения долговечности, травление приводит к более сильному эффекту за счет использования сильной кислоты. Эта кислота обычно хлористый водород. Металлы, обработанные в ваннах с хлористым водородом, называются металлами, протравленными HCl.
Эта кислота обычно хлористый водород. Металлы, обработанные в ваннах с хлористым водородом, называются металлами, протравленными HCl.
Соляная кислота часто используется на одной стадии обработки кожи на кожевенных заводах. Дубление кож включает введение соли хрома, чтобы изменить сеть коллагена внутри и избежать окрашивания в будущем. Во время этого процесса в ванну добавляют соли хрома с pH от 2,5 до 3 вместе с хлоридом натрия. Это этап травления. Затем хром прикрепляется к шкуре, что увеличивает pH и так называемую стадию подщелачивания.Для достижения низкого pH стадии травления необходим хлористый водород.
Еще одним применением хлористого водорода в промышленности является производство неорганических соединений, таких как полиалюминийхлорид (PAC), хлорид железа (III) (трихлорид железа) и хлоргидрат алюминия. Использование хлористого водорода необходимо в начале производственных процессов этих соединений, например, добавление 20% HCl и серной кислоты в бокситы для производства ПАУ. Соли алюминия используются в косметической промышленности (например, в дезодорантах-антиперспирантах) или на этапах химической коагуляции и флокуляции питьевой воды и очистки сточных вод, где добавленные катионы алюминия (или железа) нейтрализуют заряд коллоидных частиц загрязняющих веществ и позволяют им соединяться с образованием хлопья (флокуляция) их можно удалить с помощью сифона.
Соли алюминия используются в косметической промышленности (например, в дезодорантах-антиперспирантах) или на этапах химической коагуляции и флокуляции питьевой воды и очистки сточных вод, где добавленные катионы алюминия (или железа) нейтрализуют заряд коллоидных частиц загрязняющих веществ и позволяют им соединяться с образованием хлопья (флокуляция) их можно удалить с помощью сифона.
HCl также используется для «очистки» соли, используемой в производстве продуктов питания и на наших столах. В насыщенном растворе NaCl присутствует постоянное равновесие между отдельными положительными ионами натрия и отрицательными ионами хлора и неионизированным NaCl. Пропуская через этот раствор газообразный HCl, он диссоциирует с образованием ионов H + и Cl-. Поскольку ион хлорида является общим как для хлорида натрия, так и для хлористого водорода, его концентрация увеличивается и создает сдвиг в соответствии с принципом Ле Шателье. Это означает, что доступных иона натрия с большей вероятностью будут связываться со свободно доступным хлоридом с повышенными отложениями NaCl в результате . Этот процесс называется очисткой солей. В качестве альтернативы вы можете добавить соляную кислоту к гидроксиду натрия (NaOH) или карбонату натрия (Na 2 Co 3 ), и обе реакции будут образовывать соль хлорида натрия.
Этот процесс называется очисткой солей. В качестве альтернативы вы можете добавить соляную кислоту к гидроксиду натрия (NaOH) или карбонату натрия (Na 2 Co 3 ), и обе реакции будут образовывать соль хлорида натрия.
Естественно, сильная кислота, такая как хлористый водород, также используется для регулирования кислотности широкого спектра растворов, используемых в фармацевтических продуктах, в пищевых добавках, включая фруктозу, лимонную кислоту и гидролизованный растительный белок, в щелочных отходах и в наших продуктах. питьевая вода.
Соляная кислота также используется для увеличения добычи нефти из нефтяных скважин. При закачке в базовую породу образуются более крупные поры, которые могут транспортировать больше нефти в скважину. Это лишь некоторые из наиболее распространенных применений соляной кислоты в промышленности.
В доме
Использование хлористоводородной кислоты в домашних условиях ограничено более низкими концентрациями, которые менее агрессивны, но все же демонстрируют превосходные характеристики очистки и регулирования pH. Те, у кого есть бассейны, могут попробовать смешать десять частей воды с одной частью раствора HCl, чтобы удалить пятна от затирки плитки.
Те, у кого есть бассейны, могут попробовать смешать десять частей воды с одной частью раствора HCl, чтобы удалить пятна от затирки плитки.
Этот же раствор удаляет пятна с металлов и поэтому используется в продуктах, продаваемых для очистки железа, меди, латуни и других металлов. Эффекты аналогичны травлению стали: окисление поверхностных слоев для удаления пятен и загрязнений. Большинство кислот, включая хлористый водород, также удаляют отложения известкового налета, но следует обращать внимание на используемую концентрацию. Большинство сильнодействующих чистящих средств, которые мы используем дома, содержат HCl. Если вы пролили соляную кислоту на нежную поверхность, добавьте пасту из гидрокарбоната соды и воды, чтобы нейтрализовать ее; подготовьте его и держите под рукой, чтобы избежать максимального ущерба.
Кислотно-основные реакции часто используются для создания реакции шипения, которая, как говорят, увеличивает эффективность кислотного чистящего средства; однако вы только ускоряете реакцию, добавляя щелочь, тогда как в идеале добавленная кислота должна нейтрализовать щелочи на грязной поверхности. Соляная кислота реагирует с большинством карбонатов и металлов, например, с карбонатом кальция, с образованием хлорида кальция, диоксида углерода и воды или с магнием, который дает хлорид магния, диоксид углерода и воду.
Соляная кислота реагирует с большинством карбонатов и металлов, например, с карбонатом кальция, с образованием хлорида кальция, диоксида углерода и воды или с магнием, который дает хлорид магния, диоксид углерода и воду.
В человеческом теле
Желудок является участком ранних стадий пищеварения, но играет не менее важную роль в устранении потенциальных патогенных микроорганизмов, которые могли быть проглочены, благодаря очень кислой среде с pH 1,5-3,5. Этот уровень кислотности является результатом производства хлористого водорода в желудке. .
В организме человека HCl вырабатывается париетальными клетками слизистой оболочки желудка. Цитоплазма париетальных клеток соединяется с водой и углекислым газом с образованием угольной кислоты.Фермент карбоангидраза превращает один ион угольной кислоты в один ион водорода (H + ) и один ион бикарбоната (HCO3 — ). Ион водорода транспортируется в желудок через канал АТФазы H + — K + , обменивая положительные внеклеточные ионы калия с положительными внутриклеточными ионами водорода. В то же время ионы бикарбоната переносятся из клетки в кровь через анионообменник, который обменивает ионы бикарбоната на отрицательные ионы хлорида.Париетальные клетки также имеют в мембранах хлоридные каналы. Отрицательные ионы хлора попадают в желудок при увеличении внутриклеточной концентрации.
В то же время ионы бикарбоната переносятся из клетки в кровь через анионообменник, который обменивает ионы бикарбоната на отрицательные ионы хлорида.Париетальные клетки также имеют в мембранах хлоридные каналы. Отрицательные ионы хлора попадают в желудок при увеличении внутриклеточной концентрации.
Париетальная клетка
В результате этого процесса в желудке появляются ионы водорода и хлора. Как отрицательные и противоположные ионы, они притягивают и образуют соляную кислоту. Соляная кислота — важный компонент желудочного сока, необходимый для уничтожения широкого спектра потенциально патогенных бактерий до того, как содержимое желудка попадет в среду с высокой абсорбцией в кишечнике.
Человеческое тело может регулировать выработку соляной кислоты из-за непроизвольной нейрональной стимуляции, во-первых, во время стимуляции блуждающего нерва, когда пищу видят или разжевывают. Когда пища достигает желудка и желудок растягивается, возникающие нервные импульсы также стимулируют блуждающий нерв на производство большего количества ацетилхолина, который увеличивает секрецию, такую как слюна и желудочный сок, и усиливает перистальтику кишечника. Третий и основной метод — это секреция гастрина из G-клеток слизистой оболочки желудка, аналогичным образом активируемых блуждающим нервом, но также и пептидами, продуцируемыми желудком, такими как связанный с гастрином пептид.Гастрин — это гормон, который перемещается через кровь к париетальным клеткам, где они связываются с гормонами холецистокинина (CKK) посредством рецепторов CKK B и является частью связи между кишечником и мозгом, контролирующей чувство сытости и аппетит.
Третий и основной метод — это секреция гастрина из G-клеток слизистой оболочки желудка, аналогичным образом активируемых блуждающим нервом, но также и пептидами, продуцируемыми желудком, такими как связанный с гастрином пептид.Гастрин — это гормон, который перемещается через кровь к париетальным клеткам, где они связываются с гормонами холецистокинина (CKK) посредством рецепторов CKK B и является частью связи между кишечником и мозгом, контролирующей чувство сытости и аппетит.
При увеличении выработки гастрина и ацетилхолина происходит еще одна реакция в виде высвобождения гистамина из энтерохромаффиноподобных клеток (клеток ECL), которые располагаются близко к париетальным клеткам в слизистой оболочке желудка. Этот гистамин связывается с рецепторами париетальных клеток, побуждая их производить больше желудочной кислоты.
Выстилка желудка
Противоположный эффект — снижение выработки соляной кислоты — происходит в периоды голодания, когда в желудке нет пищи и повышается кислотность. Высокая кислотность останавливает экскрецию ионов водорода и хлорида в париетальных клетках . Он также стимулирует D-клетки к выработке соматостатина, который снижает выработку гормона гастрина. Пища, попадающая в двенадцатиперстную кишку, также запускает рефлекс, известный как энтерогастральный рефлекс, нервный путь кишечной нервной системы, который снижает стимуляцию блуждающего нерва.Пища в кишечнике также снижает доступность (и, следовательно, действие) холецистокинина, а также секретина, который снижает выработку кислотных компонентов желудочного сока и увеличивает выработку щелочных компонентов. Таким образом, можно с уверенностью сказать, что секреция соляной кислоты в пищеварительной системе регулируется гормональными и нервными путями, которые включают гастрин, гистамин, соматостатин, ряд полипептидов и блуждающий нерв.
Высокая кислотность останавливает экскрецию ионов водорода и хлорида в париетальных клетках . Он также стимулирует D-клетки к выработке соматостатина, который снижает выработку гормона гастрина. Пища, попадающая в двенадцатиперстную кишку, также запускает рефлекс, известный как энтерогастральный рефлекс, нервный путь кишечной нервной системы, который снижает стимуляцию блуждающего нерва.Пища в кишечнике также снижает доступность (и, следовательно, действие) холецистокинина, а также секретина, который снижает выработку кислотных компонентов желудочного сока и увеличивает выработку щелочных компонентов. Таким образом, можно с уверенностью сказать, что секреция соляной кислоты в пищеварительной системе регулируется гормональными и нервными путями, которые включают гастрин, гистамин, соматостатин, ряд полипептидов и блуждающий нерв.
В войне
Использование соляной кислоты в войне чаще всего связано с производством и воздействием иприта или сернистого иприта, использовавшегося в позиционной войне во время Первой мировой войны, , однако недавно она использовалась в гражданской войне в Сирии , хотя химическая Конвенция об оружии запретила его использование в 1993 году. Этот агент, вызывающий образование пузырей, обычно не является смертельным, если не подвергается воздействию высоких концентраций через регулярные промежутки времени. Он поражает кожу и слизистые оболочки дыхательных путей и пищеварительного тракта, вызывая ожоги, отек, раздражение и заполненные гноем волдыри. Горчичный газ также вызывает мутации в ДНК и является известным канцерогеном. Противоядия нет.
Этот агент, вызывающий образование пузырей, обычно не является смертельным, если не подвергается воздействию высоких концентраций через регулярные промежутки времени. Он поражает кожу и слизистые оболочки дыхательных путей и пищеварительного тракта, вызывая ожоги, отек, раздражение и заполненные гноем волдыри. Горчичный газ также вызывает мутации в ДНК и является известным канцерогеном. Противоядия нет.
Используются различные методы производства иприта, но только в одном из них — метод Мейера-Кларка — используется концентрированная соляная кислота.
Еще один газ, используемый в войне, — это фосген, имеющий формулу COCl 2 .В отличие от горчичного газа, имеющего слегка зеленовато-желтый оттенок, фосген бесцветен и пахнет свежескошенным сеном. Это результат воздействия окиси углерода, активированного угля и газообразного хлора. Соляная кислота не используется в производстве фосгена, но создается в присутствии воды . Вода в больших количествах содержится на слизистых оболочках. Это означает, что при вдыхании или проглатывании фосген превращается в угольную и соляную кислоты. Хотя горчичный газ привел к ряду смертельных случаев, считается, что по меньшей мере 80 000 жертв Первой мировой войны были вызваны более суровым и более непосредственным воздействием фосгена.Это примерно 85% от общего числа смертей, связанных с химическим оружием, за этот период.
Это означает, что при вдыхании или проглатывании фосген превращается в угольную и соляную кислоты. Хотя горчичный газ привел к ряду смертельных случаев, считается, что по меньшей мере 80 000 жертв Первой мировой войны были вызваны более суровым и более непосредственным воздействием фосгена.Это примерно 85% от общего числа смертей, связанных с химическим оружием, за этот период.
Факты о соляной кислоте
Хлористый водород представляет собой соединение, состоящее из водорода и хлора в соотношении один к одному . В отсутствие молекул воды хлористый водород представляет собой бесцветный, но токсичный газ. При добавлении воды водород высвобождает многие из своих молекул водорода, образуя очень кислый раствор. Чуть более 97% молекулярной массы HCl приходится на один хлорид-ион.Этот хлорид-ион имеет атомную массу 35,543, а ион водорода — 1,00794. Поскольку имеется только один атом каждого, молярная масса HCl рассчитывается путем сложения этих двух цифр — 36,46094 г / моль. Как уже упоминалось, формула хлороводорода — HCl.
Как уже упоминалось, формула хлороводорода — HCl.
В случае молекулярной массы результаты зависят от количества молей HCl. Например, в растворе, в котором имеется много атомов растворенного хлорида (Cl 2 ) для количества молекулярных атомов водорода (H 2 ), мы можем с уверенностью сказать, что 4 моля HCl произведут 4.00 моль HCl.
Используя уравнение Масса HCl = Моль HCl x Молярная масса HCl, мы можем определить, что 4,00 моль x 36,46 г моль -1 составляет 146 г.
Плотность, pH, точка плавления и кипения соляной кислоты зависят от концентрации. Например, 10% раствор HCl имеет плотность 1048 кг / л, pH -0,5, температуру плавления -18 ° C и температуру кипения 103 ° C. 30% раствор HCl имеет плотность 1,149 кг / л, pH -1, а температуру плавления и кипения -52 ° C и 90 ° C соответственно.
Обращение с соляной кислотой — рекомендация MSDS
Соляная кислота является опасной жидкостью и имеет собственный паспорт безопасности материала (MSDS). Это информация, в которой перечислены факторы безопасности и гигиены труда, связанные с ее использованием, и она должна быть доступной и легко обнаруживаемой в местах обнаружения потенциально опасных материалов.
Это информация, в которой перечислены факторы безопасности и гигиены труда, связанные с ее использованием, и она должна быть доступной и легко обнаруживаемой в местах обнаружения потенциально опасных материалов.
Соляная кислота вызывает коррозию; концентрированные формы также выделяют токсичный кислотный туман. Если кислота или туман попадут на кожу, глаза или внутренние органы, любое повреждение может быть необратимым или, возможно, смертельным. Хотя HCl не классифицируется как канцероген, его промышленное использование требует средств индивидуальной защиты , таких как паровой респиратор, резиновые перчатки и обувь, а также маска для лица. Кроме того, любое помещение, где используется соляная кислота, должно иметь доступ к системе промывки глаз. Даже при домашней чистке разбавленными средствами брызги на глаза или кожу могут вызвать ожоги.
Рекомендация
MSDS по контакту соляной кислоты с кожей заключается в ополаскивании этой области в течение не менее 15 минут и снятии любых предметов одежды, которые соприкасались с раствором. При видимых ожогах рекомендуется умыться антибактериальным мылом или использовать антибактериальный крем, а также посетить медицинский центр. Попадание в глаза требует промывочной системы, которая промывает пораженный глаз не менее 15 минут и требует медицинской помощи.
При видимых ожогах рекомендуется умыться антибактериальным мылом или использовать антибактериальный крем, а также посетить медицинский центр. Попадание в глаза требует промывочной системы, которая промывает пораженный глаз не менее 15 минут и требует медицинской помощи.
Проглатывание соляной кислоты любой концентрации может вызвать ожоги внутри рта, горла и пищевода. Несмотря на то, что желудочный сок очень кислый, он остается в резервуаре желудка. Расстройство желудка, вызванное попаданием кислоты желудочного сока в нижнюю часть пищевода, может вызвать эзофагит Барретта и повысить риск рака пищевода. Распространенным заболеванием желудочно-кишечного тракта является гастроэзофагеальная рефлюксная болезнь или ГЭРБ . На изображении ниже показаны признаки и симптомы этой часто болезненной патологии. При проглатывании HCl важно не вызвать рвоту, а немедленно обратиться за медицинской помощью. Вдыхание тумана HCl также требует посещения отделения неотложной помощи.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ)
Информация о хранении
MSDS настаивает на том, что соляную кислоту следует хранить в закрытом и подходящем контейнере в прохладном, сухом и хорошо вентилируемом помещении.Его также следует хранить вдали от органических материалов, окислителей, металлов и щелочей, поскольку они могут вступать в реакцию с ними и увеличивать концентрацию легковоспламеняющегося газообразного водорода.
Викторина
1. Какие из следующих органических соединений выводятся из производства пластмасс?
A. Фосген
B. BPA
C. Серная кислота
D. HCl
Ответ на вопрос № 1
B правильный.BPA или бисфенол A — канцерогенное вещество, используемое в производстве пластмасс и смол. Многие пластмассы теперь не содержат бисфенола А, и эта тенденция, несомненно, сохранится.
2. Что делать в первую очередь, если вы проглотили хлористый водород?
Что делать в первую очередь, если вы проглотили хлористый водород?
A. Пейте много воды
B. Рвота
C. Выпейте раствор бикарбоната
D. Обратитесь за медицинской помощью
Ответ на вопрос № 2
D правильный. Питьевая вода содержит дополнительные молекулы водорода и может повысить уровень кислотности, но, что более важно, она только вымывает кислоту дальше в пищевод и увеличивает площадь поврежденной поверхности.Рвота увеличивает кислотность из-за наличия кислоты в желудке. Бикарбонат или щелочные продукты вызовут летучую реакцию, возможно, перфорируя пищеварительный тракт. Важное значение имеет медицинское лечение, включающее различные вмешательства, от промывания желудка до интубации и перевода в отделение интенсивной терапии.
3. Где происходит коагуляция и флокуляция в отношении HCl?
A. Травление металлов
B. Водоподготовка
Водоподготовка
C. Обработка ожогов
D. Очистка соли
Ответ на вопрос № 3
B правильный. Коагуляция и флокуляция загрязняющих веществ в воде позволяют легче удалять их, обеспечивая менее загрязненную воду.
4. Какие клетки производят гастрин?
A. Париетальные клетки
B. Т-клетки
C. G-клетки
D. ECL-клетки
Ответ на вопрос № 4
C правильный.Клетки ECL производят гистамин, Т-клетки участвуют в иммунитете, париетальные клетки выделяют ионы водорода и хлора, а также внутренний фактор. Буква G указывает нам правильное направление — G-клетки производят гастрин.
5. Какой черепной нерв больше всего участвует в регуляции выработки желудочного сока?
A. Блуждающий нерв
B. Отводящий нерв
C. Подъязычный нерв
Подъязычный нерв
D. Глазодвигательный нерв
Ответ на вопрос № 5
A правильный.И отводящие нервы, и глазодвигательные нервы играют роль в движении глаз. Подъязычный нерв управляет языком. Блуждающий нерв важен для множества нервных путей, которые заканчиваются во многих внутренних органах, таких как сердце, пищеварительная система и легкие.
Как проводить тест на соляную кислоту
В рамках урока химии вам, возможно, придется идентифицировать немаркированные растворы. Если у вас есть раствор, который, как вы подозреваете, может быть соляной кислотой, но не знаете наверняка, самый быстрый способ проверить — использовать раствор нитрата серебра.Этот тест также является хорошим введением в процесс осаждения, когда нерастворимое твердое вещество выходит из жидкого раствора.
TL; DR (слишком долго; не читал)
Самый простой способ проверить соляную кислоту — с помощью раствора нитрата серебра. Добавьте раствор нитрата серебра к исследуемому раствору в пробирке и наблюдайте за реакцией. Если образуется белый осадок, значит, присутствует соляная кислота.
Добавьте раствор нитрата серебра к исследуемому раствору в пробирке и наблюдайте за реакцией. Если образуется белый осадок, значит, присутствует соляная кислота.
Свойства соляной кислоты
Соляная кислота (HCl) — это сильная коррозионная кислота, образующаяся при растворении хлористого водорода в воде.Он часто используется в качестве химического реагента, а также естественным образом вырабатывается в организме. Большая часть желудочного сока (пищеварительная кислота человека) состоит из соляной кислоты.
Элементы группы 7
Хлороводород образуется при взаимодействии водорода с хлором. Атом водорода и атом хлора соединены ковалентной связью с образованием молекул. Соляная кислота образуется при растворении хлористого водорода в воде. В этот момент молекулы расщепляются на ионы.
В периодической таблице элементы 7-й группы называются галогенами, химически активными неметаллами, которые всегда находятся в соединениях с другими элементами. Хлор, бром и йод — все это примеры галогенов. Их ионы называются галогенид-ионами. Например, хлорид — это галогенид-ион хлора. Обычной тестовой реакцией для хлорид-ионов является взаимодействие с нитратом серебра.
Хлор, бром и йод — все это примеры галогенов. Их ионы называются галогенид-ионами. Например, хлорид — это галогенид-ион хлора. Обычной тестовой реакцией для хлорид-ионов является взаимодействие с нитратом серебра.
Тест с нитратом серебра
Если раствор нитрата серебра добавить к пробе воды, содержащей галогенид-ионы, галогенид серебра выпадает в осадок, поскольку все галогениды серебра нерастворимы в воде. Если присутствуют ионы хлорида, ионы серебра реагируют с ними, образуя белый осадок хлорида серебра.
Для проведения теста промойте пробирку чистой водой. Добавьте 20 капель тестового раствора в пробирку, подкислите его несколькими каплями разбавленной азотной кислоты, затем добавьте несколько капель раствора нитрата серебра. Азотная кислота реагирует и удаляет любые другие ионы, которые могут исказить результаты. Осторожно встряхните пробирку, чтобы перемешать содержимое, затем проверьте раствор. Белый осадок свидетельствует о наличии хлорид-ионов. С другой стороны, кремовый осадок указывает на наличие бромид-ионов, а желтый осадок указывает на иодид-ионы.
С другой стороны, кремовый осадок указывает на наличие бромид-ионов, а желтый осадок указывает на иодид-ионы.
Надевайте защитные очки и перчатки при проведении теста на нитрат серебра, чтобы избежать попадания раствора в глаза или на кожу.
Соляная кислота | Подкаст | Chemistry World
Meera Senthilingam
На этой неделе кислотное соединение, используемое на протяжении всей истории, в промышленности, а также в нашем организме. Вот Брайан Клегг:
Брайан Клегг
Большинство из нас впервые сталкивается с трио сильных кислот — соляной, азотной и серной — когда заходит в химическую лабораторию в школе.Это не те вещества, которые вы найдете в кухонном шкафу дома. Тем не менее, я могу гарантировать, что одно из этих соединений было частью вашей жизни каждый день с самого детства. Потому что соляная кислота играет важную роль в вашем организме.
Эта сильнодействующая кислота, водный раствор хлористого водорода, известна давно. Ранние названия кислоты имеют довольно морской привкус, отражающий производство кислоты из поваренной соли. Алхимики назвали бы его «духи соли», в то время как его обычное название до появления современных конвенций было соляной кислотой, где «соляная кислота» была причудливым термином для соленой кислоты.Как сказал один Н. Грю в 1675 году, «Муриатик — это соленость, соединенная с некоторой остротой».
Неизвестно, когда именно была впервые получена соляная кислота. Алхимики были склонны создавать смеси, которые вполне могли содержать соляную кислоту, и некоторые предполагают, что Джабир ибн Хайян создал ее еще в девятом веке. В средневековье он наверняка использовался в царской водке, смеси соляной и азотной кислот. Мы действительно знаем, что в одном из газовых экспериментов Джозефа Пристли 1772 года был получен чистый газообразный хлористый водород, и что Хамфри Дэви успешно показал, что это соединение содержит водород и хлор в 1818 году.
Мы склонны довольно свободно называть соляную кислоту HCl, но когда хлористый водород растворяется в воде, положительный ион водорода соединяется с водным H 2 O с образованием гидрокония (H 3 O + ), оставляя отрицательный хлорид-ион. Концентрированная соляная кислота составляет около 38% хлористого водорода.
Первоначально большая часть промышленного хлористого водорода представляла собой отходы, которые выбрасывались в воздух, но к середине девятнадцатого века уровень загрязнения уже считался неприемлемым.К счастью, к этому времени отработанный хлористый водород стал ценным для производства соляной кислоты. Хотя используемые процессы изменились, перейдя от побочного продукта производства карбоната натрия к производству, в основном, наряду с органическими соединениями, соляная кислота по-прежнему в основном представляет собой повторное использование отходов, мармита кислотного мира.
Большая часть промышленного производства соляной кислоты идет на травление и используется в различных химических производственных процессах.Рассматриваемое травление не связано с луком, а является способом удаления поверхностного обесцвечивания стали и других металлов.
В промышленных химических процессах соляная кислота используется для производства молекул, содержащих хлор, для пластмассовых изделий, таких как диохлорэтан и винилхлорид (используется для производства ПВХ). Поскольку большая часть мирового производства хлористого водорода происходит как побочный продукт других химических процессов, соляная кислота часто производится и потребляется на месте, эффективно рециркулируя в процессе, а не когда-либо становится отдельным коммерческим продуктом.
Хотя соляная кислота действительно играет роль в пищевой промышленности, где она используется для контроля pH воды при производстве продуктов питания, она играет гораздо более фундаментальную роль, когда речь идет о потреблении пищи. Ваш желудок содержит большое количество соляной кислоты и может иметь pH всего 1.
Часть роли этой мощной кислоты — предотвращение инфекции, но ее основная функция — пищеварение. Кислота атакует белки в процессе, известном как денатурирование, что заставляет их распадаться, что облегчает их расщепление ферментами для пищеварения.Возможно, наиболее знакомым примером денатурации является денатурация белков яичного белка при варке, превращаясь из прозрачной жидкости в непрозрачное твердое вещество. Здесь нарушение структуры приводит к образованию запутанной массы денатурированного белка, но в желудке результатом является выполнение первоначальной работы по разрушению, позволяющей ферментам, таким как пепсин, расщеплять белки на более мелкие фрагменты.
Ваш желудок защищен от содержащейся в нем кислоты толстым слоем слизи, а мощная мышца закрывает верхнюю часть желудка.Но задействованные механизмы иногда могут работать неправильно, в результате чего кислота попадает в пищевод, вызывая жжение при кислотном рефлюксе, или просто вызывает расстройство желудка.
Хотя сейчас существуют сложные лекарства, которые снижают в первую очередь производство кислоты, многие из нас по-прежнему прибегают к простой неорганической химической реакции и глотают пару таблеток антацида при заболеваниях желудка. На рынке есть различные лекарства, но многие из них содержат карбонат кальция или магния, что приводит к простой реакции, которая нейтрализует кислоту с образованием хлорида, воды и углекислого газа.
Будь то очистка ржавого металла, производство ПВХ или расщепление белков, соляная кислота — это соединение, которое просто выполняет свою работу. Соляная кислота может быть причиной неудобных ночей, когда мы слишком много ели и страдаем от последствий избытка кислоты в желудке, но это более чем компенсируется ее повседневной ролью в превращении пищи в топливо.
Мира Сентилингам
И поскольку это топливо помогает нам прожить день, я уверен, что мы можем простить несколько бессонных ночей из-за несварения желудка.Это был научный писатель Брайан Клегг с химией, лежащей в основе широко используемого и, возможно, недооцененного соединения, соляной кислоты. Теперь, учитывая, насколько мы все любим есть, на следующей неделе мы встретимся с комплексом у источника всей этой пищи.
Дункан Макмиллан
Это, вероятно, недостаточно признанная истина, что мы обязаны своим существованием и поддерживающей нас паутиной жизни пище, производимой светом. У подножия почти каждого древа жизни, от тундры до саванны до коралловых рифов и океанских желобов, всю тяжелую работу выполняет фотосинтезирующий организм.И молекула, которая заставляет это происходить, — хлорофилл.
Мира Сентилингам
И чтобы узнать, как именно хлорофилл использует свет для производства продуктов питания и как это соединение также вдохновляло известных художников на протяжении веков из-за его использования в определенном духе, присоединяйтесь к Динкану Макмиллану на следующей неделе в презентации Chemistry in its element . А пока спасибо за внимание. Я Мира Сентилингам.
Хлористый водород против соляной кислоты — видео и стенограмма урока
Химическая формула
HCl — это химическая формула хлористого водорода и соляной кислоты.Основное различие заключается в их состоянии. Хлороводород — это газ, а соляная кислота — водный раствор. Водный просто означает, что он растворен в воде. Вот почему важно указывать состояние вопроса в скобках. Для газообразной версии мы пишем HCl (g), а для кислотной версии мы пишем HCl (aq). Давайте углубимся в каждое из этих состояний.
HCl (г)
Как мы уже обсуждали, хлористый водород — это газ.Мы можем нарисовать точечную структуру Льюиса HCl (г), которая показывает расположение электронов в связи между водородом и хлором. Диаграмма 1 показывает точечную структуру Льюиса газообразного хлористого водорода.
Точки на диаграмме 1 представляют электроны внешней оболочки. Между водородом и хлором делятся два электрона, что делает его ковалентной молекулой . Что-то особенное происходит, когда газообразный хлористый водород проходит через воду.Давай проверим.
HCl (водн.)
Полярное вещество в целом электрически нейтрально, но одна его сторона заряжена положительно, а другая — отрицательно. Диаграмма 2 показывает полярную природу воды.
Когда газообразный хлористый водород попадает в воду, молекулы воды захватывают атом водорода в HCl (г) и отводят его от атома хлора.Это процесс растворения , при котором образуется соляная кислота. Теперь у нас есть кислый раствор, потому что в нем присутствуют ионы h4 O + 1, которые носят название гидрокония. На диаграмме 3 показан ион гидроксония.
Напишем реакцию.
HCl (г) + h3 O (л) → h4 O + 1 + Cl-1
На диаграмме 4 показано, как газообразный хлористый водород может попасть в воду.
Давайте теперь рассмотрим свойства газообразного хлористого водорода и соляной кислоты.
Свойства
Мы будем иметь дело со свойствами газообразного хлористого водорода и соляной кислоты, наблюдаемыми при комнатной температуре. Газообразный хлористый водород очень агрессивен и легко вступает в реакцию с водой, даже с водяным паром в воздухе. Несмотря на то, что он едкий, он не воспламеняется. Если бы хлористый водород был выпущен в замкнутом пространстве, он выглядел бы слегка желтым и опускался бы к полу.Он имеет характерный запах, который может гореть при вдыхании, потому что вступает в реакцию с влагой во рту, легких и носовых проходах, образуя соляную кислоту.
Соляная кислота также очень агрессивна и имеет такой же светло-желтый оттенок. Его точка кипения немного выше, чем точка кипения воды, и он очень реактивен с металлами. Сила кислоты измеряется ее значением pH. Значения pH, приближающиеся к нулю, сильнее. Чем больше хлористого водорода пропускается через заданное количество воды, тем выше pH полученной соляной кислоты.
Итоги урока
Давайте рассмотрим. Хлороводородный газ и соляная кислота имеют одинаковую химическую формулу: HCl. Разница между ними состоит в том, что хлористый водород представляет собой газ, а соляная кислота представляет собой водный раствор.
В HCl (г) атом водорода имеет два общих электрона с атомом хлора. Когда этот газ барботируется через воду, молекулы воды отделяют атом водорода от атома хлора, что называется растворением .Свободный ион водорода связывается с молекулой воды, образуя гидроксоний h4 O + 1. Реакция:
HCl (г) + h3 O (l) → h4 O + 1 + Cl-1
Газообразный хлористый водород тяжелее воздуха, слегка желтоватого цвета, негорючий и обладает высокой реакционной способностью по отношению к воде.
Соляная кислота также имеет слегка желтоватый оттенок, и ее силу можно измерить по значению pH. Чем ниже pH, тем сильнее кислота. Соляная кислота очень реактивна с металлами.
Обе формы HCl вызывают коррозию.
Руководство по изучению минералов — Кислота HCl
Инструкции: «Кислотный» тест
Предпосылки — Минералы представляют собой химические соединения, и некоторые минералы в некоторой степени нестабильны в присутствии кислотного раствора. То есть кислый раствор может разорвать химические связи минерального соединения, и минерал растворится. Одно химическое испытание проводится с использованием раствора холодной разбавленной (10%) соляной кислоты — HCl. Под этим раствором сильно реагирует только один обычный минерал.
Раствор состоит примерно из 10% соляной кислоты (90% воды и 10% концентрированной HCl). Раствор хранят при комнатной температуре в безопасном пластиковом «флаконе-капле» для использования.
Осторожно — Не следует пытаться использовать разбавленный раствор соляной кислоты без инструкций по технике безопасности, обычно предоставляемых инструктором.
Материалы для теста
Процедура теста
Осторожно сожмите предохранительный флакон, чтобы выпустить на образец одну или две капли холодной разбавленной HCl.
Наблюдайте за образцом на наличие любых признаков химической реакции.
Промокните бумажной салфеткой любые капли кислоты из образца.
Возможные результаты испытаний и интерпретация
Образец реагирует немедленно, быстро образуя множество пузырьков, которые лопаются и шипят. Мы интерпретируем эту реакцию как «сильную» или «энергичную». Мы пришли к выводу, что образец состоит из химического соединения CaCO3 — карбоната кальция, единственного распространенного минерала, который бурно реагирует с холодной разбавленной HCl.
