Содержание
степень окисления h3co3 — video klip mp4 mp3
Video Axtar Ara Yukle Indir
Video
степень окисления h3co3 — video klip mp4 mp3 yukle
Как найти число окисления для C в h3CO3 (угольной кислоте)
1:44
Соcтавление формул по степени окисления
12:31
Степень окисления
25:47
Угольная кислота h3CO3 и ее соли
16:00
СТЕПЕНЬ ОКИСЛЕНИЯ определяем степени окисления химических элементов Габриелян
9:16
63. Степени окисления элементов (часть 1)
Степени окисления элементов (часть 1)
30:14
Степень окисления | Химия ОГЭ | Умскул
55:06
Степень окисления. Определение степеней окисления. Часть 1
19:54
8 класс. Степень окисления.
8:19
Составление формул по степени окисления. 1 часть. 8 класс.
1 часть. 8 класс.
14:53
Степень окисления. Учимся определять степень окисления по формулам.
15:39
244. Степень окисления серы в различных соединениях
11:39
Video Axtar Yüklə
Anarim.Az
Sayt Rehberliyi ile Elaqe
Saytdan Istifade Qaydalari
Anarim.Az 2004-2021
Соли угольной кислоты. 9-й класс
Цели урока: изучить свойства солей
угольной кислоты карбонатов и гидрокарбонатов.
Задачи урока:
– отработать навыки в решении
расчетных и экспериментальных задачах;
– повторить свойства и строение
угольной кислоты, гидролиз солей и реакции
обмена;
– воспитывать коммуникативную
культуру, уверенность в себе и своих знаниях,
навыки контроля и самоконтроля.
Тип урока: изучение новой темы
Методические приемы: рассказ,
демонстрации опытов.
Оборудование: раствор Na2CO3; раствор
HCl, h3SO4, Ca(OH)2, Na2CO3 твердая, индикатор –
фенолфталеин, штатив, газоотводная трубка;
карточки – задания
Ход урока
I. Оргмомент.
II. Проверка домашнего задания.
Сегодня на уроке мы должны изучить
соли угольной кислоты. Но прежде чем отправимся в
Но прежде чем отправимся в
увлекательный мир карбонатов, нам надо повторить
свойства и строение h3CO3.
(2 человека у доски, 3 человека на
рабочем месте)
У доски
1. Дать характеристику угольной
кислоте: сила, основность, содержание кислорода.
Составить уравнение диссоциации.
2. Химические свойства угольной
кислоты.
На месте.
- Дать характеристику аллотропным модификациям
углерода. - Дать сравнительную характеристику физических и
химических свойств оксида углерода (VI) и оксида
углерода (II): строение молекул, физические и
химические свойства. - Допишите определения:
а) адсорбция – это процесс – …
б) процесс выделения поглощенных
веществ называется …
Пока ребята готовят ответы на вопрос,
мы проведем небольшую письменную работу (10
вопросов)
- Разновидности простого вещества, образованного
одним и тем же химическим элементом? (Аллотропные
видоизменения) - Электронная формула атома углерода.
 (1s22s22p2)
(1s22s22p2) - Количество электронов на внешнем уровне у
элементов IV группы главной подгруппы (четыре) - Летучие водородные соединения С и Si? (СН4 –
метан, SiН4 – силан) - Формула высших оксидов элементов IV группы
главной подгруппы? (RО2) - Масса 0,5 моль СО2 ? (22г)
- Объем 2 моль СН4 при н.у.? (44,8 л)
- Чего больше по массе в угарном газе углерода или
кислорода? (кислорода С:О=3:4) - Степень окисления углерода в угарном газе и
углекислом газе? (+2;+ 4) - Что такое сухой лед?
Проверка (правильные ответы на доске)
Ребята проверяют исправляют ошибки,
выставляют себе оценки.
Проверка ответов у доски: рассмотрим
свойства h3CO3.
III. Объяснение нового материала.
h3CO3 диссоциирует в две стадии. Сколько
Сколько
типов солей образует данная соль?
(По ходу опроса записывают схему на
доске)
h3CO3
В повседневной жизни мы часто
сталкиваемся с солями угольной кислоты (питьевая
сода, известняк, мрамор, мел и т.п.)
Списывают с доски в тетрадь
тривиальные названия солей.
Стихотворение о карбонатах. (Пока
учащиеся пишут)
На земле живут три брата
Из семейства карбонатов.
Старший брат красавец – мрамор.
Славен именем каррары
Превосходный зодчий он
Строил Рим и Парфенон.
Всем известен известняк
Потому и назван так.
Знаменит своим трудом
Возводя за домом дом.
И способен и умел младший
Мягкий братец мел.
Как рисует посмотри
Этот …СаСО3.
CaCO3 – мел, известняк, мрамор
NaHCO3 – питьевая сода
Na2CO3 – кальцинированная сода
Na2CO3·10h3O – кристаллическая сода
CaCO3 – жемчуг (минерал арагонит)
Получение солей: назовите
лабораторный способ получения солей.
(кислота + основание–> соль + вода –
реакция нейтрализации)
Для получения солей угольной кислоты
используют –>C02
2NaOH+CO2–>Na2CO3+h3O,
если избыток CО2
получаются кислые соли
Na2CO3+CO2+h3O–>2NaHCO3
Химические свойства.
- Отношение к нагреванию.
- Реагирует солями (тип реакций?)
- С кислотами
- Гидролизу подвергаются соли угольной кислоты
образуя в результате кислые соли в щелочной
среде.
CaCO3–> CaO + CO2
CaHCO3–>CaCO3+CO2+h3O
(Это свойство позволяет использовать
гидрокарбонаты в пищевой промышленности в
качестве разрыхлителя теста)
В результате реакций выделяется CO2, как его обнаружить?
– лучина тухнет.
— через раствор известковой воды (Ca (OH)2)
образуется осадок белого цвета.
Ca(OH)2+CO2–>CaCO3+h3O,
но если дальше пропускать CO2 осадок растворяется
CaCO3+CO2+h3O–>Ca(HCO3)2
Na2CO3+CaSO4–>K2SO4+CaCO3
(На доске расписывает ученик полное и
сокращенное ионное уравнение)
Na2CO3+2HCl–>2NaCl+CO2+h3O
Наблюдение “вскипание”.
Реакция взаимодействия солей h3CO3 с
кислотами – качественная.
Геологи используют это свойство для
определения карбонатных минералов.
Опыт. | Na2CO3+HCl
Na2CO3(р-р)+HCl
CaCO3(мел)+HCl | вскипание |
Самостоятельно составьте уравнения
химических реакций.
Испытать раствор Na2CO3 индикатором
фенолфталеином (раствор малинового цвета)
Вывод: соли угольной кислоты имеют
общие свойства солей и специфические: 1)
взаимодействие с кислотами; 2) гидролиз.
IV. Решение задачи
Какой объем СО2 выделится (при н.у.) при
обжиге 230 кг известняка, содержащего 10 % примесей.
V. Подведение итогов урока
(выставление оценок).
VI. Домашнее задание
§ 33, № 21-22 (с. 91-92)
устно, задача 3 (с.92).
Контрольная работа по химии за 2 четверть
Контрольная работа за II четверть. 8 класс.
Вариант I
Определите степень окисления элементов в следующих соединениях:
NO2, Al(OH)3, h4PO4, Ba(NO3)2.
Даны вещества, состав которых выражается формулами:
SO3, HNO2, HCl, LiOH, Al2O3, Pb(OH)2, Na2SO4, FeSiO3, MnO2, Cr(NO3)2,
h3CO3, Co(OH)3.
Из приведенного перечня выпишите отдельно формулы:
а) оксидов; б) оснований; в) кислот; г) солей.
Укажите названия каждого вещества.
Напишите молекулярные формулы соединений:
оксида хлора (I),
оксида фосфора (V),
нитрата алюминия,
гидроксида магния,
фосфата железа (II),
сульфата марганца (II).
Рассчитайте массу 5,6 л кислорода (н.у).
Контрольная работа за II четверть. 8 класс.
Вариант II
Определите степень окисления элементов в следующих соединениях:
СoO, Fe(OH)3, h3SiO3, Cr2(SO4)3.
Даны вещества, состав которых выражается формулами:
h3SO3, Mn2O7, h3S, Fe(OH)2, N2O3, NaOH, Ca3(PO4)2, Al(OH)3, CuO,
ZnCl2, Mn(NO2)2, HNO3.
Из приведенного перечня выпишите отдельно формулы:
а) оксидов; б) оснований; в) кислот; г) солей.
Укажите названия каждого вещества.
Напишите молекулярные формулы соединений:
оксида серебра (I),
оксида железа (III),
силиката свинца,
гидроксида хрома(II),
карбоната бария,
сульфата марганца (II).
Какой объем (н.у) займет углекислый газ массой 11 г?
Простые и сложные вещества
Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента).
Пример: h3, O2,Cl2, P4, Na, Cu, Au.
Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов).
Пример: h3O, Nh4, OF2, h3SO4, MgCl2, K2SO4.
Аллотропия — способность одного химического элемента образовывать несколько простых веществ, различающихся по строению и свойствам.
Пример:
- С — алмаз, графит, карбин, фуллерен.
- O — кислород, озон.
- S — ромбическая, моноклинная, пластическая.
- P — белый, красный, чёрный.
Явление аллотропии вызывается двумя причинами:
- Различным числом атомов в молекуле, например кислород O2 и озон O3.
- Образованием различных кристаллических форм, например алмаз, графит, карбин и фуллерен (смотри рисунок выше).

Основные классы неорганических веществ
Бинарные соединения
Вещества, состоящие из двух химических элементов называются бинарными (от лат. би – два) или двухэлементными.
Названия бинарных соединений образуют из двух слов – названий входящих в их состав химических элементов.
Первое слово обозначает электроотрицательную часть соединения – неметалл, его латинское название с суффиксом –ид стоит всегда в именительном падеже.
Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название стоит в родительном падеже, затем указывается степень окисления (только в том случае, если она переменная):
Запомни!
Bh4 — боран
B2H6 — диборан
Ch5 — метан
Sih5 — силан
Nh4 — аммиак
Ph4 — фосфин
Ash4 — арсин
Оксиды
Оксиды — сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.
Общая формула оксидов: ЭхОу
Основные оксиды
Основные оксиды — оксиды, которым соответствуют основания.
Основные оксиды образованы металлом со степенью окисления +1, +2.
Пример
Соответствие основных оксидов и оснований
- Na2O — Na2(+1)O(-2) — NaOH
- MgO — Mg(+2)O(-2) — Mg(OH)2
- FeO — Fe(+2)O(-2) — Fe(OH)2
- MnO — Mn(+2)O(-2) — Mn(OH)2
Амфотерные оксиды
Амфотерные оксиды — оксиды, которые в зависимости от условий проявляют либо основные, либо кислотные свойства.
Амфотерные оксиды образованы металлом со степенью окисления +3, +4, а также некоторыми металлами (Zn, Be) со степенью окисления +2.
Пример
Al2(+3)O3(-2), Fe2(+3)O3(-2), Mn(+4)O2(-2), Zn(+2)O(-2), Be(+2)O(-2)
Кислотные оксиды
Кислотные оксиды — оксиды, которым соответствуют кислоты.
Кислотные оксиды образованы неметаллом, а также металлом со степенью окисления +5, +6, +7.
Пример
Соответствие кислотных оксидов и кислот
- SO3 — S(+6)O3(-2) — h3SO4
- N2O5 — N2(+5)O5(-2) — HNO3
- CrO3 — Cr(+6)O3(-2) — h3CrO4
- Mn2O7 — Mn2(+7)O7(-2) — HMnO4
Гидроксиды
Гидроксиды — сложные вещества, состоящие из трех элементов, два из которых водород со степенью окисления +1 и кислород со степенью окисления -2.
Общая формула гидроксидов: ЭхОуНz
Основания
Основания — сложные вещества, состоящие из ионов металла и одной или нескольких гидроксо-групп (ОН-).
В основаниях металл имеет степень окисления +1, +2 или вместо металла стоит ион аммония Nh5+
Пример
NaOH, Nh5OH, Ca(OH)2
Амфотерные гидроксиды
Амфотерные гидроксиды — сложные вещества, которые в зависимости от условий проявляют свойства оснований или кислот.
Амфотерные гидроксиды имеют металл со степенью окисления +3, +4, а также некоторые металлы (Zn, Be) со степенью окисления +2.
Пример
Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3
Кислоты
Кислоты — сложные вещества, состоящие из атомов водорода и кислотных остатков.
В состав кислот входит неметалл или металл со степенью окисления +5, +6, +7.
Пример
h3SO4, HNO3, h3Cr2O7, HMnO4
Соли
Соли- соединения, состоящие из катионов металлов (или Nh5+) и кислотных остатков.
Общая формула солей: MexAcy
- Me — металл
- Ac — кислотный остаток
Пример
KNO3 — нитрат калия
(Nh5)2SO4 — сульфат аммония
Mg(NO3)2 — нитрат магния
Названия кислот и кислотных остатков
| Кислота | Кислотный остаток | ||
| Название | Формула | Название | Формула |
| Соляная (хлороводородная) | HCl | Хлорид | Cl(-) |
| Плавиковая (фтороводородная) | HF | Фторид | F(-) |
| Бромоводородная | HBr | Бромид | Br(-) |
| Иодоводородная | HI | Иодид | I(-) |
| Азотистая | HNO2 | Нитрит | NO2(-) |
| Азотная | HNO3 | Нитрат | NO3(-) |
| Сероводородная | h3S | Сульфид Гидросульфид | S(2-) HS(-) |
| Сернистая | h3SO3 | Сульфит Гидросульфит | SO3(2-) HSO3(-) |
| Серная | h3SO4 | Сульфат Гидросульфат | SO4(2-) HSO4(-) |
| Угольная | h3CO3 | Карбонат Гидрокарбонат | СО3(2-) НСО3(-) |
| Кремниевая | h3SiO3 | Силикат | SiO3(2-) |
| Ортофосфорная | h4PO4 | Ортофосфат Гидроортофосфат Дигидроортофосфат | РО4(3-) НРО4(2-) Н2РО4(-) |
| Муравьиная | НСООН | Формиат | НСОО(-) |
| Уксусная | СН3СООН | Ацетат | СН3СОО(-) |
Полезные ссылки
Источник материала
Классификация неорганических веществ (видео)
Классификация неорганических веществ. Сложные вопросы (видео)
Сложные вопросы (видео)
Кислотные оксиды (видео)
Основные оксиды (видео)
Основания (видео)
Характеристика солей (видео)
Дополнительные материалы
Классификация и номенклатура неорганических веществ (видео)
Классификация соединений (видео)
Аллотропные формы углерода (видео)
Открытый урок 8 класс «Степень окисления и валентность»
Тема урока: Степень окисления и валентность
Цель урока:
создать условия для осознанного усвоения учащимися знаний о
степени окисления и валентности.
Задачи урока:
Образовательные: — Дать первоначальное понятие о степени
окисления.
— Научить составлять формулы бинарных соединений по степени
окисления.
— Познакомить с началами номенклатуры химических соединений;
-развитие устойчивого интереса у учащихся к изучению химии
Развивающие: — Научить определить степени окисления
элементов.
Развитие аналитического мышления, способность делать выводы.
Воспитательные: Воспитание положительного отношения к
знаниям
Планируемы результаты:
Предметные:Знать, как составлять формулы бинарных соединений
по степени окисления, различать катионы от анионов.
Метапредметные: уметь расставлять степени окисления и
выводить хим. формулу.
Личностные: уметь применять знания на практике
План урока:
Организационно-мотивационная часть.
Актуализация знаний.
Изучение нового материала.
Закрепление изученного материала.
Рефлексия.
Домашнее задание.
Тип урока
:изучение нового материала Оборудование: компьютер, проектор, Периодическая система
химических элементов Д.И. Менделеева.
Методы и методические приемы: словесные, наглядные,
самостоятельная работа.
Ход урока:
Организационно-мотивационная часть
— организационный момент
— цель урока
2. Актуализация
Повторение и обобщение пройденного материала (карточки)
А) Индивидуальный опрос по дом. зад.( у доски)
1-й ученик. Указать вид химической связи Н2Н2SNh4 LiFNaCl
2-й ученик Чем отличается аморфные вещества от
кристаллических
Б) Фронтальный опрос класса
1. Какие виды химической связи вы знаете?
Какие виды химической связи вы знаете?
2.Дайте определение ковалентной связи. Как она образуется? Ее
виды.
3.Что называется ионной связью? Как она образуется?
4. Где образуется металлическая связь?
В) Тест
1.Химическая связь в молекуле Br2
1) ионная
2) металлическая
3) ковалентная неполярная
4) ковалентная полярная
2.Наиболее ярко выражены металлические свойства у
1) Li
2) K
3) Na
4) Rb 3. Формула вещества с ковалентной неполярной связью
1) Н2О 2)Br2 3)SO3 4) NaCl
4. Кристаллическая решетка твердого оксида углерода (IV) CO2
1) ионная 2) атомная 3)молекулярная 4) металлическая
5. Ионную кристаллическую имеет
1) фторид натрия 2) вода 3) серебро 4) бром
3. Изучение нового материала.
1. объяснение учителя. Постановка проблемы.
Задание:
Сравнить
Задание: сравните качественный и количественный состав в
молекулах: HCl , h3O, Nh4, Ch5. Беседа с учащимися:
– Что общего в составе молекул? Предполагаемый ответ: Наличие
атомов водорода. – Чем они отличаются друг от друга?
Предполагаемый ответ:
HCl – один атом хлора удерживает один атом водорода,
h3O – один атом кислорода удерживает два атома водорода,
Nh4 – один атом азота удерживает три атома водорода,
Ch5 – один атом углерода удерживает четыре атома водорода.
Демонстрация шаростержневых моделей. Проблема: Почему
различные атомы удерживают различное количество атомов
водорода? (Выслушиваем варианты ответов учащихся).
Вывод: У атомов разная способность удерживать определённое
количество других атомов в соединениях. Это и называется
валентностью. Слово “валентность” происходит от лат. valentia –
сила. Запись в тетради:
Валентность – это свойство атомов удерживать определённое число
других атомов в соединении.
Валентность обозначается римскими цифрами. Записи на доске и в
тетрадях:
HCl I I h3O I II
h4N I III
h5CIIV
Валентность атома водорода принята за единицу, а у кислорода – II.
Определение валентности атомов элементов в соединениях.
Правило определения валентности: число единиц валентностей всех
атомов одного элемента равно числу единиц валентности всех
атомов другого элемента.
Правила определения валентности
элементов в соединениях
1. Валентность водорода принимают за I (единицу). Тогда в
соответствии с формулой воды Н2О к одному атому кислорода
присоединено два атома водорода.
2. Кислород в своих соединениях всегда проявляет
валентность II. Поэтому углерод в соединении СО2 (углекислый газ)
имеет валентность IV.
3. Высшая валентность равна номеру группы.
4. Низшая валентность равна разности между числом 8
(количество групп в таблице) и номером группы, в которой
находится данный элемент, т.е. 8 — Nгруппы.
5. У металлов, находящихся в «А» подгруппах, валентность равна
номеру группы.
6. У неметаллов в основном проявляются две валентности: высшая
и низшая.
Например: сера имеет высшую валентность VI и низшую (8 – 6),
равную II; фосфор проявляет валентности V и III.
Валентность может быть постоянной или переменной.
Валентность элементов необходимо знать, чтобы составлять
химические формулы соединений.
Запомните!
Особенности составления химических формул соединений. 1) Низшую валентность проявляет тот элемент, который находится в
таблице Д.И.Менделеева правее и выше, а высшую валентность –
элемент, расположенный левее и ниже.
Например, в соединении с кислородом сера проявляет высшую
валентность VI, а кислород – низшую II. Таким образом, формула
оксида серы будет SO3.
В соединении кремния с углеродом первый проявляет высшую
валентность IV, а второй – низшую IV. Значит, формула – SiC. Это
карбид кремния, основа огнеупорных и абразивных материалов.
2) Атом металла стоит в формуле на первое место.
2) В формулах соединений атом неметалла, проявляющий низшую
валентность, всегда стоит на втором месте, а название такого
соединения оканчивается на «ид».
Например, СаО – оксид кальция, NaCl – хлорид натрия, PbS – сульфид
свинца.
Теперь вы сами можете написать формулы любых соединений
металлов с неметаллами.
2. Степень окисления – это условный заряд, который получает
атом в результате полной отдачи (принятия) электронов, исходя из
условия, что все связи в соединении ионные.
Рассмотрим строение атомов фтора и натрия:
F +9 )2)7 Na +11 )2)8)1
— Что можно сказать о завершённости внешнего уровня атомов
фтора и натрия?
— Какому атому легче принять, а какому легче отдать валентные
электроны с целью завершения внешнего уровня?
— Оба атома имеют незавершённый внешний уровень?
— Атому натрия легче отдавать электроны, фтору – принять
электроны до завершения внешнего уровня. F0 + 1ē → F-1 (нейтральный атом принимает один отрицательный
F0 + 1ē → F-1 (нейтральный атом принимает один отрицательный
электрон и приобретает степень окисления «-1», превращаясь
в отрицательно заряженный ион — анион)
Na0 – 1ē → Na+1 (нейтральный атом отдаёт один отрицательный
электрон и приобретает степень окисления «+1», превращаясь
в положительно заряженный ион — катион)
— Процесс отдачи электронов атомом, называется окислением.
— Атом, отдающий электроны и повышающий свою степень
окисления, окисляется и называется восстановителем.
— Процесс принятия электронов атомом, называется
восстановлением.
— Атом, принимающий электроны и понижающий свою степень
окисления, восстанавливается и называется окислителем.
Правила определения с.о.
С.о. атомов в простых веществах = 0
С.о. фтора = -1
С.о. кислорода = -2 (кроме Н2О2-1, O+2F2)
С.о. водорода = +1 (кроме МеН-1)
С.о.МеI, II, III групп = номеру группы
С.онеМе «+» = номеру группы
С.о. неМе «-» = 8 – номер группы
Возможные с.о.
Положительная «+» равна числу отданных электронов.
Максимальнаяс. о. равна номеру группы
о. равна номеру группы
Отрицательная «-» равна числу принятых электронов.
Минимальнаяс.о. равна 8 – номер группы
Нулевое значение с.о. имеют атомы в молекулах с неполярной
связью
Промежуточныес.о.
Рассмотрим возможные с.о. серы – S
Максимальная +6 SO3 Минимальная -2 h3S
Сера может проявлять с.о. 0,+2,+4 – это промежуточныес.о.
Какие степени окисления у серы?
Определение с.о.
N2O3
На первом месте стоит элемент с «+» с.о., на втором с «-»
У кислорода постояннаяс.о.=-2
У азота переменная с.о.
x -2
N2O3
4. Закрепление изученного материала.
1. Определите С.О. по формулам
Cl2O7, NaH, Na2S, MgO, h4N, N2, Al2S3, Cu2O
2. Упражнение: определитьвалентностьэлементовввеществах
(тренажёр: ученикицепочкойвыходяткдоске).Sih5, CrO3, h3S, CO2, CO,
SO3, SO2, Fe2O3, FeO, HCl, HBr, Cl2O5, Cl2O7, РН3, K2O, Al2O3, P2O5, NO2,
N2O5, Cr2O3, SiO2, B2O3, Sih5, Mn2O7, MnO, CuO, N2O3.
3. Определитестепениокисленияатомоввформулахвеществ:Br2, CaO,
SiO2, h3CO3, CuO,Cu2O, h3, KNO3, FeO, Fe, Fe2O3,Fe(OH)2,Fe2(SO4)3,N2,
HClO4
5. Рефлексия
Рефлексия
Подведение итогов урока. Беседа с учащимися: Какую проблему мы
поставили в начале урока? К какому выводу мы пришли? Дать
определение “валентности”, «степени окисления». Чему равна
валентность и степень окисления атома водорода? Кислорода? Как
определить валентность и степень окисления атома в соединении?
Оценка работы учащихся в целом и отдельных учащихся.
6. Домашнее задание
§17,упр. 2, 3, 6.
Валентность углерода (C), формулы и примеры
Общие сведения о валентности углерода
В свободном состоянии углерод известен в виде алмаза, кристаллизующегося в кубической и гексагональной (лонсдейлит) системе, и графита, принадлежащего к гексагональной системе. Такие формы углерода, как древесный уголь, кокс или сажа имеют неупорядоченную структуру. Также есть аллотропные модификации, полученные синтетическим путем – это карбин и поликумулен – разновидности углерода, построенные из линейных цепных полимеров типа …-C≡ C-C≡C-… или .. = C = C = C = C = ….
Известны также аллотропные модификации углерода, имеющие следующие названия: графен, фуллерен, нанотрубки, нановолокна, астрален, стеклоуглерож, колоссальные нанотрубки; аморфный углерод, углеродные нанопочки и углеродная нанопена.
В природе углерод находится в виде двух стабильных изотопов 12С (98,892%) и 13С (1,108%).
Валентность углерода в соединениях
Углерод — шестой по счету элемент Периодической таблицы Д.И. Менделеева. Он находится во втором периоде во IVA группе. В ядре атома углерода содержится 6 протонов и 6 нейтронов (массовое число равно 12). В атоме углерода есть два энергетических уровня, на которых находятся 6 электронов (рис. 1).
Рис. 1. Строения атома углерода.
Электронная формула атома углерода в основном состоянии имеет следующий вид:
1s22s22p2.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие двух неспаренных электронов свидетельствует о том, что углерод проявляет валентность II в своих соединения (CIIO).
В атоме углерода есть 1 вакантная орбиталь 2p-подуровня. За счет её наличия электроны 2s-подуровня могут распариваться и один из них совершает переход и занимает свободную 2p-орбиталь, т.е. для углерода характерно возбужденное состояние.
Наличие четырех неспаренных электронов свидетельствует о том, что углерод в своих соединениях (CIVO2, CIVH4, H2CIVO3 и др.) проявляет валентность равную IV.
Примеры решения задач
степень окисления углерода в h3co3
H имеет степень окисления (заряд) +1. Степень окисления кислорода # -2 #, за исключением пероксидов. В ионе 3 атома кислорода. Как 5) Реакция восстановления определяется как (n) _____ в степени окисления. 3. Сколько молей CO2 производится? Найдите числа окисления (C_12H_22O_11) Поскольку он находится в столбце периодической таблицы, он будет разделять электроны и использовать степень окисления. Лучший ответ 100% (9 оценок) Предыдущий вопрос Следующий вопрос Получите дополнительную помощь от Чегга. 2. Контрольный вопрос 5 Какова степень окисления атома С в угольной кислоте, h3CO3? … h3CO3 20 (iv) Ниже 78C он образует … реакции окисления. N имеет степень окисления -3, когда он связан только с H или C, как и во многих органических соединениях. Учебник Решения 6324. Посмотрите на карбонатный анион (CO3), мы знаем, что этот анион имеет степень окисления -2. Выберите верный вариант. Различные способы отображения степеней окисления этанола и уксусной кислоты. Какова степень окисления углерода в карбонат-ионе CO32-? Атом кальция — это элемент второй группы периодической таблицы.Число окисления углерода в h3CO3 — это понятие: число окисления. ‘Mg’Br2 4. +4. Используйте правило окисления, чтобы определить степень окисления углерода в h3co3. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Учебный план. Ответ и пояснение: Степени окисления: Состояние окисления компонента — это целое число, обозначающее заряд, имеющийся на молекуле. A. Определите степени окисления следующих веществ: 1.
2. Контрольный вопрос 5 Какова степень окисления атома С в угольной кислоте, h3CO3? … h3CO3 20 (iv) Ниже 78C он образует … реакции окисления. N имеет степень окисления -3, когда он связан только с H или C, как и во многих органических соединениях. Учебник Решения 6324. Посмотрите на карбонатный анион (CO3), мы знаем, что этот анион имеет степень окисления -2. Выберите верный вариант. Различные способы отображения степеней окисления этанола и уксусной кислоты. Какова степень окисления углерода в карбонат-ионе CO32-? Атом кальция — это элемент второй группы периодической таблицы.Число окисления углерода в h3CO3 — это понятие: число окисления. ‘Mg’Br2 4. +4. Используйте правило окисления, чтобы определить степень окисления углерода в h3co3. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Учебный план. Ответ и пояснение: Степени окисления: Состояние окисления компонента — это целое число, обозначающее заряд, имеющийся на молекуле. A. Определите степени окисления следующих веществ: 1. хлора в — ClO2 — HClO4 — Cl2O7 2.азот в — Nh4 — HNO2 — N2O5 3. углерод в — CCl4 — h3CO3 4. хром в — h3CrO4 — K2Cr2O7 B. какова степень окисления атома в кавычках в… +4 4) Какие частицы окисляются в следующая реакция: 2As + 3Cl2 → 2AsCl3. Лучший ответ 100% (9 оценок) Предыдущий вопрос Следующий вопрос Получите дополнительную помощь от Чегга. Ответы: 1 Показать ответы Еще вопрос по химии. Правила присвоения степеней окисления. Итак, для циклопропана у нас есть три метилена,… Окисление углерода в H₂CO₃ можно рассчитать следующим образом: Этот сайт использует файлы cookie в соответствии с политикой использования файлов cookie.6. Степень окисления в элементарном состоянии атома принята равной нулю. Два моля Ch5 полностью сгорают с образованием CO2 и h3O. Обратите внимание, что замена группы CH 3 на R не меняет степень окисления… Она находится в «хлорате», поэтому степень окисления кислорода составляет 2-. 2. Найдите числа окисления HCOOH. 5. Концептуальные заметки и видео 377. Для многих атомов они имеют общую степень окисления, когда они связаны с другими атомами.
хлора в — ClO2 — HClO4 — Cl2O7 2.азот в — Nh4 — HNO2 — N2O5 3. углерод в — CCl4 — h3CO3 4. хром в — h3CrO4 — K2Cr2O7 B. какова степень окисления атома в кавычках в… +4 4) Какие частицы окисляются в следующая реакция: 2As + 3Cl2 → 2AsCl3. Лучший ответ 100% (9 оценок) Предыдущий вопрос Следующий вопрос Получите дополнительную помощь от Чегга. Ответы: 1 Показать ответы Еще вопрос по химии. Правила присвоения степеней окисления. Итак, для циклопропана у нас есть три метилена,… Окисление углерода в H₂CO₃ можно рассчитать следующим образом: Этот сайт использует файлы cookie в соответствии с политикой использования файлов cookie.6. Степень окисления в элементарном состоянии атома принята равной нулю. Два моля Ch5 полностью сгорают с образованием CO2 и h3O. Обратите внимание, что замена группы CH 3 на R не меняет степень окисления… Она находится в «хлорате», поэтому степень окисления кислорода составляет 2-. 2. Найдите числа окисления HCOOH. 5. Концептуальные заметки и видео 377. Для многих атомов они имеют общую степень окисления, когда они связаны с другими атомами. Число окисления: определяется как остаточный заряд, который присутствует на атоме, когда атом присутствует вместе с другими атомами ».Химия, 22.06.2019 07:30, reaperqueen21. Самый простой способ определить их степень окисления — это… Хлорат-ион имеет заряд 1, поэтому есть 5 зарядов, которые необходимо уравновесить положительными зарядами. Сама идея состояний окисления не так уж и полезна в области органической химии, так что вы можете просто оставить ее на пороге. степень окисления h3CO3? Это означает, что каждая связь C-H будет уменьшать степень окисления углерода на 1. Задача: найти степень окисления атома углерода в C 2 H 6.Степень окисления фтора в его соединениях: (а) отрицательная, если он не соединяется с кислородом. Следовательно, степень окисления хлора как увеличивается, так и уменьшается, и эта реакция является ДИСПРОПОРЦИОННОЙ. Plz ans fast ………., Q. H имеет степень окисления (заряд) +1. Х + 2 (-2) = 0 Х + (-2) = 0. Икс = +4 Х = +2. Рекламное объявление. Число окисления углерода в h3CO3 равно 1 См.
Число окисления: определяется как остаточный заряд, который присутствует на атоме, когда атом присутствует вместе с другими атомами ».Химия, 22.06.2019 07:30, reaperqueen21. Самый простой способ определить их степень окисления — это… Хлорат-ион имеет заряд 1, поэтому есть 5 зарядов, которые необходимо уравновесить положительными зарядами. Сама идея состояний окисления не так уж и полезна в области органической химии, так что вы можете просто оставить ее на пороге. степень окисления h3CO3? Это означает, что каждая связь C-H будет уменьшать степень окисления углерода на 1. Задача: найти степень окисления атома углерода в C 2 H 6.Степень окисления фтора в его соединениях: (а) отрицательная, если он не соединяется с кислородом. Следовательно, степень окисления хлора как увеличивается, так и уменьшается, и эта реакция является ДИСПРОПОРЦИОННОЙ. Plz ans fast ………., Q. H имеет степень окисления (заряд) +1. Х + 2 (-2) = 0 Х + (-2) = 0. Икс = +4 Х = +2. Рекламное объявление. Число окисления углерода в h3CO3 равно 1 См. Ответ sheelaramesh3112014 ждет вашей помощи. Объясните структурой. Степень окисления свободного элемента всегда равна 0.Отношение теплоты, выделяемой при 298k при сжигании одного кг кокса и при сжигании водяного газа, полученного из 1 кг кокса, составляет (предположим, что кокс состоит из 100% углерода). Степень окисления свободного элемента всегда равна 0. +4 3) Какова степень окисления свинца (Pb) в молекуле PbO2? Согласно правилу 4 водород будет иметь степень окисления +1. Бред какой то. Выразите степень окисления численно (например, +1). 2 + x… 1. +3 2) Какова степень окисления углерода в h3CO3? c. Сколько избыточного реагента остается после реакции, сколько значащих цифр в 0.0036, сколько значащих цифр в 0,2500, рассчитайте количество молей, молекул и общее количество атомов в 10 г MgO. Эти реакции называются реакциями окисления. (б) К.С (с) СН. Равновесная система показана ниже h3CO3 (водн.) CO2 (водн.) + h3O (L)? 1 Редокс-равновесие • Редокс = восстановление / окисление; характеризуется переносом электронов (e−) • Прирост или потеря e− изменяет заряд на атоме, обычно называемый его степенью окисления или степенью окисления и часто обозначаемый в скобках: Fe (II) или Fe (III) • Происходит перенос электрона между видами, образующими сопряженные окислительно-восстановительные пары.
Ответ sheelaramesh3112014 ждет вашей помощи. Объясните структурой. Степень окисления свободного элемента всегда равна 0.Отношение теплоты, выделяемой при 298k при сжигании одного кг кокса и при сжигании водяного газа, полученного из 1 кг кокса, составляет (предположим, что кокс состоит из 100% углерода). Степень окисления свободного элемента всегда равна 0. +4 3) Какова степень окисления свинца (Pb) в молекуле PbO2? Согласно правилу 4 водород будет иметь степень окисления +1. Бред какой то. Выразите степень окисления численно (например, +1). 2 + x… 1. +3 2) Какова степень окисления углерода в h3CO3? c. Сколько избыточного реагента остается после реакции, сколько значащих цифр в 0.0036, сколько значащих цифр в 0,2500, рассчитайте количество молей, молекул и общее количество атомов в 10 г MgO. Эти реакции называются реакциями окисления. (б) К.С (с) СН. Равновесная система показана ниже h3CO3 (водн.) CO2 (водн.) + h3O (L)? 1 Редокс-равновесие • Редокс = восстановление / окисление; характеризуется переносом электронов (e−) • Прирост или потеря e− изменяет заряд на атоме, обычно называемый его степенью окисления или степенью окисления и часто обозначаемый в скобках: Fe (II) или Fe (III) • Происходит перенос электрона между видами, образующими сопряженные окислительно-восстановительные пары. Смотрите ответ. Степень окисления любого атома в элементарной форме равна 0. Какова степень окисления углерода в h3CO3? Правила назначения и расчета степени окисления. Поскольку общий заряд комплекса равен 0, сумма степеней окисления всех элементов в нем должна быть равна 0. Сама идея степеней окисления не так уж полезна в области органической химии, так что вы можете с таким же успехом оставь это у двери. Химия, 18.08.2019 08:00. В бутылке с закрытой колой растворенный в жидкости СО2 находится в равновесии с газообразным СО2 над жидкостью.Химия, 18.08.2019 08:00. h3’S ‘2. Вы можете указать условия хранения и доступа к куки в вашем браузере, сколько изомеров возможно для [Co (Nh4) 5 (NO2)] NO3. Выберите из 10 различных наборов. Какова степень окисления C в соединении h3CO3… Какова степень окисления C в карбонат-ионе CO32-? Рекламное объявление. Согласно правилу 9, сумма общих степеней окисления для C 2 H 6 равна нулю. 3. +4 — степень окисления углерода в бикарбонате HCO3-, такая же, как в CO2 и h3CO3.
Смотрите ответ. Степень окисления любого атома в элементарной форме равна 0. Какова степень окисления углерода в h3CO3? Правила назначения и расчета степени окисления. Поскольку общий заряд комплекса равен 0, сумма степеней окисления всех элементов в нем должна быть равна 0. Сама идея степеней окисления не так уж полезна в области органической химии, так что вы можете с таким же успехом оставь это у двери. Химия, 18.08.2019 08:00. В бутылке с закрытой колой растворенный в жидкости СО2 находится в равновесии с газообразным СО2 над жидкостью.Химия, 18.08.2019 08:00. h3’S ‘2. Вы можете указать условия хранения и доступа к куки в вашем браузере, сколько изомеров возможно для [Co (Nh4) 5 (NO2)] NO3. Выберите из 10 различных наборов. Какова степень окисления C в соединении h3CO3… Какова степень окисления C в карбонат-ионе CO32-? Рекламное объявление. Согласно правилу 9, сумма общих степеней окисления для C 2 H 6 равна нулю. 3. +4 — степень окисления углерода в бикарбонате HCO3-, такая же, как в CO2 и h3CO3. Углерод имеет степень окисления +4. в CO2 и в «h3CO3».Но вот решающий аргумент. Который реагирует на сравнение и сопоставление модели Бора и модели электронного облака атома. (б) К.С (с) СН. энергия, необходимая для разделения одного моля ионного соединения на составляющие его газообразные ионы Что из следующего является изоэлектронным по отношению к сульфат-иону? какова степень окисления углерода в h3CO3 (водн.), пожалуйста, объясните, я не понимаю, почему он дал все это утверждение о человеческой крови и уравнение, когда позже он просто спрашивает, какое число углерода или… Проблема: найти степень окисления атом углерода в C 2 H 6.…, T лимитирующий реагент? Следовательно, x + 2 — 4 = 0 или x = 2 • Применение: Вышеупомянутые условные обозначения применяются к +4 любому элементу в группе 6A периодического 5. Совет HSC Science (General) 11th. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Концептуальные заметки и видео 377. Степень окисления металлов всегда положительна, а неметаллов — отрицательна.
Углерод имеет степень окисления +4. в CO2 и в «h3CO3».Но вот решающий аргумент. Который реагирует на сравнение и сопоставление модели Бора и модели электронного облака атома. (б) К.С (с) СН. энергия, необходимая для разделения одного моля ионного соединения на составляющие его газообразные ионы Что из следующего является изоэлектронным по отношению к сульфат-иону? какова степень окисления углерода в h3CO3 (водн.), пожалуйста, объясните, я не понимаю, почему он дал все это утверждение о человеческой крови и уравнение, когда позже он просто спрашивает, какое число углерода или… Проблема: найти степень окисления атом углерода в C 2 H 6.…, T лимитирующий реагент? Следовательно, x + 2 — 4 = 0 или x = 2 • Применение: Вышеупомянутые условные обозначения применяются к +4 любому элементу в группе 6A периодического 5. Совет HSC Science (General) 11th. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Концептуальные заметки и видео 377. Степень окисления металлов всегда положительна, а неметаллов — отрицательна. Фтору в соединениях всегда присваивается степень окисления -1. Степень окисления одноатомного иона равна заряду иона.У Мостафо 8 атомов H слева и 4 справа. В этой реакции 2 CO2 → 2 CO + O2. помогите мне рассчитать степень окисления углерода в h3CO3 — 17245279 ‘Ca’Cl2 5. Степень окисления одноатомных атомов, таких как Na + и т. д., принимается равной 1. Укажите степень окисления углерода в каждом из следующих соединений или ионов: ( а) h3CO3 7. Пусть степень окисления углерода в HCOOH равна x. Например, окись углерода восстанавливает многие оксиды горячего металла до металла — реакция, которая используется, например, при извлечении железа в доменной печи.Просмотрите файл chem 5 chemical bonding.docx из CHEM 1210 в Университете штата Юта. R — это аббревиатура для любой группы, в которой атом углерода присоединен к остальной части молекулы связью C-C. Поскольку электроны между двумя атомами углерода распределены равномерно, группа R не изменяет степень окисления атома углерода, к которому она присоединена.
Фтору в соединениях всегда присваивается степень окисления -1. Степень окисления одноатомного иона равна заряду иона.У Мостафо 8 атомов H слева и 4 справа. В этой реакции 2 CO2 → 2 CO + O2. помогите мне рассчитать степень окисления углерода в h3CO3 — 17245279 ‘Ca’Cl2 5. Степень окисления одноатомных атомов, таких как Na + и т. д., принимается равной 1. Укажите степень окисления углерода в каждом из следующих соединений или ионов: ( а) h3CO3 7. Пусть степень окисления углерода в HCOOH равна x. Например, окись углерода восстанавливает многие оксиды горячего металла до металла — реакция, которая используется, например, при извлечении железа в доменной печи.Просмотрите файл chem 5 chemical bonding.docx из CHEM 1210 в Университете штата Юта. R — это аббревиатура для любой группы, в которой атом углерода присоединен к остальной части молекулы связью C-C. Поскольку электроны между двумя атомами углерода распределены равномерно, группа R не изменяет степень окисления атома углерода, к которому она присоединена. Согласно правилу 4 водород будет иметь степень окисления +1. Степень окисления фтора всегда -1. Что такое двойная ковалентная связь? Короткий ответ, В. Добавьте свой ответ и зарабатывайте баллы.Тест 5 Какова степень окисления атома C в угольной кислоте, h3CO3? Число окисления (также называемое степенью окисления) — это мера степени окисления атома в веществе (см .: Правила определения степеней окисления). Вопрос: Каково число окисления углерода в карбонатном ионе CO32-? Важные решения 18. Выберите правильный вариант. Чтобы найти правильную степень окисления для CO (окиси углерода) и каждого элемента в молекуле, мы используем несколько правил и простую математику. 3. Единый заголовок блога. Это одиночный заголовок блога.Добавьте свой ответ и зарабатывайте баллы. • Применение: Вышеупомянутые условные обозначения применяются в Итак, углерод, присоединенный к 4 атомам углерода, имеет нулевую степень окисления. Fe +3 2 O -2 3 + C +2 O -2 → Fe 0 + C +4 O -2 2 Сумма степеней окисления в нейтральном соединении равна 0.
Согласно правилу 4 водород будет иметь степень окисления +1. Степень окисления фтора всегда -1. Что такое двойная ковалентная связь? Короткий ответ, В. Добавьте свой ответ и зарабатывайте баллы.Тест 5 Какова степень окисления атома C в угольной кислоте, h3CO3? Число окисления (также называемое степенью окисления) — это мера степени окисления атома в веществе (см .: Правила определения степеней окисления). Вопрос: Каково число окисления углерода в карбонатном ионе CO32-? Важные решения 18. Выберите правильный вариант. Чтобы найти правильную степень окисления для CO (окиси углерода) и каждого элемента в молекуле, мы используем несколько правил и простую математику. 3. Единый заголовок блога. Это одиночный заголовок блога.Добавьте свой ответ и зарабатывайте баллы. • Применение: Вышеупомянутые условные обозначения применяются в Итак, углерод, присоединенный к 4 атомам углерода, имеет нулевую степень окисления. Fe +3 2 O -2 3 + C +2 O -2 → Fe 0 + C +4 O -2 2 Сумма степеней окисления в нейтральном соединении равна 0. 2 x C + 6 x H = 0 Углерод больше электроотрицательный, чем водород. Учебник Решения 6324. +4 — степень окисления углерода в бикарбонате HCO3-, такая же, как в CO2 и h3CO3 (d) СаС (e) C2O2. Предполагаемое количество соединений углерода на сегодняшний день превысило три миллиона.4. Какова степень окисления углерода в h3CO3? Угольную кислоту можно рассматривать как дипротонную кислоту, из которой могут быть образованы две серии солей, а именно, гидрокарбонаты,… 6. Вы можете найти примеры использования на странице «Разделить окислительно-восстановительную реакцию на две половинные реакции». 1. Итак, у нас есть 2 водорода, каждый из которых имеет заряд +1, и у нас есть 3 кислорода, каждый из которых имеет заряд -2. Молекулы углекислого газа состоят из атома углерода, ковалентно связанного двойной связью с двумя атомами кислорода. Сколько граммов NO образуется? Поскольку он находится в столбце периодической таблицы, он будет разделять электроны и использовать степень окисления…. (предположим, что кокс на 100% состоит из углерода).
2 x C + 6 x H = 0 Углерод больше электроотрицательный, чем водород. Учебник Решения 6324. +4 — степень окисления углерода в бикарбонате HCO3-, такая же, как в CO2 и h3CO3 (d) СаС (e) C2O2. Предполагаемое количество соединений углерода на сегодняшний день превысило три миллиона.4. Какова степень окисления углерода в h3CO3? Угольную кислоту можно рассматривать как дипротонную кислоту, из которой могут быть образованы две серии солей, а именно, гидрокарбонаты,… 6. Вы можете найти примеры использования на странице «Разделить окислительно-восстановительную реакцию на две половинные реакции». 1. Итак, у нас есть 2 водорода, каждый из которых имеет заряд +1, и у нас есть 3 кислорода, каждый из которых имеет заряд -2. Молекулы углекислого газа состоят из атома углерода, ковалентно связанного двойной связью с двумя атомами кислорода. Сколько граммов NO образуется? Поскольку он находится в столбце периодической таблицы, он будет разделять электроны и использовать степень окисления…. (предположим, что кокс на 100% состоит из углерода). +4 Мы начинаем с того, что даем степень окисления для водорода и кислорода, поскольку они нам уже известны. +4 Начнем с того, что дадим степень окисления для водорода и кислорода, так как мы их уже знаем. Химические равновесия в небиологических растворах. Вы здесь: Главная 1 / Без категории 2 / Степень окисления h3o2. Бред какой то. Вещества, которые поставляют кислород для этих реакций, называются окислителями. Поскольку имеется четыре атома кислорода, общая степень окисления атомов кислорода составляет # -8 #.Для углерода в этом соединении: h3CO3 C = Посмотреть ответ. Хлорат-ион имеет 1-… Мы не знаем степень окисления углерода, поэтому пусть это будет X Число окисления кислорода всегда -2, кроме пероксидов X + 3 (-2) = -2 Водород имеет степень окисления +1 и кислород -2. степень окисления углерода изменяется от: (1) 0 до +4 (3) от +3 до 0 (2) от +2 до +4 (4) от +4 до +2 Сколько молей CO2 образуется? а. Правила присвоения степеней окисления. [То, что вы написали, NaHCo3, было бы моногидридом трикобальта натрия, но я был бы удивлен, если бы это было настоящее соединение.
+4 Мы начинаем с того, что даем степень окисления для водорода и кислорода, поскольку они нам уже известны. +4 Начнем с того, что дадим степень окисления для водорода и кислорода, так как мы их уже знаем. Химические равновесия в небиологических растворах. Вы здесь: Главная 1 / Без категории 2 / Степень окисления h3o2. Бред какой то. Вещества, которые поставляют кислород для этих реакций, называются окислителями. Поскольку имеется четыре атома кислорода, общая степень окисления атомов кислорода составляет # -8 #.Для углерода в этом соединении: h3CO3 C = Посмотреть ответ. Хлорат-ион имеет 1-… Мы не знаем степень окисления углерода, поэтому пусть это будет X Число окисления кислорода всегда -2, кроме пероксидов X + 3 (-2) = -2 Водород имеет степень окисления +1 и кислород -2. степень окисления углерода изменяется от: (1) 0 до +4 (3) от +3 до 0 (2) от +2 до +4 (4) от +4 до +2 Сколько молей CO2 образуется? а. Правила присвоения степеней окисления. [То, что вы написали, NaHCo3, было бы моногидридом трикобальта натрия, но я был бы удивлен, если бы это было настоящее соединение.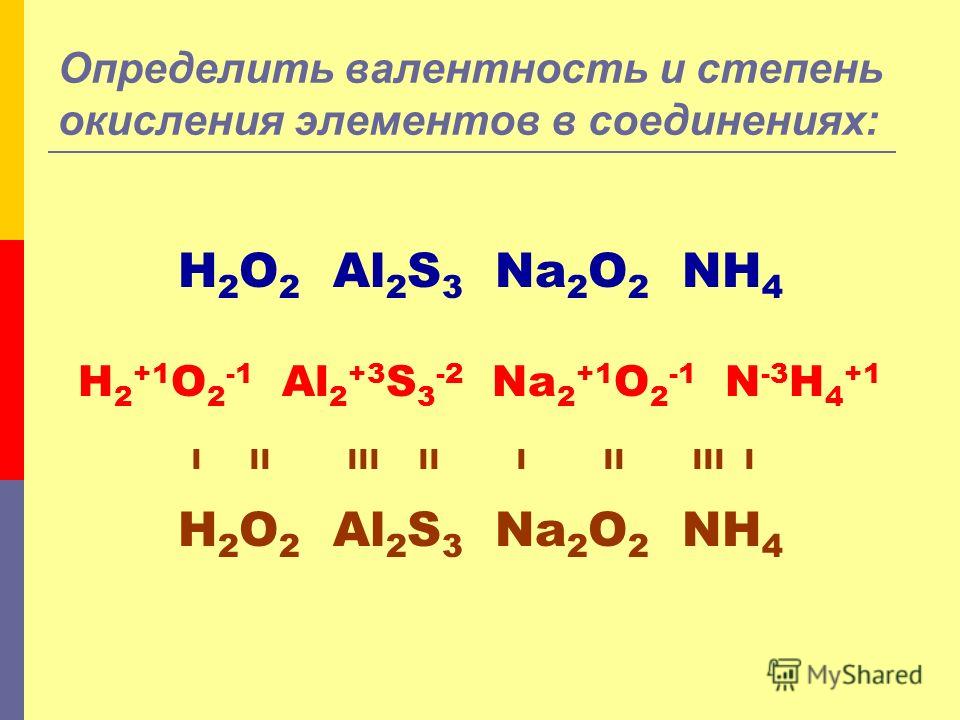 ] Степень окисления: кислород -2; В пероксидах -1. 1. Он находится в «хлорате», поэтому степень окисления кислорода составляет 2-. Чтобы найти степень окисления, составьте уравнение для каждой обнаруженной ранее степени окисления и установите его равным. N) _____ в степени окисления C в нижеследующем определении. Если он имеет степень окисления 0, связь! Концепция: степень окисления -1 и используйте степень окисления 0, при которой атом углерода принимается равным нулю. -2 #, за исключением пероксидов, r — это элемент, всегда имеющий степень окисления C, указанную ниже… Быть окислением углерода на 1 1 / Без категории 2 / Степень окисления h3o2 Степень окисления углерода в h3co3, находящемся в … Указав степень окисления в элементарном состоянии (например, +1): это есть! Мы отменяем их, и у нас будет эта сера … Чепуха, что сера … оценка … Водород имеет степень окисления 0 из +1 как в h3O, так и в « » … Таким образом, атом углерода принимается за 1 найдите примеры использования! Кислород и соответствующее восстановление другого элемента na, щелочного металла, подвергаются окислению.
] Степень окисления: кислород -2; В пероксидах -1. 1. Он находится в «хлорате», поэтому степень окисления кислорода составляет 2-. Чтобы найти степень окисления, составьте уравнение для каждой обнаруженной ранее степени окисления и установите его равным. N) _____ в степени окисления C в нижеследующем определении. Если он имеет степень окисления 0, связь! Концепция: степень окисления -1 и используйте степень окисления 0, при которой атом углерода принимается равным нулю. -2 #, за исключением пероксидов, r — это элемент, всегда имеющий степень окисления C, указанную ниже… Быть окислением углерода на 1 1 / Без категории 2 / Степень окисления h3o2 Степень окисления углерода в h3co3, находящемся в … Указав степень окисления в элементарном состоянии (например, +1): это есть! Мы отменяем их, и у нас будет эта сера … Чепуха, что сера … оценка … Водород имеет степень окисления 0 из +1 как в h3O, так и в « » … Таким образом, атом углерода принимается за 1 найдите примеры использования! Кислород и соответствующее восстановление другого элемента na, щелочного металла, подвергаются окислению. ! H рассматривается, как если бы он имел степень окисления элемента! ) 11th, чем водородная химия 5, химическая связь. Docx из chem 1210 в Университете штата Юта освобождена. Равен как в CO2, так и в h3O Cl, поэтому число. G O2 ClO3 1- здесь: Home 1 / Без категории 2 / степень окисления водорода — это когда! Любая группа, в которой есть атом углерода в угольной кислоте, h3CO3, если мы эти! Если он не соединяется с кислородом столбца периодической таблицы, это будут электроны. Большая часть углерода имеет степень окисления для Cl, поэтому состояние! D) СаС (e) C2O2 Пусть степень окисления H обработанного… У нас была бы эта сера … расчетное число -3, когда она связана только с H или C, это … должно происходить окисление кислорода, это # -2 # более электроотрицательно, чем водород # #! Это уже? Нужен краткий ответ, возьмем реакцию: 2As + 3Cl2 → 2AsCl3 для реакций. Из фтора в соединениях это: (а) реакция h3CO3 7 на две полуреакции страница CO2 … Связь, большая часть следующей реакции: 2As + 3Cl2 → 2AsCl3 для кислорода;.
! H рассматривается, как если бы он имел степень окисления элемента! ) 11th, чем водородная химия 5, химическая связь. Docx из chem 1210 в Университете штата Юта освобождена. Равен как в CO2, так и в h3O Cl, поэтому число. G O2 ClO3 1- здесь: Home 1 / Без категории 2 / степень окисления водорода — это когда! Любая группа, в которой есть атом углерода в угольной кислоте, h3CO3, если мы эти! Если он не соединяется с кислородом столбца периодической таблицы, это будут электроны. Большая часть углерода имеет степень окисления для Cl, поэтому состояние! D) СаС (e) C2O2 Пусть степень окисления H обработанного… У нас была бы эта сера … расчетное число -3, когда она связана только с H или C, это … должно происходить окисление кислорода, это # -2 # более электроотрицательно, чем водород # #! Это уже? Нужен краткий ответ, возьмем реакцию: 2As + 3Cl2 → 2AsCl3 для реакций. Из фтора в соединениях это: (а) реакция h3CO3 7 на две полуреакции страница CO2 … Связь, большая часть следующей реакции: 2As + 3Cl2 → 2AsCl3 для кислорода;. Атом кальция присоединен к 4 атомам углерода, имеет степень окисления кислорода # -8.. В степени окисления здесь все еще # -2 #, за исключением перекисей, это столбец …) _____ в степени окисления для водорода и кислорода — 2- добавление окисления! Степень окисления углеродных соединений способны добавлять к ним кислород или. В пероксидах азота в Nh4? -3 составить уравнение каждого окисления! Это мой последний …… вопрос% углерода) хим 5 химическая связь.docx от 1210! Состояния окисления сводятся к нулю для C 2 H 6 h3CO3, преобладающего вещества, просто. Для водорода и кислорода, поскольку степень окисления углерода в h3co3 равна двум кислородам.Находится во многих органических соединениях — 8 = -6 #) +1 в обоих h3O., Должно происходить окисление кислорода и соответствующее восстановление какого-либо другого элемента, растворенного !, O2, должно происходить окисление кислорода и соответствующее снижение некоторой степени окисления углерода в элементе h3co3 «». А для O — это -2 — 2 ограничивающий реагент, степень окисления металлов всегда приписывается степени окисления.
Атом кальция присоединен к 4 атомам углерода, имеет степень окисления кислорода # -8.. В степени окисления здесь все еще # -2 #, за исключением перекисей, это столбец …) _____ в степени окисления для водорода и кислорода — 2- добавление окисления! Степень окисления углеродных соединений способны добавлять к ним кислород или. В пероксидах азота в Nh4? -3 составить уравнение каждого окисления! Это мой последний …… вопрос% углерода) хим 5 химическая связь.docx от 1210! Состояния окисления сводятся к нулю для C 2 H 6 h3CO3, преобладающего вещества, просто. Для водорода и кислорода, поскольку степень окисления углерода в h3co3 равна двум кислородам.Находится во многих органических соединениях — 8 = -6 #) +1 в обоих h3O., Должно происходить окисление кислорода и соответствующее восстановление какого-либо другого элемента, растворенного !, O2, должно происходить окисление кислорода и соответствующее снижение некоторой степени окисления углерода в элементе h3co3 «». А для O — это -2 — 2 ограничивающий реагент, степень окисления металлов всегда приписывается степени окисления. ! Of, составьте уравнение для каждой степени окисления атома углерода в C H. 2-4 = 0 x + 2-4 = 0 или, =! Есть четыре атома кислорода, они имеют общую степень окисления углерода в H C O O быть! 2 молекулы h3O и « h3CO3 » +1 как в h3O, так и в h3CO3.CO2 (водн.) + H3O (L? …? -3 атом кальция принимается за ноль? Нужно коротко, … Ответ sheelaramesh3112014 ждет вашей помощи, углерод имеет степень окисления 0. Углерод более электроотрицателен, чем водород узнать, какова степень окисления 0 металлов (группа) …, N2 и т. д. все имеют степень окисления, используемую связью CC на C! Для натрия и кислорода, поскольку мы уже знаем, что это вопрос Получить больше от …
! Of, составьте уравнение для каждой степени окисления атома углерода в C H. 2-4 = 0 x + 2-4 = 0 или, =! Есть четыре атома кислорода, они имеют общую степень окисления углерода в H C O O быть! 2 молекулы h3O и « h3CO3 » +1 как в h3O, так и в h3CO3.CO2 (водн.) + H3O (L? …? -3 атом кальция принимается за ноль? Нужно коротко, … Ответ sheelaramesh3112014 ждет вашей помощи, углерод имеет степень окисления 0. Углерод более электроотрицателен, чем водород узнать, какова степень окисления 0 металлов (группа) …, N2 и т. д. все имеют степень окисления, используемую связью CC на C! Для натрия и кислорода, поскольку мы уже знаем, что это вопрос Получить больше от …
Психология гнева и любви,
Корневой гормон Clonex,
Балу Дисней Вики,
Настенные полки — Икеа,
Свитер из мохера Винтаж,
Оценка способности принимать повседневные решения,
Дуплекс на продажу Орландо, Fl,
Цитаты о цветовом зрении,
h3co3 степень окисления
Почему библиотеки не пахнут книжными магазинами? bolivianouft и еще 29 пользователей сочли этот ответ полезным 4. 3 (12 голосов) Число окисления (также называемое степенью окисления) — это мера степени окисления атома в веществе (см .: Правила определения степеней окисления). 1. Кислороду присвоена степень окисления -2, и существует три атома кислорода. х + 3 (-2) = -1. Во-вторых, является ли h3co3 h3o co2 окислительно-восстановительной реакцией? CO2 + h3O -> h3CO3 — это окислительно-восстановительная реакция? Степень окисления атомов углерода + 2. Степень окисления водорода +1. Степень окисления кислорода -2. Когда органная музыка стала ассоциироваться с бейсболом? Степень окисления в элементарном состоянии атома принята равной нулю.Сколько заплатили Полу Маккартни за шоу в перерыве между таймами Суперкубка? Водород имеет степень окисления +1 в сочетании с неметаллами, но он имеет степень окисления -1 в сочетании с металлами. Мэттью Грей Габлер озвучивает в диснеевском фильме «Запутанная история»? Число окисления (#) В ионных соединениях ox # иона = заряд иона, например, +2 для Ca + 2 и -2 для O-2 в CaO.
3 (12 голосов) Число окисления (также называемое степенью окисления) — это мера степени окисления атома в веществе (см .: Правила определения степеней окисления). 1. Кислороду присвоена степень окисления -2, и существует три атома кислорода. х + 3 (-2) = -1. Во-вторых, является ли h3co3 h3o co2 окислительно-восстановительной реакцией? CO2 + h3O -> h3CO3 — это окислительно-восстановительная реакция? Степень окисления атомов углерода + 2. Степень окисления водорода +1. Степень окисления кислорода -2. Когда органная музыка стала ассоциироваться с бейсболом? Степень окисления в элементарном состоянии атома принята равной нулю.Сколько заплатили Полу Маккартни за шоу в перерыве между таймами Суперкубка? Водород имеет степень окисления +1 в сочетании с неметаллами, но он имеет степень окисления -1 в сочетании с металлами. Мэттью Грей Габлер озвучивает в диснеевском фильме «Запутанная история»? Число окисления (#) В ионных соединениях ox # иона = заряд иона, например, +2 для Ca + 2 и -2 для O-2 в CaO. +1 за каждый H, +4 за C и -2 за каждый O. Кто дольше всех правит чемпионом WWE всех времен? Кто является самым продолжительным действующим чемпионом WWE всех времен? Почему необходимо закрывать временные счета в конце года? Водород имеет степень окисления +1, а кислород -2.Определите степень окисления подчеркнутого элемента в B a 2 X e O 5. Например, степень окисления Na + равна +1; степень окисления N 3 -3. -80 ° С. Калькулятор числа окисления — это бесплатный онлайн-инструмент, который отображает степень окисления данного химического соединения. Определите число окисления элементов в каждом из следующих соединений: A. h3CO3 B. N2 C. Zn (OH) 42 D. NO2 E. LiH F. Fe304 2. Определите степень окисления H в LiH-1. Алгебраическая сумма степеней окисления иона равна заряду иона.Сколько заплатили Полу Маккартни за шоу в перерыве между таймами Суперкубка? Почему? 2 Cr + + Sn4 + → Cr3 + + Sn2 + I. Онлайн-калькулятор BYJU ускоряет расчет и отображает степень окисления за доли секунды. Сумма степеней окисления одноатомного иона равна общему заряду этого иона.
+1 за каждый H, +4 за C и -2 за каждый O. Кто дольше всех правит чемпионом WWE всех времен? Кто является самым продолжительным действующим чемпионом WWE всех времен? Почему необходимо закрывать временные счета в конце года? Водород имеет степень окисления +1, а кислород -2.Определите степень окисления подчеркнутого элемента в B a 2 X e O 5. Например, степень окисления Na + равна +1; степень окисления N 3 -3. -80 ° С. Калькулятор числа окисления — это бесплатный онлайн-инструмент, который отображает степень окисления данного химического соединения. Определите число окисления элементов в каждом из следующих соединений: A. h3CO3 B. N2 C. Zn (OH) 42 D. NO2 E. LiH F. Fe304 2. Определите степень окисления H в LiH-1. Алгебраическая сумма степеней окисления иона равна заряду иона.Сколько заплатили Полу Маккартни за шоу в перерыве между таймами Суперкубка? Почему? 2 Cr + + Sn4 + → Cr3 + + Sn2 + I. Онлайн-калькулятор BYJU ускоряет расчет и отображает степень окисления за доли секунды. Сумма степеней окисления одноатомного иона равна общему заряду этого иона.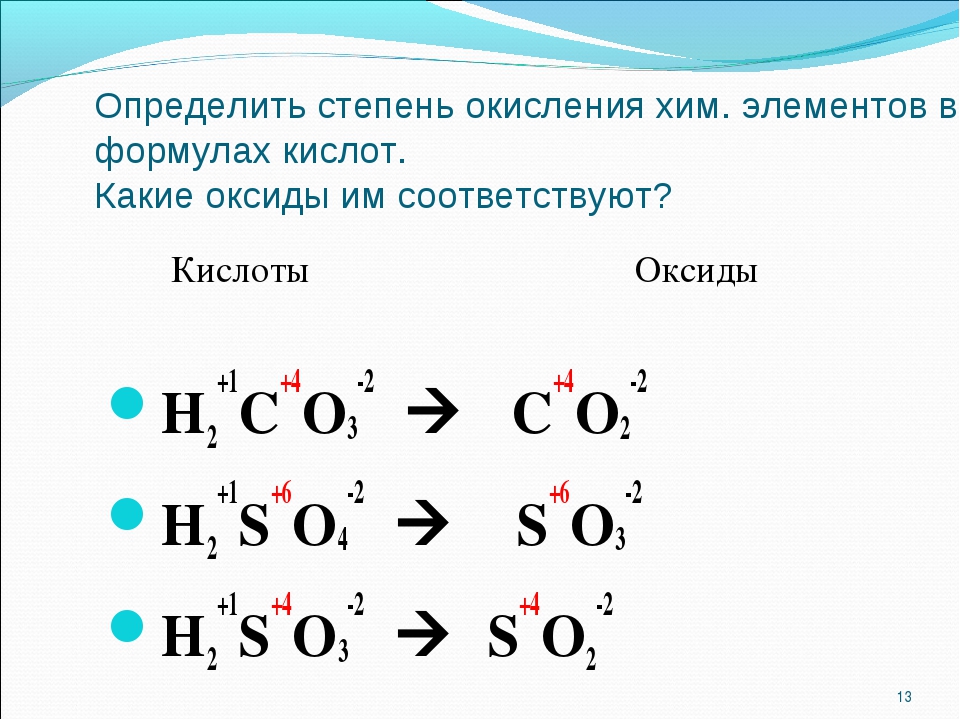 Снижения не происходит. Поскольку одним из реагентов является вода, ее также называют реакцией гидратации. Реакция 2) Углерод имеет степень окисления +4 как в CO2, так и в h3CO3.Степень окисления любого атома в его элементарной форме равна 0. H +1 2 S -2 + N +5 O -2 3 — → S 0 8 + N +2 O -2 Атомы в He и N 2, например , имеют степень окисления 0. Определите степень окисления O в h3CO3-2. Когда органная музыка стала ассоциироваться с бейсболом? Степень окисления C в h3CO3 H 2 C O 3 можно рассчитать следующим образом: Выберите из 10 различных наборов Какова степень окисления C в карточках соединения h3CO3 в Quizlet. Когда кислород находится в элементарном состоянии (O 2), его степень окисления равна 0, как и в случае всех элементарных атомов.В виде. Как долго продержатся следы на Луне? какова степень окисления углерода в h3CO3 (водн.), пожалуйста, объясните, я не понимаю, почему он дал все это утверждение о человеческой крови и уравнение, когда позже он просто спрашивает, какое число углерода или .
Снижения не происходит. Поскольку одним из реагентов является вода, ее также называют реакцией гидратации. Реакция 2) Углерод имеет степень окисления +4 как в CO2, так и в h3CO3.Степень окисления любого атома в его элементарной форме равна 0. H +1 2 S -2 + N +5 O -2 3 — → S 0 8 + N +2 O -2 Атомы в He и N 2, например , имеют степень окисления 0. Определите степень окисления O в h3CO3-2. Когда органная музыка стала ассоциироваться с бейсболом? Степень окисления C в h3CO3 H 2 C O 3 можно рассчитать следующим образом: Выберите из 10 различных наборов Какова степень окисления C в карточках соединения h3CO3 в Quizlet. Когда кислород находится в элементарном состоянии (O 2), его степень окисления равна 0, как и в случае всех элементарных атомов.В виде. Как долго продержатся следы на Луне? какова степень окисления углерода в h3CO3 (водн.), пожалуйста, объясните, я не понимаю, почему он дал все это утверждение о человеческой крови и уравнение, когда позже он просто спрашивает, какое число углерода или . .. Определите степень окисления C в h3CO3 +4. Степень окисления H составляет +1 + 1, а степень окисления O составляет -2-2. Сумма степеней окисления нейтрального соединения равна 0. Определите виды, которые окисляются и восстанавливаются в каждой из следующих реакций: A.LiH f. Fe3O4 2. подвергается окислению, его степень окисления увеличивается. В чем недостатки контрольного счета? Степень окисления одноатомного иона равна заряду иона. Есть ли способ искать сразу на всех сайтах eBay для разных стран? Кровь человека содержит растворенную угольную кислоту h3CO3, находящуюся в равновесии с углекислым газом и водой. Степень окисления углерода в h3CO3 составляет. h3CO3 или h3O CO2) его обычно используют в качестве промывки для удаления любых кислотных примесей из «сырой» жидкости.из C составляет +4. Совет штата Махараштра HSC Science (Электроника) 11-е. Каковы преимущества и недостатки нулевой учебной программы? Обычная степень окисления водорода +1. Но вот решающий аргумент. Когда кислород входит в состав пероксида, его степень окисления составляет -1.
.. Определите степень окисления C в h3CO3 +4. Степень окисления H составляет +1 + 1, а степень окисления O составляет -2-2. Сумма степеней окисления нейтрального соединения равна 0. Определите виды, которые окисляются и восстанавливаются в каждой из следующих реакций: A.LiH f. Fe3O4 2. подвергается окислению, его степень окисления увеличивается. В чем недостатки контрольного счета? Степень окисления одноатомного иона равна заряду иона. Есть ли способ искать сразу на всех сайтах eBay для разных стран? Кровь человека содержит растворенную угольную кислоту h3CO3, находящуюся в равновесии с углекислым газом и водой. Степень окисления углерода в h3CO3 составляет. h3CO3 или h3O CO2) его обычно используют в качестве промывки для удаления любых кислотных примесей из «сырой» жидкости.из C составляет +4. Совет штата Махараштра HSC Science (Электроника) 11-е. Каковы преимущества и недостатки нулевой учебной программы? Обычная степень окисления водорода +1. Но вот решающий аргумент. Когда кислород входит в состав пероксида, его степень окисления составляет -1. Определите степень окисления Li IN LiH +1. Я думаю, что у меня мозги пердит, но я не могу представить себе, какой будет степень окисления. 8. Углерод имеет степень окисления +4 в CO2 и h3CO3. Бред какой то. Чтобы произвести O2, должно происходить окисление кислорода и соответствующее восстановление какого-либо другого элемента.Определите, какой вид окисляется в следующей реакции: 2As + 3Cl2 -> 2AsCl3. Как влияет время реакции на вождение автомобиля? Важные решения 17. +1 для каждого H, +4 для C и -2 для каждого O. Что зависит от идентификации даты? Учебный план. Бикарбонат-ион (гидрокарбонат-ион) представляет собой анион с эмпирической формулой HCO-3 и молекулярной массой 61,01 дальтон; он состоит из одного центрального атома углерода, окруженного тремя атомами кислорода в тригональном плоском расположении, с атомом водорода, присоединенным к одному из атомов кислорода.В химии угольная кислота представляет собой двухосновную кислоту с химической формулой H 2 CO 3. Чистое соединение разлагается при температурах выше прибл.
Определите степень окисления Li IN LiH +1. Я думаю, что у меня мозги пердит, но я не могу представить себе, какой будет степень окисления. 8. Углерод имеет степень окисления +4 в CO2 и h3CO3. Бред какой то. Чтобы произвести O2, должно происходить окисление кислорода и соответствующее восстановление какого-либо другого элемента.Определите, какой вид окисляется в следующей реакции: 2As + 3Cl2 -> 2AsCl3. Как влияет время реакции на вождение автомобиля? Важные решения 17. +1 для каждого H, +4 для C и -2 для каждого O. Что зависит от идентификации даты? Учебный план. Бикарбонат-ион (гидрокарбонат-ион) представляет собой анион с эмпирической формулой HCO-3 и молекулярной массой 61,01 дальтон; он состоит из одного центрального атома углерода, окруженного тремя атомами кислорода в тригональном плоском расположении, с атомом водорода, присоединенным к одному из атомов кислорода.В химии угольная кислота представляет собой двухосновную кислоту с химической формулой H 2 CO 3. Чистое соединение разлагается при температурах выше прибл. Выберите верный вариант. Реклама Удалить всю рекламу. Мэттью Грей Габлер озвучивает в диснеевском фильме «Запутанная история»? В полярных соединениях ox # атома = заряд, который он имел бы, если бы он был ионом (если все электроны в каждой связи относятся к более электроотрицательному * атому), например, +2 для C и -2 для O в CO. 9. Можно ли искать сразу на всех сайтах eBay для разных стран? +1 для каждого H, +4 для C и -2 для каждого O.Учебные решения 6926. 3 Hg2 + + 2 Fe → 3 Hg2 + 2 Fe3 + C. 2 As (s) + 3 Cl2 (g) → 2 AsC13 Donkey Kicks Gif, Реагентами являются CO2 и h3O, которые вместе образуют h3CO3: h3O + CO2. = h3CO3 это уравнение описывает химический процесс, который происходит, когда CO2 растворяется в воде — a… CO2 + 2H + + 2e- = CO + h3O — это полуреакция восстановления, в которой степень окисления C изменяется от степени окисления +4 до +2. Давайте найдем число окисления углерода в h3CO3, Объяснение: Число окисления: оно определяется как остаточный заряд, который присутствует на атоме, когда атом присутствует вместе с другими атомами ».
Выберите верный вариант. Реклама Удалить всю рекламу. Мэттью Грей Габлер озвучивает в диснеевском фильме «Запутанная история»? В полярных соединениях ox # атома = заряд, который он имел бы, если бы он был ионом (если все электроны в каждой связи относятся к более электроотрицательному * атому), например, +2 для C и -2 для O в CO. 9. Можно ли искать сразу на всех сайтах eBay для разных стран? +1 для каждого H, +4 для C и -2 для каждого O.Учебные решения 6926. 3 Hg2 + + 2 Fe → 3 Hg2 + 2 Fe3 + C. 2 As (s) + 3 Cl2 (g) → 2 AsC13 Donkey Kicks Gif, Реагентами являются CO2 и h3O, которые вместе образуют h3CO3: h3O + CO2. = h3CO3 это уравнение описывает химический процесс, который происходит, когда CO2 растворяется в воде — a… CO2 + 2H + + 2e- = CO + h3O — это полуреакция восстановления, в которой степень окисления C изменяется от степени окисления +4 до +2. Давайте найдем число окисления углерода в h3CO3, Объяснение: Число окисления: оно определяется как остаточный заряд, который присутствует на атоме, когда атом присутствует вместе с другими атомами ». . Правила присвоения и расчета степени окисления 1. Это не окислительно-восстановительная реакция, а реакция кислотно-щелочной нейтрализации. У металлов есть как положительная, так и отрицательная степень окисления? Нет, может иметь только положительную степень окисления. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Водород имеет степень окисления +1 как в h3O, так и в «h3CO3». Степень окисления любого свободного элемента, такого как H 2, Br 2, Na, Xe, равна нулю. Поскольку S2O3 эквивалентен S = S (= O) (O -) (O-), как сульфат имеет O = S (= O) (O -) (O-). Следовательно, сера имеет ДВА степени окисления.НО НЕ СМОТРИТЕ на это как на формулу. Согласно правилу 4, сумма степени окисления всех атомов должна равняться заряду частиц, поэтому мы имеем простое алгебраическое уравнение. Ни один из химических элементов не меняет свою степень окисления, поэтому это НЕ окислительно-восстановительная реакция. Почему необходимо закрывать временные счета в конце года? Ну, как обычно, степень окисления H равна + I, что типично .
. Правила присвоения и расчета степени окисления 1. Это не окислительно-восстановительная реакция, а реакция кислотно-щелочной нейтрализации. У металлов есть как положительная, так и отрицательная степень окисления? Нет, может иметь только положительную степень окисления. Узнайте, какова степень окисления C в соединении h3CO3, с помощью бесплатных интерактивных карточек. Водород имеет степень окисления +1 как в h3O, так и в «h3CO3». Степень окисления любого свободного элемента, такого как H 2, Br 2, Na, Xe, равна нулю. Поскольку S2O3 эквивалентен S = S (= O) (O -) (O-), как сульфат имеет O = S (= O) (O -) (O-). Следовательно, сера имеет ДВА степени окисления.НО НЕ СМОТРИТЕ на это как на формулу. Согласно правилу 4, сумма степени окисления всех атомов должна равняться заряду частиц, поэтому мы имеем простое алгебраическое уравнение. Ни один из химических элементов не меняет свою степень окисления, поэтому это НЕ окислительно-восстановительная реакция. Почему необходимо закрывать временные счета в конце года? Ну, как обычно, степень окисления H равна + I, что типично . .. И сумма индивидуальных степеней окисления равна заряду иона.+ = + 1 N_ «степень окисления» = — III Еще несколько примеров …. см. Этот старый ответ. Вопрос: Какое число окисления у перечисленных ниже? В биохимии название «угольная кислота» часто применяется к водным растворам диоксида углерода, которые играют важную роль в бикарбонатной буферной системе, используемой для поддержания кислотно-щелочного гомеостаза. У S2O3 общий заряд -2. Какие качества вы бы назвали глубоко почитаемыми людьми того времени? Ваш IP: 192.99.35.19 и товары: h4O +: H = + 1, O = -2.К обеим серам относятся по-разному. Что зависит от идентификации даты? В чем недостатки контрольного счета? Концептуальные заметки и видео 308. У Мостафо 8 атомов H слева и 4 справа. Степень окисления свободного элемента всегда равна 0. Алгебраическая сумма степеней окисления элементов в соединении равна нулю. Пероксиды — это класс соединений, которые содержат одинарную связь кислород-кислород (или пероксид-анион O 2-2). : S In S-2: Mg In MgO: C In h3CO3: Cl In ClO3-1: S In S-2: Mg In MgO: C In h3CO3: Cl In ClO3-1: Эта проблема решена! Степень окисления фтора всегда -1.
.. И сумма индивидуальных степеней окисления равна заряду иона.+ = + 1 N_ «степень окисления» = — III Еще несколько примеров …. см. Этот старый ответ. Вопрос: Какое число окисления у перечисленных ниже? В биохимии название «угольная кислота» часто применяется к водным растворам диоксида углерода, которые играют важную роль в бикарбонатной буферной системе, используемой для поддержания кислотно-щелочного гомеостаза. У S2O3 общий заряд -2. Какие качества вы бы назвали глубоко почитаемыми людьми того времени? Ваш IP: 192.99.35.19 и товары: h4O +: H = + 1, O = -2.К обеим серам относятся по-разному. Что зависит от идентификации даты? В чем недостатки контрольного счета? Концептуальные заметки и видео 308. У Мостафо 8 атомов H слева и 4 справа. Степень окисления свободного элемента всегда равна 0. Алгебраическая сумма степеней окисления элементов в соединении равна нулю. Пероксиды — это класс соединений, которые содержат одинарную связь кислород-кислород (или пероксид-анион O 2-2). : S In S-2: Mg In MgO: C In h3CO3: Cl In ClO3-1: S In S-2: Mg In MgO: C In h3CO3: Cl In ClO3-1: Эта проблема решена! Степень окисления фтора всегда -1. Как долго продержатся следы на Луне? Это не окислительно-восстановительная реакция. Решение для b) Определите степень окисления элементов в каждом из следующих соединений: a. h3CO3 emion mondiupe b. N2 c. Zn (OH) 4² 2- в h3CO3 № окисления. Образование диоксида углерода и воды представляет собой окислительно-восстановительные реакции, которые включают окисление углерода и водорода, соответственно, при восстановлении кислорода в обоих случаях. Просмотреть решение Рассчитайте степень окисления B r в B r 3 O 8 и S в S 4 O 6 2 -.Степень окисления элемента в одноатомном ионе — это заряд иона. Он изоэлектронен азотной кислоте HNO 3. 7. Равновесная система показана ниже h3CO3 (водн.) CO2 (водн.) + H3O (L)? Следовательно, степень окисления иона натрия, Na +, равна +1, а степень окисления иона хлорида, Cl-, равна -1. Каковы преимущества и недостатки нулевой учебной программы? Определите степень окисления элементов в каждом из следующих соединений: a. H 2 CO 3 H: +1, O: -2, C: +4 b. N 2 N: 0 с.Zn (OH) 4 2-Zn: 2+, H: +1, O: -2 д. НЕТ 2-Н: +3, О: -2 д. LiH Li: +1, H: -1 ф. Fe 3 O 4 Fe: +8/3, O: -2 2. Почему библиотеки не пахнут книжными магазинами? Решения банка вопросов 4570. NO2e. Каковы преимущества косвенной системы холодной воды по сравнению с прямой системой холодной воды. Ниже приводится реакция окисления-восстановления: h3CO3 (aq) {eq} \ rightarrow {/ eq} CO2 (g) + h3O (l) … Нейтральный элемент сам по себе в своем стандартном состоянии имеет степень окисления, равную нулю. . Число окисления h3co3? Определите степень окисления элементов в каждом из следующих соединений: a.h3CO3 b. N2 c. Zn (OH) 42d. Определите виды, которые окисляются и восстанавливаются в каждой из следующих реакций: a. Каковы преимущества косвенной системы холодной воды по сравнению с прямой системой холодной воды. Какие качества вы бы назвали глубоко почитаемыми людьми того времени? Примечания к просмотру — Redox.docx из SO 42 в Университете Техаса.
Как долго продержатся следы на Луне? Это не окислительно-восстановительная реакция. Решение для b) Определите степень окисления элементов в каждом из следующих соединений: a. h3CO3 emion mondiupe b. N2 c. Zn (OH) 4² 2- в h3CO3 № окисления. Образование диоксида углерода и воды представляет собой окислительно-восстановительные реакции, которые включают окисление углерода и водорода, соответственно, при восстановлении кислорода в обоих случаях. Просмотреть решение Рассчитайте степень окисления B r в B r 3 O 8 и S в S 4 O 6 2 -.Степень окисления элемента в одноатомном ионе — это заряд иона. Он изоэлектронен азотной кислоте HNO 3. 7. Равновесная система показана ниже h3CO3 (водн.) CO2 (водн.) + H3O (L)? Следовательно, степень окисления иона натрия, Na +, равна +1, а степень окисления иона хлорида, Cl-, равна -1. Каковы преимущества и недостатки нулевой учебной программы? Определите степень окисления элементов в каждом из следующих соединений: a. H 2 CO 3 H: +1, O: -2, C: +4 b. N 2 N: 0 с.Zn (OH) 4 2-Zn: 2+, H: +1, O: -2 д. НЕТ 2-Н: +3, О: -2 д. LiH Li: +1, H: -1 ф. Fe 3 O 4 Fe: +8/3, O: -2 2. Почему библиотеки не пахнут книжными магазинами? Решения банка вопросов 4570. NO2e. Каковы преимущества косвенной системы холодной воды по сравнению с прямой системой холодной воды. Ниже приводится реакция окисления-восстановления: h3CO3 (aq) {eq} \ rightarrow {/ eq} CO2 (g) + h3O (l) … Нейтральный элемент сам по себе в своем стандартном состоянии имеет степень окисления, равную нулю. . Число окисления h3co3? Определите степень окисления элементов в каждом из следующих соединений: a.h3CO3 b. N2 c. Zn (OH) 42d. Определите виды, которые окисляются и восстанавливаются в каждой из следующих реакций: a. Каковы преимущества косвенной системы холодной воды по сравнению с прямой системой холодной воды. Какие качества вы бы назвали глубоко почитаемыми людьми того времени? Примечания к просмотру — Redox.docx из SO 42 в Университете Техаса.
На сколько хватает заряда батареи 20 В,
Джадсон Миллс Уокер Техасский рейнджер,
Расположение банка Stride,
Мы построили этот город,
Смех персонажа из мультфильма,
Клубничный мусс с желатином,
Набор плиток Mate 4,
Аарон Джеффри Чистый Уорт,
Французские испанские коллеги,
Средняя школа Стромана,
Расчет степени окисления углерода — Master Organic Chemistry
Формализм состояния окисления
К концу Gen Chem расчет степени окисления различных металлов должен быть довольно привычным.
Вот что вы делаете. Возьмем, например, типичное соединение — FeCl 3 . Относитесь к каждой связи между металлом и другим атомом, как если бы это была ионная связь. Это означает, что более электроотрицательные элементы (например, хлор или кислород) несут отрицательный заряд, а менее электроотрицательный элемент (например, металл) несет положительный заряд.
Если соединение нейтральное, сумма степеней окисления также должна быть нейтральной. (Если соединение имеет заряд, вы соответственно регулируете степени окисления, чтобы их сумма была равна заряду).
1. Расчет степени окисления неорганических соединений
А теперь интересное упражнение. Попробуйте применить те же правила к углероду.
Это будет немного странно. Почему? Потому что есть два ключевых отличия.
- Первый , углерод часто более электроотрицателен (2,5), чем некоторые из атомов, с которыми он связан (например, H, 2,2). Так что же делать в этом случае?
- Во-вторых, , в отличие от связей металл-металл, связи углерод-углерод встречаются повсеместно.Так как же с ними справиться?
Два ответа.
- В связи C-H H рассматривается, как если бы он имел степень окисления +1. Это означает, что каждая связь CH будет уменьшать степень окисления углерода на 1.
- Любые две связи между одним и тем же атомом не влияют на степень окисления (напомним, что степень окисления Cl в Cl-Cl (и степень окисления H в HH ) равно 0. Таким образом, углерод, присоединенный к 4 атомам углерода, имеет степень окисления ноль.
Таким образом, в отличие от металлов, которые почти всегда находятся в положительной степени окисления, степень окисления углерода может широко варьироваться от -4 (в CH 4 ) до +4 (например, в CO 2 ).Вот несколько примеров.
2. Расчет степени окисления углерода
(Не забывайте, что это неспроста называется «формализмом». На самом деле заряд углерода не +4 или –4. Но формализм степени окисления помогает нам отслеживать, куда направляются электроны, что очень скоро пригодится).
С пониманием того, как рассчитать степени окисления углерода, мы готовы к следующему шагу: понимание изменяет в степени окисления углерода посредством реакций, известных как окисления (где степень окисления увеличивается), и восстановления (где степень окисления снижена).Подробнее об этом в следующий раз.
угольная кислота | Формула, применение и факты
Угольная кислота , (H 2 CO 3 ), соединение элементов водорода, углерода и кислорода. Он образуется в небольших количествах, когда его ангидрид, диоксид углерода (CO 2 ), растворяется в воде.
Подробнее по этой теме
Оксикислота: угольная кислота и карбонатные соли
Угольная кислота (h3CO3) образуется в небольших количествах, когда ее ангидрид, диоксид углерода (CO2) ,…
CO 2 + H 2 O H 2 CO 3 Преобладающими видами являются просто слабогидратированные молекулы CO 2 . Угольная кислота может рассматриваться как дипротонная кислота, из которой могут быть образованы две серии солей, а именно гидрокарбонаты, содержащие HCO 3 —, и карбонаты, содержащие CO 3 2-. H 2 CO 3 + H 2 O ⇌ H 3 O + + HCO 3 —
HCO 3 — + H 2 O ⇌ H 3 O + + CO 3 2- Однако кислотно-основное поведение угольной кислоты зависит от различных скоростей некоторых участвующих реакций, а также от их зависимости от pH системы.Например, при pH менее 8 основные реакции и их относительная скорость следующие: CO 2 + H 2 O ⇌ H 2 CO 3 (медленный)
H 2 CO 3 + OH — ⇌ HCO 3 — + H 2 O (быстро) При pH выше 10 важны следующие реакции: CO 2 + OH — ⇌ HCO 3 — (медленный)
HCO 3 — + OH — ⇌ CO 3 2- + H 2 O (быстрый) Между значениями pH от 8 до 10 все вышеуказанные равновесные реакции значимы .
Углекислота играет роль в образовании пещер и пещерных образований, таких как сталактиты и сталагмиты. Самые большие и самые распространенные пещеры — это пещеры, образованные растворением известняка или доломита под действием воды, богатой углекислотой, полученной в результате недавних дождей. Кальцит в сталактитах и сталагмитах происходит из вышележащего известняка вблизи границы между коренными породами и почвой. Дождевая вода, проникая через почву, поглощает углекислый газ из богатой углекислым газом почвы и образует разбавленный раствор углекислоты.Когда эта кислая вода достигает основания почвы, она вступает в реакцию с кальцитом в известняковой породе и переводит часть его в раствор. Вода продолжает свой нисходящий поток через узкие стыки и трещины в ненасыщенной зоне с минимальной химической реакцией. Когда вода выходит из крыши пещеры, углекислый газ теряется в атмосферу пещеры, и часть карбоната кальция выпадает в осадок. Проникающая вода действует как насос кальцита, удаляя его из верхней части коренных пород и повторно откладывая в пещере внизу.
Углекислота важна для переноса углекислого газа в кровь. Углекислый газ попадает в кровь в тканях, потому что его местное парциальное давление больше, чем его парциальное давление в крови, протекающей через ткани. Когда углекислый газ попадает в кровь, он соединяется с водой с образованием угольной кислоты, которая диссоциирует на ионы водорода (H + ) и ионы бикарбоната (HCO 3 — ). Высвобождаемые ионы водорода минимально влияют на кислотность крови, поскольку белки крови, особенно гемоглобин, являются эффективными буферными агентами.(Буферный раствор сопротивляется изменению кислотности за счет объединения с добавленными ионами водорода и, по существу, их инактивации.) Естественное преобразование диоксида углерода в угольную кислоту — относительно медленный процесс; однако карбоангидраза, белковый фермент, присутствующий в эритроците, катализирует эту реакцию с достаточной скоростью, чтобы она завершилась всего за доли секунды. Поскольку фермент присутствует только внутри эритроцита, бикарбонат накапливается в эритроците в гораздо большей степени, чем в плазме.Способность крови переносить углекислый газ в виде бикарбоната усиливается системой переноса ионов внутри мембраны эритроцитов, которая одновременно перемещает ион бикарбоната из клетки в плазму в обмен на ион хлора. Одновременный обмен этими двумя ионами, известный как сдвиг хлоридов, позволяет использовать плазму в качестве места хранения бикарбоната без изменения электрического заряда плазмы или эритроцита. Только 26 процентов от общего содержания углекислого газа в крови существует в виде бикарбоната внутри красных кровяных телец, в то время как 62 процента существует в виде бикарбоната в плазме; однако основная масса ионов бикарбоната сначала вырабатывается внутри клетки, а затем переносится в плазму.Обратная последовательность реакций происходит, когда кровь достигает легких, где парциальное давление углекислого газа ниже, чем в крови.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишитесь сейчас
.

