Содержание
Углеводороды гомологические ряды — Справочник химика 21
Составьте молекулярную формулу углеводорода гомологического ряда метана, содержащего а) 15 атомов углерода б) 20 атомов углерода. [c.133]
Номенклатура насыщенных углеводородов. Гомологический ряд алканов, структ ные изомеры. Углеводородные заместители. [c.188]
Составьте молекулярную формулу углеводорода гомологического ряда метана, в молекуле которого а) 40 атомов водорода [c.133]
Приведите общую формулу углеводородов гомологического ряда алкенов. Какие виды структурной изомерии характерны для алкенов [c.16]
Ароматические углеводороды (арены) можно рассматривать как производные бензола СбН . Общая формула углеводородов гомологического ряда бензола С Н2 -б (при и 5= 6). [c.209]
Составьте молег.улярную формулу углеводорода гомологического ряда метана, содержащего а) 18 атомов водорода [c. 133]
133]
С большей точностью можно рассчитать предел воспламенения какого-либо вещества, если известны пределы воспламенения не менее двух его гомологов. Зависимость 1/фп=/(С) для веществ одного и того же гомологического ряда представляет собой прямую. Следовательно, если для каждого из изученных углеводородов гомологического ряда составить условное уравнение вида [c.17]
Углеводороды (гомологические ряды) [c.54]
В соответствии со сказанным выше следует внести некоторые уточнения в употребление терминов парафин и церезин и указать в каком значении они будут применяться в дальнейшем изложении. Название церезин будет сохранено только за соответствующими техническими или товарными продуктами. Парафины как товарные и технические продукты будут называться технический парафин или товарный парафин . Термин же парафин будет применяться как обобщающее понятие для обозначения все твердых кристаллических углеводородов, входящих в состав различных нефтяных продуктов, независимо от их молекулярного веса и химического строения, а также от того, в какие исходные нефтяные продукты — в дистиллятные или остаточные, в технические парафины или церезины, либо в какие-нибудь еще продукты эти углеводороды входят.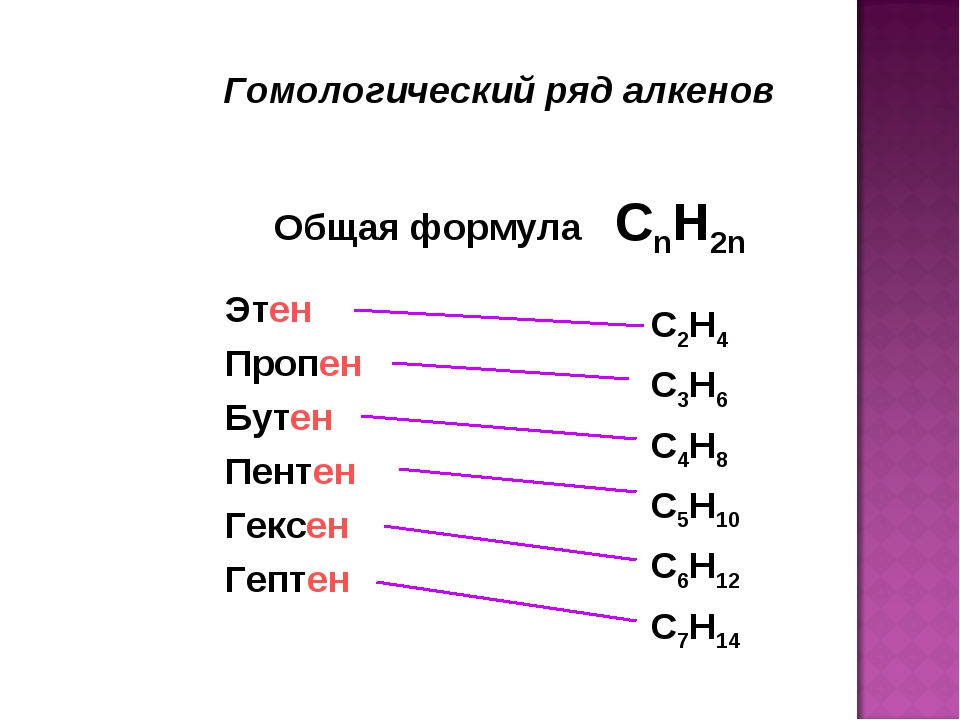 Название парафин может при необходимости поясняться тем или иным определением, например легкоплавкий , мелкокристаллический и др. Чтобы избежать смешивания понятия парафин в указанном выше смысле со старым термином парафин , обозначавшим в прежней литературе углеводороды гомологического ряда алканов и встречающимся в этом значении в некоторых литературных источниках, особенно зарубежных, и в настоящее время, то здесь будет использована установленная в органической химии терминология и углеводороды ряда алканов будут именоваться только алканами. Все же другие применявшиеся иногда в литературе для этих углеводородов названия (например парафиновые, метановые, жирного ряда и пр.) употребляться не будут. [c.80]
Название парафин может при необходимости поясняться тем или иным определением, например легкоплавкий , мелкокристаллический и др. Чтобы избежать смешивания понятия парафин в указанном выше смысле со старым термином парафин , обозначавшим в прежней литературе углеводороды гомологического ряда алканов и встречающимся в этом значении в некоторых литературных источниках, особенно зарубежных, и в настоящее время, то здесь будет использована установленная в органической химии терминология и углеводороды ряда алканов будут именоваться только алканами. Все же другие применявшиеся иногда в литературе для этих углеводородов названия (например парафиновые, метановые, жирного ряда и пр.) употребляться не будут. [c.80]
В настоящее время уже никто не сомневается, что твердые углеводороды нефти и озокерита, получившие название парафины и церезины, состоят не полностью из углеводородов гомологического ряда метана (нормального и разветвленного строения), а представляют смесь их с углеводородами гибридного или смешанного строения. Содержание гибридных структур углеводородов в смесях и их строение зависят от химической природы нефти, из которой твердые углеводороды выделены, и от методов выделения (или технологии переработки нефти). Таким образом, даже наиболее простая составляющая высокомолекулярной части нефти представляет собой сложную смесь, которую нелегко разделить методами, не вызывающими химических изменений. Поэтому стали все чаще и успешнее применять физические методы разделения и исследования твердых углеводородов нефти. [c.84]
Содержание гибридных структур углеводородов в смесях и их строение зависят от химической природы нефти, из которой твердые углеводороды выделены, и от методов выделения (или технологии переработки нефти). Таким образом, даже наиболее простая составляющая высокомолекулярной части нефти представляет собой сложную смесь, которую нелегко разделить методами, не вызывающими химических изменений. Поэтому стали все чаще и успешнее применять физические методы разделения и исследования твердых углеводородов нефти. [c.84]
Мольная теплоемкость ароматических СпН п-в) и алифатических углеводородов гомологических рядов С Я2п и С Я2 +2 в твердом или жидком состоянии в первом приближении может быть рассчитана по уравнению Шелеста [c.112]
СНа С ( HJ — СН = СН2 — ненасыщенный углеводород гомологического ряда диенов С Н2 2> бесцветная жидкость, т. кип. 34,076° С растворим в спирте. В зависимости от условий, И. способен образовывать полимеры с линейным или разветвленным цис- и транс-строением макромолекул — изопреновые каучуки. И. применяют для получения синтетических каучуков как самостоятельно, так и в смеси с другими мономерами. [c.104]
И. применяют для получения синтетических каучуков как самостоятельно, так и в смеси с другими мономерами. [c.104]
Масс-спектрометрия органических соединений предназначена преимущественно для решения структурных проблем [12П. Благодаря своим особенностям масс-спектрометрия дает информацию о молекулах, хорошо дополняющую данные других спектроскопических методов. Кроме того, масс-спектрометрия предназначена для проведения количественного изотопного анализа [1201 и для анализа смесей однотипных веществ (например, углеводородов гомологического ряда). Однако использование ее в структурном анализе, где масс-спектрометрия дает информацию о молекулярном весе, брутто- й структурной рмулах, является доминирующим. [c.288]
Химические свойства. Как уже было указано, предельные, или насыщенные, углеводороды — это вещества, трудно вступающие в реакции при обычных температурах. Для всех углеводородов гомологического ряда метана характерна неспособность к реакциям присоединения. При определенных условиях они вступают в реакции замещения, в результате которых атомы водорода их молекул замещаются другими атомами или группами и образуются производные углеводородов. При энергичном воздействии температур или химических реагентов молекулы углеводородов разлагаются с разрушением углеродного скелета. [c.52]
При определенных условиях они вступают в реакции замещения, в результате которых атомы водорода их молекул замещаются другими атомами или группами и образуются производные углеводородов. При энергичном воздействии температур или химических реагентов молекулы углеводородов разлагаются с разрушением углеродного скелета. [c.52]
Предельные углеводороды. Гомологический ряд предельных углеводородов. Метан, строение, природа химической связи, химические свойства. [c.330]
I. Ациклические соединения, иначе называемые соединениями жирного ряда или алифатическими соединениями. Сюда относятся все углеводороды и нх производные, не содержащие в молекулах колец, или циклов, а только так называемые открытые цепи углеродных атомов. Название жирный ряд является устарелым, хотя все еще очень употребительным, и произошло от того, что к этому классу соединений относятся природные жиры. Ациклические соединения разделяются на производные углеводородов гомологического ряда метана, общей формулы С и. 2п+2, и на соединения других гомологических рядов, изологичных данному, т. е. содержащих в молекулах кратные (двойные или тройные) связи атомов углерода. [c.148]
2п+2, и на соединения других гомологических рядов, изологичных данному, т. е. содержащих в молекулах кратные (двойные или тройные) связи атомов углерода. [c.148]
При выполнении условий, необходимых для количественной оценки (разд. 1.2), в случае газохроматографического анализа химически сходных веществ (например, углеводородов гомологического ряда) доли площадей [c.292]
Следовательно, при сформулированном подходе задача определения теплоты образования сложной фракции углеводородов сводится к отысканию п модельных углеводородов и определению относительного весового содержания углеводородов гомологических рядов во всей фракции. Подобная задача в настоящее время успешно решается при помощи хроматографии и масс-спектрометрии. [c.164]
Какие виды изомерии характерны для углеводородов гомологического ряда ацетилена [c.326]
Однако из уравнения (9.7) следует, что десорбция двух углеводородов гомологического ряда будет описываться единой кинетической кривой, если соблюдается следующее условие [c. 195]
195]
Если скорость десорбции всех углеводородов гомологического ряда может быть отражена при соответствующих правильно выбранных температурах одной кинетической кривой, следовательно, для каждого углеводорода существуют характерные температуры, имеющие первостепенное значение для выбора оптимального температурного режима процесса [26]. [c.198]
Пропилен и последующие углеводороды гомологического ряда этилена реагируют с галогеноводородами согласно правилу В. В. Марковникова [c.420]
Алкены, или олефины,— цепные ненасыщенные углеводороды с одной двойной связью С =С в молекулах. Их называют также непредельными углеводородами гомологического ряда этилена. Общая суммарная формула Hs . [c.463]
Мольная теплоемкость ароматических С Н2 -е и алифатических углеводородов гомологических рядов С Н2п и С Н2 +2 в твердом или жидком состоянии (по Шелесту) [c.210]
Выбор стационарной фазы определяется качественным и количественным составом смеси. На неполярной жидкой фазе смесь разделяется в зависимости от числа углеродных атомов у ее компонентов, и поэтому такая жидкая фаза оказывается удобной для разделения углеводородов гомологического ряда (например, метана, этана, пропана и т. д.). Порядок вымывания отдельных групп угле водородов на фазах данного типа следующий изопарафины. олефины, парафины, нафтены. [c.118]
На неполярной жидкой фазе смесь разделяется в зависимости от числа углеродных атомов у ее компонентов, и поэтому такая жидкая фаза оказывается удобной для разделения углеводородов гомологического ряда (например, метана, этана, пропана и т. д.). Порядок вымывания отдельных групп угле водородов на фазах данного типа следующий изопарафины. олефины, парафины, нафтены. [c.118]
Предельные углеводороды, или парафины. Они характеризуются малой реакционной способностью. Это углеводороды гомологического ряда метана [c.200]
Какова общая формула углеводородов гомологического ряда циклоалканов Напишите структурные формулы изомерных циклоалканов состава С4Н8 и С5Н10 и назовите их. [c.16]
Какова общая формула углеводородов гомологического ряда алкенов Объясните причину изомерии различных гомологических рядов на примере пропилена и циклопропана. Укажите типы связей в йтих соединениях. [c.18]
Какова общая формула углеводородов гомологического ряда алкинов Напишите структурные формулы алкинов состава sHs и назовите их по рациональной и современной заместительной номенклатурам.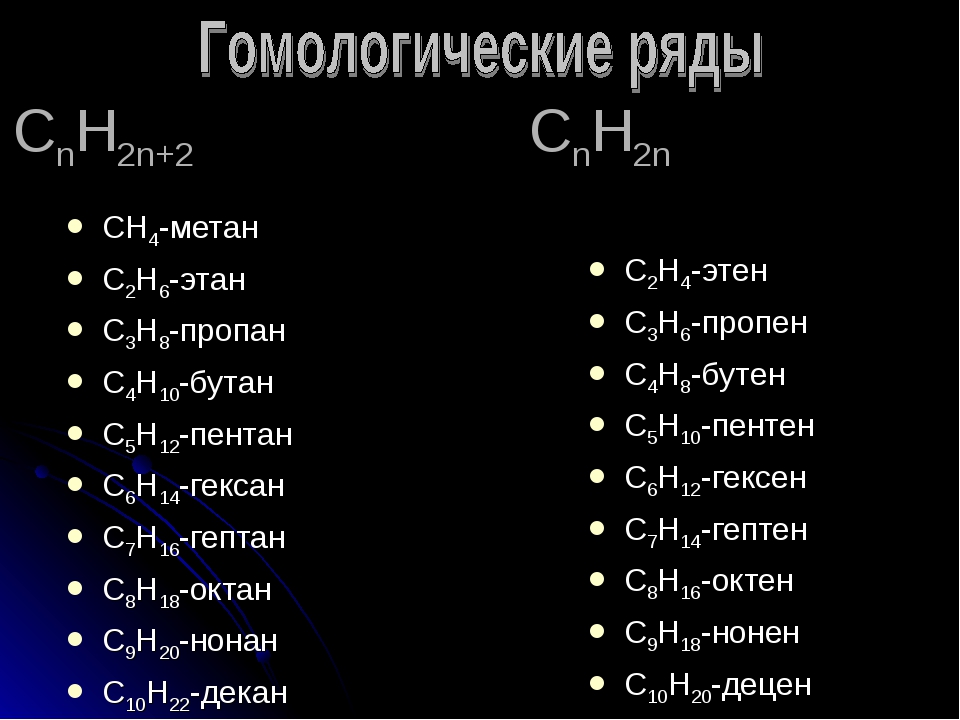 [c.26]
[c.26]
Какова общая формула углеводородов гомологического ряда бензола К каким другим гомологиче- [c.32]
Отличие химии кремния от углерода в основном обусловлено большими размерами его атома и возможностью использования свободных Зй-орбиталей. Из-за дополнительного связывания (по донорно-акцепторному механизму) связи кремния с кислородом 81—0—31 и фтором 51—Р (табл. 17.23) более прочны, чем у углерода, а из-за большего размера атома 51 по сравнению с атомом С связи 51—И и 51—51 менее прочны, чем у углерода. Атомы кремния практически не способны давать цепи. Аналогичный углеводородам гомологический ряд кремневодородов 51пН2я-(-2 (си-ланы) получен лишь до состава 514Ню. Из-за большего размера у атома 51 слабо выражена и способность к л-перекрыванию, поэтому не только тройные, но и двойные связи для него малохарактерны. [c.465]
Сырая нефть представляет собой нерастворимую в аоде маслянистую коричневую пли черную жидкость с плотностью 0,75—0,95. Обычно она содержит 83—87% углерода, И—14% водорода и небольшое количество азота, кислорода, серы. В одних сортах нефтн преобладают углеводороды гомологического ряда метаиа, в других — циклические. [c.316]
Обычно она содержит 83—87% углерода, И—14% водорода и небольшое количество азота, кислорода, серы. В одних сортах нефтн преобладают углеводороды гомологического ряда метаиа, в других — циклические. [c.316]
Продуктами реакции углерода с водородом, кроме метана, могут быть углеводороды гомологического ряда как насыщенные, так и ненасыщенные. Содержание углеводородов гомологического ряда в продуктах реакции значительно меньше, чем метана. На рис. 53 приведены кривые изменения выхода углеводородов в зависимости от температуры реакции. С повышением температуры реакции выход высших гомологов углеводородов уменьшается, продуктом реакции является метан. Отсутствие среди получающихся углеводородов изогомологов (например, изобутана) показывает, что при взаимодействии с водородом происходит разрыв только краевых связей плоских углеродных сеток. С повышением температуры вероятность разрыва связей становится соизмеримой со скоростью присоединения водорода, и при 1000 °С реакция, возможно, контролируется скоростью присоединения водорода.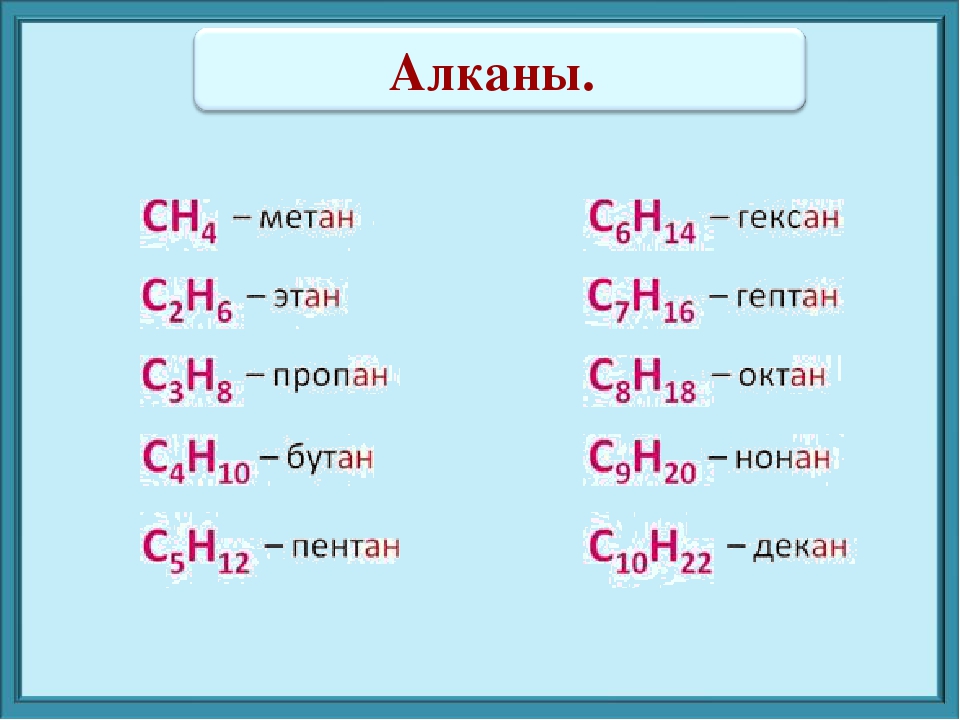 На это косвенно указывает значение энергии активации процесса при указанной температуре, близкое к энергии активации хемосорбции водорода на графите [77]. [c.126]
На это косвенно указывает значение энергии активации процесса при указанной температуре, близкое к энергии активации хемосорбции водорода на графите [77]. [c.126]
В 141 ступени обработки нефти карбамидом извлекается самая широкая гамма нормальных углеводородов — гомологический ряд от С до С42, максимальное содержание приходится на углеводороды от С23 до С29 во 2-й ступени (от Сю до С 40), максимальное содержание составляют углеводородыСг з — Сз 1 в 3-й от Се до Сз в 4-й от Се ДО С3 3 в 5-й от Се Д0С34 в 6-й от Се доСзо. [c.88]
Число углеродных атомов для значительно большей части углеводородов, извлеченных из нефти карбамидами, вьш1е 17. Поэтому карбамид целесообразно брать по массовому отношению 3,3 г карбамида на 1 г нормальных углеводородов [40] и рассчитьюать на содержание каждого углеводорода гомологического ряда, определенного ГЯО . [c.109]
Степень сходства углеводородов гомологических рядов проявляется в значениях х (см. третью графу табл. 44). Так, они близки для н-алканов и 2-метилалканов, для 1-алкинов и 1,2-диенов. По значению х можно заключить, чем 1-алкены несколько ближе по свойствам к транс-2- лкь- [c.304]
третью графу табл. 44). Так, они близки для н-алканов и 2-метилалканов, для 1-алкинов и 1,2-диенов. По значению х можно заключить, чем 1-алкены несколько ближе по свойствам к транс-2- лкь- [c.304]
Насыщенная фракция (алканы и цикланы) углеводороды гомологических рядов от С Н2п+2 до С Н2п-4 ПОЛНОСТЬЮ прсвращаются в бен-. ин ОТ С Н2 б ДО С Н2п-1о превращаются в бензин (до атомного отношения водород углерод, равного 1,7) остаток молекулы превращается в кокс. [c.160]
Альдегиды можно также рассматривать как вещества, происшедшие от замещения в парафиновых углеводородах атома водорода на альдегидную группу, т, е. как однозамещенные производные углеводородов гомологического ряда метана. Следовательно, здесь гомология и изомерия те же, что и для других однозамещенных производных предельных углеводородов. [c.235]
Кроме метана могут быть проконвертированы с водяным паром и другие углеводороды гомологического ряда метана (этан, пропан, бутан), а также их смеси. Взаимодействие водяного пара с алифатическими углеводородами может быть представлено следуюш,ими общими уравнениями [c.141]
Взаимодействие водяного пара с алифатическими углеводородами может быть представлено следуюш,ими общими уравнениями [c.141]
Общие формулы углеводородов в химии
Определение и общие формулы углеводородов
К углеводородам относится обширная группа органических соединений. Однако, лишь единственное из них – метан – содержит атом углерода, остальные имеют в своем составе связанные друг с другом атомы углерода, начиная с двух (этана, этилен, ацетилен) и кончая сотнями тысяч в высокомолекулярных углеводородах.
В соответствии со строением углеродного скелета углеводорода делятся на алифатические (с открытой углеродной цепью) и циклические (с замкнутой углеводородной цепью).
В зависимости от типа связей между атомами углерода алифатические углеводороды делятся на насыщенные, содержащие только s-связи и ненасыщенные, содержащие как s-, так и p-связи. К насыщенным углеводородам принадлежат алканы. Ненасыщенные углеводороды в зависимости от характера кратной связи подразделяются на алкены (с двойной связью) и алкины (с тройной связью). Кроме этого, выделяются отдельные группы по числу кратных связей в молекуле, например алкадиены (с двумя двойными связями).
Ненасыщенные углеводороды в зависимости от характера кратной связи подразделяются на алкены (с двойной связью) и алкины (с тройной связью). Кроме этого, выделяются отдельные группы по числу кратных связей в молекуле, например алкадиены (с двумя двойными связями).
Общая формула гомологического ряда алканов CnH2n+2. Представители алканов: метан (CH4), этан (C2H6), пропан (C3H8), бутан (C4H10) и др.
Общая формула гомологического ряда алкенов CnH2n. Представители алкенов: этилен (C2H4), пропен (C3H6), бутен (C4H8) и др.
Алкадиенами называются ненасыщенные углеводороды, молекулы которых содержат две двойные связи. Общая формула гомологического ряда алкадиенов CnH2n-2. Представители алкадиенов: пропадиен-1,2 (C3H4), бутадиен-1,4 (C4H6) и др.
Общая формула гомологического ряда алкинов CnH2n — 2. Представители алкинов: ацетилен (C2H2), пропин-1 (C3H4), бутин-1 (C4H6) и др.
Циклические углеводороды также как и алифатические могут иметь насыщенный и ненасыщенный характер, кроме этого циклические углеводороды делятся на алициклические и ароматические.
Насыщенные и ненасыщенные карбоциклические углеводороды, объединяют общим названием алициклические, подчеркивая приставкой али- их сходство с алифатическими углеводородами.
Насыщенные алициклические углеводороды называют циклоалканами (общая формула CnH2n, представители – циклопропан, циклобутан, циклопентан и др.), ненасыщенные с одной двойной связью – циклоалкенами, с двумя двойными связями – циклоалкадиенами. Известны алициклические углеводороды и с тройной связью, как правило, в макроцикле.
Среди ароматических соединений наибольшее значение имеют вещества, в молекулах которых содержится одно или несколько бензольных колец (рис.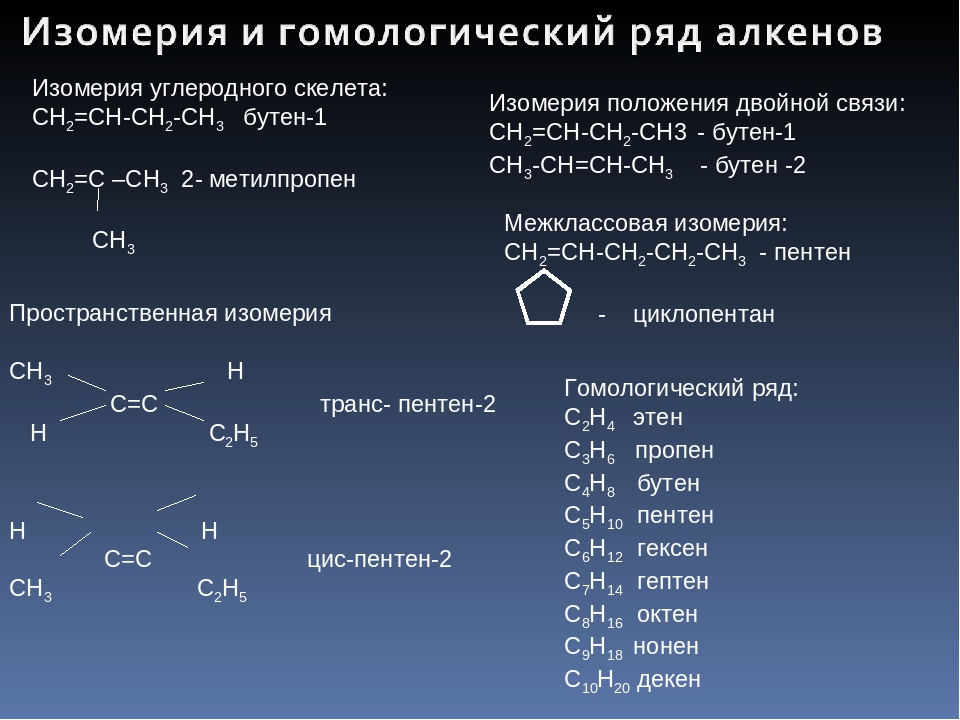 1). Структурным родоначальником этих веществ служит углеводород бензол C6H6. Углеводороды этого ряда носят общее называние – арены, а их общая формула — CnH2n – 6.
1). Структурным родоначальником этих веществ служит углеводород бензол C6H6. Углеводороды этого ряда носят общее называние – арены, а их общая формула — CnH2n – 6.
Рис. 1. Ароматические углеводороды.
Примеры решения задач
Как написать общую молекулярную формулу органических веществ?
В данной статье я вам покажу, как написать общую молекулярную формулу органических веществ любого класса, отталкиваясь от структурной формулы любого из его представителей.
Поехали.
Что вам нужно помнить железно, так это общую формулу алканов, она имеет вид CnH2n+2.
Далее, если вас просят, написать общую формулу, например предельных альдегидов:
1) вам следует записать формулу любого из них. Например:
2) Написать молекулярную формулу выбранного выше соединения, посчитав все атомы, входящие в состав его молекулы. В формуле выбранного в п.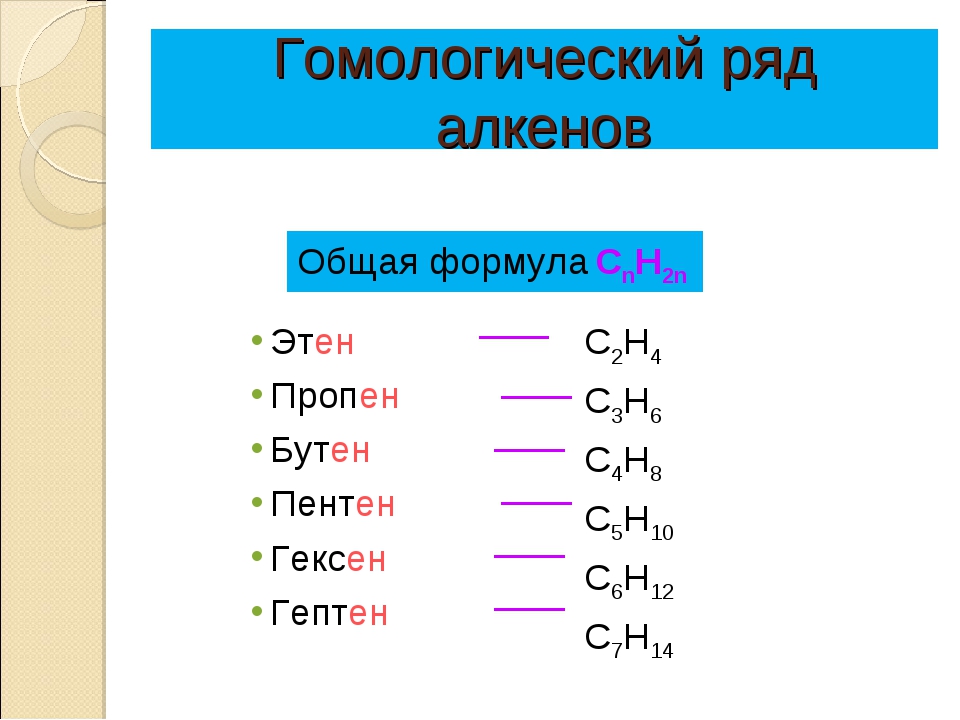 1. соединения мы обнаруживаем 3 атома углерода, 6 атомов водорода и 1 атом кислорода. Таким образом, оно имеет молекулярную формулу С3Н6O
1. соединения мы обнаруживаем 3 атома углерода, 6 атомов водорода и 1 атом кислорода. Таким образом, оно имеет молекулярную формулу С3Н6O
3) Записать формулу алкана с таким же числом атомов углерода в молекуле. В нашем случае, с тремя атомами. Подставляя значение n=3 в формулу CnH2n+2 получаем С3Н8
4) Посмотреть, чем отличаются друг от друга молекулярные формулы полученного алкана и исходного вещества. В исходном веществе на два атома водорода меньше, и на один атом кислорода больше.
5) Внести изменения в общую формулу алканов, т.е. CnH2n+2 в соответствии с установленной разницей, т.е. уменьшить число атомов водорода на два и добавить один атом О в формулу. Т.е.
CnH2n+2-2O
или
CnH2nO
Для того чтобы были очевидны преимущества данного метода, давайте попробуем записать общую формулу гомологического ряда ароматических сложных эфиров.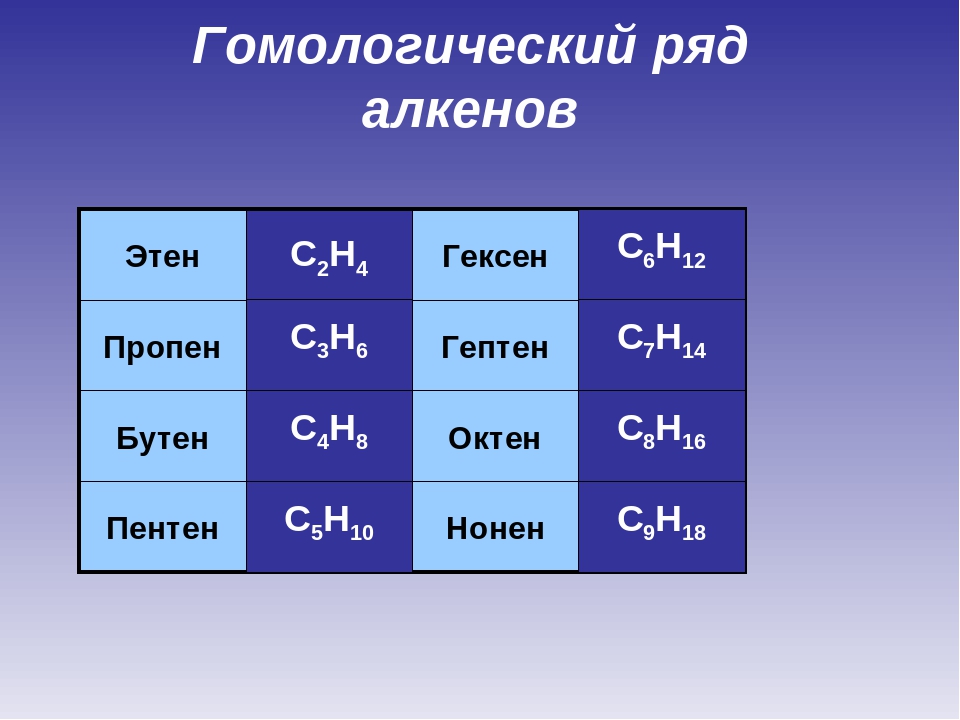 Ароматический значит в его структурной формуле есть бензольное кольцо, а сложные эфиры это вещества со сложноэфирной группой –С(O)-O-. Запишем формулу любого такого вещества, например:
Ароматический значит в его структурной формуле есть бензольное кольцо, а сложные эфиры это вещества со сложноэфирной группой –С(O)-O-. Запишем формулу любого такого вещества, например:
Для удобства ведения подсчетов атомов дорисуем не отображенные на структурной формуле выше атомы водорода, получим:
1) молекула выше состоит из 9 атомов С, 10 атомов Н, двух атомов O. Т.е. молекулярная формула данного вещества С9Н10O2
2) алкан с тем же числом атомов углерода имеет формулу C9H20. Сравнивая эту формулу с формулой изначального вещества С9Н10O2 мы видим, что в ней на 10 атомов H меньше и на два атома О больше, чем в соответствующем алкане.
3) Разница составов молекул исходного вещества и алкана с таким же числом атомов углерода будет той же самой и для общих формул гомологических рядов. Т.е.
CnH2n+2-10O2
или
CnH2n-8O2
| Домашнее задание по теме «Углеводороды» Консультация – 16. Минимальный уровень
а) 2,2-диметилпропан б) бутена-1, в) 2-метилгексина-3.
б) С какими из нижеперечисленных веществ будет реагировать ацетилен: бром, метан, водород, хлороводород? Напишите уравнения возможных реакций, укажите условия их протекания и назовите образующиеся вещества. в) Составьте уравнения реакций бензола с водородом, бромом, азотной кислотой. Укажите условия протекания реакций и назовите образовавшиеся вещества. Уровень 1
б) Составьте структурные формулы всех пространственных изомеров алкенов, имеющих относительную молекулярную массу 70. Укажите цис- и трансизомеры. в) Может ли существовать углеводород разветвленного строения, содержащий четыре атома углерода и тройную связь? Ответ поясните. г) Структурную формулу бензола нередко представляют в виде шестиугольника с окружностью внутри. Что данная окружность выражает?
б) Как опытным путем доказать, что каучук является непредельным углеводородом? в) Как распознать на основании химических свойств три жидкости: бензол, гексан и гексен?
а) Карбид алюминия → метан →хлорметан → этан → хлорэтан → н- бутан→ 2-метилпропан б) пропан → пропен→ пропанол — 2→пропен → 2-бромпропан→пропен→1,2- дибромпропан в) этан → бромэтан →1,1-дибромэтан →ацетилен →этилен →этиленгликоль г) метан → ацетилен → бензол → бромбензол.
б) Вычислите массу бромной воды, которую может обесцветить пропен, объем, которого при нормальных условиях составляет 10,08 л. Массовая доля брома в бромной воде 4%. в) Из 31,6 л (н.у.) этана с выходом 85% был получен этилен. Найдите массу воды, которую может присоединить данное количество этилена. г) Какую массу нитробензола можно получить из 23,4 г бензола и 23,21 г 95%-ной азотной кислоты? Уровень 2
б) Приведите формулу углеводорода, в молекуле которого все четыре атома углерода находятся в состоянии sp-гибридизации. в) Углеводород имеет структурную формулу: СН2=СН – СН2 – СH= СH – СН3 Назовите данное соединение по международной номенклатуре и укажите тип гибридизации каждого атома углерода.
а)
б)
в)
г)
а) Найдите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 14, 3%. Относительная плотность этого вещества по водороду 21. б) Найдите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 11, 1%. Относительная плотность этого вещества по воздуху равна 1,863. в) Массовые доли углерода и водорода в углеводороде равны соответственно 83,33% и 16,67%. Определите состав данного углеводорода. в) При сжигании углеводорода массой 11,2 г получили 35,2 г оксида углерода (IV) и 14,4 г воды. Относительная плотность углеводорода по воздуху равна 1,93. Установите молекулярную формулу углеводорода. г) При сжигании 3,9 г ароматического углеводорода образовалось 13,2 г оксида углерода (IV) и 2, 7 г воды. Установите молекулярную формулу ароматического углеводорода. Смесь пропина и пропена при сгорании образует 40,32 л (н.у.) углекислого газа и 27,9 г воды. Определите массовые доли компонентов исходной смеси. д) Смесь пропана и пропена обесцвечивает 800 г бромной воды с массовой долей брома 3%. При сгорании такого же количества этой смеси образуется 26,1 л воды. Определите массовые доли компонентов исходной смеси. Ответ: (C3H6) = 36,42%, (C3H8) = 63,58%. Достарыңызбен бөлісу: |
Ответы | § 24. Строение и физические свойства алканов — Химия, 9 класс
1. Приведите общую формулу алканов.
Общая формула алканов $\mathrm{C}_n\mathrm{H}_{2n+2},$ где $n$ — число атомов углерода в молекуле алкана.
2. Приведите определение гомологического ряда алканов и гомологической разности.
Гомологическим рядом называют ряд веществ, в котором молекулярные формулы соседних членов отличаются друг от друга на группу атомов $\mathrm{-CH_2-},$ называемую гомологической разностью.
3. Напишите молекулярные формулы углеводородов с числом атомов углерода в молекулах, равным: а) 3; б) 4.
$а)\, \mathrm{C_3H_8};$ $б)\, \mathrm{C_4H_{10}}.$
4. Какие из веществ, молекулярные формулы которых приведены, относятся к насыщенным углеводородам: а) $\mathrm{C_3H_8};$ б) $\mathrm{C_2H_4};$ в) $\mathrm{C_2H_6}?$
а) $\mathrm{C_3H_8}$ и в) $\mathrm{C_2H_6}.$
5. Молекула органического соединения изображена следующим образом:
Сколько атомов углерода и водорода составляют указанную молекулу?
Молекулярная формула изображённого соединения $\mathrm{C_5H_{12}}.$ Она содержит 5 атомов углерода и 12 атомов водорода.
6. Определите молекулярную формулу алкана, массовая доля углерода в котором равна 81,82 %.
Дано:
$\omega \mathrm{(C)}=81.82\%$
Найти: молекулярная формула — ?
Решение:
$\omega (элемента)= \dfrac{n·A_{эл.}}{M_{вещ.}};$
$0.8182=\dfrac{n·12}{12n+2n+2};$
$n=3.$ Формула алкана $C_3H_8.$
7. Напишите структурную формулу соединения $\mathrm{(CH_3)_3CH}.$
8. Определите, сколько различных соединений изображено следующими структурными формулами:
Изображено одно единственное соединение с молекулярной формулой $\mathrm{C_4H_{10}}.$
9. Укажите число атомов углерода в молекуле органического соединения
а) 6; б) 7; в) 8; г) 9.
В молекуле данного органического соединения содержится 8 атомов углерода — в) 8.
10. Напишите уравнение реакции этана химическим количеством 1 моль с бромом химическим количеством 1 моль при освещении.
$$\mathrm{CH_3CH_3+Br_2} \xrightarrow{hv} \mathrm{CH_3CH_2Br+HBr}$$
Присоединяйтесь к Telegram-группе @superresheba_9,
делитесь своими решениями и пользуйтесь материалами, которые присылают другие участники группы!
Предельные углеводороды. Свойства предельных углеводородов. Гомологический ряд углеводородов
Предельные углеводороды
Предельные углеводороды — их название говорит за себя! Это сложные химические вещества, молекулы которых состоят из атомов водорода и атомов углерода.
Предельные углеводороды образуют гомологический ряд углеводородов, каждое химическое вещество в таком ряду отличается от предыдущего в химическом строении на одно и тоже количество атомов водорода и углерода.
Гомологический ряд углеводородов
- CH4 — метан
- C2H6 — этан
- C3H8 — пропан
- C4H10 — бутан
- C5H12 — пентан
- C6H14 — гексан
- C7H16 — гептан
- C8H18 — октан
- C9H20 — нонан
- C10H22 — декан …
Гомологический ряд углеводородов характеризуется общей формулой, по которой можно определить формулу любого вещества данного ряда. Для предельных углеводородов — эта формула
CnH2n+2
C увеличением молекулярной массы вещества (увеличивается количество атомов углерода и водорода в молекуле) происходит увеличение температуры кипения этого вещества. Поэтому следует отметить, что вещества с CH4 по C4H10 — газы, с C5H12 по C15H32 — жидкости, далее — это твёрдые вещества!
Предельные углеводороды имеют ещё несколько названий — насыщенные углеводороды или парафины.
Предельные углеводороды образуют изомеры — вещества, которые имеют одинаковое число атомов одних и тех же элементов, но разное пространственное строение. Например, группа CH3 (или метил), может соединяться не с первым, а со вторым или третьим атомом водорода.
Изомеры характерны для предельных углеводородов, начиная с C4H10 — бутана.
Слева — формула газа — бутан, справа — тот же бутан, только в форме изомера.
Если от предельного углеводорода отсоединить один атом водорода — то образуется очень активное химическое вещество, которое, практически, не существует в свободном состоянии, мгновенно вступает в реакцию.
В химическом отношении при комнатной температуре все алканы инертные (то есть не вступают в химические реакции). Но при повышении температур — проявляют достаточную химическую активность.
Свойства предельных углеводородов
— реакция замещения: (реакция галогенирования)
— реакция нитрования:
— реакция дегидрогенизации (отщепление водорода):
— реакция горения
— реакция крекинга (расщепление большой молекулы на более мелкие молекулы)
▶▷▶ контрольные работы по химии 10 класс углеводороды с ответами
▶▷▶ контрольные работы по химии 10 класс углеводороды с ответами
| Интерфейс | Русский/Английский |
| Тип лицензия | Free |
| Кол-во просмотров | 257 |
| Кол-во загрузок | 132 раз |
| Обновление: | 03-11-2018 |
контрольные работы по химии 10 класс углеводороды с ответами — Yahoo Search Results Yahoo Web Search Sign in Mail Go to Mail» data-nosubject=»[No Subject]» data-timestamp=’short’ Help Account Info Yahoo Home Settings Home News Mail Finance Tumblr Weather Sports Messenger Settings Yahoo Search query Web Images Video News Local Answers Shopping Recipes Sports Finance Dictionary More Anytime Past day Past week Past month Anytime Get beautiful photos on every new browser window Download Контрольные работы Химия 10 класс Габриелян скачать wwwyangteacherru 10 класс Химия Контрольные работы создан в соответствии с учебной программой по Химии 10 класса Контрольная работа по химии Алканы 10 класс testschoolru/2017/08/12/kontrolnaya-rabota-po Cached Контрольная работа по химии Алканы 10 класс Контрольная работа по химии Алканы с ответами для учащихся 10 класса Химия 10 класс Контрольные и проверочные работы Базовый allengorg/d/chem/chem186htm Cached Базовый уровень 10 класс », переработанный в соответствии со ФГОС Учебное издание состоит из текстов контрольных и проверочных работ, соответствующих программе по химии для 10 класса О С Контрольные работы по химии 10 класс infourokru/kontrolnie-raboti-po-himii-klass Cached cкачать: Контрольные работы по химии 10 класс Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления Контрольные работы по химии 10 класс с ответами multiurokru/files/kontrol-nyie-raboty-po-khimii Cached 10 класс Контрольная работа 1 по теме «Предельные и непредельные углеводороды » Контрольные работы по химии 10 класс Итоговая контрольная работа onlyegeru/kontrolnye-raboty-po-ximii- 10 -klass Cached Контрольные работы по химии 10 класс Итоговая контрольная работа по химии 10 класс Вариант подготовила Субханова Г Р Контрольная работа по химии «Углеводороды» (10 класс) infourokru/kontrolnaya-rabota-po-himii Cached cкачать: Контрольная работа по химии » Углеводороды » 10 класс Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления Габриелян О С Химия 10 класс : контрольные и проверочные edu-libcom/izbrannoe/gabrielyan-o-s-himiya- 10 Cached Габриелян химия, Габриелян химия 10 класс , контрольные работы к учебнику Габриеляна, контрольные работы по химии , контрольные работы по химии для 10 класса, проверочные работы , проверочные Контрольная работа к уроку химии «Углеводороды» 10 класс wwwuchportalru/load/61- 1-0 -43319 Cached Методическая разработка Контрольная работа к уроку химии » Углеводороды » 10 класс по предмету Химия Категория: Контрольные работы по химии Контрольные работы по химии — 10 класс — Химия — Учительский wwwuchportalru/load/61-1-2-0-0- 10 -0 Cached Контрольные , практические и лабораторные работы по химии для качественной проверки знаний учащихся Контрольные работы по химии для учителей школ 10 класс Promotional Results For You Free Download | Mozilla Firefox ® Web Browser wwwmozillaorg Download Firefox — the faster, smarter, easier way to browse the web and all of Yahoo 1 2 3 4 5 Next 36,600 results Settings Help Suggestions Privacy (Updated) Terms (Updated) Advertise About ads About this page Powered by Bing™
- состоящих из 7 заданий в тестовой форме с выбором ответа (соответствует части Читать ещё Контрольная работа состоит из 7 заданий с выбором ответа и 1 задачи Максимальное число баллов – 13 Система оценивания уменьшает вероятность случайного выбора ответа учениками Приведены 6 вариантов контрольной работы и ответы к ним 10 -й класс Медведева Елена Леонидовна
- 256с) Размер: 2
- переработанный в соответствии со ФГОС Учебное издание состоит из текстов контрольных и проверочных работ
переработанный в соответствии со ФГОС Учебное издание состоит из текстов контрольных и проверочных работ
скачать: drivegoogle Скрыть Тесты по химии ( 10 класс ) с ответами онлайн
- размещенные на сайте
- проверочные работы
- размещенные на сайте
контрольные работы по химии 10 класс углеводороды с ответами — Все результаты Химия 10 классКонтрольная работа «Углеводороды» — Инфоурок › Химия Похожие Контрольная работа по теме « Углеводороды » Вариант 1 1К классу алканов относится 1) C2h5 2) Ch5 3) C3H6 4) C5H 10 2Установите Контрольная работа по теме «Углеводороды» 10 класс 6 дек 2013 г — Методическая разработка по химии ( 10 класс ) по теме: Контрольная работа по теме « Углеводороды » 10 класс Внимательно прочитай каждое задание и проанализируй все варианты предложенных ответов Контрольная работа в 10 классе по теме УГЛЕВОДОРОДЫ Похожие 7 янв 2015 г — Скачать: контрольная работа в 10 классе по теме углеводороды Часть Б Задания со свободным ответом Перечислите Напишите уравнения химических реакций для следующих превращений: 6 баллов Контрольная работа «Углеводороды» 10-й класс открытыйурокрф/статьи/615054/ Приведены 6 вариантов контрольной работы и ответы к ним тестов “ Химия 10-11” [3], текста учебника “ Химия 10 класс ” Рудзитис ГЕ, Фельдман ФГ Контрольная работа по химии 10 класс Углеводороды — Документ Контрольная работа по химии 10 класс Углеводороды Вариант 1 ЧАСТЬ А Тестовые задания с выбором ответа 1 (2 балла) Общая формула аренов: Контрольная работа по теме «Углеводороды» 10 класс — Мультиурок 6 мар 2015 г — Контрольная работа по теме » Углеводороды » 10 класс Часть Б Задания со свободным ответом Перечислите области применения алкенов 2 балла Напишите уравнения химических реакций для следующих Контрольная работа по теме «Углеводороды» — Учителю химии uchiucozru › Статьи › По предмету › Учителю химии Похожие 24 февр 2012 г — Контрольная работа по теме « Углеводороды » Укажите к какому классу относится УВ с формулой СН3 – СН3 1) алканов 2) алкенов 3) 10 Определите, сколько молей углекислого газа образуется при полном сгорании метана 1) 1 моль 2) 2 Часть Б Задания со свободным ответом 12 Контрольная работа по теме «Углеводороды» 10 класс 15 нояб 2015 г — Контрольная работа по теме » Углеводороды » 10 класс (базовый уровень) по разделу » Углеводороды » курса органической химии ( 10 класс , из 3-х частей, задания — тесты и вопросы со свободными ответами Контрольная работа по химии 10 класс углеводороды ответы на Контрольная работа по химии 10 класс углеводороды ответы на все варианты Контрольная работа «углеводороды» (тест) — Главное меню ( химия 10 класс , ОС Габриелян, контрольные и проверочные работы к учебнику ОС Габриеляна « Химия 10») (2 балла) Углеводород с формулой СН3-СН3 относится к классу: Часть Б Задания со свободным ответом 11 Ответы MailRu: Контрольная работа по теме «Углеводороды» › Образование › Школы Похожие Углеводород с формулой СН3—СН3 относится к классу : А Алканов Б 10 ( 2 балла) При полном сгорании 1 л газообразного углеводорода (н у) Контрольная работа по теме «Углеводороды» (10 класс, базовый Похожие 8 дек 2015 г — Контрольная работа по теме » Углеводороды » ( 10 класс , базовый структурные формулы углеводородов , уравнения химических Картинки по запросу контрольные работы по химии 10 класс углеводороды с ответами «crea»:»Компьютер»,»id»:»QrpzayY3FAwC6M:»,»iss»:0,»ml»:»600″:»bh»:90,»bw»:120,»oh»:375,»ou»:» «,»ow»:529,»pt»:»videourokinet/img/files/uf/2016/01/98726152-14527″,»rh»:»videourokinet»,»rid»:»fX0eQ2OINK01GM»,»rt»:0,»ru»:» «,»sc»:1,»st»:»Видеоуроки»,»th»:90,»tu»:» \u003dtbn:ANd9GcSAqHj9tc6oWs9-zsKpgQaoShhm2wNW2lwBGmDG-1lpDjYNOVuche_5Dw»,»tw»:127 «cl»:12,»cr»:3,»ct»:12,»id»:»3iax60aYieShsM:»,»ml»:»600″:»bh»:90,»bw»:66,»oh»:651,»ou»:» «,»ow»:513,»pt»:»ipinimgcom/originals/da/ea/fb/daeafb8072ab685d07″,»rh»:»pinterestcom»,»rid»:»0nYeb1_DQtnQAM»,»rt»:0,»ru»:» «,»sc»:1,»st»:»Pinterest»,»th»:94,»tu»:» \u003dtbn:ANd9GcR9qOi9PLzt0KZ_-qtKBXppBYX1aT5N6hddrUt6fDwqhdqTtKpgwZvQWA»,»tw»:74 «id»:»REkcNqG1SmWyrM:»,»ml»:»600″:»bh»:90,»bw»:63,»oh»:1419,»ou»:» «,»ow»:1000,»pt»:»ipinimgcom/originals/28/8a/4b/288a4bcfcf93789dbc»,»rh»:»pinterestcom»,»rid»:»AEFlGbjxJaf5DM»,»rt»:0,»ru»:» «,»sc»:1,»st»:»Pinterest»,»th»:99,»tu»:» \u003dtbn:ANd9GcRbJVeIGikMM0KVy9GxsSWTv-m_so8wyFATwaFz7SnBg8VgrMvbGnGOBg»,»tw»:70 «id»:»B_g9ivHgR22N_M:»,»ml»:»600″:»bh»:90,»bw»:120,»oh»:843,»ou»:» «,»ow»:1429,»pt»:»arhivurokovru/kopilka/uploads/user_file_54896e7f6″,»rh»:»kopilkaurokovru»,»rid»:»i0y82Vjg91CZJM»,»rt»:0,»ru»:» «,»sc»:1,»th»:90,»tu»:» \u003dtbn:ANd9GcRoNvd3peSOIt5gxvK-xIjswk9r9aUBKT0XU-kihJ5YavDzQWac-483jWE»,»tw»:153 «cl»:12,»id»:»TdQvlV-VZdBZBM:»,»ml»:»600″:»bh»:90,»bw»:85,»oh»:800,»ou»:» «,»ow»:800,»pt»:»otvetimgsmailru/download/213241978_21bf39b1bc0ef»,»rh»:»otvetmailru»,»rid»:»odInyI-XOawxIM»,»rt»:0,»ru»:» «,»st»:»Ответы@MailRu»,»th»:90,»tu»:» \u003dtbn:ANd9GcQHrmjqFmM5wJ2xMOIP8tM3bhTdfl4sBA_h-N312kymL6p4ZuI-CQnr5Vg»,»tw»:90 «cb»:18,»cl»:12,»cr»:6,»ct»:6,»id»:»HF9qe9H6QqPkfM:»,»ml»:»600″:»bh»:90,»bw»:59,»oh»:708,»ou»:» «,»ow»:500,»pt»:»znanioru/static/files/cache/08/f9/08f91133f340802″,»rh»:»znanioru»,»rid»:»YMXIi77WYlZ1zM»,»rt»:0,»ru»:» «,»sc»:1,»st»:»Знанио»,»th»:99,»tu»:» \u003dtbn:ANd9GcQdQcb87JiSmhP0N-60l7yrD6gDm2Y0faQCDcsh4fo1GFVX57t6I33QeQ»,»tw»:70 «crea»:»Игоревич»,»id»:»e8NlxxD2xo7JfM:»,»iss»:0,»ml»:»600″:»bh»:90,»bw»:63,»oh»:500,»ou»:» «,»ow»:354,»pt»:»wwwuchportalru/_ld/797/10489006jpg»,»rh»:»uchportalru»,»rid»:»c0SPcrVIQfEJjM»,»rt»:0,»ru»:» «,»sc»:1,»st»:»Учительский портал»,»th»:99,»tu»:» \u003dtbn:ANd9GcSLJmRHKVLEK6kuNonD6RpBYzvybKQy3lhWPeZyib3uuppNvrSow4lTdCA»,»tw»:70 Другие картинки по запросу «контрольные работы по химии 10 класс углеводороды с ответами» Жалоба отправлена Пожаловаться на картинки Благодарим за замечания Пожаловаться на другую картинку Пожаловаться на содержание картинки Отмена Пожаловаться Все результаты КОНТРОЛЬНЫЕ РАБОТЫ, 10 класс Контрольная работа 1 КОНТРОЛЬНЫЕ РАБОТЫ , 10 класс Контрольная работа 1 «Предельные 4 ) оба суждения неверны Часть В Ответом к заданиям этой части (В1 В13) A10 Сходство химических свойств бензола и предельных углеводородов Разноуровневые контрольные работы по химии на тему — компэду 3 нояб 2017 г — составлена контрольная полугодовая по химии за 10 класс на тему: Контрольная работа за 1 полугодие « Углеводороды » 10 класс Контрольные работы по химии — 10 класс — Химия — Учительский Контрольные, практические и лабораторные работы по химии для качественной Контрольная работа к уроку химии » Углеводороды » 10 класс [PDF] Химия 10 класс Контрольная работа №1 (10 класс (2)pdf Похожие Углеводород с формулой СН3—СН3 относится к классу: а) алканов Часть Б Задания со свободным ответом Итоговая контрольная работа 10 класс Контрольная работа по химии 10 класс по теме : «Углеводороды Похожие Контрольная работа по химии 10 класс по теме : « Углеводороды » Для вещества, формула которого СН3-СН2-СН-СН=СН2 назовите класс, тип Контрольная работа по химии на тему «Углеводороды» — Видеоуроки Похожие 10 янв 2016 г — Контрольная работа включает классы алканы, циклоалканы, алкены, диены, алкины и Проверочные работы по химии 10 класс 0 Контрольная работа по химии номер 1 углеводороды 10 класс Контрольная работа по химии номер 1 углеводороды 10 класс Рабочая тетрадь по географии 8 класс ответы сиротин бесплатно Group, Blog, Algebra итоговая контрольная работа по химии в 10 классе ответы 2 Контрольная работа » Углеводороды » 10 -й класс открытыйурокрф/статьи/ 615054/ Приведены 6 вариантов контрольной работы и ответы к ним “ Химия [PDF] Углеводороды и их природные источники wwwshkola10-baikonuredusiteru//5b2e4b1a-31b9-4c26-ae4c-fd4af2ec03e7pdf Преподавание ведется по учебнику Химия 10 класс : учебник для при ответе обнаружено непонимание учащимся основного содержания учебного материала или Контрольная работа № 2 по теме « Углеводороды » Подготовка к контрольной работе по теме «Углеводороды»; 10 класс pedsovetsu › Файлы для скачивания › Химия › Презентации Похожие 23 апр 2012 г — ПОДГОТОВКА К КОНТРОЛЬНОЙ РАБОТЕ ПО ТЕМЕ « Углеводороды » 10 класс Автор: Ким НВ Учитель химии МБОУ «СОШ № 6» г Контрольная работа» Углеводороды»10 класс физико myhimsiteru/kontrolnaya-rabota-uglevodorody-10-klass-fiziko-matematicheskiy-profil Похожие Контрольная работа » Углеводороды » 10 класс физико — математический профиль Составьте уравнения химических реакций, схемы которых: А С2 Н4+Сl2 Б С2 Н4+h3O Г СН4+Сl2 Часть С (3 варианта ответов ) 1 10 класс Химия Тематическая контрольная работа Углеводороды 10 класс Химия Тематическая контрольная работа Углеводороды Вариант 1 Проверка знаний Итоговая контрольная работа по химии в 10 классе — Урокрф 20 апр 2017 г — Методические разработки по Химии для 10 класса по УМК ГЕ Рудзитис, ФГ Итоговая контрольная работа по химии в 10 классе « Углеводороды » В заданиях 1-3 выберите по одному правильному ответу 1 Дубинина Н | Контрольные работы 9 класс | Журнал «Химия him1septemberru/view_articlephp?ID=201001004 Похожие Контрольные работы 9 класс Продолжение Cм в № 22, 24/2009 К каждому заданию части А даны несколько ответов , из которых только один верный В промышленности ароматические углеводороды получают из: выделится при гидролизе 20 г карбида кальция, содержащего 10 % примесей Химия 10 класс контрольные Комбинированные контрольные контрольные работы « Химия 10 класс Базовый уровень» Назовите предельный углеводород (кроме метана), в молекуле которого нет первичных Ответом к заданиям 1, 2 является последовательность из трех цифр, которые КОНТРОЛЬНАЯ РАБОТА ПО ТЕМЕ «УГЛЕВОДОРОДЫ КОНТРОЛЬНАЯ РАБОТА ПО ТЕМЕ « УГЛЕВОДОРОДЫ » — УГЛЕВОДОРОДЫ — Настольная книга учителя химии 10 класс — поурочные разработки Проверочная и контрольная работы по теме: «Углеводороды» в uchkopilkaru//3512-proverochnaya-i-kontrolnaya-raboty-po-teme-uglevodorody- Похожие 20 февр 2014 г — В этом разделе категории » Химия » опубликованы контрольные и Контрольная работа №1 « Углеводороды » 10класс Вариант3 Контрольная работа по химии 10 класс углеводороды вариант 3 Контрольная работа по химии 10 класс углеводороды вариант 3 ответы , контрольная работа окружающий мир 3 класс 2 четверть 2100 Контрольная контрольная работа по химии 10 класс по теме «Углеводороды контрольная работа по химии 10 класс по теме » Углеводороды » — в разделе Контроль знаний, по направлениям Химия , Методические и учебные Не найдено: ответами Подготовка к контрольной работе по теме «Углеводороды» alximikiblogspotcom/2013/11/blog-post_28html Похожие 28 нояб 2013 г — «Кто не понимает ничего, кроме химии , тот и ее понимает недостаточно» ( Георг Контрольная работа проводится по вариантам в тестовой форме по аналогии с уровня с развернутым ответом , которые оцениваются тремя баллами (максимально 6 баллов) Ярлыки: 10 класс , к уроку [PDF] Рабочая программа по химии 10 А (соц-гум) — МОУ СОШ №33 г Программа курса химии 10 класса , при 1-часовом изучении, отражает учебный материал Контрольная работа № 1 по теме « Углеводороды » при ответе обнаружено непонимание учащимся основного содержания учебного Проверочная работа по теме: «Углеводороды» предназначена для obrazbaseru//951-proverochnaya-rabota-po-teme-uglevodorody-prednaznachena-d Похожие 23 февр 2015 г — Проверочная работа по теме: \» Углеводороды \», 10 класс Части В и С представляют собой задания со свободным ответом повышенного уровня сложности Tags: 10 класс , контрольная работа , Химия контрольная работа по химии 10 класс органическая химия ответы h-hostercom//kontrolnaia-rabota-po-khimii-10-klass-organicheskaia-khimiia-otvety контрольная работа по химии 10 класс органическая химия ответы по химии 10 класс углеводороды габриелян ответы Итоговая контрольная работа Контрольная работа химия 10 класс углеводороды ответы — ИФХАН ifhanru/component/k2/itemlist/user/1359 Похожие Контрольная работа химия 10 класс углеводороды ответы , контрольная работа no 4 русский язык 10 класс Контрольная работа химия 10 класс Контрольная работа по теме «Углеводороды» | Образовательный Похожие 5 дек 2016 г — Предмет: химия , класс : 10 (базовый уровень) УМК: программа курса 1 часть: тест (задания с одним правильным ответом ) 2 часть: задания с Контрольная работа № 1 по теме: « Углеводороды » Вариант № 1 Вариант контрольной работы по теме «Углеводороды и их diva106blogspotcom//Variant-kontrolnoj-raboty-po-teme-Uglevodorody-i-ih-prir Вариант контрольной работы по теме » Углеводороды и их природные источники» задания с развернутым ответом : 13 — 15 (13 — 5 баллов, 14 — 3 балла, Всероссийская проверочная работа по химии — 2017 (11 класс) Главная → 10 класс → базовый уровень → Вариант контрольной работы по теме [DOC] 10-11 автор: ИВ Баженова — Цитируется: 2 — Похожие статьи Химия 10-11 классы Составители: Баженова ИВ, учитель химии , биологии в 10 классе — 68часов, из них практических работ — 6, контрольных работ -4 зачет-1 Отметка «2» :при ответе обнаружено непонимание учащимся основного содержания Контрольная работа №2 по теме: Углеводороды Ответы контрольная работа по химии 10 класс тема углеводороды smokussusraru/165/ 9 апр 2018 г — Телешколы по химии 10 класс Тема: Углеводороды в природе Тема Ответы к тесту по химии на тему Углеводороды 2 варианта Углеводороды: от алканов до аренов Химия 10 класс Разработка › › Разработки уроков (конспекты уроков) Деятельность учащихся (возможные варианты ответов ) Слайд (усл обозн) Химия Базовый уровень 10 класс Контрольные и проверочные работы Решебник по химии за 10 класс к дидактическому материалу Решебник по химии за 10 класс к дидактическому материалу химия АМ Радецкий 10-11кл Тема II Предельные углеводороды (алканы, или парафины) Работа 4 Итоговая работа по теме II Вариант 2 ( ответы : 2- метилпропан [PDF] 1 Пояснительная записка Рабочая программа по химии для 10 менталитетекатеринбургрф/file/download/3815 Рабочая программа по химии для 10 класса (ФГОС) МАОУ Гимназия № 202 Углеводороды », «Производные углеводородов », «Вещества живых клеток», 10 класс : контрольных работ – 2, практических работ – 3, лабораторных Критерии оценивания устных ответов и письменных работ по химии контрольная работа природные источники углеводородов 10 класс profcareerru//kontrolnaia-rabota-prirodnye-istochniki-uglevodorodov-10-klassxml контрольная работа природные источники углеводородов 10 класс 1 Контрольная работа по химии 10 класс углеводороды габриелян ответы Контрольная работа по химии:»Углеводороды», 10 класс Похожие Контрольная работа по химии по разделу: » Углеводороды «, 10 класс Содержит 14 заданий: с выбором одного правильного ответа и с полным ответом 3 ЗАВУЧинфо — Методическая библиотека | Химия | Контрольные wwwzavuchru/methodlib/134/ Похожие Контрольная работа по химии 8 класс Контрольная работа » Углеводороды 10 класс » Часть 1 включает 10 заданий с кратким ответом базового и Контрольная работа по Химии за 1 полугодие «Углеводо¬роды › Химия 14 июн 2017 г — Здесь Вы можете скачать Контрольная работа по Химии за 1 полугодие « Углеводо¬роды» 10 класс Контрольная работа за 1 полугодие « Углеводороды » 10 класс Оценка «5» — от 15 до 17 правильных ответов [DOC] 11Радецкий АМ Контрольные работы по химии в 10-11 классах Учебный план ОУ Программа базового курса химии 10 класса отражает современные Контрольная работа №2 по теме: « Углеводороды » при ответе обнаружено непонимание учащимся основного содержания учебного Система контрольных и зачетных работ по химии для учащихся 10 mirznaniicom//sistema-kontrolnykh-i-zachetnykh-rabot-po-khimii-dlya-uchashchik Похожие Химические реакции в органической химии » 10 класс 10 класс Контрольная работа № 2 по темам «Алканы и алкены» Углеводороды Приведены также вопросы на ответы тестов и примерные критерии оценок, исходя из Вместе с контрольные работы по химии 10 класс углеводороды с ответами часто ищут контрольная работа по химии 10 класс углеводороды ответы габриелян контрольная работа по химии 10 класс углеводороды вариант 1 ответы контрольная работа по теме углеводороды 11 класс контрольная работа по химии 10 класс органическая химия ответы подготовка к контрольной работе по химии 10 класс углеводороды химия 10 класс углеводороды контрольная работа по теме углеводороды 10 класс базовый уровень контрольная работа по химии 10 11 класс Навигация по страницам 1 2 Следующая Ссылки в нижнем колонтитуле Россия — Подробнее… Справка Отправить отзыв Конфиденциальность Условия Аккаунт Поиск Карты YouTube Play Новости Почта Контакты Диск Календарь Google+ Переводчик Фото Ещё Документы Blogger Hangouts Google Keep Подборки Другие сервисы Google
Яндекс Яндекс Найти Поиск Поиск Картинки Видео Карты Маркет Новости ТВ онлайн Музыка Переводчик Диск Почта Коллекции Все Ещё Дополнительная информация о запросе Показаны результаты для Нижнего Новгорода Москва 1 Контрольная работа в 10 классе по теме metod-kopilkaru › …10_klasse_po_teme_uglevodorody… Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Контрольная работа по теме « Углеводороды » Вариант 1 Часть А Тестовые задания с выбором ответа Часть А Тестовые задания с выбором ответа За задание 1 балл 1 Укажите общую формулу алкенов 1) Cnh3n +2 2) Cnh3n 3) Cnh3n—2 4) Cnh3n -6 Укажите к какому классу относится УВ с формулой Читать ещё Контрольная работа по теме « Углеводороды » Вариант 1 Часть А Тестовые задания с выбором ответа За задание 1 балл Укажите общую формулу аренов 1) Cnh3n +2 2) Cnh3n 3) Cnh3n—2 4) Cnh3n -6 Укажите к какому классу относится УВ с формулой СН3 – СН3 1) алканов 2) алкенов 3) алкинов 4) аренов Укажите название изомера для вещества, формула которого СН2 = СН – СН2 – СН3 Часть А Тестовые задания с выбором ответа За задание 1 балл 1 Укажите общую формулу алкенов 1) Cnh3n +2 2) Cnh3n 3) Cnh3n—2 4) Cnh3n -6 Укажите к какому классу относится УВ с формулой СН3 – С = СН2 | СН3 1) алканов 2) алкенов 3) алкинов 4) аренов Скрыть 2 Методическая разработка по химии ( 10 класс ) по теме nsportalru › Школа › Химия › …-uglevodorody-10-klass Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Сайт – выбор пользователей Подробнее о сайте Контрольная работа по теме « Углеводороды » (Проектирование теста учебных достижений в формате ЕГЭ) На выполнение контрольной работы по химии отводится 40 минут Работа состоит из 3 частей и включает 10 заданий Часть1 включает 7 заданий (А1-А7) базового уровня Читать ещё Контрольная работа по теме « Углеводороды » (Проектирование теста учебных достижений в формате ЕГЭ) составила: Шаншаева Сапижат Исаевна учитель химии МБОУ «СОШ № 2» гТарко-Сале 2013г Кодификатор элементов содержания проверочного контроля по теме « Углеводороды » Общие формулы классов углеводородов Изомерия и гомология Типы химических связей Характерные химические свойства углеводородов Способы получения углеводородов Генетическая связь между классами углеводородов На выполнение контрольной работы по химии отводится 40 минут Работа состоит из 3 частей и включает 10 заданий Часть1 включает 7 заданий (А1-А7) базового уровня Скрыть 3 Контрольные работы по химии 10 класс infourokru › kontrolnie…po-himii-klass-2240101html Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Сайт – выбор пользователей Подробнее о сайте КИМ химия 10 класс Контрольная работа 1: Углеводороды Вариант 1 Часть А Тестовые задания с выбором ответа 5(2б) Молекулярная формула углеводорода с относительной молекулярной массой 58 Читать ещё КИМ химия 10 класс Контрольная работа 1: Углеводороды Вариант 1 Часть А Тестовые задания с выбором ответа 1 (2 балла) Общая формула Сn Н2n+2 соответствует: А алканам Б алкенам В алкинам Г аренам 5(2б) Молекулярная формула углеводорода с относительной молекулярной массой 58: АС4Н10 БС5Н10 ВС5Н12 ГС4Н8 Скрыть 4 Контрольная работа » Углеводороды » 10 -й класс открытыйурокрф › статьи/615054/ Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Контрольная работа состоит из 7 заданий с выбором ответа и 1 задачи 10 -й класс Медведева Елена Леонидовна, учитель химии В работе 6 вариантов, состоящих из 7 заданий в тестовой форме с выбором ответа (соответствует части Читать ещё Контрольная работа состоит из 7 заданий с выбором ответа и 1 задачи Максимальное число баллов – 13 Система оценивания уменьшает вероятность случайного выбора ответа учениками Приведены 6 вариантов контрольной работы и ответы к ним 10 -й класс Медведева Елена Леонидовна, учитель химии Разделы: Химия Контрольная работа проводится в 10 -м классе социально-гуманитарного профиля Время проведения: 40-45 минут В работе 6 вариантов, состоящих из 7 заданий в тестовой форме с выбором ответа (соответствует части А заданий ЕГЭ — базовый уровень) и 1 задача Максимальное число баллов – 13 Скрыть 5 Контрольная работа по теме » Углеводороды » 10 класс multiurokru › files/kontrol-naia…po…10-klasshtml Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Часть Б Задания со свободным ответом 10 Перечислите области применения алканов Просмотр содержимого документа « Контрольная работа по теме Задания к контрольной работе по химии по теме » Углеводороды Читать ещё Часть Б Задания со свободным ответом 10 Перечислите области применения алканов 2 балла Просмотр содержимого документа « Контрольная работа по теме » Углеводороды » 10 класс » Контрольная работа по теме « Углеводороды » Вариант 1 Часть А Тестовые задания с выбором ответа За задание 1 балл Укажите общую формулу алканов 1) Cnh3n +2 2) Cnh3n 3) Cnh3n—2 4) Cnh3n -6 Укажите к какому классу относится УВ с формулой СН3 – СН3 1) алканов 2) алкенов 3) алкинов 4) аренов Укажите название изомера для вещества, формула которого СН2 = СН – СН2 – СН3 Задания к контрольной работе по химии по теме » Углеводороды Спирты» ( 10 класс ) Скрыть 6 Разноуровневые контрольные работы по химии на тему compeduru › …kontrolnye…po-khimii…uglevodorodyhtml Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Контрольная работа за 1 полугодие « Углеводороды » 10 класс Первый уровень Вариант 1 Найдите молекулярную формулу углеводорода Сохранить у себя: Разноуровневые контрольные работы по химии на тему: » Углеводороды » Скачать разработку Похожие файлы Углеводы Презентация к уроку Читать ещё Контрольная работа за 1 полугодие « Углеводороды » 10 класс Первый уровень Вариант 1 Задание 1 Для вещества, формула которого СН3 – СН2 – СН2 – СН2 – СН3+ Найдите молекулярную формулу углеводорода Сохранить у себя: Разноуровневые контрольные работы по химии на тему: » Углеводороды » Скачать разработку Похожие файлы Углеводы Презентация к уроку химии в 10 классе Методические рекомендации по проведению дидактических игр на уроках химии Контрольная работа № 1 Урок для учащихся 5-7 классов «Экскурсия в кабинет химии » Презентация «Пропедевтика химии в 7 классе» Получите свидетельство о публикации сразу после загрузки работы Скрыть 7 Контрольная работа по химии 10 класс Углеводороды gigabazaru › doc/6733html Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Углеводороды Вариант 1 ЧАСТЬ А Тестовые задания с выбором ответа Контрольная работа по химии ( 9 класс ) ОРГАНИЧЕСКИЕ ВЕЩЕСТВА Вариант 4 ЧАСТЬ для сгорания 2 л этана: А 2 л Б 4 л В 5 л Г 10 л (2 балла) Этилен не взаимодействует с веществом Контрольная работа по теме Читать ещё Углеводороды Вариант 1 ЧАСТЬ А Тестовые задания с выбором ответа 1 (2 балла) Общая формула аренов Контрольная работа по химии ( 9 класс ) ОРГАНИЧЕСКИЕ ВЕЩЕСТВА Вариант 4 ЧАСТЬ для сгорания 2 л этана: А 2 л Б 4 л В 5 л Г 10 л (2 балла) Этилен не взаимодействует с веществом Контрольная работа по теме « Углеводороды » Скрыть 8 Контрольные работы по химии 10 класс Углеводороды с ответами — смотрите картинки ЯндексКартинки › контрольные работы по химии 10 класс углеводороды Пожаловаться Информация о сайте Ещё картинки 9 Контрольная работа «Предельные углеводороды » 10 uchitelyacom › Химия › …-uglevodorody-10… Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Контрольная работа по теме «Предельные углеводороды » Вариант №1 1А Диметилпропан относится к классу углеводородов , общая формула которого В гомологическом ряду метана изомерия начинается с углеводорода , содержащего 1) 3 атома углерода 2) 4 атома углерода 3) 5 атомов углерода 4) 6 Читать ещё Контрольная работа по теме «Предельные углеводороды » Вариант №1 1А Диметилпропан относится к классу углеводородов , общая формула которого 1) C n В гомологическом ряду метана изомерия начинается с углеводорода , содержащего 1) 3 атома углерода 2) 4 атома углерода 3) 5 атомов углерода 4) 6 атомов углерода 6А Число σ-связей в молекуле 2 – метилпропана равно 1) 10 2) 11 3) 13 4) 12 7А Скрыть 10 Химия 10 класс Контрольные и проверочные работы allengorg › d/chem/chem186htm Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте 10 класс », переработанный в соответствии со ФГОС Учебное издание состоит из текстов контрольных и проверочных работ , соответствующих программе по химии для 10 класса ОС Габриеляна Пособие предназначено для проведения текущего и итогового контроля по основным темам курса Формат: pdf (2015, 256с) Читать ещё 10 класс », переработанный в соответствии со ФГОС Учебное издание состоит из текстов контрольных и проверочных работ , соответствующих программе по химии для 10 класса ОС Габриеляна Пособие предназначено для проведения текущего и итогового контроля по основным темам курса Формат: pdf (2015, 256с) Размер: 2,4 Мб Смотреть, скачать: drivegoogle Скрыть Тесты по химии ( 10 класс ) с ответами онлайн, итоговые obrazovakaru › testy/po-himii/10-klass Сохранённая копия Показать ещё с сайта Пожаловаться Информация о сайте Тест Предельные и непредельные углеводороды ( 10 класс ) 10 вопросов Готовые ответы позволяют сразу запоминать то, что «упущено» для быстрой подготовки к текущему контролю и контрольным работам за полугодие и год Для более качественной подготовки рекомендуется дополнять краткие Читать ещё Тест Предельные и непредельные углеводороды ( 10 класс ) 10 вопросов Уровень: знаток 4 Кислород- и азотсодержащие органические соединения и их природные источники Готовые ответы позволяют сразу запоминать то, что «упущено» для быстрой подготовки к текущему контролю и контрольным работам за полугодие и год Для более качественной подготовки рекомендуется дополнять краткие ответы теста материалом из учебных пособий Тематические вопросы касаются теории выученных разделов (законы, классификации, правила), предполагают знание свойств химических веществ, особенностей их взаимодействия Более сложные задания являют собой задачи и уравнения Скрыть Вместе с « контрольные работы по химии 10 класс углеводороды с ответами » ищут: контрольные и проверочные работы по химии 10 класс габриелян ответы контрольные и проверочные работы по химии 10 класс контрольные работы по физике 10 класс мякишев с решениями контрольные работы по химии 8 класс сумма коэффициентов в уравнении реакции полного сгорания этана равна 1 2 3 4 5 дальше Браузер Для безопасных прогулок в сети 0+ Скачать
12.2: Структура и названия алканов
- Последнее обновление
- Сохранить как PDF
- Ключевые вынос
Цели обучения
- Для идентификации и наименования простых (с прямой цепью) алканов по формулам и записи формул для алканов с прямой цепью с указанием их названий.
Мы начинаем изучение органической химии с углеводородов, простейших органических соединений, которые состоят только из атомов углерода и водорода. Как мы уже отметили, существует несколько различных видов углеводородов. Их различают типы связи между атомами углерода и свойства, возникающие в результате этой связи. Углеводороды, имеющие только одинарные связи углерод-углерод (C – C) и существующие как непрерывная цепочка атомов углерода, также связанных с атомами водорода, называются алканами (или насыщенными углеводородами). Насыщенный , в данном случае, означает, что каждый атом углерода связан с четырьмя другими атомами (водородом или углеродом) — наиболее вероятным; в молекулах нет двойных или тройных связей.
Слово насыщенный имеет то же значение для углеводородов, что и для пищевых жиров и масел: молекула не имеет двойных связей углерод-углерод (C = C).
Ранее мы ввели три простейших алкана — метан (CH 4 ), этан (C 2 H 6 ) и пропан (C 3 H 8 ), и они снова показаны на рисунке \ ( \ PageIndex {1} \).
Рисунок \ (\ PageIndex {1} \): Три простейших алкана
Показанные плоские изображения не точно отображают валентные углы или геометрию молекул. Метан имеет четырехгранную форму, которую химики часто изображают с клиньями, указывающими на связи, идущие к вам, и пунктирными линиями, обозначающими связи, отходящие от вас. Обычная сплошная линия обозначает связь в плоскости страницы. Напомним, что теория VSEPR правильно предсказывает тетраэдрическую форму молекулы метана (рисунок \ (\ PageIndex {2} \)).
Рисунок \ (\ PageIndex {2} \): Тетраэдрическая молекула метана
Метан (CH 4 ), этан (C 2 H 6 ) и пропан (C 3 H 8 ) являются началом ряда соединений, в которых любые два члена в последовательности различаются одним атомом углерода и двумя атомами водорода, а именно единицей CH 2 . Первые 10 членов этой серии приведены в таблице \ (\ PageIndex {1} \).
| Имя | Молекулярная формула (C n H 2n + 2 ) | Концентрированная структурная формула | Количество возможных изомеров |
|---|---|---|---|
| метан | СН 4 | Канал 4 | – |
| этан | С 2 В 6 | СН 3 СН 3 | – |
| пропан | С 3 В 8 | Канал 3 Канал 2 Канал 3 | – |
| бутан | С 4 В 10 | Канал 3 Канал 2 Канал 2 Канал 3 | 2 |
| пентан | С 5 В 12 | Канал 3 Канал 2 Канал 2 Канал 2 Канал 3 | 3 |
| гексан | С 6 В 14 | Канал 3 Канал 2 Канал 2 Канал 2 Канал 2 Канал 3 | 5 |
| гептан | С 7 В 16 | Канал 3 Канал 2 Канал 2 Канал 2 Канал 2 Канал 2 Канал 3 | 9 |
| октановое число | С 8 В 18 | Канал 3 Канал 2 Канал 2 Канал 2 Канал 2 Канал 2 Канал 2 Канал 3 | 18 |
| нонан | С 9 В 20 | канал 3 канал 2 канал 2 канал 2 канал 2 канал 2 канал 2 канал 2 канал 3 | 35 |
| декан | С 10 В 22 | канал 3 канал 2 канал 2 канал 2 канал 2 канал 2 канал 2 канал 2 канал 2 канал 3 | 75 |
Рассмотрим ряд на рисунке \ (\ PageIndex {3} \).Последовательность начинается с C 3 H 8 , и на каждом шаге вверх по серии добавляется блок CH 2 . Любое семейство соединений, в котором соседние члены отличаются друг от друга определенным фактором (здесь группа CH 2 ), называется гомологическим рядом. Члены такого ряда, называемые гомологами , обладают свойствами, которые изменяются регулярным и предсказуемым образом. Принцип гомологии обеспечивает организацию органической химии во многом так же, как периодическая таблица Менделеева обеспечивает организацию неорганической химии.Вместо ошеломляющего множества отдельных углеродных соединений мы можем изучить несколько членов гомологического ряда и на их основе вывести некоторые свойства других соединений в этом ряду.
Рисунок \ (\ PageIndex {3} \): члены гомологического ряда. Каждая последующая формула включает на один атом углерода и на два атома водорода больше, чем предыдущая формула.
Принцип гомологии позволяет нам написать общую формулу для алканов: C n H 2 n + 2 .Используя эту формулу, мы можем написать молекулярную формулу для любого алкана с заданным числом атомов углерода. Например, алкан с восемью атомами углерода имеет молекулярную формулу C 8 H (2 × 8) + 2 = C 8 H 18 .
Ключевые вынос
- Простые алканы существуют в виде гомологического ряда, в котором соседние члены различаются единицей CH 2 .
алканов | MCC Organic Chemistry
Ключевые термины
Убедитесь, что вы можете определить и использовать в контексте следующие ключевые термины.
- алкан с разветвленной цепью
- конституциональный или структурный изомер
- гомологическая серия
- изомер
- углеводород насыщенный
- алкан с прямой цепью (или нормальный алкан)
Учебные заметки
Серия соединений, в которой последовательные члены отличаются друг от друга единицей CH 2 , называется гомологической серией. Таким образом, серии CH 4 , C 2 H 6 , C 3 H 8 .. . C n H 2n + 2 , является примером гомологической серии.
Важно сохранить в памяти названия первых 10 алканов с прямой цепью (т.е. от CH 4 до C 10 H 22 ). Вы будете использовать эти имена неоднократно, когда начнете учиться получать систематические названия большого количества разнообразных органических соединений. Вам не нужно запоминать возможное количество изомеров для алканов, содержащих более семи атомов углерода. При необходимости такая информация доступна в справочниках.Рисуя изомеры, будьте осторожны, чтобы не обмануть себя, думая, что вы можете нарисовать больше изомеров, чем предполагалось. Помните, что каждый изомер можно нарисовать несколькими разными способами, и вы можете случайно подсчитать один и тот же изомер более одного раза.
Алканы — это органические соединения, которые полностью состоят из одинарных атомов углерода и водорода и лишены каких-либо других функциональных групп. Алканы имеют общую формулу [латекс] C_nH_ {2n + 2} [/ латекс] и могут быть подразделены на следующие три группы: линейные алканы с прямой цепью, разветвленные алканы и циклоалканы.Алканы также являются насыщенными углеводородами.
Циклоалканы представляют собой циклические углеводороды, что означает, что атомы углерода в молекуле расположены в форме кольца. Циклоалканы также являются насыщенными, что означает, что все атомы углерода, составляющие кольцо, одинарно связаны с другими атомами (без двойных или тройных связей). Существуют также полициклические алканы, которые представляют собой молекулы, содержащие два или более циклоалкана, которые соединены, образуя несколько колец.
Это вводная страница об алканах, таких как метан, этан, пропан, бутан и остальных обычных алканах.На этой странице рассматриваются их формулы и изомерия, их физические свойства и введение в их химическую реакционную способность.
Молекулярные формулы
Алканы — простейшее семейство углеводородов — соединений, содержащих только углерод и водород. Алканы содержат только углерод-водородные связи и одинарные углерод-углеродные связи. Первые шесть алканов следующие:
| метан | СН 4 |
| этан | С 2 В 6 |
| пропан | С 3 В 8 |
| бутан | С 4 В 10 |
| пентан | С 5 В 12 |
| гексан | С 6 В 14 |
Вы можете определить формулу любого из алканов, используя общую формулу C n H 2n + 2
Изомерия
Все алканы, содержащие 4 или более атомов углерода, демонстрируют структурную изомерию, что означает, что для каждой молекулярной формулы можно нарисовать две или более различных структурных формул.
Пример
Пример: бутан или метилпропан
C 4 H 10 может быть любой из этих двух разных молекул:
Называются бутан и 2-метилпропан соответственно
Что такое структурная изомерия?
Изомеры — это молекулы, которые имеют одинаковую молекулярную формулу, но имеют другое расположение атомов в пространстве. Это исключает любые другие устройства, которые возникают просто из-за вращения молекулы как целого или вращения вокруг определенных связей.Например, обе следующие молекулы являются одной и той же молекулой. Они не изомеры; оба бутана.
Есть также бесконечное количество других возможных способов, которыми эта молекула могла бы скручиваться. Все одинарные углерод-углеродные связи вращаются полностью свободно. Если бы перед вами была модель молекулы, вам пришлось бы разобрать ее на части и перестроить, если вы хотите сделать изомер этой молекулы. Если вы можете создать явно другую молекулу, просто вращая одинарные связи, она не будет отличаться — это все та же молекула.
В структурной изомерии атомы расположены в совершенно другом порядке. В этом легче убедиться на конкретных примерах. Далее рассматриваются некоторые способы возникновения структурных изомеров. Названия различных форм структурной изомерии, вероятно, не имеют большого значения, но вы должны знать о различных возможностях, когда приступаете к рисованию изомеров.
Цепная изомерия
Эти изомеры возникают из-за возможности разветвления углеродных цепей.Например, есть два изомера бутана, C 4 H 10 . В одном из них атомы углерода образуют «прямую цепь», а в другом — разветвленную.
Будьте осторожны, чтобы не нарисовать «ложные» изомеры, которые являются просто скрученными версиями исходной молекулы. Например, эта структура представляет собой версию бутана с прямой цепью, вращающуюся вокруг центральной углерод-углеродной связи.
В этом легко убедиться на модели. Это пример, который мы уже использовали в верхней части этой страницы.
Пример
Пример 1: Цепные изомеры в пентане
Пентан, C 5 H 12 , имеет три цепных изомера. Если вы думаете, что можете найти какие-то другие, это просто искаженные версии приведенных ниже. Если сомневаетесь, сделайте несколько моделей.
Упражнения
Вопрос
Указать все изомеры гексанола с прямой цепью.
Решение
углеводородов | Определение, типы и факты
Алканы, углеводороды, в которых все связи одинарные, имеют молекулярные формулы, которые удовлетворяют общему выражению C n H 2 n + 2 (где n — целое число ).Углерод s p 3 гибридизирован (три пары электронов участвуют в связывании, образуя тетраэдрический комплекс), и каждая связь C-C и C-H является сигма-связью ( см. Химическое связывание ). ). В порядке увеличения числа атомов углерода метан (CH 4 ), этан (C 2 H 6 ) и пропан (C 3 H 8 ) являются первыми тремя членами ряда.
Метан, этан и пропан — единственные алканы, однозначно определяемые их молекулярной формулой.Для C 4 H 10 два разных алкана удовлетворяют правилам химической связи (а именно, что углерод имеет четыре связи, а водород — одну в нейтральных молекулах). Одно соединение, называемое n -бутан, где префикс n — обозначает нормальный, имеет четыре атома углерода, связанные в непрерывную цепь. Другой, называемый изобутаном, имеет разветвленную цепь.
Различные соединения, имеющие одинаковую молекулярную формулу, называются изомерами. Говорят, что изомеры, которые различаются порядком соединения атомов, имеют различное строение и называются структурными изомерами.(Старое название — структурные изомеры.) Соединения n -бутан и изобутан являются конституциональными изомерами и единственно возможными для формулы C 4 H 10 . Поскольку изомеры представляют собой разные соединения, они могут иметь разные физические и химические свойства. Например, n -бутан имеет более высокую температуру кипения (-0,5 ° C [31,1 ° F]), чем изобутан (-11,7 ° C [10,9 ° F]).
Нет простой арифметической зависимости между числом атомов углерода в формуле и числом изомеров.Теория графов была использована для расчета количества структурных изомеров алканов, возможных для значений n в C n H 2 n + 2 от 1 до 400. Количество структурных изомеров резко увеличивается по мере увеличения количество атомов углерода увеличивается. Вероятно, не существует верхнего предела возможного количества атомов углерода в углеводородах. Алкан CH 3 (CH 2 ) 388 CH 3 , в котором 390 атомов углерода связаны в непрерывную цепь, был синтезирован в качестве примера так называемого сверхдлинного алкана.Несколько тысяч атомов углерода объединены в молекулы углеводородных полимеров, таких как полиэтилен, полипропилен и полистирол.
| молекулярная формула | количество конституционных изомеров |
|---|---|
| С 3 В 8 | 1 |
| С 4 В 10 | 2 |
| С 5 В 12 | 3 |
| С 6 В 14 | 5 |
| С 7 В 16 | 9 |
| С 8 В 18 | 18 |
| С 9 В 20 | 35 год |
| С 10 В 22 | 75 |
| С 15 В 32 | 4 347 |
| С 20 В 42 | 366 319 |
| С 30 В 62 | 4,111,846,763 |
Необходимость дать каждому соединению уникальное имя требует большего разнообразия терминов, чем доступно с описательными префиксами, такими как n — и iso-.Присвоение названий органическим соединениям упрощается за счет использования формальных систем номенклатуры. Номенклатура в органической химии бывает двух типов: общая и систематическая. Общие имена возникают по-разному, но имеют общую черту, заключающуюся в отсутствии необходимой связи между именем и структурой. Имя, соответствующее определенной структуре, нужно просто запомнить, как и выучить имя человека. С другой стороны, систематические имена привязаны непосредственно к молекулярной структуре в соответствии с общепринятым набором правил.Наиболее широко используемые стандарты для номенклатуры органических веществ возникли на основе предложений, сделанных группой химиков, собранных для этой цели в Женеве в 1892 году, и регулярно пересматриваются Международным союзом чистой и прикладной химии (IUPAC). Правила IUPAC регулируют все классы органических соединений, но в конечном итоге основаны на названиях алканов. Соединения из других семейств рассматриваются как производные алканов путем присоединения функциональных групп к углеродному скелету или иным образом его модификации.
Правила IUPAC присваивают неразветвленным алканам названия в соответствии с числом их атомов углерода. Метан, этан и пропан сохраняются для CH 4 , CH 3 CH 3 и CH 3 CH 2 CH 3 соответственно. Префикс n — не используется для неразветвленных алканов в систематической номенклатуре ИЮПАК; следовательно, CH 3 CH 2 CH 2 CH 3 определяется как бутан, а не n -бутан.Начиная с пятиуглеродных цепей, названия неразветвленных алканов состоят из латинского или греческого корня, соответствующего количеству атомов углерода в цепи, за которым следует суффикс -ан. Группа соединений, таких как неразветвленные алканы, которые отличаются друг от друга последовательным введением групп CH 2 , составляют гомологичный ряд.
| формула алкана | название | формула алкана | название |
|---|---|---|---|
| CH 4 | метан | Канал 3 (Канал 2 ) 6 Канал 3 | октан |
| Канал 3 Канал 3 | этан | Канал 3 (Канал 2 ) 7 Канал 3 | нонан |
| Канал 3 Канал 2 Канал 3 | пропан | Канал 3 (Канал 2 ) 8 Канал 3 | декан |
| Канал 3 Канал 2 Канал 2 Канал 3 | бутан | Канал 3 (Канал 2 ) 13 Канал 3 | пентадекан |
| Канал 3 (Канал 2 ) 3 Канал 3 | пентан | Канал 3 (Канал 2 ) 18 Канал 3 | икозан |
| Канал 3 (Канал 2 ) 4 Канал 3 | гексан | Канал 3 (Канал 2 ) 28 Канал 3 | триаконтан |
| Канал 3 (Канал 2 ) 5 Канал 3 | гептан | Канал 3 (Канал 2 ) 98 Канал 3 | гектан |
Алканы с разветвленными цепями названы на основе названия самой длинной цепи атомов углерода в молекуле, называемой родительской.Показанный алкан имеет семь атомов углерода в самой длинной цепи и поэтому назван производным гептана, неразветвленного алкана, содержащего семь атомов углерода. Положение (метильного) заместителя CH 3 в семиуглеродной цепи определяется числом (3-), называемым локантом, полученным путем последовательной нумерации атомов углерода в родительской цепи, начиная с конца, ближайшего к ответвлению. Поэтому соединение называется 3-метилгептаном.
При наличии двух или более одинаковых заместителей повторяющиеся префиксы (ди-, три-, тетра- и т. Д.)) используются вместе с отдельным локатором для каждого заместителя. Различные заместители, такие как этильная (CH 2 CH 3 ) и метильная (―CH 3 ) группы, указаны в алфавитном порядке. При расположении по алфавиту повторяющиеся префиксы игнорируются. В алканах нумерация начинается с конца, ближайшего к заместителю, который появляется первым в цепи, так что углерод, к которому он присоединен, имеет как можно более низкий номер.
Метил и этил являются примерами алкильных групп.Алкильная группа получается из алкана путем удаления одного из его атомов водорода, тем самым оставляя потенциальную точку присоединения. Метил — единственная алкильная группа, производная от метана, а этил — единственная группа из этана. Имеются две C 3 H 7 и четыре C 4 H 9 алкильные группы. Правила ИЮПАК для наименования алканов и алкильных групп охватывают даже очень сложные структуры и регулярно обновляются. Они недвусмысленны в том смысле, что, хотя одно соединение может иметь более одного правильного названия IUPAC, нет никакой возможности, чтобы два разных соединения имели одно и то же имя.
Органическая номенклатура
Обозначение органических соединений
Растущее количество органических соединений, идентифицируемых с каждым днем, вместе с тем фактом, что многие из этих соединений являются изомерами других соединений, требует разработки систематической системы номенклатуры. Подобно тому, как каждое отдельное соединение имеет уникальную молекулярную структуру, которую можно обозначить структурной формулой, каждому соединению должно быть дано характерное и уникальное имя.
По мере того, как органическая химия росла и развивалась, многим соединениям были даны тривиальные имена, которые теперь широко используются и признаются. Вот несколько примеров:
| Имя | Метан | Бутан | Ацетон | Толуол | Ацетилен | Этиловый спирт |
|---|---|---|---|---|---|---|
| Формула | CH 4 | C 4 H 10 | CH 3 COCH 3 | CH 3 C 6 H 5 | C 2 H 2 | С 2 H 5 ОН |
Такие общих названия часто происходят из истории науки и естественных источников определенных соединений, но отношения этих названий друг к другу произвольны, и никакие рациональные или систематические принципы не лежат в основе их присвоения.
Систематический подход IUPAC к номенклатуре
Рациональная система номенклатуры должна делать как минимум две вещи. Во-первых, он должен указывать, как атомы углерода данного соединения связаны вместе в характерной решетке цепочек и колец. Во-вторых, он должен идентифицировать и определять местонахождение любых функциональных групп, присутствующих в соединении. Поскольку водород является таким обычным компонентом органических соединений, его количество и расположение можно предположить, исходя из четырехвалентности углерода, и в большинстве случаев нет необходимости указывать его.
Система номенклатуры ИЮПАК — это набор логических правил, разработанных и используемых химиками-органиками для обхода проблем, вызванных произвольной номенклатурой. Зная эти правила и имея структурную формулу, можно написать уникальное имя для каждого отдельного соединения. Точно так же, получив имя IUPAC, можно написать структурную формулу. В общем, имя IUPAC будет иметь три основные характеристики:
• Корень или основание, обозначающее основную цепь или кольцо атомов углерода, присутствующих в молекулярной структуре.
• Суффикс или другой элемент (ы), обозначающий функциональные группы, которые могут присутствовать в соединении.
• Названия групп заместителей, кроме водорода, завершающих молекулярную структуру.
В качестве введения в систему номенклатуры ИЮПАК мы сначала рассмотрим соединения, не имеющие определенных функциональных групп. Такие соединения состоят только из атомов углерода и водорода, связанных вместе сигма-связями (все атомы углерода sp 3 гибридизированы).
Отличное представление органической номенклатуры представлено на странице номенклатуры. созданный Дэйвом Вудкоком.
Также доступна полная презентация Правил IUPAC.
Алканы
Углеводороды, не содержащие функциональных групп с двойной или тройной связью, классифицируются как алканы, или циклоалканы, , в зависимости от того, расположены ли атомы углерода молекулы только в цепях или также в кольцах. Хотя эти углеводороды не имеют функциональных групп, они составляют основу, на которой функциональные группы расположены в других классах соединений, и обеспечивают идеальную отправную точку для изучения и наименования органических соединений.Алканы и циклоалканы также являются членами более крупного класса соединений, называемых алифатическими . Проще говоря, алифатические соединения — это соединения, которые не содержат ароматических колец в своей молекулярной структуре.
В следующей таблице перечислены названия IUPAC, присвоенные простым алканам с непрерывной цепью от C-1 до C-10. Обычный суффикс «ane» идентифицирует эти соединения как алканы. Алканы с более длинной цепью хорошо известны, и их названия можно найти во многих справочниках и учебниках.Названия с метан по декан следует запомнить, поскольку они составляют корень многих имен ИЮПАК. К счастью, для именования цепочек из пяти или более атомов углерода используются общие числовые префиксы.
| Название | Молекулярная Формула | Структурная Формула | Изомеры | Название | Молекулярная Формула | Структурная 6 Формула | 9107 | CH 4 | CH 4 | 1 | шестигранник ane | C 6 H 14 | CH 3 (CH 2 ) 4 CH 3 | 5 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| eth ane | C 2 H 6 | CH 3 CH 3 | 1 | hept ane | C 7 H 7 ane | H 16 | CH 3 (CH 2 ) 5 CH 3 | 9 | ||||||||
| опора ane | C 3 H 8 | CH 3 CH 2 CH 3 | 1 | oct ane | C 8 H 18 | CH 3 (CH 2 ) 6 CH 3 | 18 | |||||||||
| но ane | C 4 H 10 | CH 3 CH 2 CH 2 CH 3 | 2 | non ane | C 9 H 20 | CH 3 (CH 2 ) 7 CH 3 | 35 | |||||||||
| пент ane | C 5 H 12 | CH 3 (CH 2 ) 3 CH 3 | 3 | dec ane | C 10 H 22 | СН 9 0034 3 (Канал 2 ) 8 Канал 3 | 75 |
Некоторые важные тенденции поведения и терминология:
(i) Формулы и структуры этих алканов увеличиваются равномерно
с шагом CH 2 .
(ii) Подобная однородная вариация в серии соединений называется
гомолог .
(iii) Все эти формулы подходят для C n H 2n + 2
правило. Это также максимально возможное соотношение H / C для стабильного углеводорода.
(iv) Поскольку отношение H / C в этих соединениях максимально, мы называем их
насыщенный (водородом).
Начиная с бутана (C 4 H 10 ) и становясь более многочисленным с более крупными алканами,
отметим наличие изомеров алканов.Например, есть пять C 6 H 14
изомеры, показанные ниже в виде сокращенных формул (с A по E ):
Хотя все эти различные соединения имеют одну и ту же молекулярную формулу, только одно ( A ) может называться гексаном.
Как же тогда назвать остальных?
Система IUPAC требует, чтобы, во-первых, у нас были имена для простых неразветвленных цепей, как отмечалось выше, а во-вторых, чтобы у нас были имена для простых алкильных групп, которые могут быть присоединены к цепям.Примеры некоторых общих алкильных групп приведены в следующей таблице. Обратите внимание, что суффикс «ane» заменен на « yl » в группах имен. Символ R используется для обозначения родовой (неуказанной) алкильной группы.
| Группа | СН 3 — | С 2 В 5 — | Канал 3 Канал 2 Канал 2 — | (CH 3 ) 2 CH– | Канал 3 Канал 2 Канал 2 Канал 2 — | (канал 3 ) 2 канал 2 — | Канал 3 Канал 2 Канал (Канал 3 ) — | (CH 3 ) 3 C– | R– |
| Имя | метил | Этил | Пропил | Изопропил | Бутил | Изобутил | сек -бутил | трет -бутил | Алкил |
Правила ИЮПАК по номенклатуре алканов 1. Найдите и назовите самую длинную непрерывную углеродную цепь. |
Для вышеуказанных изомеров гексана названия IUPAC: B 2-метилпентан C 3-метилпентан
D 2,2-диметилбутан E 2,3-диметилбутан
Галогеновые заместители легко адаптируются, используя названия: фтор (F-), хлор (Cl-), бром (Br-) и йод (I-).Например, (CH 3 ) 2 CHCH 2 CH 2 Br будет называться 1-бром-3-метилбутаном. Если галоген связан с простой алкильной группой, можно использовать альтернативное название «алкилгалогенид». Таким образом, C 2 H 5 Cl может быть назван хлорэтаном (для двухуглеродной цепи не требуется номер локатора) или этилхлоридом. Галогенированные алкильные заместители, такие как бромметил, BrCH 2 — и трихлорметил, CCl 3 -, могут быть перечислены и расположены в алфавитном порядке в соответствии с их полными названиями.
Для дополнительных примеров того, как эти правила используются для наименования разветвленных алканов, и для некоторых подправил номенклатуры .
Циклоалканы
Циклоалканы имеют один или несколько
кольца из атомов углерода. Простейшие примеры этого класса состоят из
одиночное незамещенное углеродное кольцо, и они образуют гомологичную серию, подобную
к неразветвленным алканам. Имена ИЮПАК первых пяти членов
эта серия представлена в следующей таблице.Последний столбец (заштрихованный желтым) дает
общая формула циклоалкана любого размера. Если простой неразветвленный
алкан превращается в циклоалкан двумя атомами водорода, по одному с каждого конца
цепи, должны быть потеряны. Отсюда общая формула циклоалкана
состоит из n атомов углерода и составляет C n H 2n . Хотя циклоалкан имеет на два атома водорода меньше, чем эквивалентный алкан, каждый атом углерода связан с четырьмя другими атомами, поэтому такие соединения по-прежнему считаются насыщенными водородом .
Замещенные циклоалканы имеют название, очень похожее на то, что используется для обозначения разветвленных алканов. Основное отличие правил и процедур заключается в системе нумерации. Поскольку все атомы углерода в кольце эквивалентны (у кольца нет концов, как у цепи),
нумерация начинается с замещенного кольцевого атома.
Правила ИЮПАК по номенклатуре циклоалканов 1. Для монозамещенного циклоалкана кольцо дает корневое имя (таблица выше), а замещающая группа называется обычным образом.Номер места указывать не нужно. |
Примеры использования этих правил для обозначения замещенных циклоалканов.
Маленькие кольца, такие как три и
четырехчленные кольца имеют значительную угловую деформацию в результате искажения
sp 3 углеродных валентных углов от идеального
От 109,5 ° до 60 ° и 90 ° соответственно. Эта угловая деформация часто увеличивает химическую активность таких соединений, что приводит к образованию продуктов расщепления кольца.Также важно
признать, что, за исключением циклопропана, циклоалкильные кольца
не плоские (плоские). Трехмерные формы, принятые обычным
кольца (особенно циклогексан и более крупные кольца) описаны и обсуждаются в разделе «Конформационный анализ».
Углеводороды, содержащие более одного кольца, являются общими и обозначаются как бициклические (два кольца), трициклические, (три кольца) и, как правило, полициклические соединения .Молекулярные формулы таких соединений имеют отношения H / C, которые уменьшаются с увеличением числа
колец. В общем, для углеводорода, состоящего из 9 · 1072 n атомов углерода, 9 · 1073
для колец м формула: C n H (2n + 2 — 2m) . Структурное соотношение колец в полициклическом соединении может варьироваться. Они могут быть отдельными и независимыми, или они могут иметь один или два общих атома. Некоторые примеры этих возможных расположений показаны в следующей таблице.
Примеры изомерного C
8 H 14 Бициклоалканы
| Изолированные кольца | Спиро-кольца | Кольца с предохранителями | Кольца с перемычкой |
|---|---|---|---|
| Общие атомы отсутствуют | Один общий атом | Одна обыкновенная облигация | Два общих атома |
Алкены и алкины
Алкены и алкины представляют собой углеводороды, которые соответственно имеют углерод-углеродную двойную связь, и углерод-углеродную тройную связь, функциональные группы.Молекулярные формулы этих ненасыщенных углеводородов отражают множественное связывание функциональных групп:
| Алкан | R – CH 2 –CH 2 –R | C n H 2n + 2 | Это максимальное отношение H / C для данного количества атомов углерода. |
|---|---|---|---|
| Алкен | R – CH = CH – R | C n H 2n | Каждая двойная связь уменьшает количество атомов водорода на 2. |
| Алкин | R – C≡C – R | C n H 2n-2 | Каждая тройная связь уменьшает количество атомов водорода на 4. |
Как отмечалось ранее в разделе «Анализ молекулярных формул», молекулярная формула углеводорода предоставляет информацию о возможных структурных типах, которые он может представлять. Например, рассмотрим соединения формулы C 5 H 8 . Формула пятиуглеродного алканпентана: C 5 H 12 , поэтому разница в содержании водорода равна 4.Это различие предполагает, что такие соединения могут иметь тройную связь, две двойные связи, кольцо плюс двойную связь или два кольца. Здесь показаны некоторые примеры, а еще как минимум четырнадцать!
Правила ИЮПАК по номенклатуре алкенов и циклоалкенов 1. Суффикс (окончание) ен указывает на алкен или циклоалкен. |
Правила IUPAC по номенклатуре алкинов 1. Суффикс (окончание) yne указывает на алкин или циклоалкин. |
Примеры того, как эти правила используются при присвоении имен алкенам, алкинам и циклическим аналогам .
Номенклатура соединений с замещенным бензольным кольцом менее систематична, чем номенклатура алканов, алкенов и алкинов. Несколько монозамещенных соединений названы с использованием названия группы в качестве префикса к «бензолу», как показано объединенными названиями, перечисленными ниже. Однако большинство этих соединений имеют единичные уникальные имена. В усвоении этих имен нет простой альтернативы запоминанию.
Две обычно встречающиеся группы заместителей, которые включают бензольное кольцо, — это фенил , сокращенно Ph-, и бензил , сокращенно Bn-.Они показаны здесь с примерами их использования. Будьте осторожны, чтобы не путать фенильную (произносится как фенил ) группу с составным фенолом (произносится как фенил ). Общее и полезное обобщенное обозначение, которое дополняет использование R- для алкильной группы, — это Ar- для арильной группы (любого ароматического кольца).
Когда в бензольном кольце присутствует более одного заместителя, относительные положения заместителей должны быть обозначены нумерацией атомов углерода в кольце или другими обозначениями.В случае дизамещенных бензолов префиксы орто, мета и пара обычно используются для обозначения 1,2-, 1,3- или 1,4-отношения соответственно. В следующих примерах первый ряд соединений показывает это использование красным цветом. Некоторые дизамещенные толуолы имеют единственные названия (например, ксилол, крезол и толуидин), а их изомеры обычно обозначаются префиксом o rtho, m eta или p ara. Некоторые дизамещенные бензолы имеют особые названия, данные конкретным изомерам (например,грамм. салициловая кислота и резорцин). Наконец, если имеется три или более группы заместителей, кольцо нумеруется таким образом, чтобы назначать заместителям наименьшие возможные номера, как показано в последней строке примеров. Заместители перечислены в алфавитном порядке в окончательном названии. Если замена симметрична (третий пример слева), нумерация соответствует алфавитному порядку.
Органические химические вещества: алканы, алкены и ацетилены
1,1,2,2-Тетраметилциклопропан, 99%
1,13-Тетрадекадиен, 90 +%
1,1,4,4-Тетрафенил-1,3-бутадиен, 99%
1,1′-бинафтил, 98%
1,1-Дифенилэтилен, 98%
1,1-дифенилгексан, 98%
1,1-дифенилпентан, 97%
1,1-дифенилпропан, 98 +%
1,2,3,4,5-Пентаметилциклопентадиен, 94%
1,2,3,4-Тетрагидронафталин, 97%
1,2,3,4-Тетраметилбензол, 95%
1,2,4,5-Тетраметилбензол, 97 +%
1,2,4-триметилбензол, 98%
1,2-бис (1-нафтил) этан, 97%
1,2-ди (3-инденил) этан, 98%
1,2-диэтилбензол, 97%
1,2-Диметилнафталин, 98%
1,2-дифенилциклопропан, цис + транс, 97%
1,2-дифенилэтан, 98 +%
1,2-ди (п-толил) этан, 98%
1- (2-Фенилэтил) -4- (фенилэтинил) бензол, 97%
1,3,5,5-Тетраметил-1,3-циклогексадиен, 94%
1,3,5,7-Циклооктатетраен, 98%, стаб.с 0,1% гидрохиноном
1,3,5-Триэтилбензол, 95%
1,3,5-Триэтинилбензол, 98%
1,3,5-Триизопропилбензол, 95%
1,3,5-трифенилбензол, 99 +%
1,3,5-Три-трет-бутилбензол, 97 +%
1,3-Циклогексадиен, 96%, стаб.с 0,1% BHT
1,3-Циклооктадиен, 97%
1,3-диэтилбензол, 97 +%
1,3-диизопропилбензол, 96%
1,3-Диизопропилциклогексан, цис + транс, 97 +%
1,3-дифенилпропан, 98%
1,3-ди-трет-бутилбензол, 99%
1,4,6,7-Тетраметилнафталин, 98%
1,4-Бис (2-метилстирил) бензол, 99%
1,4-бис (фенилэтинил) бензол, 97%
1,4-Циклогексадиен, 97% стаб.с 0,1% BHT
1,4-Дициклогексилбензол, 99%
1,4-диэтилбензол, 98%
1,4-диизопропилбензол, 98%
1,4-диизопропилциклогексан, цис + транс, 98%
1,4-ди-н-бутилбензол, 97 +%
1,4-дифенилбутадиин, 99%
1,4-ди-трет-бутилбензол, 98%
1,4-гексадиен, цис + транс, 99%
1,5,9,13-тетрадекатетраен, 95%
1,5,9-декатриен, цис + транс, 97%
1,5-Диметилнафталин, 99%
Hydrocarbon — обзор | Темы ScienceDirect
8.03.5.5 Изопреноиды
Углеводороды, формально образованные из повторяющихся звеньев изопрена C 5 ( 5 ), повсеместно присутствуют в древних отложениях и нефти. Наиболее распространенными и распространенными из них являются C 19 и C 20 регулярно разветвленные (соединение изопреновых единиц от головы к хвосту ( 6 )) соединения пристан ( 9 ) и фитан ( 10 ). которые широко рассматриваются как продукты трансформации фитола ( 11 ), этерифицирующего спирта хлорофиллов цианобактерий и зеленых растений (например,g., Chlorophyll a ( 43 )) (Didyk et al. , 1978). Токоферолы являются дополнительными растительными и фитопланктонными источниками пристана (Goosens et al. , 1984). Археол ( 12 ) (дифитанилглицерин)
является наиболее часто описываемым ядерным липидом в архее, встречающимся в обоих основных царствах, Euryarchaeota и Crenarchaeota (Kates, 1993; Koga et al. , 1993), и также является важным источник осадочного фитана ( 10 ), особенно в пробах из экстремальных сред.Однако многие масла и битумы также содержат различное количество правильно разветвленных ациклических изопреноидов C 21+ ( 6 ), которые должны происходить из предшественников> C 20 . Предполагается, что археи являются основным источником соединений этого типа. Хотя Albaiges (1980) сообщил о расширенных регулярных изопреноидах с цепями, равными C 45 в маслах, сведения об их наличии в культивируемых организмах ограничены. Langworthy et al. (1982) указали на присутствие регулярных изопреноидных цепей длиной C 30 в нейтральных липидных фракциях термоацидофилов, но это не объясняет более широкий диапазон чисел углерода в ассоциациях ископаемых.Полярные эфирные липиды крайних галофилов часто содержат C 20 –C 25 и C 25 –C 25 диэфирные аналоги археола ( 12 ) и, следовательно, являются логическим источником из C 25 и низшие регулярные ациклические изопреноидные углеводороды, которые неизменно присутствуют в битумоидах и нефтях соленых озер (например, McKirdy et al. , 1982). Другие регулярные изопреноиды C 21+ в существующих организмах могли остаться незамеченными, поскольку большинство исследований липидного профиля на сегодняшний день сосредоточено на соединениях, которые могут стать летучими для анализа с помощью ГХ-МС.Многие из недавно идентифицированных архейных липидов имеют нерегулярные изопреноидные цепи C 40 , и вполне вероятно, что существуют другие, в настоящее время неизвестные высокомолекулярные полярные предшественники липидов, которые не были обнаружены с помощью обычных аналитических окон.
Неправильно разветвленные изопреноиды также являются заметными осадочными углеводородами. Сквалан ( 15 ), состоящий из двух изопреноидных составляющих C 15 , связанных хвост-хвост ( 7 ), является очень распространенным компонентом битумов и масел, и, хотя его логический предшественник сквален встречается в большинстве организмов, археи могут быть преобладающими источниками.Сквалан и различные ненасыщенные производные присутствуют в фракциях нейтральных липидов многих архей, и их количество наиболее высоко в образцах окружающей среды с общим повышенным содержанием ациклических изопреноидов, например, из соленых озер (McKirdy et al. , 1986; ten Haven ). и др., , 1988). Связанный хвост к хвосту ( 7 ) изопреноид ликопан C 40 ( 22 ) часто обнаруживается в озерных и морских отложениях (например, Freeman et al., 1990, 1994; Wakeham et al. , 1993) и в твердых частицах органического вещества из колонн с бескислородной водой (например, Wakeham et al. , 1993). Возможные предшественники включают каротиноиды семейства ликопин ( 21 ), которые встречаются, например, в аноксигенных фототрофных бактериях (Раздел 8.03.6.1.4), или ликопадиеноподобные предшественники, продуцируемые водорослями, такими как Botryococcus braunii (Derenne ). и др. , 1990; Уэйкхэм и др. , 1993).
Основным источником бифитана ( 16 ), изопреноида C 40 с ветвлением «голова к голове» ( 8 ), является кальдархеол ( 13 ) (дибифитанил-диглицерин-тетраэфир), который является заметным основной липид в метаногенах (Koga et al., 1993) и члены королевства Crenarchaeota (например, Kates, 1993). Известно, что кренархеи и некоторые метаногены продуцируют полярные липиды с вариантами ядра кальдархея с циклопентаном и, иногда, циклогексановыми кольцами (например, ( 14 )). Эти сложные липиды были обнаружены в изобилии в фильтратах из открытых океанических вод, что свидетельствует о вероятности того, что эти археи являются важным компонентом океанического планктона (DeLong et al. , 1998; Sinninghe Damsté et al., 2002а). Бифитан ( 16 ) давно признан одним из основных осадочных углеводородов (Moldowan and Seifert, 1979) и может иметь как кренархеотное, так и эвриархеотное происхождение.
Неправильно разветвленные изопреноиды с более низкой молекулярной массой также иногда заметны в отложениях и нефтях. Неправильный хвост к хвосту ( 7 ) связан C 20 изопреноидный углеводород 2,6,11,15-тетраметилгексадекан ( 17 ) (кроцетан) и его аналог C 25 2,6,10,15 19-пентаметилкозан ( 18 ) (часто называемый PMI или в более ранней литературе PME) считаются диагностическими маркерами архей, которые играют центральную роль в метановом цикле.Эти соединения были обнаружены в различных культивируемых организмах, микробных сообществах и отложениях, содержащих метаногенные вещества (например, Brassell et al. , 1981; Koga et al. , 1993; Risatti et al. , 1984; Schouten et al. , 2001a, b, c, 1997) и метанотрофных архей (например, Bian et al. , 2001; Elvert et al. , 1999; Hinrichs et al. , 2000; Pancost et al. ). , 2000; Тиль и др. , 1999). Кроцетан также недавно обнаружен в сырой нефти (Barber et al., 2001; Barber et al. , 2002; Гринвуд и Саммонс, 2003). PMI, по-видимому, приурочен к мезозойским и более молодым породам, тогда как кроцетан, вероятно, имеет гораздо более длительную геологическую историю, поскольку он был обнаружен в породах триаса, девона и протерозоя (Greenwood and Summons, 2003).
Существуют и другие отличительные классы изопреноидов, которые, как считается, имеют весьма ограниченное биологическое происхождение. Соединения, называемые «сильно разветвленные изопреноиды» или HBI с C 20 , C 25 и C 30 (например,g., ( 19 )) биосинтезируются некоторыми диатомовыми водорослями (Volkman et al. , 1994) и поэтому считаются очень специфическими биомаркерами для этих организмов (Allard et al. , 2001; Belt et al. , 2000; Робсон и Роуленд, 1986; Роуленд и др. , 2001; Синнингх Дамсте и др. , 1999a, b; Summons и др. , 1993; Волкман и др. , 1994). Биомаркер ботриококкана ( 20 ) и родственные соединения происходят из ботриококценов, полиметилированных C 30 –C 37 и полиненасыщенных производных изомера неправильной конструкции сквалена, и, как известно, биосинтезируются только зеленой водорослью Botryococcus braunii (Metzger, Largeau, 1999).Определенные штаммы биосинтезируют циклоботриококцены (например, Metzger et al. , 1985) и полиметилсквалены, которые встречаются в виде их насыщенных углеводородных аналогов в древних отложениях и нефтях (Summons et al. , 2002).
Почему определенные соединения называются углеводородами Написать класс 11 по химии CBSE
Подсказка: Гомологический ряд соединений — это ряд соединений, которые имеют одну и ту же общую формулу, но отличаются от соседних членов группой $ -C {H} _ {2} — $.Они определяются углеводородной цепью.
Полный пошаговый ответ:
Некоторые соединения называются углеводородами, потому что они представляют собой группу соединений, состоящих из водорода и углерода.
Гомологичная группа соединений подобна алканам, алкенам, алкинам и т. Д.
Алканы имеют только атомы углерода, которые присоединены к другим атомам углерода одинарными связями.
В алкенах атомы углерода связаны по крайней мере одной двойной связью, а остальные могут быть или не быть одинарными связями.
В алкинах атомы углерода связаны по крайней мере одной тройной связью, а остальные могут быть или не быть одинарными связями.
Гомологическая группа соединений имеет одинаковую общую формулу.
Общая формула алканов гомологического ряда: $ {C} _ {n} {H} _ {2n + 2} $.
Общая формула алкенов гомологического ряда: $ {C} _ {n} {H} _ {2n} $.
Общая формула алкинов гомологического ряда: $ {C} _ {n} {H} _ {2n-2} $.
Первым членом гомологического ряда алканов является метан.
Первым членом гомологического ряда алкенов является этен.
Первым членом гомологического ряда алкинов является этин.
Этен можно превратить в этан с помощью реакции, известной как реакция каталитического гидрирования. Это называется так, потому что в качестве катализатора используется никель Ренея, платина или палладий. Реакция приведена ниже.
$ \ underset {Ethene} {{C} H_ {2} = C {H} _ {2}} \ quad + \ quad \ underset {Hydrogen} {{H} _ {2}} \ quad \ xrightarrow [ Никель] {423 \ quad K} \ quad \ underset {Ethane} {{CH} _ {3} -C {H} _ {3}} $
Необходимыми условиями для этой реакции являются наличие катализатора. Ni и температура должна быть 423К.
Примечание: Первый член гомологического ряда алкена и алкина имеет 2 атома углерода, потому что они включают двойные и тройные связи соответственно, что невозможно для одного углерода. Кроме того, если мы используем Pt или Pd в качестве катализатора, то реакцию можно проводить при комнатной температуре.

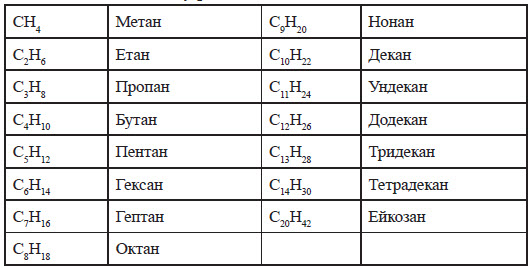 11
11
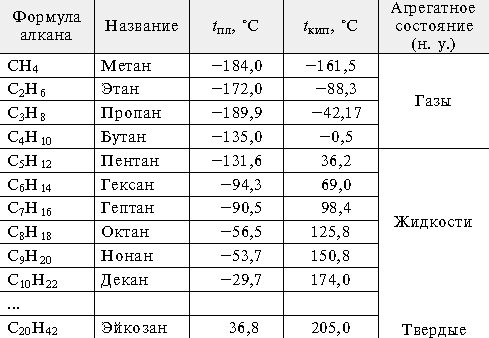
 Напишите уравнения возможных реакций данного соединения с хлороводородом. Приведите структурные формулы четырех изомеров данного углеводорода с открытой цепью углеродных атомов.
Напишите уравнения возможных реакций данного соединения с хлороводородом. Приведите структурные формулы четырех изомеров данного углеводорода с открытой цепью углеродных атомов.