РазработкиСтабильные изотопы и особо чистые веществаИспользование стабильных изотопов и особо чистых веществ лежит в основе многих наукоемких технологий в различных областях науки и техники, в частности, в медицине, атомной энергетике и электронике. В основу производства стабильных изотопов и особо чистых веществ положены уникальные технологии, разработанные в России: центробежное разделение и метод высокотемпературной ректификации воды. Номенклатура изотопной продукции
Взаимовыгодное сотрудничество в производстве и реализации изотопной продукции. |
Перспективные решения и запуск новых кооперационных проектов в микроэлектронике обсудили в РХТУ
9 декабря прошел круглый стол «Перспективные решения и запуск новых кооперационных проектов в микроэлектронике». В рамках онлайн-встречи профессиональное сообщество обсудило актуальные вопросы развития электронной промышленности, особое внимание было уделено сырьевому обеспечению отрасли – малотоннажной химии особо чистых веществ.
Мероприятие было инициировано Российским химико-технологическим университетом им. Д.И. Менделеева и Общероссийской общественной организацией «Деловая Россия». В работе круглого стола приняли участие представители промышленных компаний, предприниматели и сотрудники научных организаций.
Работу круглого стола торжественно открыл С.А. Гущин, председатель Комитета по машиностроению Общероссийской общественной организации «Деловая Россия». Сергей Анатольевич подчеркнул, что развитие отрасли возможно только в тесной связке науки и промышленности, и именно мероприятия такого формата позволяют создать доверительную коммуникационную площадку.
Сергей Анатольевич подчеркнул, что развитие отрасли возможно только в тесной связке науки и промышленности, и именно мероприятия такого формата позволяют создать доверительную коммуникационную площадку.
Модератором мероприятия выступил А.В. Масленников, директор Центра поддержки и развития технологических компаний «Акселератор Mendeleev». В ходе работы круглого стола были обсуждены вопросы формирования производственных цепочек компонентой базы для микроэлектроники и формирование комплексных научно-технологических проектов, направленных на реализацию стратегии развития электронной промышленности РФ до 2030 года.
Перебои импорта радиоэлектронных систем в 2020 поставили радиоэлектронную промышленность перед необходимостью развития российского производства компонентов и сырья для микроэлектроники. Это привело к двум крупным инициативам промышленных предприятий – ГК «Ростех» представила для согласования дорожную карту «Новые поколения микроэлектроники и создание электронной компонентной базы», а ГК «Росатом» в рамках соглашения с Правительством РФ по направлению развития в Российской Федерации высокотехнологичной области «Технологии новых материалов и веществ» инициировала совместно с Российским химико-технологическим университетом им. Д.И. Менделеева создание Ассоциации «Особо чистые вещества и материалы».
Д.И. Менделеева создание Ассоциации «Особо чистые вещества и материалы».
И.В. Мазилин, руководитель направления АО «Наука и инновации» рассказал о деятельности Ассоциации. К фокусным направлениям работы Ассоциации относится изучение и анализ успешного отечественного и международного опыта по производству особо чистых веществ и материалов, выявление приоритетных направлений развития в области особо чистых веществ и материалов и экспертиза проектов по разработке новых (восстановлению утраченных) технологий изготовления особо чистых веществ и материалов.
С сообщением выступил заместитель генерального директора по науке компании «Лассард» Б.Н. Левонович. Он рассказал о системной работе по формированию сквозных проектов по микроэлектронике, осветил принципы выстраивания матриц комплексных проектов. Сложность структуры проектов требует детальной проработки и выстраивания целостных производственных цепочек.
Достижения в области получения особо чистых веществ представили ученые РХТУ им. Д.И. Менделеева. И.Х. Аветисов осветил инициативу университета по созданию Национальной аналитической сертификационной лаборатории высокочистых веществ и материалов, которая позволит оценивать качество неорганических, органических и композиционных материалов в различных формах. И.В. Воротынцев представил достижения университета в области получения особо чистых газов новыми гибридными технологическими решениями, позволяющими снизить энергозатраты на получение целевых продуктов.
Д.И. Менделеева. И.Х. Аветисов осветил инициативу университета по созданию Национальной аналитической сертификационной лаборатории высокочистых веществ и материалов, которая позволит оценивать качество неорганических, органических и композиционных материалов в различных формах. И.В. Воротынцев представил достижения университета в области получения особо чистых газов новыми гибридными технологическими решениями, позволяющими снизить энергозатраты на получение целевых продуктов.
В ходе дискуссии В.С. Ежлов (АО «Объединенная приборостроительная корпорация») подчеркнул важность разработки законодательного поля в части нормирования требований по отнесению веществ к категориям особо чистых и высокочистых.
В.Е. Трохин (АО НЦ «Малотоннажная химия») подчеркнул необходимость проработки метрологической методологии и формирования единого терминологического поля для всех участников промышленности.
Александр Мажуга, ректор РХТУ им. Д.И. Менделеева, в заключительном слове сказал: «Российский рынок особо чистых веществ характеризуется доминированием импорта (более 95%), что ставит под угрозу функционирование стратегических отраслей промышленности. Университет обладает достаточным научным потенциалом, чтобы стать центром компетенций по развитию малотоннажной химии и обеспечению сырьевой базы для российской микроэлектроники. Но развитие промышленности возможно только в условиях кооперации и развития всей производственной цепочки, необходимо уделить внимание развитию и производственного оборудования и формированию единой базы стандартов».
Д.И. Менделеева, в заключительном слове сказал: «Российский рынок особо чистых веществ характеризуется доминированием импорта (более 95%), что ставит под угрозу функционирование стратегических отраслей промышленности. Университет обладает достаточным научным потенциалом, чтобы стать центром компетенций по развитию малотоннажной химии и обеспечению сырьевой базы для российской микроэлектроники. Но развитие промышленности возможно только в условиях кооперации и развития всей производственной цепочки, необходимо уделить внимание развитию и производственного оборудования и формированию единой базы стандартов».
По итогам круглого стола будет подготовлена резолюция для Министерства промышленности и торговли РФ и заинтересованных лиц с предложениями по развитию дорожной карты отрасли и достижению целей стратегии развития электронной промышленности РФ до 2030 года.
Абсолютно чистые вещества — Справочник химика 21
Понятие о чистоте вещества имеет принципиальное значение в современной неорганической химии. Абсолютно чистые вещества в природе не существуют, поскольку загрязнение примесями (образование ограниченных растворов) происходит самопроизвольно вследствие резкого возрастания энтропии . Поэтому нет абсолютно нерастворимых веществ и, следовательно, любое вещество загрязнено примесями. Даже в тех случаях, когда вещество очищено до очень высокой степени, абсолютное число атомов примеси в единице массы или объема все еще остается огромным. Так, в германии полупроводниковой чистоты 99,9999999% Ое содержание атомов примесей не превышает Ю ат. доли, %, т. е. один атом примеси приходится на миллиард атомов основного вещества. Тем не менее 1 см этого особо чистого германия содержит около 10 атомов примеси. Примеси коренным образом влияют на свойства вещества. Например, хорошо известная хрупкость и исключительная твердость металлического хрома, как выяснилось, является следствием наличия небольшого количества примесей, в основном кислорода. Хром, полученный в условиях глубокого вакуума, оказался мягким и пластичным.
Абсолютно чистые вещества в природе не существуют, поскольку загрязнение примесями (образование ограниченных растворов) происходит самопроизвольно вследствие резкого возрастания энтропии . Поэтому нет абсолютно нерастворимых веществ и, следовательно, любое вещество загрязнено примесями. Даже в тех случаях, когда вещество очищено до очень высокой степени, абсолютное число атомов примеси в единице массы или объема все еще остается огромным. Так, в германии полупроводниковой чистоты 99,9999999% Ое содержание атомов примесей не превышает Ю ат. доли, %, т. е. один атом примеси приходится на миллиард атомов основного вещества. Тем не менее 1 см этого особо чистого германия содержит около 10 атомов примеси. Примеси коренным образом влияют на свойства вещества. Например, хорошо известная хрупкость и исключительная твердость металлического хрома, как выяснилось, является следствием наличия небольшого количества примесей, в основном кислорода. Хром, полученный в условиях глубокого вакуума, оказался мягким и пластичным. [c.46]
[c.46]
Подобное же явление (появление второй фазы) наблюдается в точке плавления нри повышении температуры твердого тела во времени. Пересечение ординаты, соответствующей постоянной температуре, с кривой изменения температуры во времени дает точку плавления. На практике точка пересечения находится обычно путем экстраполяции. При известных значениях температуры плавления или температуры замерзания абсолютно чистого вещества этим методом можно рассчитать количество примесей, содержащихся в образце. Однако необходимо помнить о возможности существования кристаллических модификаций, которые изменяют ход кривой охлаждения. У очищенных парафинов кристаллические модификации, которые могут влиять на измерение плотности и коэффициентов расширения [234—235], встречаются вблизи точки плавления. [c.194]
I видимому, Л. Больцман. Тем не менее, большинство моделей этих систем детерминистские по своей сути. Другой недостаток, препятствующий моделированию сложных систем — стремление к описанию их на уровне взаимодействия элементарных частей системы. В сложных системах процессы являются стохастическими. Детерминированность таких систем кажущаяся. Квантовая теория изменила представления об атомах и молекулах. Одно из крупнейших достижений физики и химии XX века — теория гибридизации Л. Полинга, обычно понимается довольно узко как образование сложных электронных оболочек, хотя истинный смысл этой теории в том, что реальный атом в молекуле и изолированный атом таблицы Менделеева — разные вещества. То же относится к молекулам молекула в почве, лаборатории и организме — разные объекты. Состояние вещества зависит от среды. Природные геохимические и биогеохимические системы — почвы, нефти, водные биоценозы состоят из бесконечного числа компонентов. В природе нет и не может быть абсолютно чистого вещества. Понятие чистого вещества противоречит понятию памяти сред. В дальнейшем будет показано непостоянство закона постоянства состава.
Другой недостаток, препятствующий моделированию сложных систем — стремление к описанию их на уровне взаимодействия элементарных частей системы. В сложных системах процессы являются стохастическими. Детерминированность таких систем кажущаяся. Квантовая теория изменила представления об атомах и молекулах. Одно из крупнейших достижений физики и химии XX века — теория гибридизации Л. Полинга, обычно понимается довольно узко как образование сложных электронных оболочек, хотя истинный смысл этой теории в том, что реальный атом в молекуле и изолированный атом таблицы Менделеева — разные вещества. То же относится к молекулам молекула в почве, лаборатории и организме — разные объекты. Состояние вещества зависит от среды. Природные геохимические и биогеохимические системы — почвы, нефти, водные биоценозы состоят из бесконечного числа компонентов. В природе нет и не может быть абсолютно чистого вещества. Понятие чистого вещества противоречит понятию памяти сред. В дальнейшем будет показано непостоянство закона постоянства состава. Кроме того, для таких систем характерны законы квантовой. логики. В конечном счете, это приводит к замыканию макромира таких систем [c.22]
Кроме того, для таких систем характерны законы квантовой. логики. В конечном счете, это приводит к замыканию макромира таких систем [c.22]
Определение содержания основного вещества и примесей. В природе не существуют и принципиально не могут быть получены искусственным путем абсолютно чистые вещества. Развитие науки и производства требует применения все более и более чистых веществ и материалов. Задачей химии является разработка методов их получения и анализа. [c.74]
Абсолютно чистых веществ практически не бывает, поэтому значение заметно отличается от нуля и химическое сродство системы в исходном состоянии оказывается значительно меньше [c.135]
Из изложенного выше следует, что практически не существует абсолютно чистых веществ. Вместе с тем содержание примесей в отдельных образцах может быть весьма различным. Для вырабатываемых химической промышленностью продуктов применяются специальные наименования, обозначающие ту или иную степень их чистоты. Так, содержащий значительное количество примесей продукт носит название технического . По мере его очистки последовательно получаются следующие торговые сорта чистый , чистый для анализа , химически [c.59]
Так, содержащий значительное количество примесей продукт носит название технического . По мере его очистки последовательно получаются следующие торговые сорта чистый , чистый для анализа , химически [c.59]
Для проведения химических реакций во многих случаях используют не абсолютно чистые вещества, а так называемые технические продукты или природные материалы (сырье). Кроме основного компонента в них присутствует большее или меньшее количество примесей. Обычно предполагается, а иногда и специально указывается в условиях задач, что примеси ведут себя инертно по отношению к тем реагентам, с которыми взаимодействует основной компонент (или, во всяком случае, при их взаимодействии с данным реагентом не получаются продукты, образуемые основным компонентом). [c.93]
Вещества высокой чистоты имеют непреходящее самостоятельное значение в сугубо научном плане. Повышение степени чистоты часто приводило к открытию новых свойств вещества и новых явлений, т. е. к повышению уровня знаний о веществе как форме существования материи. Имеющиеся в нашем распоряжении материалы высокой чистоты пока представляют собой лишь слабое приближение к абсолютно чистому веществу , поскольку суммарное число примесных атомов или молекул в них всего на пять-шесть порядков меньше числа частиц основного вещества. [c.5]
е. к повышению уровня знаний о веществе как форме существования материи. Имеющиеся в нашем распоряжении материалы высокой чистоты пока представляют собой лишь слабое приближение к абсолютно чистому веществу , поскольку суммарное число примесных атомов или молекул в них всего на пять-шесть порядков меньше числа частиц основного вещества. [c.5]
Абсолютно чистое вещество получить невозможно. Применяемые в лабораторной практике вещества имеют различную степень чистоты, которая изменяется в некоторых пределах, устанавливаемых стандартами. [c.98]
При обсуждении вопроса о возможности получения абсолютно чистых веществ необходимо учесть следующее. При проведении очистки вещества, например методом зонной плавки, в основном достигается лишь вполне определенная предельная степень чистоты. Технические и временные затраты возрастают, как и в любых других методах, с ростом требований к степени чистоты и для получения абсолютно чистых веществ должны быть бесконечно большими. Кроме того, материал сосудов, в которых получают и хранят чистые вещества, всегда неизбежно является источником их загрязнений. Получение и [c.413]
Кроме того, материал сосудов, в которых получают и хранят чистые вещества, всегда неизбежно является источником их загрязнений. Получение и [c.413]
Твердые растворы. Одним из видов дефектов, связанных с при. месями, являются твердые растворы. В природе нет кристаллов, состоящих из абсолютно чистого вещества. Каждое вещество содержит то или иное количество примесей, т. е. атомов постороннего вещества. Самые чистые химические вещества включают более 10 % примесей или избытка одного из своих компонентов. А это значит, что в кристаллах размером 1 см примесных атомов не менее 10 . [c.169]
В соответствии с существующей в настоящее время теоретической концепцией получение абсолютно чистых веществ т. е. совершенно не содержащих примесей) принципиально возможно, но только в очень небольшой области концентраций для достаточно большой пробы чистого вещества и за более или менее ограниченный промежуток времени. Для контроля чистоты необходимы особо чувствительные методы анализа. Применение методов ультрамикроанализа позволяет осуществить мечту аналитиков — обнаружение отдельных атомов в матрице вещества. Одним из таких методов является лазерная спектроскопия. Вещество испаряют и атомы селективно возбуждают действием лазерного излучения в узкой области частот. Возбужденный атом затем ионизируется вторичными фотонами. Число испускаемых при этом свободных электронов фиксируют пропорциональным счетчиком. С помощью эффективно действующей лазерной установки можно ионизировать все атомы определяемого вещества. Метод, основанный на использовании этого явления, называют резонансной ионизационной опектро-скопией (РИС). Например, можно определять отдельные атомы цезия. В другом варианте метода — оптически насыщенной нерезонансной эмиссионной спектроскопии (ОНРЭС) — измеряют интенсивность флуоресцентного излучения возбужденных атомов. Чтобы отличить излучение определяемых элементов от излучения других компонентов пробы, длины волн флуоресценции сдвигают воздействием других атомов или молекул.
Для контроля чистоты необходимы особо чувствительные методы анализа. Применение методов ультрамикроанализа позволяет осуществить мечту аналитиков — обнаружение отдельных атомов в матрице вещества. Одним из таких методов является лазерная спектроскопия. Вещество испаряют и атомы селективно возбуждают действием лазерного излучения в узкой области частот. Возбужденный атом затем ионизируется вторичными фотонами. Число испускаемых при этом свободных электронов фиксируют пропорциональным счетчиком. С помощью эффективно действующей лазерной установки можно ионизировать все атомы определяемого вещества. Метод, основанный на использовании этого явления, называют резонансной ионизационной опектро-скопией (РИС). Например, можно определять отдельные атомы цезия. В другом варианте метода — оптически насыщенной нерезонансной эмиссионной спектроскопии (ОНРЭС) — измеряют интенсивность флуоресцентного излучения возбужденных атомов. Чтобы отличить излучение определяемых элементов от излучения других компонентов пробы, длины волн флуоресценции сдвигают воздействием других атомов или молекул. Этим методом также можно определять отдельные атомы вещества, например натрия. [c.414]
Этим методом также можно определять отдельные атомы вещества, например натрия. [c.414]
Когда употребляют понятие чистое вещество , имеют в виду, конечно, не абсолютно чистое вещество, а вещество определенной степени очистки. Последняя же зависит от способа использования данного вещества или от технических возможностей. В нашей стране существует следующая градация веществ по чистоте технической чистоты , чистый , чистый для анализа (ЧДА) , химически чистый (ХЧ) , спектрально чистый , особой чистоты . В специальных случаях употребляются и иные марки, например полупроводниковой чистоты , фармакопейный и др. Для каждого вещества количества примесей для каждой категории чистоты устанавливаются отдельно. Наиболее чистые вещества, производимые промышленностью, содержат 10 —10- % примесей. [c.38]
Абсолютно чистых веществ нет. Применяемые в лабораторной практике вещества имеют различную степень чистоты. Максимально допустимое количество примесей в веществе устанавливается общесоюзным стандартом (ГОСТ). [c.43]
[c.43]
Абсолютно чистых веществ нет. Применяемые в лабораторной практике вещества имеют различную степень чистоты. [c.49]
В своей практической деятельности (а значит это находит свое отражение и в задачах) мы обычно имеем дело не с абсолютно чистыми веществами, а с так называемыми техническими продуктами. Масса технического продукта (целое) состоит из массы чистого вещества (одна часть) и массы примесей (другая часть). [c.54]
Химия — наука о веществе, его составе и свойствах. Различают химические и физические свойства. Под химическими свойствами разумеют способность вещества вступать во взаимодействие с другими веществами. Каждое вещество обладает характерными для него физическими свойствами цветом, вкусом, запахом, плотностью, температурами плавления и кипения, вязкостью и др. Большинство физических свойств могут быть выражены определенными числовыми данными, или константами. Однако константы данного вещества могут изменяться, если в нем присутствуют примеси других веществ. Следует помнить, что абсолютно чистых веществ (степень чистоты 100%) практически не существует. Однако в настоящее время получают вещества с ничтожным содержанием примесей (до 10 %). [c.10]
Следует помнить, что абсолютно чистых веществ (степень чистоты 100%) практически не существует. Однако в настоящее время получают вещества с ничтожным содержанием примесей (до 10 %). [c.10]
В заключение рассмотрим вопрос о возможности получения абсолютно чистых веществ . [c.16]
Афинная хроматография основана на специфичности биомолекул Принципиально этим методом возможно получение абсолютно чистых веществ В нативном состоянии ферменты за счет своего активного центра и регуляторного участка (одного или более) взаимодействуют с небольшим числом лигандов, которые представляют собой субстраты, либо эффекторы Благодаря высокому сродству активного участка фермента к лиганду, их обратимому связыванию и отсутствию какой-либо другой реакции между лигандом и матрицей возможно эффективное проведение афинной хроматографии [c.51]
Хорошо известно, что абсолютно чистых веществ в природе не бывает. Поэтому к вопросу о чистоте растворителя следует подходить разумно. Одни и те же примеси в разных условиях могут либо вообще не влиять на результат, либо сделать анализ невозможным. Так, незначительная примесь олефинов в алкановом растворителе совершенно не мешает при работе с рефрактометром, но практически не позволяет проводить детектирование УФ-детектором при длине волны менее 260 нм. Напротив, [c.131]
Одни и те же примеси в разных условиях могут либо вообще не влиять на результат, либо сделать анализ невозможным. Так, незначительная примесь олефинов в алкановом растворителе совершенно не мешает при работе с рефрактометром, но практически не позволяет проводить детектирование УФ-детектором при длине волны менее 260 нм. Напротив, [c.131]
Абсолютно черное тело 4/1030 Абсолютно чистые вещества 3/835 [c.535]
Возможности обнаружения примесей также лежат в основе наших представлений о чистоте вещества. Начнем с того, что абсолютно чистых веществ не может быть в принципе. Этот вывод, в частности, следует из термодинамики (из уравнения 10.2 в разд. 10.5). Если концентрация какого либо реагента (примеси, от которой мы хотим избавиться) стремится к нулю, то ДС любой реакции, приводящей к ее удалению, стремится к бесконечности, и полная очистка вещества становится термодинамически невозможной. [c.442]
В природе не существует абсолютно чистых веществ. Поэтому, рассчитывая необходимые для реакции реагенты, не следует забы-ва.ть, что для химического процесса берутся и в результате процесса получаются не абсолютные вещества, а реальные химические материалы, т, е. вещества, содержащие примеси. В таких материалах различают главный компонент ( основу ) и малые компоненты ( примеси ). При этом примеси могут быть как вредными для свойств материала, так и полезными, специально вводимыми. [c.17]
Поэтому, рассчитывая необходимые для реакции реагенты, не следует забы-ва.ть, что для химического процесса берутся и в результате процесса получаются не абсолютные вещества, а реальные химические материалы, т, е. вещества, содержащие примеси. В таких материалах различают главный компонент ( основу ) и малые компоненты ( примеси ). При этом примеси могут быть как вредными для свойств материала, так и полезными, специально вводимыми. [c.17]
Говоря о чистоте химических веществ, нужно отдавать себе отчет в том, что абсолютно чистое вещество можно представить только теоретически. Абсолютно чистых веществ нет и быть не может. В зависимости от метода очистки вещество содержит определенное количество примесей. Обычными методами очистки можно достичь содержания основного вещества 99,9.. . 99,95%. Специальными методами глубокой очистки можно уменьшить содержание примесей для органических веществ до 10 .. . 10″ %. [c.15]
Для получения абсолютно чистого вещества требуется бесконечно большой расход энергии и бесконечно большая высота колонны. [c.42]
[c.42]
Химические методы анализа не всегда удовлетворяют современным требованиям, особенно при проверке чистоты веществ. Все вещества представляют собой как бы растворы примесей в основном компоненте. Поэтому получить абсолютно чистое вещество практически невозможно, так как в нем тотчас происходит «растворение» компонентов окружающей среды, т.е. примесей. Иначе говоря, небольшое количество абсолютно чистого вещества может существовать лишь очень ограниченное время. Поэтому в технике вещество считают чистым, если повторная очистка не изменяет его физических свойств. [c.323]
Методика была проверена на пяти органических соединениях, для которых были сняты кривые замерзания и плавления и вычислены температуры замерзания абсолютно чистого вещества и степень чистоты исходных образцов. [c.228]
Получить абсолютно чистое вещество практически невозможно. Самая чистая дестиллированная вода всегда содержит (хотя и в ничтожно малых количествах) растворенные примеси самые чистые соли не свободны от ничтожных загрязнений. Поэтому в практической жизни химически чистым считают вещество, содержащее очень незначительное количество примесей, как говорят, следы их, так что эти примеси не имеют никакого практического значения и не влияют заметно на числовое выражение констант данного химически чистого вещества. В дальнейшем изложении при описании свойств веществ мы всегда будем иметь в виду химически чистые вещества. [c.24]
Поэтому в практической жизни химически чистым считают вещество, содержащее очень незначительное количество примесей, как говорят, следы их, так что эти примеси не имеют никакого практического значения и не влияют заметно на числовое выражение констант данного химически чистого вещества. В дальнейшем изложении при описании свойств веществ мы всегда будем иметь в виду химически чистые вещества. [c.24]
Абсолютно чистое вещество можно представить себе только теоретически. В практике чистым называют вещество, содержащее примеси ниже онределеиного предела. Этот предел, как правило, составляет доли процента н менее. Интерес к чистым веществам обусловлен потребностями современной науки и техники в материалах с особыми механическими, электрическими, полупроводниковыми, оптическими и другими физико-химическими свойствами. Особенно возросли требования к чистоте технических материалов с развитием атомной энергетики, полупроводниковой электро- н радиотехники, лазерной техники. Например, минимальная примесь может вызвать остановку ядерного реактора. В полупроводниковых материалах ничтожные следы посторонних примесей меняют величину и тип проводимости, а в отдельных случаях вообще лишают материал его полупроводниковых свойств. Получить особо чистое вещество — чрезвычайно сложная и важная технологическая задача, решенная пока для немногих веществ. Проверить чистоту вещества можно по его химическому составу и по физическим свойствам. [c.78]
Например, минимальная примесь может вызвать остановку ядерного реактора. В полупроводниковых материалах ничтожные следы посторонних примесей меняют величину и тип проводимости, а в отдельных случаях вообще лишают материал его полупроводниковых свойств. Получить особо чистое вещество — чрезвычайно сложная и важная технологическая задача, решенная пока для немногих веществ. Проверить чистоту вещества можно по его химическому составу и по физическим свойствам. [c.78]
Так как абсолютно чистых веществ не существует (И 6), кристаллы неизбежно содержат примесные частицы, а [тогда тйк ке и более значительные включения инородных веществ или пустот. В общем, реальные кристаллы примерно так же относятся к теоретически рассматриваемым идеальным, как реальные газы к газу ндеа.мьиому. [c.384]
Абсолютно чистых веществ (степень чистоты 100%) нет. Любое вещество содержит большее или меньшее количество примесей. Чем меньше примесёй, тем выше качество химических веществ. Современная техника предъявляет высокие требования к степени чистоты различных химических продуктов. [c.42]
Современная техника предъявляет высокие требования к степени чистоты различных химических продуктов. [c.42]
Таким образом, помимо неимоверных трудностей получения абсолютно «ЧИСТЫХ веществ, работать с ними практически невозможно, а при хранении самом процессе очися ки) в нпх неизбежно постепенно накапливаются прнмеси. [c.17]
В природе не существует абсолютно Mvi Tbix веществ. Например, так называемый особо чистый алюминий. все еще содержит 0,001 % примесей других веществ. Таким образом, абсолютно чистое вещество — это абстракция. Правда, когда речь идет о каком-либо веществе, то химия пользуется этой абстракцией, т, е. считает, что вещестпо истинно чистое, хотя практически берется вещество с некоторым содержанием примесей. Конечно, кимик должен стремиться использовать в своей практике по по. шожности истые вещества, содержащие минимальное количество примесей. Следует учитывать, [c.17]
Особенно важное значение этот эффект имеет в том случае, когда электропроводность абсолютно чистого вещества мала, как, например, в твердом германии. Предположим, что концентрация примеси столь мала, что ее атомы занимают места некоторых из атомов основного вещества. Если при этом число валентных электронов у атомов примеси на один меньше, чем у атомов основного вещества (например, атомы галлия имеют три валентных электрона, атомы германия — четыре), то мы имеем полупроводник р-типа с электропроводностью, в основном обусловленной наличием положительных дырок в зоне, котО рая в отсутствие примесей была бы целиком заполненной ва лентной зоной. Аналогично этому если атом примеси имеет один дополнительный валентный электрон (например, мышьяк имеет 5 валентных электронов), то мы имеем полупроводник м-типа, в котором проводимость обусловлена избытком электронов, занимающих пустую (в отсутствие примеси) зону проводимости. [c.352]
Предположим, что концентрация примеси столь мала, что ее атомы занимают места некоторых из атомов основного вещества. Если при этом число валентных электронов у атомов примеси на один меньше, чем у атомов основного вещества (например, атомы галлия имеют три валентных электрона, атомы германия — четыре), то мы имеем полупроводник р-типа с электропроводностью, в основном обусловленной наличием положительных дырок в зоне, котО рая в отсутствие примесей была бы целиком заполненной ва лентной зоной. Аналогично этому если атом примеси имеет один дополнительный валентный электрон (например, мышьяк имеет 5 валентных электронов), то мы имеем полупроводник м-типа, в котором проводимость обусловлена избытком электронов, занимающих пустую (в отсутствие примеси) зону проводимости. [c.352]
Оствальд пытался доказать, что гомогенные неустойчивые системы не могут существовать иначе, как в состоянии превращения . Для ЭТ0Г.0 он использовал законы энергетики , являющиеся, по его мнению, самым надежным основанием общих заключений . Эти законы,— говорил он,— не определяют численную величину скорости, которая должна при этом осуществляться они требуют только, чтобы эта скорость не была строго равна нулю, а имела конечную величину [9]. Но, во-первых, Оствальд не учитывает, что здесь может быть надежная защита для сохранения неустойчивости системы (например, высокая энергия активации) в течение неограниченно долгого времени. Во-вторых, выражаясь его же словами, мера времени или скорость химических реакций не устанавливается законами энергии [3, стр. 220]. И, наконец, в-третьих, с положением о естественной скорости трудно согласовать положение о Д1а-лой вероятности протекания реакций между абсолютно чистыми веществами, выдвинутое тоже самим Оствальдом. Самое главное в критике оствальдовского допущения естественных скоростей заключается в практической невозможности их учета в тех случаях, когда реакция не происходит без катализаторов. Поэтому, не отрицая возможности медленного протекания некоторых реакций, ускоряемых катализаторами, в целом это допущение не выдерживает критики.
Эти законы,— говорил он,— не определяют численную величину скорости, которая должна при этом осуществляться они требуют только, чтобы эта скорость не была строго равна нулю, а имела конечную величину [9]. Но, во-первых, Оствальд не учитывает, что здесь может быть надежная защита для сохранения неустойчивости системы (например, высокая энергия активации) в течение неограниченно долгого времени. Во-вторых, выражаясь его же словами, мера времени или скорость химических реакций не устанавливается законами энергии [3, стр. 220]. И, наконец, в-третьих, с положением о естественной скорости трудно согласовать положение о Д1а-лой вероятности протекания реакций между абсолютно чистыми веществами, выдвинутое тоже самим Оствальдом. Самое главное в критике оствальдовского допущения естественных скоростей заключается в практической невозможности их учета в тех случаях, когда реакция не происходит без катализаторов. Поэтому, не отрицая возможности медленного протекания некоторых реакций, ускоряемых катализаторами, в целом это допущение не выдерживает критики. [c.83]
[c.83]
Поиск
Сортировать по:
| Выпуск | Название | |
| Том 15, № 1 (2019) | Способ оценки неопределенности аттестованного значения многокомпонентного стандартного образца | Аннотация PDF (Rus) |
П. В. Мигаль, С. В. Медведевских, В. А. Фирсанов В. Мигаль, С. В. Медведевских, В. А. Фирсанов | ||
| Том 15, № 2 (2019) | Разработка эталонов сравнения в виде металлов высокой чистоты | Аннотация PDF (Rus) |
Л. А. Конопелько, П. В. Мигаль, Е. П. Собина В. Мигаль, Е. П. Собина | ||
| № 3 (2014) | К ВОПРОСУ О ПРИМЕНЕНИИ ЧИСТЫХ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ В МЕТРОЛОГИИ АНАЛИТИЧЕСКИХ ИЗМЕРЕНИЙ | Аннотация PDF (Rus) |
С. В. Медведевских, Е. П. Собина, П. В. Мигаль, Л. И. Горяева, Е. М. Горбунова, Т. Н. Табатчикова, А. В. Собина, В. А. Фирсанов, М. Ю. Медведевских, М. П. Крашенинина В. Мигаль, Л. И. Горяева, Е. М. Горбунова, Т. Н. Табатчикова, А. В. Собина, В. А. Фирсанов, М. Ю. Медведевских, М. П. Крашенинина | ||
| 1 — 3 из 3 результатов | ||
Советы по поиску:
- Поиск ведется с учетом регистра (строчные и прописные буквы различаются)
- Служебные слова (предлоги, союзы и т.п.) игнорируются
- По умолчанию отображаются статьи, содержащие хотя бы одно слово из запроса (то есть предполагается условие OR)
- Чтобы гарантировать, что слово содержится в статье, предварите его знаком +; например, +журнал +мембрана органелла рибосома
- Для поиска статей, содержащих все слова из запроса, объединяйте их с помощью AND; например, клетка AND органелла
- Исключайте слово при помощи знака — (дефис) или NOT; например.
 клетка -стволовая или клетка NOT стволовая
клетка -стволовая или клетка NOT стволовая - Для поиска точной фразы используйте кавычки; например, «бесплатные издания». Совет: используйте кавычки для поиска последовательности иероглифов; например, «中国»
- Используйте круглые скобки для создания сложных запросов; например, архив ((журнал AND конференция) NOT диссертация)
Получить технические условия на реактивы и особо чистые вещества
Оставьте заявку на готовые технические условия на реактивы и особо чистые вещества
Технические условия на реактивы и особо чистые вещества Горячая линия 8 800 222 32 02
В нашей компании вы сможете заказать разработку технических условий на реактивы и особо чистые вещества.
Получить образец перед покупкой.В наличии более 5000 готовых ТУ.
Наши эксперты разработают индивидуальные технические условия под любой бизнес.— Невзоров Дмитрий Руководитель отдела проектной документации
Преимущества заказа технических условий на реактивы и особо чистые вещества
1
Все ТУ на реактивы и особо чистые вещества проходят регистрацию в ЦСМ с первого раза
2
Во все ТУ на реактивы и особо чистые вещества возможно вносить изменения
3
Свои штат экспертов по проектной документации
4
ТУ на реактивы и особо чистые вещества соответствуют всем текущим требованиям
5
ТУ на реактивы и особо чистые вещества оформляются на вашу компанию с присвоением номера
6
Максимальный ассортимент технических условий на реактивы и особо чистые вещества
Ознакомиться с перечнем ТУ на реактивы и особо чистые вещества
Выгоды при заказе технических условий на реактивы и особо чистые вещества
Быстрый вывод продукции на рынок
Возможность выхода на тендеры
Широкий ассортимент продукции
Конфиденциальность информации
Нет проблем с Роспотребнадзором
Быстрый вывод продукции на рынок
Найти нужное ТУ по базе
Самые заказываемые технические условия на реактивы и особо чистые вещества
- ТУ йод мелкокристаллический
- ТУ аммиак водный
- ТУ дихлорметан
- ТУ изооктан
- ТУ бутанол для синтеза чистый
- ТУ вода дистиллированная
- ТУ бумага индикаторная лакмусовая
- ТУ водорода перексид особый чистый
- ТУ бензоловый спирт для микроэлектроники
- ТУ набор реагентов выявления и идентификации ГМИ
Последние оформленые технические условия
В нашей компании вы сможете заказать разработку технических условий на реактивы и особо чистые вещества.
Получить образец перед покупкой. В наличии более 5000 готовых ТУ.
Наши эксперты разработают индивидуальные технические условия под любой бизнес.— Невзоров Дмитрий Руководитель отдела проектной документации
Как отличить чистое вещество от смеси веществ?
Как отличить чистое вещество от смеси веществ?
☰
Тела могут состоять из одного вещества или из смеси веществ. Причем второй вариант встречается чаще. Даже кажущиеся однородными вещества могут оказаться смесями нескольких веществ. Например, растворы представляют собой однородные смеси, состоящие из как минимум двух разных веществ. В однородных смесях очень маленькие частицы разных веществ, поэтому их нельзя увидеть отдельно друг от друга.
Если в одном стакане воды растворить ложку сахара, а в другом ложку соли, то по внешнему виду растворы будут одинаковы. Если какому-нибудь человеку предложить определить, где что находится, и при этом запретить пробовать растворы, то он сможет это сделать лишь экспериментально. Многие жидкости представляют собой растворы. Если молоко рассмотреть под микроскопом, то в нем можно увидеть вкрапления жиров и белков. Однако если смотреть невооруженным глазом, то оно кажется однородным.
Многие жидкости представляют собой растворы. Если молоко рассмотреть под микроскопом, то в нем можно увидеть вкрапления жиров и белков. Однако если смотреть невооруженным глазом, то оно кажется однородным.
Чистое же вещество, независимо от степени его увеличения, всегда будет выглядеть, состоящим из одинаковых частичек.
Однако определить, является ли вещество чистым или смесью веществ, можно, не углубляясь в микромир. Как известно из физики, чистые вещества плавятся и кипят при строго определенных температурах. Если твердое тело состоит из чистого вещества, то оно будет плавиться от начала до конца, если установится определенная температура и далее она может даже не повышаться. Смеси же веществ начинают плавиться при одной температуре, но полностью расплавиться могут лишь при более высокой. То же самое касается и температуры кипения. Например, вода при нормальном атмосферном давлении закипает кипит при 100 °C. Далее ее температура не повышается, она продолжает кипеть при этой температуре. Вся энергия уходит на кипение. Если же нагревать нефть, то она закипит при одной температуре, но ее температура продолжит повышаться.
Вся энергия уходит на кипение. Если же нагревать нефть, то она закипит при одной температуре, но ее температура продолжит повышаться.
Copyright © 2019. All Rights Reserved
Чистые вещества для хроматографии (СТХ)
Описание
Для заказа чистых веществ для хроматографии звоните по телефону 8 (812) 718-82-72 или воспользуйтесь формой заказа справа.
Чистые вещества для хроматографии представляют собой очищенные органические вещества, квалификации «ХЧ», предназначенные для качественного хроматографического анализа, а также для градуировки хроматографов в случае отсутствия соответствующих ГСО, или необязательности их использования.
Аттестованной характеристикой СО является массовая доля основного вещества, которая устанавливается хроматографически, а также определяется массовая доля воды методом кулонометрического титрования.
Стандартные образцы для хроматографии поставляются в запаянных стеклянных ампулах по 3 см3.
Срок годности экземпляров СО – 3 года.
Характеристики чистых веществ для хроматографии
| Наименование вещества | Индекс СО | Номер СОП | Массовая доля | Массовая доля воды, |
| Бензол | СТХ | 0003-03 | 99,9 | 0,05 |
| Бутанол-1 | СТХ | 0004-03 | 99,3 | 0,15 |
| Бутанол-2 | СТХ | 0005-03 | 99,3 | 0,15 |
| Бутилацетат | СТХ | 0006-03 | 99,3 | 0,15 |
| Гексан | СТХ | 0007-03 | 99,3 | 0,15 |
| Гептан | СТХ | 0008-03 | 99,3 | 0,15 |
| Декан | СТХ | 0009-03 | 99,3 | 0,15 |
| 1,2-Дихлорэтан | СТХ | 0010-03 | 99,5 | 0,10 |
| Диэтиламин | СТХ | 0011-03 | 99,5 | 0,10 |
| Додекан | СТХ | 0012-03 | 99,3 | 0,15 |
| Изооктан | СТХ | 0013-03 | 99,5 | 0,10 |
| Изопропилбензол (кумол) | СТХ | 0014-03 | 99,5 | 0,10 |
| о-Ксилол | СТХ | 0020-03 | 99,3 | 0,15 |
| м-Ксилол | СТХ | 0015-03 | 99,5 | 0,10 |
| п-Ксилол | СТХ | 0022-03 | 99,5 | 0,10 |
| Метанол | СТХ | 0016-03 | 99,8 | 0,10 |
| Метиленхлорид (хлористый метилен) | СТХ | 0017-03 | 99,7 | 0,10 |
| Метил-трет-бутиловый эфир | СТХ | 0039-03 | 99,5 | 0,10 |
| Метилэтилкетон (бутанон-2) | СТХ | 0018-03 | 99,5 | 0,10 |
| 2-Метилпропанол-1 (изобутанол) | СТХ | 0001-03 | 99,5 | 0,10 |
| Нонан | СТХ | 0019-03 | 99,3 | 0,15 |
| Октан | СТХ | 0021-03 | 99,3 | 0,15 |
| Пентан | СТХ | 0037-03 | 99,3 | 0,15 |
| Пропанол-1 | СТХ | 0023-03 | 99,5 | 0,10 |
| Пропанол-2 (изопропанол) | СТХ | 0024-03 | 99,5 | 0,10 |
| Тетрадекан | СТХ | 0041-03 | 99,0 | 0,20 |
| Тетрахлорметан (четыреххлористый углерод) | СТХ | 0025-03 | 99,8 | 0,05 |
| 1,3,5-Триметилбензол (мезитилен) | СТХ | 0036-03 | 99,0 | 0,20 |
| 1,2,4-Триметилбензол (псевдокумол) | СТХ | 0035-03 | 99,0 | 0,20 |
| Трихлорэтилен | СТХ | 0038-03 | 99,5 | 0,10 |
| Ундекан | СТХ | 0026-03 | 99,0 | 0,20 |
| Хлорбензол | СТХ | 0027-03 | 99,8 | 0,05 |
| Хлороформ | СТХ | 0028-03 | 99,5 | 0,10 |
| Циклогексан | СТХ | 0029-03 | 99,8 | 0,05 |
| Циклогексанол | СТХ | 0030-03 | 99,0 | 0,20 |
| Циклогексанон | СТХ | 0031-03 | 99,5 | 0,10 |
| Этанол | СТХ | 0032-03 | 99,5 | 0,10 |
| Этилацетат | СТХ | 0033-03 | 99,5 | 0,10 |
| Этилбензол | СТХ | 0034-03 | 99,5 | 0,10 |
Чистые вещества — Анализ и идентификация веществ — AQA — GCSE Chemistry (Single Science) Revision — AQA
1jg8t183wm0.0.0.0.1:0.1.0.$0.$1.$0″> Значение чистого
Слово «чистый» используется в химии иначе, чем его повседневное значение. Например, в магазинах продаются картонные коробки с маркировкой «чистый» апельсиновый сок. Этикетка означает, что содержимое представляет собой апельсиновый сок без добавления каких-либо других веществ. Однако сок не является чистым в химическом смысле, потому что он содержит разные вещества, смешанные вместе.В химии:
- чистое вещество состоит только из одного элемента или одного соединения
- смесь состоит из двух или более различных веществ, не связанных химически
Компоненты смеси обычно можно разделить без химических реакций
Различные типы химического вещества
- 1jg8t183wm0.0.0.0.1:0.1.0.$0.$2.$1″>
- элемент содержит только один тип атома
- соединение содержит два или более типов атома, соединенных вместе
- смесь содержит два или более различных вещества, которые не соединены вместе
- различные вещества в смеси могут быть элементами или соединениями
В таблице приведены некоторые примеры:
Обратите внимание, что различные вещества в смеси могут быть отдельными атомами, молекулами элементов или молекулами соединений
Различие между чистыми веществами и смесями
Чистые вещества имеют резкое плавление точка, но смеси плавятся в диапазоне температур. Эту разницу легче всего увидеть, если измерить температуру жидкости при ее охлаждении и замерзании. На графике показана кривая охлаждения для образца соединения, называемого салолом.
Эту разницу легче всего увидеть, если измерить температуру жидкости при ее охлаждении и замерзании. На графике показана кривая охлаждения для образца соединения, называемого салолом.
Температура остается неизменной, когда чистое вещество меняет состояние.
Горизонтальная часть графика показывает, что салол имеет резкую температуру плавления, поэтому он чистый. Нечистый салол (смесь салола и других веществ) при замерзании вызывает постепенное понижение температуры.
Температура немного меняется, когда нечистое вещество меняет состояние.
- Вопрос
Учащийся проверяет точку плавления образца серы.Он начинает плавиться при 95-101 ° C, но не тает полностью, пока температура не достигнет 113 ° C. Согласно справочнику данных, температура плавления серы составляет 115 ° C.
 Этот образец серы чистый или нечистый?
Этот образец серы чистый или нечистый?- Показать ответ
Он нечистый, потому что плавится в широком диапазоне температур, а его точка плавления отличается от «стандартной» контрольной точки плавления серы.
Элементный состав чистых веществ
Если вы считаете, что контент, доступный через Веб-сайт (как определено в наших Условиях обслуживания), нарушает одно
или другие ваши авторские права, сообщите нам, отправив письменное уведомление («Уведомление о нарушении»), содержащее
то
информацию, описанную ниже, назначенному ниже агенту.Если репетиторы университета предпримут действия в ответ на
ан
Уведомление о нарушении, он предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент
средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.
Ваше Уведомление о нарушении прав может быть отправлено стороне, предоставившей доступ к контенту, или третьим лицам, таким как
в виде
ChillingEffects.org.
Обратите внимание, что вы будете нести ответственность за ущерб (включая расходы и гонорары адвокатов), если вы существенно
искажать информацию о том, что продукт или действие нарушает ваши авторские права.Таким образом, если вы не уверены, что контент находится
на Веб-сайте или по ссылке с него нарушает ваши авторские права, вам следует сначала обратиться к юристу.
Чтобы отправить уведомление, выполните следующие действия:
Вы должны включить следующее:
Физическая или электронная подпись правообладателя или лица, уполномоченного действовать от их имени;
Идентификация авторских прав, которые, как утверждается, были нарушены;
Описание характера и точного местонахождения контента, который, по вашему мнению, нарушает ваши авторские права, в \
достаточно подробностей, чтобы позволить репетиторам университетских школ найти и точно идентифицировать этот контент; например, мы требуем
а
ссылка на конкретный вопрос (а не только на название вопроса), который содержит содержание и описание
к какой конкретной части вопроса — изображению, ссылке, тексту и т. д. — относится ваша жалоба;
д. — относится ваша жалоба;
Ваше имя, адрес, номер телефона и адрес электронной почты; а также
Ваше заявление: (а) вы добросовестно полагаете, что использование контента, который, по вашему мнению, нарушает
ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все
информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство, что вы
либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.
Отправьте жалобу нашему уполномоченному агенту по адресу:
Чарльз Кон
Varsity Tutors LLC
101 S. Hanley Rd, Suite 300
St. Louis, MO 63105
Или заполните форму ниже:
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Термохимические данные чистых веществ, 3-е издание
Загрузить флаер продукта
Загрузить флаер продукта — загрузить PDF-файл в новой вкладке.Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF-файл в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF-файл в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF-файл в новой вкладке. Это фиктивное описание.
Описание
Это переработанное, расширенное, обновленное третье издание знаменитого справочника «Термохимические данные чистых веществ».
Вводный раздел кратко обсуждает термодинамическую теорию и приложения и объясняет, как лучше всего использовать таблицы; его также расширили на руды, уголь, отходы и остатки. Тщательно изученный и составленный, он содержит подробные таблицы термодинамических данных для более чем 2500 чистых веществ в различных фазах, более 230 из которых являются органическими. Известная ясность таблиц и богатство содержащейся в них ценной информации гарантируют высокий уровень этой знаменитой работы.
Тщательно изученный и составленный, он содержит подробные таблицы термодинамических данных для более чем 2500 чистых веществ в различных фазах, более 230 из которых являются органическими. Известная ясность таблиц и богатство содержащейся в них ценной информации гарантируют высокий уровень этой знаменитой работы.
«Это, несомненно, один из самых обширных наборов доступных данных, охватывающий значительное количество соединений … перечисляющий значения для всех термодинамических переменных во всем диапазоне рассматриваемых температур». Faraday Transactions
«Введение предназначено в качестве поддержки для тех, кто плохо разбирается в химической термодинамике, но, предоставляя рабочие примеры, также помогает тем, кто более искусен, освежить забытые основы». Арцнаймиттель-Форшун
Содержание
Из содержания:
Термодинамические функции и соотношения
Расчет термохимических функций
Составление и представление термохимических данных
Подготовка таблиц
Построение таблиц
Содержание и структура таблиц
Примеры термодинамических расчетов
Основные константы и коэффициенты пересчета
Индексы:
Формулы Указатель
Модифицированная система индексации Хилла
Таблицы термохимических данных чистых веществ
Чистое вещество в химии: определение, свойства и примеры — Science Class [Видео 2021]
Чистое вещество: концепция и свойства
Представьте себе кубик сахара, который вы можете добавить в чашку горячего кофе или чая. Если вы посмотрите на коробку с сахарными кубиками, вы можете увидеть на этикетке слова «чистый тростниковый сахар». Означает ли слово «чистый» во всех случаях одно и то же и что это слово означает в контексте химии?
Если вы посмотрите на коробку с сахарными кубиками, вы можете увидеть на этикетке слова «чистый тростниковый сахар». Означает ли слово «чистый» во всех случаях одно и то же и что это слово означает в контексте химии?
Чистое вещество в химии — очень простая для понимания концепция. Чистые вещества определяются как вещества, состоящие только из одного типа атомов или только из одного типа молекул (группы атомов, связанных вместе). Мера чистоты вещества известна как чистота .Например, чистое железо будет содержать только атомы железа, и, как в упомянутом выше кубике сахара, чистый сахар будет содержать только молекулы вещества, называемого сахарозой.
Чистые вещества обладают четко определенными физическими свойствами или свойствами, которые не связаны со способностью вещества соединяться с различными веществами. Температуры плавления чистых твердых веществ, известные как точки плавления , особенно высоки, что означает, что плавление происходит при одной температуре.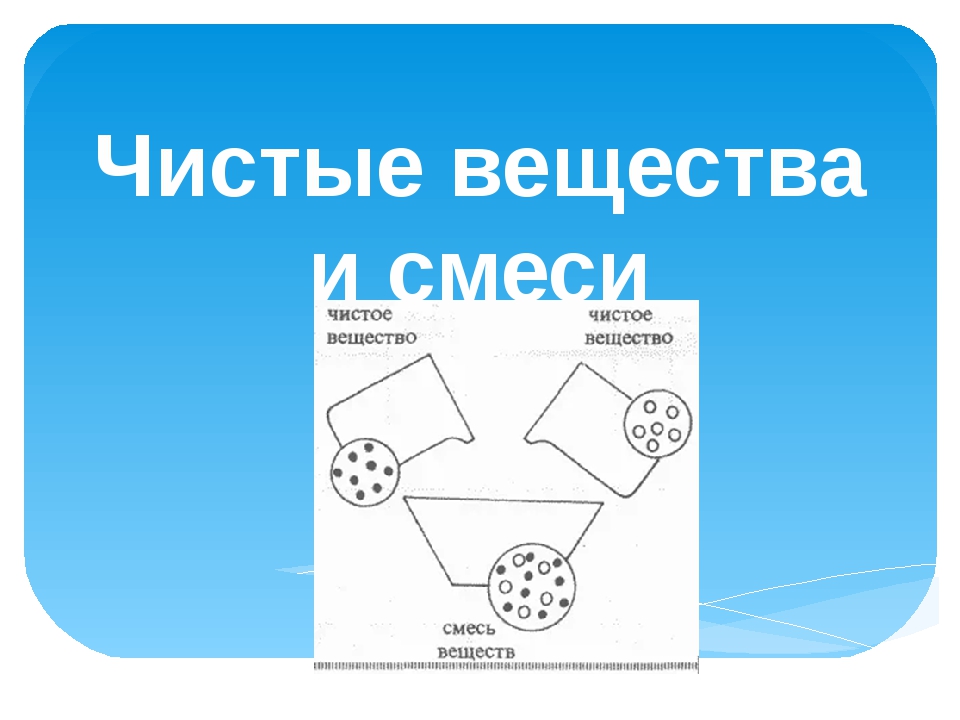 Точно так же температуры, при которых чистые жидкости начинают закипать, или точек кипения , возникают при единичных температурах, когда контролируются другие факторы, такие как давление воздуха. На способность веществ проводить электричество или проводимость сильно влияет чистота. Например, медь, которая используется в электропроводке, должна иметь очень высокую чистоту, чтобы обеспечить наиболее эффективную проводимость. С другой стороны, чрезвычайно чистая жидкая вода является очень плохим проводником электричества, потому что в ней нет растворенных электрических проводников, называемых электролитами, которые позволяли бы иметь проводимость.
Точно так же температуры, при которых чистые жидкости начинают закипать, или точек кипения , возникают при единичных температурах, когда контролируются другие факторы, такие как давление воздуха. На способность веществ проводить электричество или проводимость сильно влияет чистота. Например, медь, которая используется в электропроводке, должна иметь очень высокую чистоту, чтобы обеспечить наиболее эффективную проводимость. С другой стороны, чрезвычайно чистая жидкая вода является очень плохим проводником электричества, потому что в ней нет растворенных электрических проводников, называемых электролитами, которые позволяли бы иметь проводимость.
Чистота также может иметь важное влияние на химические свойства вещества. Чистые вещества могут образовывать предсказуемые продукты в результате химических реакций. Причина такой надежности заключается в отсутствии примесей, которые могут запустить другие реакции, которые могут помешать реакции, изучаемой химиком. Поэтому при проведении химических исследований химики часто используют вещества высокой чистоты.
Странные науки: чистая вода и водные смеси
Морская вода представляет собой смесь множества различных веществ.Некоторые из этих веществ можно наблюдать, когда вода в морской воде испаряется и оставляет после себя соль. Вода, H 2 O, представляет собой чистое вещество, соединение, состоящее из водорода и кислорода. Хотя вода является самым распространенным веществом на Земле, она редко встречается в природе в чистом виде. В большинстве случаев необходимо создавать чистую воду. Чистая вода называется дистиллированной или деионизированной водой. В дистиллированной воде все растворенные вещества, смешанные с водой, были удалены испарением.Когда вода испаряется, она перегоняется или оставляет соль. Чистая выпаренная вода собирается и конденсируется с образованием дистиллированной воды.
Водопроводная вода не дистиллированная (SF Рис. 2.9 A). В большинстве водопроводных водопроводных сетей содержится хлор.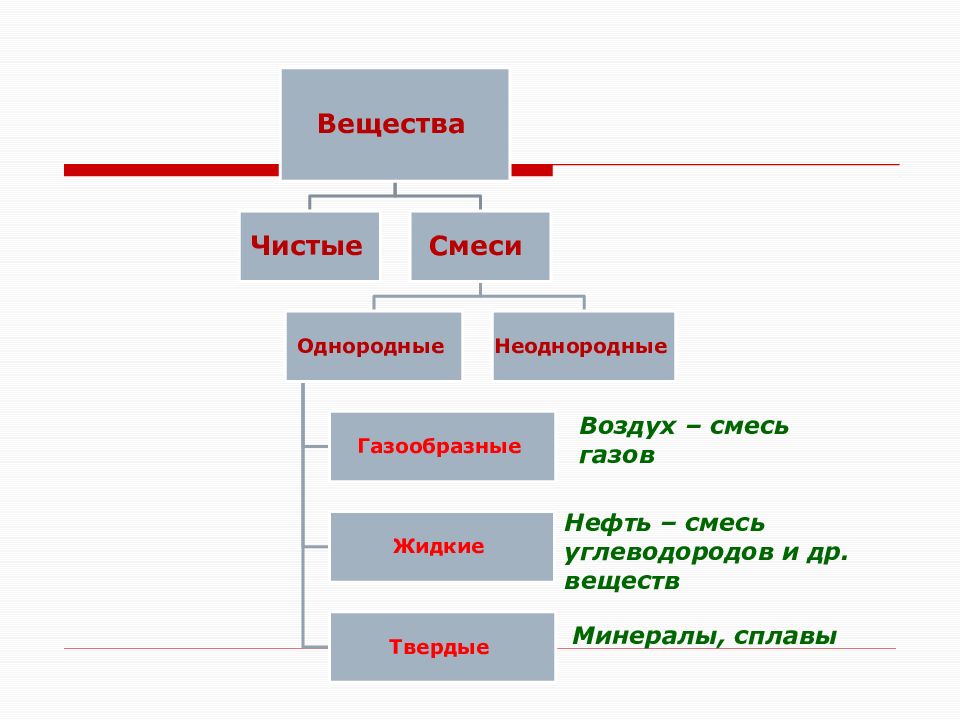 Хлор используется для уничтожения микробов в воде. В общественной водопроводной воде могут быть намеренно растворены другие минералы, например фторид, предотвращающий кариес. В некоторых районах водопроводная вода поступает прямо из колодцев и не подвергается обработке.Минеральный состав колодезной воды варьируется от места к месту и придает воде из разных регионов особый вкус (SF Рис. 2.9 B).
Хлор используется для уничтожения микробов в воде. В общественной водопроводной воде могут быть намеренно растворены другие минералы, например фторид, предотвращающий кариес. В некоторых районах водопроводная вода поступает прямо из колодцев и не подвергается обработке.Минеральный состав колодезной воды варьируется от места к месту и придает воде из разных регионов особый вкус (SF Рис. 2.9 B).
Многие люди покупают или делают дистиллированную воду самостоятельно. В районах, где вода загрязнена вредными веществами из-за окружающей среды или стихийного бедствия, употребление дистиллированной воды может сохранить здоровье людей. Если людям не нравится вкус воды в том или ином месте из-за растворенных минералов, которые придают ей характерный вкус, они могут предпочесть более нейтральный вкус дистиллированной воды.
Дистиллированная вода может быть полезной для людей, но у них может быть слишком много хорошего. может чрезмерно гидратировать или иметь слишком много воды в вашем теле. Хотя человеческие тела в основном состоят из воды, важно поддерживать правильный баланс воды и других веществ. Когда спортсмены потеют, они теряют воду и соль (SF Рис. 2.10 A.). Если спортсмен после сильного потоотделения выпьет слишком много дистиллированной или водопроводной воды, он может нарушить водно-солевой баланс в своем организме.Это влияет на способность их тел нормально функционировать. В редких случаях, если спортсмен потребляет слишком много дистиллированной или водопроводной воды, водно-солевой дисбаланс слишком велик, и спортсмен может умереть. Это причина, по которой серьезные спортсмены пьют спортивные напитки с балансом воды, солей и сахаров, чтобы поддерживать их должным образом гидратированными (SF Рис. 2.10 B). Большинство людей могут получить надлежащий баланс воды и солей с помощью обычной диеты, и им не нужно пить спортивные напитки.
Хотя человеческие тела в основном состоят из воды, важно поддерживать правильный баланс воды и других веществ. Когда спортсмены потеют, они теряют воду и соль (SF Рис. 2.10 A.). Если спортсмен после сильного потоотделения выпьет слишком много дистиллированной или водопроводной воды, он может нарушить водно-солевой баланс в своем организме.Это влияет на способность их тел нормально функционировать. В редких случаях, если спортсмен потребляет слишком много дистиллированной или водопроводной воды, водно-солевой дисбаланс слишком велик, и спортсмен может умереть. Это причина, по которой серьезные спортсмены пьют спортивные напитки с балансом воды, солей и сахаров, чтобы поддерживать их должным образом гидратированными (SF Рис. 2.10 B). Большинство людей могут получить надлежащий баланс воды и солей с помощью обычной диеты, и им не нужно пить спортивные напитки.
ФАЗОВЫЕ ДИАГРАММЫ ЧИСТЫХ ВЕЩЕСТВ На этой странице объясняется, как интерпретировать фазовые диаграммы для простых чистых веществ, включая рассмотрение частных случаев фазовых диаграмм воды и углекислого газа. Основная фазовая диаграмма Что такое фаза? В простейшем случае фаза может быть просто другим термином для твердого тела, жидкости или газа. Если у вас есть лед, плавающий в воде, у вас есть твердая фаза и жидкая фаза. Если над смесью находится воздух, то это другая фаза. Но этот термин можно использовать и в более широком смысле.Например, нефть, плавающая на воде, также состоит из двух фаз — в данном случае двух жидких фаз. Если масло и вода содержатся в ведре, то твердое ведро — это еще одна фаза. Фактически, может быть более одной твердой фазы, если ручка прикреплена к ведру отдельно, а не отформована как часть ведра. Вы можете распознать наличие различных фаз, потому что между ними существует очевидная граница — например, граница между твердым льдом и жидкой водой или граница между двумя жидкостями. Фазовые диаграммы Фазовая диаграмма позволяет точно определить, какие фазы присутствуют при любой заданной температуре и давлении. Это фазовая диаграмма для типичного чистого вещества. Эти диаграммы (включая эту) почти всегда сильно искажены, чтобы легче было увидеть, что происходит.Обычно есть два основных искажения. Мы обсудим их, когда они станут актуальными. Если вы посмотрите на диаграмму, вы увидите, что есть три линии, три области, отмеченные «твердое тело», «жидкость» и «пар», и две специальные точки, отмеченные буквами «C» и «T». Три области Это просто! Предположим, у вас есть чистое вещество при трех различных наборах условий температуры и давления, соответствующих 1, 2 и 3 на следующей диаграмме. В наборе условий 1 на диаграмме, вещество было бы твердым, потому что оно попадает в эту область фазовой диаграммы. На 2 это будет жидкость; а в точке 3 это будет пар (газ). | |
Примечание: Я использую термины пар и газ, как если бы они были взаимозаменяемыми. Между ними есть и тонких различий, которые я пока не готов объяснять. Потерпи! | |
Переход от твердого тела к жидкости путем изменения температуры: Предположим, у вас есть твердое тело, и вы увеличили температуру, сохраняя постоянное давление, как показано на следующей диаграмме.Когда температура повышается до точки, где она пересекает линию, твердое вещество превращается в жидкость. Другими словами, он тает. Если вы повторите это при более высоком фиксированном давлении, температура плавления будет выше, потому что линия между твердой и жидкой областями немного наклонена вперед. | |
Примечание: Это один из случаев, когда мы искажаем эти диаграммы, чтобы облегчить их обсуждение. | |
Так что же на самом деле представляет собой эта линия, разделяющая твердую и жидкую области диаграммы? Это просто показывает влияние давления на температуру плавления. В любом месте этой линии существует равновесие между твердым телом и жидкостью. Вы можете применить принцип Ле Шателье к этому равновесию, как если бы это было химическое равновесие. Если вы увеличите давление, равновесие будет двигаться таким образом, чтобы противодействовать только что сделанному вами изменению. Если он превратится из жидкости в твердое тело, давление снова будет уменьшаться, потому что твердое тело занимает немного меньше места для большинства веществ. Это означает, что увеличение давления на равновесную смесь твердого вещества и жидкости при ее исходной температуре плавления снова преобразует смесь в твердое тело.Другими словами, он больше не будет плавиться при этой температуре. Чтобы заставить его расплавиться при более высоком давлении, вам придется немного повысить температуру. Повышение давления повышает температуру плавления большинства твердых веществ. Вот почему для большинства веществ линия точки плавления наклонена вперед. Переход от твердого тела к жидкости путем изменения давления: Вы также можете поэкспериментировать с этим, посмотрев, что произойдет, если вы уменьшите давление на твердое тело при постоянной температуре. | |
Примечание: Вы должны быть немного осторожны с этим, потому что, что именно произойдет, если вы уменьшите давление, зависит именно от ваших начальных условий. Мы поговорим об этом подробнее, когда посмотрим на линию, отделяющую твердую область от паровой. | |
Переход от жидкости к пару: Таким же образом вы можете сделать это, изменив температуру или давление. Жидкость превратится в пар — она закипит — когда пересечет границу между двумя областями. Если вы меняете температуру, вы можете легко определить температуру кипения по фазовой диаграмме. На диаграмме выше это температура, при которой красная стрелка пересекает граничную линию. Итак, опять же, каково значение этой линии, разделяющей две области? В любом месте на этой линии будет равновесие между жидкостью и паром.Линию легче всего увидеть как эффект давления на точку кипения жидкости. Чем выше давление, тем выше температура кипения. | |
Примечание: Я не хочу придавать большого значения этому, но эта линия на самом деле точно такая же, как график влияния температуры на давление насыщенного пара жидкости. Давление насыщенного пара рассматривается на отдельной странице. Жидкость закипит, когда давление ее насыщенного пара будет равно внешнему давлению. Предположим, вы измерили давление насыщенного пара жидкости при 50 ° C, и оно оказалось 75 кПа. Вы можете изобразить это как одну точку на кривой давления пара, а затем перейти к измерению давления других насыщенных паров при различных температурах и также построить их. Теперь предположим, что вы подвергали жидкость общему внешнему давлению 75 кПа и постепенно повышали температуру. Жидкость закипит, когда давление ее насыщенного пара станет равным внешнему давлению — в данном случае при 50 ° C.Если у вас есть полная кривая давления пара, вы также можете найти точку кипения, соответствующую любому другому внешнему давлению. Это означает, что график зависимости давления насыщенного пара от температуры в точности совпадает с графиком зависимости точки кипения и внешнего давления — это всего лишь два взгляда на одно и то же. Если все, что вас интересует, это интерпретация одной из этих фазовых диаграмм, вам, вероятно, не стоит особо об этом беспокоиться. | |
Критическая точка Как вы могли заметить, эта кривая равновесия жидкость-пар имеет верхний предел, который я обозначил на фазовой диаграмме как C . Это известно как критическая точка . Температура и давление, соответствующие этому, известны как критическая температура и критическое давление . Если вы увеличите давление газа (пара) до температуры ниже критической, вы в конечном итоге пересечете линию равновесия жидкость-пар, и пар будет конденсироваться с образованием жидкости. Это работает нормально, пока температура газа ниже критической. А что, если бы ваша температура была на выше критической температуры на ? Не было бы никакой линии, которую можно было бы пересечь! Это потому, что выше критической температуры невозможно конденсировать газ в жидкость, просто увеличивая давление.Все, что вы получаете, — это сильно сжатый газ. У частиц слишком много энергии, чтобы межмолекулярное притяжение удерживало их вместе как жидкость. Очевидно, что критическая температура варьируется от вещества к веществу и зависит от силы притяжения между частицами. Чем сильнее межмолекулярное притяжение, тем выше критическая температура. | |
Примечание: Это хороший момент для быстрого комментария об использовании слов «газ» и «пар».В значительной степени вы просто используете термин, который кажется правильным. Обычно вы не говорите о «газообразном этаноле», хотя вы, , скажете, что , «пары этанола». Точно так же нельзя говорить о кислороде как о паре — вы всегда называете его газом. Существуют различные руководящие принципы, которые вы можете использовать, если хотите. Например, если вещество обычно является жидкостью при комнатной температуре или около нее, вы склонны называть то, что исходит от него, паром. Чуть более широкое использование было бы называть его паром, если вещество находится ниже своей критической точки, и газом, если оно выше нее.Конечно, было бы необычно называть что-либо паром, если он был выше своей критической точки при комнатной температуре — например, кислородом, азотом или водородом. Все это можно назвать газами. Это абсолютно НЕ то, над чем стоит волноваться! | |
Переход от твердого тела к пару: Есть еще одна линия, на которую стоит обратить внимание на фазовой диаграмме. Это линия в нижнем левом углу между твердой и паровой областями. Эта линия представляет собой равновесие твердое тело-пар. Если бы условия температуры и давления попадали точно на эту линию, твердое тело и пар находились бы в равновесии друг с другом — твердое вещество сублимировалось бы. (Сублимация — это переход непосредственно из твердого состояния в пар или наоборот без прохождения жидкой фазы.) Еще раз, вы можете пересечь эту линию, либо увеличив температуру твердого тела, либо уменьшив давление. На диаграмме показан эффект повышения температуры твердого тела при (вероятно, очень низком) постоянном давлении.Очевидно, что давление должно быть достаточно низким, чтобы жидкость не могла образоваться — другими словами, это должно происходить ниже точки, обозначенной как T . Вы можете прочитать температуру сублимации по диаграмме. Это будет температура, при которой линия пересечена. Тройная точка Точка T на схеме называется тройной точкой . Если вы думаете о трех линиях, которые встречаются в этой точке, они представляют собой условия: Там, где встречаются все три линии, у вас должна быть уникальная комбинация температуры и давления, при которой все три фазы находятся в равновесии вместе.Вот почему она называется тройной точкой . Если вы контролировали условия температуры и давления, чтобы попасть в эту точку, вы бы увидели равновесие, которое включало плавление и сублимацию твердого вещества, а также жидкость в контакте с ним, кипящую с образованием пара — и все происходящие обратные изменения также. Если вы удерживаете температуру и давление на этих значениях и держите систему закрытой, чтобы ничто не выходило, то она так и останется.Странный набор дел! Нормальные температуры плавления и кипения Нормальные точки плавления и кипения — это температуры при давлении 1 атмосфера. Их можно найти на фазовой диаграмме, проведя линию поперек при давлении в 1 атмосферу. Фазовая диаграмма для воды Есть только одно различие между этой и фазовой диаграммой, которую мы рассматривали до сих пор.Линия равновесия твердое тело-жидкость (линия точки плавления) имеет наклон назад, а не вперед. В случае воды точка плавления понижается при более высоком давлении. Почему? Если у вас есть это равновесие и вы увеличиваете давление на него, согласно принципу Ле Шателье, равновесие переместится, чтобы снова понизить давление. Это означает, что он переместится в сторону с меньшим объемом. Производится жидкая вода. Чтобы жидкая вода снова замерзла при более высоком давлении, вам придется снизить температуру.Более высокое давление означает более низкие температуры плавления (замерзания). Теперь давайте поместим числа на диаграмму, чтобы показать точное положение критической точки и тройной точки для воды. Обратите внимание, что тройная точка для воды возникает при очень низком давлении. Также обратите внимание, что критическая температура составляет 374 ° C. Было бы невозможно превратить воду из газа в жидкость, сжав ее выше этой температуры. Нормальные точки плавления и кипения воды находятся точно так же, как мы уже обсуждали — наблюдая, где линия давления в 1 атмосферу пересекает линии равновесия твердое тело-жидкость, а затем линии равновесия жидкость-пар. | |
Примечание: Далее на странице я упомянул два способа искажения этих диаграмм для облегчения понимания. Я уже указывал, что линия равновесия твердое тело-жидкость действительно должна быть намного более вертикальной. Эта последняя диаграмма иллюстрирует другое серьезное искажение, которое относится как к давлению, так и к температуре. Посмотрите, например, на промежутки между различными приведенными цифрами давления, а затем представьте, что вам пришлось изобразить их на миллиметровой бумаге! Температурная шкала также случайна. | |
И последний пример использования этой диаграммы (потому что она мне нравится). Представьте, что давление в жидкой воде снижается по линии на диаграмме ниже. Фазовая диаграмма показывает, что вода сначала замерзнет, образуя лед, когда она войдет в твердую область. Когда давление упадет достаточно низко, лед возвысится, образуя водяной пар. Другими словами, переход происходит от жидкого состояния к твердому и парообразному. Я нахожу это довольно странным! Фазовая диаграмма диоксида углерода Единственная особенность этой фазовой диаграммы — это положение тройной точки, которая намного выше атмосферного давления. | |



 Это будет длинная страница, потому что я постарался сделать все как можно мягче.
Это будет длинная страница, потому что я постарался сделать все как можно мягче. В случаях, которые мы рассмотрим на этой странице, фазы будут просто твердым, жидким или парообразным (газовым) состоянием чистого вещества.
В случаях, которые мы рассмотрим на этой странице, фазы будут просто твердым, жидким или парообразным (газовым) состоянием чистого вещества.
 На практике эта линия гораздо более вертикальна, чем мы обычно ее рисуем. Температура плавления при более высоком давлении будет очень незначительной. Диаграмму было бы очень сложно проследить, если бы мы ее немного не преувеличивали.
На практике эта линия гораздо более вертикальна, чем мы обычно ее рисуем. Температура плавления при более высоком давлении будет очень незначительной. Диаграмму было бы очень сложно проследить, если бы мы ее немного не преувеличивали.