Содержание
Почему развитая страна не может жить без органической химии » Федеральное государственное бюджетное учреждение науки Институт органической химии имени Н. Д. Зелинского РАН
И.П.Белецкая, В.П.Анаников, Журнал органической химии, 2015, т. 51, вып. 2, с. 159 — 161.
Загрузить полный текст:
Написать эту статью нас побудили два обстоятельства, которые, как мы надеемся, будут поняты и поддержаны нашими коллегами. Первое — любовь к своей профессии, которой мы посвятили жизнь и которой мы гордимся, считая ее творческой, бесконечно интересной и необходимой людям. Второе – бедственное состояние органической химии в стране, которая дала миру блестящую плеяду химиков-органиков – А.М. Бутлерова, В.В. Марковникова, Н.Н. Зинина, А.Е. Фаворского, А.М. Зайцева, А.Е. Чичибабина, Н.Д. Зелинского, И.Н. Назарова, А.Н. Несмеянова и многих других. Без этих имен невозможно представить историю органической химии.
На наш взгляд органическая химия, а особенно органический синтез, лежат в самом сердце химии. Достаточно оглянуться вокруг, чтобы убедиться, что без результатов этого синтеза не могла бы существовать современная цивилизация. Качество жизни человека напрямую зависит от развития в стране органической химии и основанной на ней промышленности. Нам нужны лекарства с самым различным спектром действия, нужны ростовые вещества и средства борьбы с вредителями сельского хозяйства. Нам нужны пластические массы, материалы с разнообразными свойствами, волокна, заменяющие шерсть и шелк, а для этого нужны мономеры, синтез которых основан на открытых химиками-органиками реакциях. Нам нужны красители, повсеместное распространение которых для самого различного применения, делает наш мир ярким и красочным. Нам нужны взрывчатые вещества и средства для тушения пожаров. Нам много всего нужно и с каждым днем все больше химических соединений становятся жизненно необходимыми. Но в основе всего этого многообразия лежит синтез молекул, обеспечивающих создание новых нужных человеку веществ и материалов.
Достаточно оглянуться вокруг, чтобы убедиться, что без результатов этого синтеза не могла бы существовать современная цивилизация. Качество жизни человека напрямую зависит от развития в стране органической химии и основанной на ней промышленности. Нам нужны лекарства с самым различным спектром действия, нужны ростовые вещества и средства борьбы с вредителями сельского хозяйства. Нам нужны пластические массы, материалы с разнообразными свойствами, волокна, заменяющие шерсть и шелк, а для этого нужны мономеры, синтез которых основан на открытых химиками-органиками реакциях. Нам нужны красители, повсеместное распространение которых для самого различного применения, делает наш мир ярким и красочным. Нам нужны взрывчатые вещества и средства для тушения пожаров. Нам много всего нужно и с каждым днем все больше химических соединений становятся жизненно необходимыми. Но в основе всего этого многообразия лежит синтез молекул, обеспечивающих создание новых нужных человеку веществ и материалов.
На сегодняшний день химики синтезировали более 88 миллионов соединений, и порядка 15000 новых химических соединений регистрируется ежедневно [1]. Это количество значительно больше того, что создала природа, и такая безграничность структур поражает воображение самих исследователей. Практически ученые создали целый химический мир, где можно найти молекулы с ранее неизвестными свойствами.
Это количество значительно больше того, что создала природа, и такая безграничность структур поражает воображение самих исследователей. Практически ученые создали целый химический мир, где можно найти молекулы с ранее неизвестными свойствами.
Органическая химия в цифровую эпоху.
У органической химии есть проблемы, общие для всех стран. Поскольку она создает молекулы (органические субстанции), а не конечные продукты – ее часто не замечают или, что еще хуже, обвиняют в загрязнении окружающей среды. Химику-органику трудно объяснить, чем он занимается, поскольку он привык думать на языке формул, малопонятном неспециалисту. Отсюда возникает трудность в популяризации нашей науки. Между тем пренебрежение органической химией (и вообще химией – а мы часто не видим этой области в государственных программах), может оказаться весьма драматичным.
Мы не без зависти смотрим, как развивается наша наука не только в индустриально развитых странах: Западная Европа, США и Япония, но и в странах Азиатского региона, таких как Китай, Индия, Южная Корея, Тайвань и др. Достигнуты впечатляющие результаты в целом ряде направлений органической химии, таких как: создание новых методов получения связей углерод-углерод и углерод-гетероатом, совершенствование методов C‑H функционализации, проведение многокомпонентных реакций, синтез сложных природных соединений, и, конечно, развитие асимметрического синтеза и органокатализа. Одновременно достигнуты успехи в создании безотходных (или малоотходных) методов синтеза. Тесное переплетение органического синтеза, катализа и металлорганической химии за короткое время изменили лицо органической химии [2]. Причем многие находки химиков-органиков в настоящее время очень быстро переходят в индустрию развитых стран.
Достигнуты впечатляющие результаты в целом ряде направлений органической химии, таких как: создание новых методов получения связей углерод-углерод и углерод-гетероатом, совершенствование методов C‑H функционализации, проведение многокомпонентных реакций, синтез сложных природных соединений, и, конечно, развитие асимметрического синтеза и органокатализа. Одновременно достигнуты успехи в создании безотходных (или малоотходных) методов синтеза. Тесное переплетение органического синтеза, катализа и металлорганической химии за короткое время изменили лицо органической химии [2]. Причем многие находки химиков-органиков в настоящее время очень быстро переходят в индустрию развитых стран.
|
Органокатализ — ускорение химических превращений с помощью каталитических или суб-стехиометрических добавок органических веществ,не содержащих металлов.
|
Эту небольшую статью, обращенную к нашим коллегам, мы решили написать под впечатлением школы-конференции, проведенной для аспирантов разных университетов и Институтов кафедрой органической химии Химического факультета МГУ. На это мероприятие в качестве лекторов были приглашены признанные ученые не только из нашей страны, но и наши соотечественники из США и Канады. Нужно было видеть, какой интерес проявили наше молодое поколение к этому мероприятию. Они задавали, действительно, умные вопросы, они участвовали в дискуссиях и сами выступали с короткими, но яркими докладами. Их энтузиазм заразил и нас, и мы чувствовали свой долг перед ними. Они – наше будущее и мы должны не только дать им знания, к которым они так стремятся, но и обеспечить возможность для них работать в нашей стране, дать уверенность, что они ей нужны.
Если говорить о современной органической химии, то хотелось бы отметить ряд вопросов, по которым нам интересно узнать мнение химиков-органиков нашей страны. В данный момент отечественная наука получила несомненную поддержку в виде весомых грантов Российского научного фонда [3]. Целенаправленная поддержка фундаментальных исследований, которой в достойном объеме не было уже многие годы, дает шанс для развития науки в стране, и, конечно же, для наиболее интересной для нас части химической науки – органической химии. Однако многое зависит от того, насколько успешно нам удастся этим шансом распорядится, и от того, как мы сможем найти свое место в бурно развивающемся химическом мире после длительного периода выживания и вынужденного простоя (отставания).
Практически все лекарственные препараты – продукт органической химии.
Безусловным флагманом, задававшим основной тренд в развитии органической химии последних двух десятилетий, являются фармацевтические, биологические и биохимические приложения. В этой сфере были достигнуты впечатляющие успехи и на сегодняшний день укрепилось мнение, что с помощью арсенала современного органического синтеза можно за разумное время синтезировать практически любую стабильную органическую молекулу с массой до 1500 — 2000 Да. Прослеживается тенденция в проведении химических трансформаций с «атомарной точностью» даже для очень сложных органических молекул [4]. Такая концентрация ресурсов на одном направлении у некоторых химиков-органиков даже вызвала небезоснавательное опасение, что яркие и востребованные приложения в какой-то момент могут вытеснить саму науку органической химии на второй план [5].
В этой сфере были достигнуты впечатляющие успехи и на сегодняшний день укрепилось мнение, что с помощью арсенала современного органического синтеза можно за разумное время синтезировать практически любую стабильную органическую молекулу с массой до 1500 — 2000 Да. Прослеживается тенденция в проведении химических трансформаций с «атомарной точностью» даже для очень сложных органических молекул [4]. Такая концентрация ресурсов на одном направлении у некоторых химиков-органиков даже вызвала небезоснавательное опасение, что яркие и востребованные приложения в какой-то момент могут вытеснить саму науку органической химии на второй план [5].
Эффективные синтетические методики для быстрого получения разнообразных органических молекул, в особенности асимметрический синтез, будут активно востребованы в науках о жизни и в ближайшее десятилетие. Эта область по-прежнему будет значимой и будет давать работу множеству химиков-органиков. Тем не менее, передовой край науки смещает свой центр тяжести, поскольку для обычных скрининговых приложений человека вполне успешно заменили роботизированные синтетические комплексы [6]. Автоматизированный синтез тысяч органических молекул из стандартных билдинг-блоков уже является рутинной процедурой [7].
Автоматизированный синтез тысяч органических молекул из стандартных билдинг-блоков уже является рутинной процедурой [7].
Молекулярное конструирование материалов нового поколения.
На наш взгляд, наиболее интересные задачи для органической химии будут поставлены в тех междисциплинарных областях, которые активно выходят в сферу практического применения. Яркими примерами таких областей является биотехнологии, геномные технологии для медицины, исследования стволовых клеток, нейрохимия, тераностика, и ряд других областей [8,9]. В этой сфере успешно сочетается фундаментальная наука, востребованность научных результатов на уровне стартапов и готовность выделения существенного финансирования из частных и государственных источников по всему миру. Нужно отметить, что такой тесный контакт наук о жизни с химическими науками отнюдь не случаен и благоприятствует развитию обеих областей [10].
| Тераностика — новое направление в современной медицине, сочетающее в себе терапию и диагностику. Планируется создание лекарственных препаратов, одновременно обладающих диагностическими и лечебными свойствами. |
Материаловедение является вторым ключевым игроком, оказывающим существенное влияние на химические науки. Эволюция физико-химических методов исследования и развитие нашего понимания сложных процессов, лежащих в основе функционирования материалов нового поколения, позволило связать свойства материалов с их молекулярной структурой. Это достижение закладывает основы для управления свойствами материалов и конечных устройств за счет конструирования нужных молекул – традиционной сферой деятельности органической химии. К примеру, создание множества передовых материалов для молекулярной электроники, солнечных элементов, специализированных устройств поглощения/испускания света, химических сенсоров и интерфейсов основано на применении реакций кросс-сочетания, реакции Хека и других металл-катализируемых превращений. Прогресс в этой области во многом будет зависеть от доступности сложных органических молекул и стоимости их производства.
Прогресс в этой области во многом будет зависеть от доступности сложных органических молекул и стоимости их производства.
Эволюционное развитие методических основ органического синтеза проходило под влиянием концепции Зеленой химии (Green Chemistry) и парадигмы устойчивого развития (Sustainable Chemistry). Ряд жестких требований по экономии природных ресурсов, охране окружающей среды и эффективности химических процессов сориентировали химиков в первую очередь на каталитические технологии. Беспрецедентно сложные критерии по активности, селективности, стабильности и регенерируемости каталитических систем нацелили исследователей на разработку так называемых «идеальных» каталитических систем [11]. И все же, надо сказать, что, не смотря на значительные успехи, данная область еще далека от достижения поставленной цели.
Есть еще целый ряд областей и достижений органической химии, о которых очень хочется упомянуть. Но такой подробный обзор не является задачей этого короткого эссе. Нам будет интересно услышать отклики читателей по этим непростым вопросам и по возможным планам развития органической химии в нашей стране в ближайшем будущем. Наиболее интересные отклики будут опубликованы для дальнейшей дискуссии. Вне всяких сомнений, в современном мире развитая страна не может существовать без органической химии. И мы считаем, что химики-органики нашей страны не могут находиться в стороне, когда обстоятельства требуют нашего активного участия.
Нам будет интересно услышать отклики читателей по этим непростым вопросам и по возможным планам развития органической химии в нашей стране в ближайшем будущем. Наиболее интересные отклики будут опубликованы для дальнейшей дискуссии. Вне всяких сомнений, в современном мире развитая страна не может существовать без органической химии. И мы считаем, что химики-органики нашей страны не могут находиться в стороне, когда обстоятельства требуют нашего активного участия.
Благодарность. И.П.Б. выражает признательность за поддержку гранту РНФ 14-23-00186, В.П.А. выражает признательность за поддержку гранту РНФ 14-50-00126. Авторы благодарят Е.Г.Гордеева за предоставленные иллюстрации.
СПИСОК ЛИТЕРАТУРЫ
1CAS REGISTRY and CAS Registry Number, American Chemical Society, 2014-2015. http://www.cas.org/content/chemical-substances/faqs
2 I. P. Beletskaya, V. P. Ananikov, Organometallics, 2011, 30, 5 – 6. [doi: 10.1021/om100982z]
P. Beletskaya, V. P. Ananikov, Organometallics, 2011, 30, 5 – 6. [doi: 10.1021/om100982z]
3Конкурсный отбор научных, научно-технических программ и проектов, Российский научный фонд, 2014-2015. http://www.rscf.ru/
4 В.П.Анаников, Л.Л.Хемчян, Ю.В.Иванова, В.И.Бухтияров, А.М.Сорокин, И.П.Просвирин, С.З.Вацадзе, А.В.Медведько, В.Н.Нуриев, А.Д.Дильман, В.В.Левин, И.В.Коптюг, К.В.Ковтунов, В.В.Живонитко, В.А.Лихолобов, А.В.Романенко, П.А.Симонов, В.Г.Ненайденко, О.И.Шматова, В.М.Музалевский, М.С.Нечаев, А.Ф.Асаченко, О.С.Морозов, П.Б.Джеваков, С.Н.Осипов, Д.В.Воробьева, М.А.Топчий, М.А.Зотова, С.А.Пономаренко, О.В.Борщев, Ю.Н.Лупоносов, А.А.Ремпель, А.А.Валеева, А.Ю.Стахеев, О.В.Турова, И.С.Машковский, С.В.Сысолятин, В.В.Малыхин, Г.А.Бухтиярова, А.О.Терентьев, И.Б.Крылов, Успехи химии, 2014, 83 (10), 885 – 985. [doi: 10.1070/RC2014v083n10ABEH004471]
5 М.П. Егоров, Успехи химии, 2014, 83 (10), стр.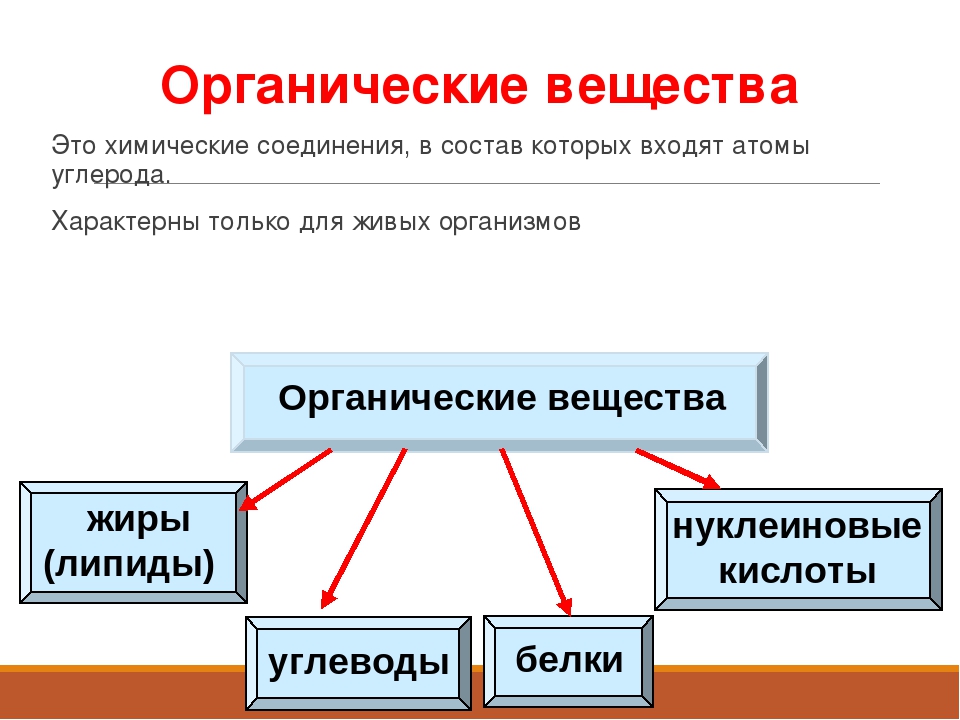 iii.
iii.
[link: http://www.uspkhim.ru/php/content_rus.phtml?journal_id=rc&year_id=2014&issue=10]
6 M. Peplow, Nature, 2014, 512, 20 – 22. [doi: 10.1038/512020a]
7 E. M. Woerly, J. Roy and M. D. Burke, Nat Chem, 2014, 6, 484–491. [doi: 10.1038/nchem.1947]
8 B.W. Agranoff, History of Neurochemistry, in Encyclopedia of Life Sciences, 2001, John Wiley & Sons, Ltd. [doi: 10.1038/npg.els.0003465].
9 E.-K. Lim, T. Kim, S. Paik, S. Haam, Y.-M. Huh and K. Lee, Chem. Rev., 2014, 115, 327 – 394. [doi: 10.1021/cr300213b]
10 C.H. Arnaud, Chem. Eng. News, 2014, 92 (50)28 – 30.
[link: http://cen.acs.org/articles/92/i50/Confronting-Irreproducibility-Life-Sciences-Research.html]
11 I. P. Beletskaya, V. P. Ananikov, Organometallics, 2012, 31, 1595 – 1604.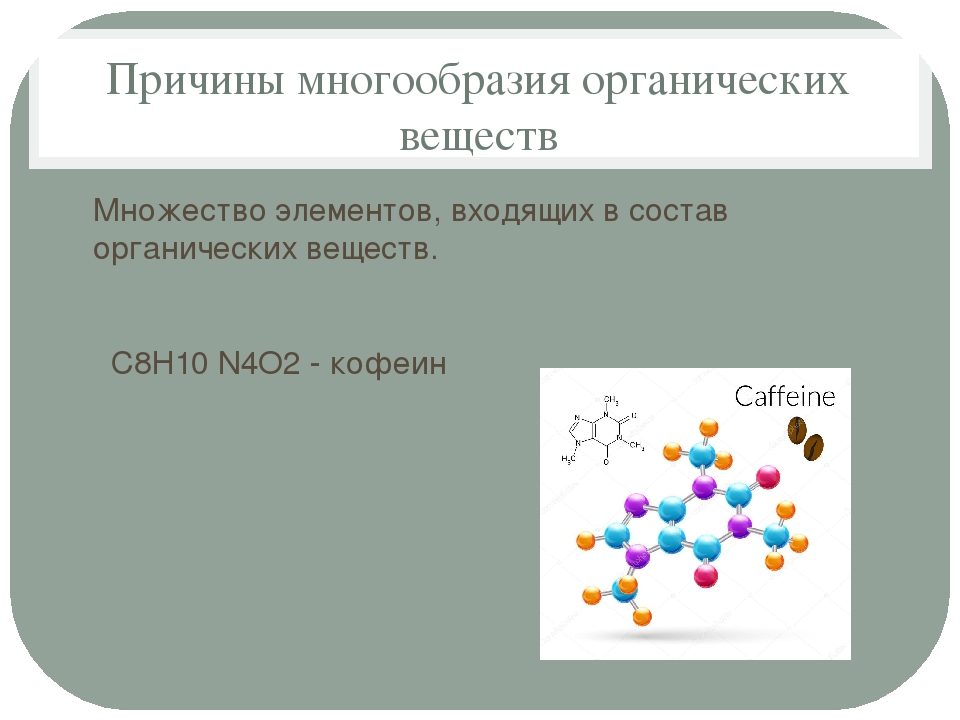 [doi: 10.1021/om201120n]
[doi: 10.1021/om201120n]
И.П.Белецкая, В.П.Анаников, Журнал органической химии, 2015, т. 51, вып. 2, с. 159 — 161.
Загрузить полный текст:
Органические вещества — Справочник химика 21
Так вот, атом водорода карбоксильной группы отделяется от нее в миллион раз легче, чем от гидроксильной группы фенола. Поэтому всякое органическое вещество, содержащее карбоксильную группу, обладает ярко выраженными кислотными свойствами. Такие вещества носят название карбоновых кислот. [c.153]
Химики делят все вещества на два класса. К одному относятся, например, масло, сахар, крахмал, клей, желатин, шелк, каучук, бумага и пенициллин. Все это органические вещества. К, другому относятся воздух, вода, песок, глина, соль, золото, серебро, железо, латунь, стекло и цемент. Это неорганические вещества. [c.9]
Еще более заметным для первых химиков было другое различие. Органические вещества можно было обработать теплом или какими-нибудь другими способами и превратить в неорганические. Однако не было известно такого способа, чтобы взять неорганическое вещество и превратить его в органическое. [c.10]
Органические вещества можно было обработать теплом или какими-нибудь другими способами и превратить в неорганические. Однако не было известно такого способа, чтобы взять неорганическое вещество и превратить его в органическое. [c.10]
Поэтому Берцелиус и назвал вещества, которые можно добыть из живых организмов, органическими, а все остальные— неорганическими. Первые — продукт жизни, а вторые — нет. Если вы знаете детскую игру про животное, растительное и минеральное царства, то органические вещества вы отнесете к царству животных или [c.9]
В 1807 г. Берцелиус предложил вещества, подобные оливковому маслу или сахару, которые типичны для живой природы, называть органическими. Вещества, подобные воде и соли, которые характерны для неживой природы, он назвал неорганическими. [c.69]
Химиков не переставало удивлять, что органические вещества при нагревании или каком-либо другом жестком воздействии легко превращаются в неорганические вещества. (Возможность обратного превращения, т. е. превращения неорганического вещества в органическое, была установлена несколько позднее.) То время было временем господства витализма — учения, рассматривающего жизнь [c.69]
(Возможность обратного превращения, т. е. превращения неорганического вещества в органическое, была установлена несколько позднее.) То время было временем господства витализма — учения, рассматривающего жизнь [c.69]
Немецкий химик Юстус Либих (1803—1873) усовершенствовал методику анализа и в 1831 г. смог получить весьма достоверные эмпирические формулы . Два года спустя французский химик Жан Батист Андре Дюма (1800—1884) модифицировал метод Либиха. Пользуясь разработанным им методом, можно было наряду с прочими продуктами сгорания собирать также и азот и, следовательно, определять содержание азота в органическом веществе. [c.75]
Однако в 1827 году было сделано великое открытие. Оно касалось органического вещества, называемого мочевина. Это твердое вещество белого цвета, которое содержится в выделениях организма. Взрослый человек в день выделяет примерно 30 г этого вещества с мочой. [c.10]
А вскоре химики получали в лаборатории уже много других органических веществ из неорганических. Разделение химических веществ на два класса утратило свой первоначальный смысл. [c.11]
Разделение химических веществ на два класса утратило свой первоначальный смысл. [c.11]
Однако гораздо больше его в другой фракции того же угля. После того как уголь нагрет и из него выделился коксовый газ, в угле еще остается немного органического вещества. Если еще сильнее нагреть уголь, выделяется и оно если его собрать, получится густая черная жидкость, которая называется каменноугольной смолой. Тонна угля может дать около 60 фунтов каменноугольной смолы. [c.62]
С органическими соединениями, молекулы которых отличались внушительными размерами, дело обстояло сложнее. Используя методы начала XIX в., было очень тяжело, вероятно и невозможно, установить точную эмпирическую формулу даже такого довольно простого по сравнению, например, с белками органического соединения, как морфин. В настоящее время известно, что в молекуле морфина содержатся 17 атомов углерода, 19 атомов водорода, 3 атома кислорода и 1 атом азота ( ijHisNOa). Эмпирическая формула уксусной кислоты (С2Н4О2) намного проще, чем формула морфина, но и относительно этой формулы в первой половине XIX в. не было единога мнения. Однако, поскольку химики собирались изучать строение молекул органических веществ, начинать им необходимо было с установления эмпирических формул. [c.74]
не было единога мнения. Однако, поскольку химики собирались изучать строение молекул органических веществ, начинать им необходимо было с установления эмпирических формул. [c.74]
Органические вещества во многом отличаются от неорганических. Например, они гораздо менее прочны и менее долговечны, чем неорганические. Воду (а это неорганическое вещество) можно вскипятить, а получившийся пар нагреть до тысячи градусов без всякого для него вреда. Если вы охладите пар, из него снова получится вода. А если нагревать растительное масло (это — органическое вещество), то оно начнет дымить и гореть и перестанет быть растительным маслом. Соль (неорганическое вещество) вы можете нагревать до тех пор, пока она не расплавится и не раскалится докрасна. Охладите ее — и она останется той же солью. Если же нагревать сахар (органическое вещество), начнут выделяться газы, а потом сахар обуглится и почернеет. После охлаждения уже никогда не удастся снова получить сахар. [c.10]
Однако до Дюма никто не подумал объединить и обобщить все эти отдельные наблюдения в революционное для тогдашнего времени учение о способности атома хлора заменять атом водорода в органическом веществе.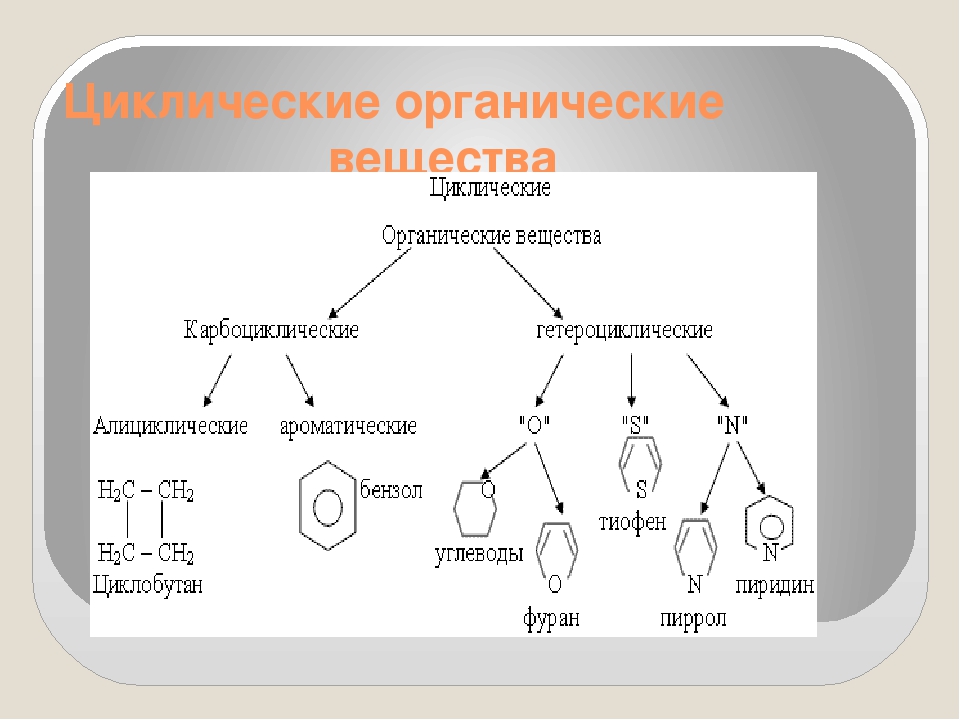 Ведь тогда еще считали, что хлор соединяется с органическим веществом только в двойные комплексы, и сомневались в том, что отрицательный элемент хлор может вступить на место положительного элемента водорода. [c.530]
Ведь тогда еще считали, что хлор соединяется с органическим веществом только в двойные комплексы, и сомневались в том, что отрицательный элемент хлор может вступить на место положительного элемента водорода. [c.530]
Казалось, что органические вещества могут быть только составной частью живой ткани. Первые химики думали, что для их получения нужна некая таинственная жизненная сила . Они полагали, что жизненная сила содержится только в живой ткани и что воспроизвести природные процессы в лаборатории невозможно. [c.10]
Сравнительно недавно удалось получить фумаровую кислоту пропусканием см еси 1 г-мол паров дихлорпентана со 188 г-мол воздуха над пятиокисью ванадия при 425° и объемной скорости 50—60 час (около 57 л газа на 1 л катализатора в час в пересчете на органическое вещество). Выход достигает около 28,4% вес. [208]. [c.229]
В настоящее время разработаны стабилизаторы перекиси водорода. В качестве стабилизаторов используются ортофосфорная и пи-рофосфорная кислоты и их соли. Смеси концентрированной перекиси водорода с органическими веществами (бензолом, толуолом, спиртами) являются взрывчатыми веществами. Попадание концентрированной перекиси водорода на кожу вызывает сильные ожоги. Лучшей помощью в этом случае является обильное промывание водой пораженных мест. [c.126]
Смеси концентрированной перекиси водорода с органическими веществами (бензолом, толуолом, спиртами) являются взрывчатыми веществами. Попадание концентрированной перекиси водорода на кожу вызывает сильные ожоги. Лучшей помощью в этом случае является обильное промывание водой пораженных мест. [c.126]
В ЭТОЙ книге я время от времени буду пользоваться такими формулами. Не нужно их пугаться. Каждую формулу я буду объяснять по ходу дела, и вы поймете, что разобраться в них не так уж трудно. Больше того, вам будет очень трудно, даже невозможно узнать что-нибудь об органических веществах, не прибегая к таким формулам. Это то же самое, что пытаться собрать сложную машину, которую вы до сих пор никогда не видели, без всяких чертежей. [c.16]
Каждое органическое соединение, для которого известно строение молекулы, имеет официальное название по женевской номенклатуре. Впрочем, ими пользуются не всегда. Во-первых, многие органические вещества получили имена задолго до 1892 года, и к этим традиционным названиям химики привыкли. А во-вторых, названия, соответствующие правилам женевской номенклатуры, нередко оказываются такими сложными и длинными, что химики удобства ради придумывают более короткие и пользуются ими. [c.43]
Во-первых, многие органические вещества получили имена задолго до 1892 года, и к этим традиционным названиям химики привыкли. А во-вторых, названия, соответствующие правилам женевской номенклатуры, нередко оказываются такими сложными и длинными, что химики удобства ради придумывают более короткие и пользуются ими. [c.43]
В 1845 г. Адольф Вильгельм Герман Кольбе (1818—1884), ученик Вёлера, успешно синтезировал уксусную кислоту, считавшуюся в его время несомненно органическим веществом. Более того, он синтезировал ее таким методом, который позволил проследить всю цепь химических превращений — от исходных элементов (углерода, водорода и кислорода) до конечного продукта — уксусной кислоты. Именно такой синтез из элементов, или полный синтез, и был необходим. Если синтез мочевины Вёлера породил сомнения относительно существования жизненной силы , то синтез уксусной кислоты Кольбе позволил решить этот вопрос. [c.71]
Из-за -Таких геометрических фигур большинство формул органических веществ кажутся не специалистам такими сложными. На самом же деле если вы запомнит [c.57]
На самом же деле если вы запомнит [c.57]
Некоторые полезные органические вещества представляют собой природные соединения — их извлекают из тканей какого-нибудь живого организма, или в результате действия живого организма на окружающую его среду, или из остатков живых организмов. Другие органические вещества в природе не существуют — их создают химики, это синтетические соединения. Примером их может служить и ДДТ. [c.76]
Когда органическая молекула полностью окислена, все ее атомы углерода превращаются в двуокись углерода, или углекислый газ. Его молекула состоит из одного атома углерода и двух атомов кислорода. А водородные атомы, входившие в состав органического вещества, превращаются в воду, молекулы которой состоят из двух молекул водорода и одной молекулы кислорода. [c.83]
У нижнего конца кварцевой трубки в ходе процесса можно отбирать пробы. Когда определение гидролизующегося хлора титрованием пробы покажет, что желательная степень превращения уже достигнута, то реакцию прекращают, содержимое трубки спускают и перерабатывают. Такая установка пригодна также и для испытания небольших количеств других органических веществ в отношении их способности к сульфохлорированию. [c.399]
Этим еще раз был подтвержден факт, установленный ранее Гей-Люссаком и другими, что органическое вещество, обработанное хлором, обладает способностью удерживать этот элемент. Некоторые исследователи указывали также, что количество поглощенного хлора эквивалентно выделившемуся хлористому водороду. [c.530]
Вёлер, Кольбе и Бертло синтезировали относительно простые органические соединения, тогда как для живой природы характерны значительно более сложные соединения типа крахмала, жиров и белков. Изучать такие соединения гораздо труднее непросто даже установить их точный элементный состав. В целом изучение органических веществ обещало разгадку многих проблем, но подступиться к этим веществам химику прошлого века было совсем непросто. [c.71]
В 80-х годах XVIII столетия Лавуазье пытался определить относительное содержание углерода и водорода в органических соединениях. Он сжигал изучаемое соединение и взвешивал выделившиеся углекислый газ и воду. Результаты такого определения были не очень точными. В первые годы XIX в. Гей-Люссак (автор закона объемных отношений, см. гл. 5) и его коллега французский химик Луи Жак Тенар (1777—1857) усовершенствовал этот метод. Они сначала смешивали изучаемое органическое соединение с окислителем и лишь потом сжигали. Окислитель, например хлорат калия, при нагревании выделяет кислород, который хорошо смешивается с органическим веществом, в результате чего сгорание происходит быстрее и полнее. Собирая выделяющиеся при сгорании углекислый газ и воду, Гей-Люссак и Тенар могли определить соотношение углерода и водорода в исходном соединении. С помощью усовершенствованной к тому времени теории Дальтона это соотношение можно было выразить в атомных величинах. [c.74]
Но все это не годится, когда речь идет об органических веществах. Их так много, что часто у двух или нескольких разных соединений молекулы состоят из одних и тех же атомов в одних и тех же количествах. Например, у двух органических соединений — этилового спирта и диметилового эфира — молекулы состоят из двух атомов углерода, шести атомов водорода и одного атома, кислорода. Формула обоих соединений оказывается одинаковой — СаНбО (такие вeцie твa получили [c.14]
Органические смазки. В качестве загустителей консистентных смазок было предложено несколько органических веществ, таких как фталоцианиновые соединения, производные мочевины, гетероциклические соединения и др. Органические смазки имеют очень хорспиие эксплуатационные свойства и могут применяться как универсальные для различных механизмов и условий применения. [c.190]
Ароматические углеводороды могут быть получены и из некоторых сортов каменного угля. Такой уголь, обычно называемый жирным , на 70—80 процентов состоит из углерода, Остальные же 20—30 процентов — это водород и органические вещества, преимущественно углеводороды. Если такой уголь нагревать без доступа воздуха (чтобы он не загорелся), из него выделяется все, кроме углерода. Остающийся чистый углерод называют коке м. А вещества, выделившиеся из угля под действием нагревания, образуют газ, получивший название коксового газа. Он состоит в основном из водброда и метана, но есть в нем и пары более сложных соединений, которые можно отделить. Это главным образом бензол, толуол и ксилолы. Каждая тонна такого угля может дать их примерно 3 галлона. [c.60]
Так как при окислении парафина кислород распределяется по всем метиленовым группам примерно равномерно, нри окислении получаются кислоты разного молекулярного веса, из которых нерегопкой отделяют кислоты, пригодные для мыловарения. Окисление проводят при возможно низких температурах порядка 105—120° [69]. Образующиеся жирные кислоты, особенно высокомолекулярные, окисляются далее, при этом образуются оксикислоты, кетокислоты и двухосновные жирные кислоты, не растворимые в бензине. Чтобы свести к минимуму образование этих нежелательных побочных продуктов, окисление ограничивают 30—50%-ным превращением всей окисляемой углеводородной смеси. В качестве катализатора применяют в большинстве случаев перманганат калия в количестве 0,3% вес. от всего парафина. Перманганат калия вводят нри перемешивании в нагретый до 150° парафин в виде концентрированного водного раствора, вода испаряется, а перманганат восстанавливается органическим веществом до двуокиси марганца, которая распределяется в реакционной смеси в исключительно тонко распыленном состоянии. Окисление ведут без применения давления. Важно, чтобы применяемый для окисления воздух поступал в парафин в возможно тонко распыленном состоянии. [c.162]
Наилучшие результаты дает омыление содовым раствором, так как в этом случае сводится к минимуму образование побочного продукта — диаллилового эфира, которого получается тем больше, чем концентрированное омыляющип раствор щелочи. При применении соды в качестве омыляю-щего раствора необходимо непрерывно удалять образующуюся углекислоту. При этом имеют место значительные потери органического вещества. Для избежания этого в реакционную смесь непрерывно добавляют натриевую щелочь в количестве, необходимом для поддержания щелочности среды, [c.174]
Достижение равновесия 502С12 502+ СЬ ускоряется не только твердыми катализаторами, ш и многочисленными органическими веществами. [c.185]
Синтетические моющие средства, особенно соли сульфокислот и алкилсульфлты, пе обладают способностью удерживать смытую грязь в растворе, т. е. способностью предотвращать товторное поглощение волокном окрашенной грязи — свойством, которым мыло обладает в очень высокой мере. Окрашенные загрязнения, состоящие из пыли и прочих неорганических составных частей, частично удерживаются на ткани органическими веществами, именно как жиры, масла и пот. Если эти вещества моющим средством извлекаются из ткани, переходя в эмульгированное состояние, то загрязнения в значительной мере теряют свою связь и также отделяются от волокна и связываются с мицеллами натурального мыла, что препятствует их обратному поглощению волокном. В случае синтетических средств типа солей сульфокислот, у которых вследствие слабовыраженного коллоидного характера мицеллы образуются лишь в меньшей мере, способность удержания смытой грязи в растворе выражена значительно слабее. Синтетические моющие средства обладают большой диспергирующей способностью, в результате чего грязь, переходя в раствор, оказывается сильно диспергированной и в таком виде вновь частично поглощается хлопчатобумажным волокном. Это приводит к тому, что со временем наблюдается посерение белья, которое, правда, становится заметным лишь после повторных стирок. Чтобы предупредить такое посерение белья, необходимо к синтетическим моющим веществам, не обладающим способностью удержания смытой грязи в растворе, прибавлять вещества, способные выполнить роль мицелл мыла. Такие вещества были найдены, -например, в виде тилозы НВК (эфира целлюлозы и гликолевой кислоты, являющегося продуктом реакции алкилцеллюлозы с моно-хлоруксуснокислым натрием — карбоксиметилцеллюлозы), применяемой либо самостоятельно, либо в смеси с силикатом натрия. В настоящее время их прибавляют в определенном количестве к каждому синтетическому моющему средству, особенно к мыльным порошкам. [c.409]
Перманганат калия вводят в виде концентрированного водносо раствора в нагретый до 150° парафин. Вода испаряется, и перманганат, находящийся в жидкости в результате хорошего перемешивания в виде очень тонкой взвеси, частично восстанавливается органическим веществом в чрезвычайно дисперсный МпОг. Таким образом удается снизить температуру до ПО—120° и тем не менее сохранить технически приемлемую скорость лроцесса. [c.450]
Из 1000 весовых частей синтетического парафинового гача получают 270 весовых частей водного конденсата, из которых органических веществ 90—120 весовых частей. Прюкнер приводит следующий состав (в %) конденсаторной воды [68]. [c.469]
Караш, Уоллинг и Майо [53] смогли подтвердить результаты Лауера и Стодола и показали, что ни присутствие перекисей или других органических веществ, ни температура, растворитель или природа галоидоводорода не оказывают никакого влияния на количественное соотнощение, в котором образуются изомерные бромпентаны [c.551]
В заключение следует сказать несколько слов о технике безопасности в лаборатории количественного анализа. Все операции с ядовитыми газами и жидкостями (НгЗ, Вгг, СЬ, ртуть и ее соединения, соединения мышьяка и т. п.) необходимо проводить под тягой. С большой осторожностью нужно работать с фтористоводородной и хлорной кислотами. Первая может причинить серьезные ожоги, вторая взрывается при нагревании в присутствии органических веществ. Выпаривание всех сильных кислот и растворов, содержащих пахучие вещества, необходимо проводить в вытяжном шкафу, при отмеривании едких и ядовитых жидкостей нужно пользоваться мерными цилиндрами и специальными пипет ками. [c.41]
С1пределение описанным методом далеко не всегда дает достаточно правильное представление о количестве гигроскопической воды. Действительно, потеря в массе во время высушивания зависит от удаления из вещества не только гигроскопической, но и кристаллизационной воды, равно как и других летучих составнЬ1Х частей вещества. Другим часто встречающимся источником погрешностей рассматриваемого метода является окисление исследуемого вещества кислородом воздуха при нагревании. Потеря в массе вследствие этого оказывается меньшей, чем должна была бы быть, судя по действительному содержанию гигроскопической воды. Это наблюдается при анализе многих органических веществ, например муки, кожи и т. п. [c.165]
Органическая химия (1968) — [
c.22
]
Качественный полумикроанализ (1949) — [
c.0
]
Аналитическая химия висмута (1953) — [
c.0
]
Аналитическая химия брома (1980) — [
c.0
]
Очистка сточных вод (2004) — [
c.0
]
Санитарно-химический контроль воздушной среды (1978) — [
c.32
]
Двойной слой и кинетика электродных процессов (1967) — [
c.0
]
Химия промышленных сточных вод (1983) — [
c.0
]
Аналитическая химия промышленных сточных вод (1984) — [
c.0
]
Перекись водорода (1958) — [
c.0
]
Курс органической химии (1979) — [
c.0
]
Эмиссионный спектральный анализ Том 2 (1982) — [
c.0
]
Очерк общей истории химии (1969) — [
c.40
,
c.69
,
c.94
,
c.152
,
c.161
,
c.173
,
c.358
,
c.359
]
Технический анализ Издание 2 (1958) — [
c.0
]
Неорганическая химия (1950) — [
c.193
]
Курс органической химии (1970) — [
c.0
]
Объёмный анализ Том 2 (1952) — [
c.0
]
Органическая химия (1972) — [
c.14
]
Фотометрический анализ методы определения неметаллов (1974) — [
c.0
]
Курс химического качественного анализа (1960) — [
c.621
]
Органическая химия (1972) — [
c.14
]
Курс химического и качественного анализа (1960) — [
c.62
]
Краткий справочник химика Издание 4 (1955) — [
c.0
]
Курс органической химии _1966 (1966) — [
c.0
]
Органическая химия Издание 4 (1970) — [
c.0
]
Методы аналитической химии — количественный анализ неорганических соединений (1965) — [
c.0
]
Биохимия Издание 2 (1962) — [
c.6
,
c.8
,
c.15
,
c.229
]
Происхождение жизни Естественным путем (1973) — [
c.14
,
c.68
,
c.74
,
c.75
,
c.82
,
c.94
,
c.96
,
c.104
,
c.129
,
c.131
,
c.139
,
c.148
,
c.175
,
c.177
,
c.179
,
c.191
,
c.192
,
c.200
,
c.207
,
c.221
,
c.271
,
c.285
,
c.287
,
c.304
,
c.305
,
c.310
,
c.311
,
c.367
,
c.380
,
c.385
,
c.387
,
c.389
,
c.390
,
c.392
]
Помогите ответить на вопросы. 1. Что такое органические вещества? Примеры
2. Особенности
1) класс химических соединений, в состав которых входит углерод (спирт C2H5OH, глюкоза C6h22O6 )
2)1) атомы углерода способны соединяться друг с другом;
2) образуют цепи и кольца, что не так типично для неорганических соединений. Это одна из причин многообразия органических соединений;
3) одной из важных особенностей органических соединений, которая накладывает отпечаток на все их химические свойства, является характер связей между атомами в их молекулах.
3)Причины многообразия органических веществ: химическое строение, элементарный (качественный) состав.
4)Гомологи — отличаются на одну или несколько групп Ch3 и имеют сходное химическое строение. Например: Бутан и Пропан
5)Структурная формула — это разновидность химической формулы, графически описывающая расположение и порядок связи атомов . Ch4-Ch3-Ch3-Ch4
6)Изомеры — одинаковы по атомному составу и молекулярной массе, но различаются по строению или расположению атомов в пространстве и, вследствие этого, по свойствам. Бутен-1, Бутен-2; Пропанол-1, Пропанол-2.
7)Способность атомов химических элементов образовывать определённое число химических связей. Валентность Углерода (С) — 4. Он может присоединять к себе только 4 элемента, например: Ch5, в данном веществе атом углерода присоединил к себе 4 атома водорода, Ch4Cl, а в это углерод присоединил три атома водорода и и один хлора, но по прежнему образовал 4 связи.
8)В 1812 году итальянский физик и химик Амедео Авогадро, изучая молекулярные веса газов (водорода, кислорода,азота, хлора), выдвинул молекулярную гипотезу строения вещества. Однако работа Авогадро долгое время не получала признания, что тормозило развитие основных идей в области химического строения молекул. Лишь после убедительного доклада Станислао Канниццаро на первом международном съезде химиков в Карлсруэ (1860) атомные веса, определённые с помощью закона Авогадро, стали общепринятыми. На съезде разграничили понятия «атом», «молекула», утвердили атомно-молекулярное учение, основное положение которого «атомы при взаимодействии образуют молекулу».
9)Первые теоретические представления в органической химии берут свое начало от Лавуазье. Согласно его учению, органические вещества можно рассматривать как состоящие из двух частей: кислорода и радикала.
10)Основные положения теории хим. строения орг. веществ А.М. Бутлерова (1861 г)
1) Атомы друг с другом соединяются в четко в определенной последовательности согласно их валентности.
2) По свойствами вещества можно определить его строение, и наоборот.
3) Атомы и группы атомов оказывают влияние друг на друга.
4) Свойства веществ зависят не только от количества атомов, но и от порядка их соединения
12)является важнейшей частью теоретического фундамента органической химии
Органические вещества в сельском хозяйстве
Органические вещества играют важнейшую роль в сельском хозяйстве, поэтому широко используются для повышения урожайности путем создания плодородной почвы. К органическим удобрениям относятся вещества, выведенные биологическим способом, исключая присутствие химии. Ведь в органическом сельском хозяйстве минимизируется использование синтетических удобрений, стимуляторов и добавок – они заменяются натуральными аналогами настолько, насколько это возможно.
Основной целью использования органических веществ в сельском хозяйстве является получение безопасной, но в то же время устойчивой к различным неблагоприятным внешним воздействиям продукции. В результате активизируется эффект севооборота и поступление в почву биологических веществ. Биологические удобрения для органического земледелия – это уникальная производственная система, которая поддерживает здоровье почв и экосистем. Применяемые методы зависят не только от экологических процессов, но и от биологического разнообразия и природных циклов, исключая использование неблагоприятных ресурсов.
Преимущества использования органических удобрений
Стандартные органические вещества в сельском хозяйстве усиливают биологическую активность почвенной составляющей. Наиболее распространенными из них являются навоз, компосты и птичий помет, которые богаты питательными веществами.
Основные преимущества биологических удобрений:
- улучшают текстуру почвы, аэрацию и дренаж;
- содержат вторичные микроэлементы;
- обеспечивают постепенное питание растительности;
- повышают плодородность почвы;
- обладают доступностью и простотой использования.
Живая почва, богатая перегноем и микроэлементами, служит ключом к появлению богатого урожая, так как ингредиенты готовых смесей чаще всего сопоставляются с конкретными потребностями почвы. Таким образом, при внесении готовой смеси в почвенный состав, органические удобрения устраняют недостаток определенных веществ. Удобрения для органического земледелия отличаются легкостью усвояемости растительностью, находящейся на участке.
Виды удобрений на органике
Навоз – несмотря на то, что свежий навоз чрезвычайно богат всеми необходимыми микро- и макроэлементами, специалисты рекомендуют вносить его в почву после компостирования. Перегной по сравнению со свежим удобрением в 2 раза повышает содержание азота и фосфора, а калия – в 1,5 раза. Свежий навоз способен делать растения чувствительными к разным заболеваниям.
Особенности состава навоза:
- коровий навоз содержит фосфора 50% от азота, а содержание калия несколько выше азота;
- в конском навозе состав азота еще выше, а другие элементы находятся в таком же процентном отношении, что и в коровьем;
- в овечьем навозе, по сравнению с коровьим, азота больше на 50-60%, фосфора – на 60-70%, калия – на 55%;
- в свином – такое же содержание азота, фосфора в 2 раза больше, а калий находится на таком же уровне, что и в коровьем навозе.
Птичий помет – из числа птичьих пометов (куриного, утиного, гусиного, голубиного) наибольшей концентрацией микроэлементов обладает куриный: в среднем в нем содержится 4,5% азота, 3,9% фосфора, 1,9% калия. На втором месте по содержанию питательных составляющих находится голубиный помет, и заканчивает ряд гусиный помет с содержанием азота 0,7%, фосфора – 0,6%, калия – 1,3%.
Компост – для приготовления компоста применяется навоз с дополнительными растительными остатками, например, с соломой или листьями. В процессе разложения все составляющие перемешиваются между собой и образуют питательную массу – гумус. В таком сырье обитает обильная микрофлора, которая дополнительно обогащает состав смеси.
Костная мука – данный вид удобрений получают из отходов мясокомбината. Костная мука богата фосфорными соединениями и кальцием, что благотворно влияет на рост множества растений. Костную муку можно вносить как в почву, так и добавлять в компосты или другие питательные смеси.
Торф – масса, которая состоит из слаборазложившихся растительных остатков, поэтому в ней мало питательных веществ и минералов (так как масса медленно минерализуется). В качестве самостоятельной добавки не используется. Торф вносят в почву для улучшения ее физических свойств, аэрации и дренажа. Чаще всего служит для приготовления торфо-навозного компоста.
Универсальные органические вещества в сельском хозяйстве включают в свой состав остатки растительности, компост, дерновую землю, сидераты и многие другие компоненты биологического происхождения. Готовые добавочные смеси минеральных удобрений превращают компосты в органично-минеральные составы, увеличивая их ценность.
Формы выпуска
Для наиболее удобного использования продукции и максимального всасывания питательных веществ корневищем производители выпускают готовые смеси в разных формах:
- водорастворимые гранулы;
- жидкие смеси и растворы для дальнейшего растворения в воде;
- таблетированная форма;
- водорастворимый порошок.
Срок годности указывается на каждом изделии в индивидуальном порядке и составляет не менее 3-х лет при хранении в закрытой таре.
Советы по выбору
Чтобы повысить урожайность и улучшить физические свойства почвы, необходимо правильно подбирать удобрения для органического земледелия. Специалисты советуют перед тем как использовать готовую смесь, выяснить, в каких именно микроэлементах нуждается почва.
Потребности обычно обусловлены:
- конкретными почвенными условиями;
- типами выращиваемых растений;
- ранее используемыми удобрениями.
Проводить анализ почвы необходимо каждый год перед посевом растений или высадкой рассады, кустарников, деревьев.
Перечень средств производства
для применения в системе органического земледелия
на основе международных принципов органического сельского хозяйства
Измерение CO2 зачастую недостаточно | Protronix S.r.o.
В настоящее время качество внутреннего воздуха, если вообще, оценивается по температуре, влажности и концентрации диоксида углерода (CO2). Однако, зачастую люди жалуются на качество воздуха даже в тех случаях, если все эти значения показывают оптимальный уровень. Комфорт людей, которые проводят время в помещениях, также снижают запахи, дым, испарения от оборудования интерьеров, и т. д. Большинство из этих веществ, которые мы воспринимаем обонянием (но даже те, которые мы не в состоянии различить), относится к группе летучих органических веществ.
Летучие органические соединения или же VOC (volatile organic compounds) представляют собой химические вещества, которые освобождаются в виде газов из твердых или жидких веществ и легко испаряются в воздух даже при комнатной температуре. Концентрация этих веществ в помощениях может быть даже в 100 раз выше, чем снаружи. Множество изделий, которые мы используем каждый день, или же воздействию которых мы подвергаемся каждый день, выделяют в воздух летучие органические вещества. В то время, как все VOC предрасположены к тому, чтобы быть вредными, существует несколько VOC, которые могут быть особенно опасны, и, несмотря на это, выделяются рядом изделий в наших домах. Этими VOC являются формальдегид, бензол и фенол, определяемые как опасные загрязнители воздуха по классификации Агентства по охране окружающей среды США (EPA), US Green Building Council (USGBC) и Европейского союза (ЕС). Исследования утверждают, что значение выше 500 нг/л (нанограмм на литр) летучих органических веществ может представлять опасность для здоровья жителей домов. Тем не менее, данные тысяч тестированных домов показывают, что среднее значение составляет 1200 нг/л – более двухкратного размера допустимого уровня. Даже умеренно повышенные уровни этих химических веществ в воздухе могут вызывать у людей проблемы со здоровьем, особенно у маленьких детей, пожилых людей, беременных женщин, а также у тех, кто страдает от аллергии и астмы.
Воздух в интерьерах | Типичные вещества | Решения | ||
| Источник загрязнения | Источник выбросов | VOC | Другое | |
|
Присутствие людей и их деятельность
| дыхание | CO2, влажность | управляемое проветривание по реальной необходимости
| |
| дыхание кожи и потоотделение | н-Октаналь, н-Деканаль, α-Пинен | |||
| влажность | ||||
| косметика | лимонен, эвкалипт, силоксаны | |||
| моющие средства | спирты, сложные эфиры, лимонен | |||
| сгорание (оборудование, табачный дым, варка, выпекание, замораживание…) | несгоревшие углеводороды | |||
| СО, СО2, влажность | ||||
| Строительные материалы, мебель, офисное оборудование, …
| краски, клеи, растворители, ковры | формальдегид, алканы, спирты, альдегиды, кетоны, силиконы | постоянная вентиляция на 5–10 % (особенно в недавно отремонтированных интерьерах)
| |
| ПВХ | толуол, ксилол, углеводород | |||
| принтеры, копировальные аппараты, компьютеры | бензол, стирол, фенолы | |||
Отсюда очевидно, что оценка качества воздуха только на основании диоксида углерода в некоторых случаях недостаточна. Вентиляция согласно концентрации СО2 играет важную роль в управлении современными системами вентиляции, но этот газ не является единственным (и не самым вредным) веществом, загрязняющим внутренние пространства. Сам диоксид углерода в небольших концентрациях для человека не опасен, тем не менее, этот газ считается надежным показателем при оценке качества воздуха.
Между концентрацией VOC и СО2 в воздухе помещений часто наблюдается некая корреляция, которая дана в первую очередь присутствием людей. Согласно таблицы видно, что метаболизм человека производит как CO2 самим дыханием, так и VOC. Однако реальные измерения показывают, что повышенная концентрация вредных веществ в воздухе не обязательно означает повышенную концентрацию СО2, но все же воздух содержит множество вредных для здоровья веществ. Таким образом, система вентиляции логически должна реагировать и на эту ситуацию, а не только на концентрацию CO2.
Для измерения качества воздуха не только по содержанию СО2 в последнее время все чаще используют «датчики качества воздуха», что является общим названием датчиков летучих органических веществ. Это широкоспектральные датчики смешанных газов, способные определить количество различных видов газа и их соединений. В характеристике этих датчиков отмечают, что их измерения очень подобны человеческому восприятию запахов. Кроме того, датчики распознают также вещества, не улавливаемые человеческим обонянием.
Датчики VOC в основном работают по принципу косвенно накаливаемой полупроводниковой структуры, использующей МОП технологию (металл-оксид-полупроводник), проявляющую отличную чувствительность к VOC и изменяющую ее проводимость именно в зависимости от концентрации VOC . Полупроводниковые сенсоры характерны чрезвычайно длительным сроком службы. Это связано с принципом функции, когда газ адсорбируется на поверхности сенсора, в следствие изменяется сопротивление полупроводника. Полупроводник требует химическую стабильность, поэтому не используется кремний, а оксиды олова. Для правильного функционирования датчик, помимо полупроводника, также включает в себя нагревательный элемент, который накаляет датчик до рабочей температуры (сто и более °C) для облегчения химических реакций на поверхности полупроводника. Изменение проводимости затем используется для преобразования с помощью электроники в соответствующий сигнал со значением, свидетельствующем о текущем качестве воздуха.
Широкий диапазон обнаруживаемых газов позволяет следить за различными концентрациями газов, что упрощает мониторинг качества воздуха. Обнаруженные концентрации колеблются в диапазоне от единиц ppm до тысяч ppm. Недостатком данной универсальности является возможность реакции даже на нежелательные вещества, поэтому для различных приложений необходимо оснастить датчик селективным фильтром, который захватит нежелательный газ.
Для датчиков VOC характерно оперативное время реакции, относительно высокая чувствительность, но они проявляют более широкую дисперсию измеренных значений. Эт свойства предопределяют данные датчики к использованию в менее загруженных пространствах, таких как дома, общественные помещения, школы, спортивные залы, и т. д.
CO2 | VOC | |
| Школы | x | |
| Общественные помещения | x | |
| Офисы | x | |
| Жилые помещения | x | x |
| Раздевалки | x | |
| Столовые | x | |
| Кухни | x | |
| Спортивные залы, фитнес-центры | x |
Использованием датчиков VOC мы не заменяем сенсоры CO2, а только дополняем их и лучше оцениваем качество воздуха. Вопрос всегда состоит в конечном применении датчиков CO2 или VOC. Все зависит от подходящего размещения датчика. Датчики VOC хорошо использовать в интерьерах, где диоксид углерода не является единственным загрязняющим элементом.
примеров органической химии в повседневной жизни
Органическая химия — это изучение соединений углерода, которое распространяется на понимание химических реакций в живых организмах и продуктах, полученных из них. В повседневной жизни можно встретить множество примеров органической химии.
Они все вокруг нас
Вот примеры работы органической химии:
- Полимеры состоят из длинных цепей и ответвлений молекул. Обычные полимеры, с которыми вы сталкиваетесь каждый день, представляют собой органические молекулы.Примеры включают нейлон, акрил, ПВХ, поликарбонат, целлюлозу и полиэтилен.
- Нефтехимия — это химические вещества, полученные из сырой нефти или нефтепродуктов. При фракционной перегонке сырье разделяется на органические соединения в зависимости от их температуры кипения. Примеры включают бензин, пластмассы, моющие средства, красители, пищевые добавки, природный газ и лекарства.
- Хотя и то, и другое используются для чистки, мыло и моющее средство являются двумя разными примерами органической химии. Мыло образуется в результате реакции омыления, которая реагирует на гидроксид с органической молекулой (например,g., животный жир) для производства глицерина и сырого мыла. Хотя мыло является эмульгатором, моющие средства устраняют масляные, жирные (органические) загрязнения, главным образом потому, что они являются поверхностно-активными веществами, которые снижают поверхностное натяжение воды и увеличивают растворимость органических соединений.
- Независимо от того, исходит ли парфюмерный аромат цветок или лаборатория, молекулы, которые вы нюхаете и которыми наслаждаетесь, являются примером органической химии.
- Косметическая промышленность — прибыльный сектор органической химии. Химики изучают изменения в коже в ответ на метаболические факторы и факторы окружающей среды, разрабатывают продукты для решения проблем кожи и повышения красоты, а также анализируют, как косметика взаимодействует с кожей и другими продуктами.
Продукты с обычными органическими химическими веществами
В этих распространенных продуктах используется органическая химия:
- Шампунь
- Бензин
- Духи
- Лосьон
- Наркотики
- Пищевые продукты и пищевые добавки
- Пластмассы
- Бумага
- Средство от насекомых
- Ткани синтетические (нейлон, полиэстер, вискоза)
- Краска
- Нафталин (нафталин)
- Ферменты
- Жидкость для снятия лака
- Дерево
- Уголь
- Природный газ
- Растворители
- Удобрения
- Витамины
- Красители
- Мыло
- Свечи
- Асфальт
Большинство продуктов, которые вы используете, связаны с органической химией.Ваш компьютер, мебель, дом, автомобиль, еда и тело содержат органические соединения. Каждое живое существо, с которым вы сталкиваетесь, органично. Неорганические предметы, такие как камни, воздух, металлы и вода, также часто содержат органические вещества.
3.11: Органические соединения — Chemistry LibreTexts
Цели обучения
- Идентификация алканов, алкенов, алкинов и ароматических соединений.
- Перечислить некоторые свойства углеводородов.
Простейшие органические соединения состоят всего из двух элементов: углерода и водорода.Эти соединения называются углеводородами . Сами углеводороды делятся на два типа: алифатические углеводороды и ароматические углеводороды.
Алифатические углеводороды — это углеводороды на основе цепочек атомов C. Есть три типа алифатических углеводородов. Алканы представляют собой алифатические углеводороды только с одинарными ковалентными связями. Алкены — это углеводороды, содержащие по крайней мере одну двойную связь C – C, а Алкины — углеводороды, содержащие тройную связь C – C.Иногда мы находим алифатический углеводород с кольцом из атомов углерода; эти углеводороды называют циклоалканов (или циклоалкенов или циклоалкинов ).
Ароматические углеводороды имеют специальное шестиуглеродное кольцо, называемое бензольным кольцом . Электроны в бензольном кольце обладают особыми энергетическими свойствами, которые придают бензолу физические и химические свойства, заметно отличающиеся от алканов. Первоначально термин ароматический использовался для описания этого класса соединений, потому что они были особенно ароматными.Однако в современной химии термин ароматический означает наличие шестичленного кольца, которое придает молекуле различные уникальные свойства.
У простейших алканов атомы C связаны в прямую цепь; они называются нормальными алканами. Они названы в соответствии с количеством атомов углерода в цепи. Самый мелкий алкан — метан:
Рисунок \ (\ PageIndex {1} \) — Трехмерное представление метана. Рисунок \ (\ PageIndex {1} \) Трехмерное представление метана © Thinkstock.Молекула метана трехмерна, с атомами H в четырех углах тетраэдра.
Следующий по величине алкан имеет два атома углерода, ковалентно связанные друг с другом. Чтобы каждый атом C образовал четыре ковалентные связи, каждый атом C должен быть связан с тремя атомами H. Полученная молекула, формула которой C 2 H 6 , представляет собой этан:
Пропан имеет основу из трех атомов C, окруженных атомами H. Вы должны убедиться, что молекулярная формула пропана — C 3 H 8 :
Диаграммы, представляющие алканы, называются структурными формулами , потому что они показывают структуру молекулы.По мере того как молекулы становятся больше, структурные формулы становятся все более сложными. Один из способов обойти это — использовать сжатую структурную формулу , в которой перечислены формулы каждого атома углерода в основной цепи молекулы. Например, конденсированная структурная формула для этана — CH 3 CH 3 , а для пропана — CH 3 CH 2 CH 3 . Таблица \ (\ PageIndex {1} \) — Первые 10 алканов, дает молекулярные формулы, сжатые структурные формулы и названия первых 10 алканов.
| Молекулярная формула | Концентрированная структурная формула | Имя |
|---|---|---|
| CH 4 | СН 4 | метан |
| C 2 H 6 | Канал 3 Канал 3 | этан |
| C 3 H 8 | Канал 3 Канал 2 Канал 3 | пропан |
| C 4 H 10 | Канал 3 Канал 2 Канал 2 Канал 3 | бутан |
| C 5 H 12 | Канал 3 Канал 2 Канал 2 Канал 2 Канал 3 | пентан |
| C 6 H 14 | Канал 3 (Канал 2 ) 4 Канал 3 | гексан |
| C 7 H 16 | Канал 3 (Канал 2 ) 5 Канал 3 | гептан |
| C 8 H 18 | Канал 3 (Канал 2 ) 6 Канал 3 | |
| C 9 H 20 | Канал 3 (Канал 2 ) 7 Канал 3 | нонан |
| C 10 H 22 | Канал 3 (Канал 2 ) 8 Канал 3 | декан |
Поскольку алканы имеют максимальное количество атомов H, возможное в соответствии с правилами ковалентных связей, алканы также называют насыщенными углеводородами .
Алкены имеют двойную связь C – C. Поскольку они содержат меньше максимально возможного количества атомов H, они представляют собой ненасыщенных углеводородов . Наименьший алкен — этен — имеет два атома углерода и известен также под общим названием этилен:
.
Следующий по величине алкен — пропен — имеет три атома углерода с двойной связью между двумя атомами углерода. Он также известен как пропилен:
.
Что вы заметили в названиях алканов и алкенов? Названия алкенов такие же, как и соответствующие им алканы, за исключением того, что окончание — ene , а не — ane .Как мы увидим, использование стержня для обозначения количества атомов C в молекуле и окончания для обозначения типа органического соединения является обычным явлением в органической химии.
С появлением следующего алкена, бутена, мы начинаем видеть главную проблему с органическими молекулами: выбор. С четырьмя атомами C двойная связь C – C может проходить между первым и вторым атомами C или между вторым и третьим атомами C:
(Двойная связь между третьим и четвертым атомами углерода такая же, как между первым и вторым атомами углерода, только перевернутая.) Правила наименования в органической химии требуют, чтобы эти два вещества имели разные названия. Первая молекула называется 1-бутен , а вторая молекула — 2-бутен . Число в начале названия указывает на происхождение двойной связи. Наименьшее возможное число используется для нумерации функции в молекуле; следовательно, называть вторую молекулу 3-бутеном было бы неправильно. Числа — общие части названий органических химических веществ, потому что они указывают, какой атом углерода в цепи содержит отличительную особенность.
Соединения 1-бутен и 2-бутен имеют разные физические и химические свойства, даже несмотря на то, что они имеют одинаковую молекулярную формулу — C 4 H 8 . Различные молекулы с одинаковой молекулярной формулой называются изомерами . Изомеры широко используются в органической химии и вносят свой вклад в ее сложность.
Пример \ (\ PageIndex {1} \):
На основании названий молекул бутена предложите название для этой молекулы.
Решение
С пятью атомами C мы будем использовать стержень pent -, а с двойной связью C – C это алкен, поэтому эта молекула является пентеном.При нумерации атомов C мы используем номер 2 , потому что это нижняя возможная метка. Итак, эта молекула называется 2-пентеном.
Упражнение \ (\ PageIndex {1} \)
На основании названий молекул бутена предложите название для этой молекулы.
- Ответ
3-гексен
Алкины с тройной связью C – C названы аналогично алкенам, за исключением того, что их названия заканчиваются на — yne .Самый мелкий алкин — этин, также известный как ацетилен:
Пропин имеет структуру
С бутином нам нужно начать нумерацию позиции тройной связи, как мы это делали с алкенами:
Ароматические соединения содержат бензольное звено. Сам бензол состоит из шести атомов C в кольце с чередующимися одинарными и двойными связями C – C:
Чередующиеся одинарные и двойные связи C – C придают бензольному кольцу особую стабильность, и оно не реагирует как алкен, как можно было бы предположить.Бензол имеет молекулярную формулу C 6 H 6 ; в более крупных ароматических соединениях другой атом заменяет один или несколько атомов H.
Какими бы фундаментальными ни были углеводороды для органической химии, их свойства и химические реакции довольно банальны. Большинство углеводородов неполярны из-за близкой электроотрицательности атомов C и H. По существу, они очень мало растворяются в H 2 O и других полярных растворителях. Небольшие углеводороды, такие как метан и этан, являются газами при комнатной температуре, тогда как более крупные углеводороды, такие как гексан и октан, являются жидкостями.Даже более крупные углеводороды являются твердыми при комнатной температуре и имеют мягкую воскообразную консистенцию.
Углеводороды довольно инертны, но они участвуют в некоторых классических химических реакциях. Одной из распространенных реакций является замещение атомом галогена путем объединения углеводорода с элементарным галогеном. Иногда для ускорения реакции используют свет, например, между метаном и хлором:
\ [CH_ {4} + Cl_ {2} \ overset {light} {\ rightarrow} CH_ {3} Cl + HCl \ nonumber \]
Галогены также могут реагировать с алкенами и алкинами, но реакция другая.В этих случаях галоген реагирует с двойной или тройной связью C – C и внедряется на каждый атом C, участвующий в кратных связях. Эта реакция называется реакцией присоединения . Один из примеров —
.
Условия реакции обычно мягкие; во многих случаях галоген самопроизвольно реагирует с алкеном или алкином.
Водород также может быть добавлен через кратную связь; эта реакция называется реакцией гидрирования . Однако в этом случае условия реакции могут быть не мягкими; может потребоваться высокое давление газа H 2 .Платиновый или палладиевый катализатор обычно используется для ускорения реакции:
\ [CH_ {2} = CH_ {2} + H_ {2} \ overset {metal \: Catalyst} {\ rightarrow} CH_ {3} CH_ {3} \ nonumber \]
Наиболее распространенной реакцией углеводородов является горение, которое представляет собой комбинацию углеводорода с O 2 с образованием CO 2 и H 2 O. Сжигание углеводородов сопровождается выделением энергии и основной источник производства энергии в нашем обществе (Рисунок \ (\ PageIndex {2} \) — Горение).{8} H_ {18} + 25O_ {2} \ rightarrow 16CO_ {2} + 18H_ {2} O + \ sim 5060 кДж \ nonumber \]
Рисунок \ (\ PageIndex {2} \) Combustion © Thinkstock. Сжигание углеводородов — основной источник энергии в нашем обществе.
Ключевые выводы
- Простейшие органические соединения — это углеводороды, состоящие из углерода и водорода.
- Углеводороды могут быть алифатическими или ароматическими; алифатические углеводороды делятся на алканы, алкены и алкины.
- Сжигание углеводородов — основной источник энергии для нашего общества.
Упражнение \ (\ PageIndex {1} \)
- Определите углеводород . Какие два основных типа углеводородов?
- Какие три различных типа алифатических углеводородов? Как они определены?
- Укажите, является ли каждая молекула алифатическим или ароматическим углеводородом; если алифатический, идентифицируйте молекулу как алкан, алкен или алкин.
- Укажите, является ли каждая молекула алифатическим или ароматическим углеводородом; если алифатический, идентифицируйте молекулу как алкан, алкен или алкин.
- Укажите, является ли каждая молекула алифатическим или ароматическим углеводородом; если алифатический, идентифицируйте молекулу как алкан, алкен или алкин.
- Укажите, является ли каждая молекула алифатическим или ароматическим углеводородом; если алифатический, идентифицируйте молекулу как алкан, алкен или алкин.
- Назовите и нарисуйте структурные формулы для четырех самых маленьких алканов.
- Назовите и нарисуйте структурные формулы для четырех наименьших алкенов.
- Что означает термин « ароматический » относительно органической молекулы?
- Что означает термин нормальный , когда он используется для алканов?
- Объясните, почему название 1-пропен неверно.Какое собственное название этой молекулы?
- Объясните, почему название 3-бутен неправильное. Какое собственное название этой молекулы?
- Назовите и нарисуйте структурную формулу каждого изомера пентена.
- Назовите и нарисуйте структурную формулу каждого изомера гексина.
- Напишите химическое уравнение реакции метана и брома.
- Напишите химическое уравнение реакции этана и хлора.
- Изобразите структуру продукта реакции брома с пропеном.
- Изобразите структуру продукта реакции хлора с 2-бутеном.
- Изобразите структуру продукта реакции водорода с 1-бутеном.
- Изобразите структуру продукта реакции водорода с 1-бутеном.
- Напишите вычисленное химическое уравнение горения гептана.
- Напишите вычисленное химическое уравнение горения нонана.
Ответы
- органическое соединение, состоящее только из углерода и водорода; углеводороды алифатические и ароматические
- алифатический; алкан
- ароматический
- алифатический; алкен
- алифатический; алкан
- алифатический; алкен
- ароматический
- Ароматический означает, что в молекуле есть бензольное кольцо.
- 1 не требуется. Название соединения просто пропен .
- CH 4 + Br 2 → CH 3 Br + HBr
- C 7 H 16 + 11O 2 → 7CO 2 + 8H 2 O
Разработка молекулярной картины взаимодействия органического вещества почвы с минералами путем количественной оценки органо-минерального связывания
Леманн, Дж. И Клебер, М. Спорный характер почвенного органического вещества. Природа
528 , 60–68 (2015).
ADS
CAS
Статья
PubMed
Google Scholar
Schmidt, M. W. I. et al. Стойкость органического вещества почвы как свойство экосистемы. Природа
478 , 49–56 (2011).
ADS
CAS
Статья
PubMed
Google Scholar
Клебер, М., Соллинс, П. и Саттон, Р. Концептуальная модель органо-минеральных взаимодействий в почвах: самосборка органических молекулярных фрагментов в зональные структуры на минеральных поверхностях. Биогеохимия
85 , 9–24 (2007).
Артикул
Google Scholar
Kleber, M. et al. Минерально-органические ассоциации: формирование, свойства и актуальность в почвенных средах. Adv.Агрон.
130 , 1–140 (2015).
Артикул
Google Scholar
Doetterl, S. et al. Хранение углерода в почве контролируется взаимодействием геохимии и климата. Нат. Geosci.
8 , 780–783 (2015).
ADS
CAS
Статья
Google Scholar
Дэвидсон, Э.A. Биогеохимия: почвенный углерод в пивной банке. Нат. Geosci.
8 , 748–749 (2015).
ADS
CAS
Статья
Google Scholar
Lutzow, M. V. et al. Стабилизация органического вещества в почвах умеренного пояса: механизмы и их значение в различных почвенных условиях — обзор. евро. J. Почвоведение.
57 , 426–445 (2006).
Артикул
Google Scholar
Путешествие, Дж. С., Андерсон, Р. М. и Эссингтон, М. Э. Адсорбция 2-кетоглюконата гетитом. Почвоведение. Soc. Являюсь. J.
74 , 1119–1128 (2010).
ADS
CAS
Статья
Google Scholar
Баррос Н., Сальгадо Дж. И Фейхоо С. Калориметрия и почва. Thermochim. Acta
458 , 11–17 (2007).
CAS
Статья
Google Scholar
Наир, Н. Н., Шрейнер, Э. и Маркс, Д. Глицин на границе раздела пирит-вода: роль поверхностных дефектов. J. Am. Chem. Soc.
128 , 13815–13826 (2006).
CAS
Статья
PubMed
Google Scholar
Ридель Т., Бистер Х. и Дитмар Т. Молекулярное фракционирование растворенного органического вещества солями металлов. Environ. Sci. Technol.
46 , 4419–4426 (2012).
ADS
CAS
Статья
PubMed
Google Scholar
Бейли, В. Л., Смит, А. П., Тфейли, М. и Фанслер, С. Дж. Различия в химическом составе растворимого органического углерода в поровых водах, отобранных из областей с разным размером пор. Soil Biol. Биохим.
107 , 133–143 (2017).
CAS
Статья
Google Scholar
Sulchek, T.A. et al. Спектроскопия динамических сил параллельных индивидуальных связей Mucin1-антитело. Proc. Natl Acad. Sci. США
102 , 16638–16643 (2005).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Фриддл Р. В., Ной А. и Де Йорео Дж. Дж. Интерпретация широко распространенных спектров нелинейных сил межмолекулярных связей. Proc. Natl Acad. Sci. США
109 , 13573–13578 (2012).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Буллерян Дж. Т., Штурм С. и Крой К. Теория спектроскопии быстрых сил. Нат. Коммуна . 5 , 4463 (2014).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Tao, J. et al. Энергетическая основа молекулярной организации кости. Proc. Natl Acad. Sci. США
112 , 326–331 (2015).
ADS
CAS
Статья
PubMed
Google Scholar
Hamm, L. M. et al. Согласование несопоставимых взглядов на зародышеобразование, направленное по шаблону, путем измерения кинетики зародышеобразования кальцита и энергий связи. Proc. Natl Acad. Sci. США
111 , 1304–1309 (2014).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Friddle, R. W. et al. Одномолекулярное определение специфической для лица адсорбции С-конца амелогенина на гидроксиапатите. Angew. Chem. Int. Эд. Англ.
50 , 7541–7545 (2011).
CAS
Статья
PubMed
PubMed Central
Google Scholar
Кале, М., Клебер, М. и Ян, Р. Удержание растворенного органического вещества фракциями филлосиликатов и почвенной глины в зависимости от минеральных свойств. Org. Геохим.
35 , 269–276 (2004).
CAS
Статья
Google Scholar
Клебер М., Микутта Р., Торн М. С. и Ян Р. Плохо кристаллические минеральные фазы защищают органическое вещество в кислых подпочвенных горизонтах. евро. J. Почвоведение.
56 , 717–725 (2005).
CAS
Google Scholar
Лал Р. Энциклопедия почвоведения 3-е изд. (CRC Press, 2016).
Zhao, H. et al. Зондирование потенциалов поверхностного заряда глинистых базальных плоскостей и кромок путем прямых измерений силы. Ленгмюр
24 , 12899–12910 (2008).
CAS
Статья
PubMed
Google Scholar
Хиемстра, Т. и Ван Римсдейк, В. Х. Подход к адсорбции ионов со структурой поверхности: модель распределения заряда (CD). J. Colloid Interface Sci.
179 , 488–508 (1996).
ADS
CAS
Статья
Google Scholar
Yeasmin, S. et al. Влияние минеральных характеристик на удерживание низкомолекулярных органических соединений: периодическое исследование сорбции-десорбции и ATR-FTIR. J. Colloid Interface Sci.
432 , 246–257 (2014).
ADS
CAS
Статья
PubMed
Google Scholar
Эванко, К. Р., Джомбак Д. А. Влияние структурных особенностей на сорбцию органических кислот, аналогичных НОМ, на гетите. Environ. Sci. Technol.
32 , 2846–2855 (1998).
ADS
CAS
Статья
Google Scholar
Бойли, Дж. Ф. и Фелми, А. Р. О протонировании оксо- и гидроксогрупп поверхности гетита (α-FeOOH): исследование FTIR-спектроскопии валентных колебаний поверхности O – H. Геохим. Космохим. Acta
72 , 3338–3357 (2008).
ADS
CAS
Статья
Google Scholar
Tournassat, C., Neaman, A., Villiéras, F., Bosbach, D. & Charlet, L. Наноморфология частиц монтмориллонита: оценка плотности участка сорбции края глины с помощью адсорбции газа при низком давлении и АСМ наблюдения. Am. Минеральная.
88 , 1989–1995 (2003).
ADS
CAS
Статья
Google Scholar
Li, H.Z. et al. Анализ и последствия краевой структуры диоктаэдрических филлосиликатов. Publ. Astron. Soc. Pac.
127 , 1–15 (2015).
ADS
CAS
Статья
Google Scholar
Лю, X., Лу, X., Ван, Р., Чжоу, Х. и Сюй, С. Поверхностные комплексы ацетата на краевых поверхностях филлосиликата типа 2: 1: выводы из расчета теории функционала плотности . Геохим. Космохим. Acta
72 , 5896–5907 (2008).
ADS
CAS
Статья
Google Scholar
Норен К. и Перссон П. Адсорбция монокарбоксилатов на границе вода / гетит: важность водородных связей. Геохим. Космохим. Acta
71 , 5717–5730 (2007).
ADS
Статья
Google Scholar
Перссон П. и Акс, К. Адсорбция оксалата и малоната на границе раздела вода-гетит: определение молекулярной поверхности по данным ИК-спектроскопии. Геохим. Космохим. Acta
69 , 541–552 (2005).
ADS
CAS
Статья
Google Scholar
Йонссон, К. М., Перссон, П. и Сьёберг, С. Адсорбция глифосата на гетите (α-FeOOH): моделирование поверхностного комплексообразования, объединяющее спектроскопические и адсорбционные данные. Environ. Sci. Technol.
42 , 2464–2469 (2008).
ADS
CAS
Статья
PubMed
Google Scholar
Chassé, A. W. et al. Данные спектроскопии химических сил подтверждают послойную модель связывания органических веществ с минеральными поверхностями (окси) гидроксида железа. Environ. Sci. Technol.
49 , 9733–9741 (2015).
ADS
Статья
PubMed
Google Scholar
Обри, К., Гутьеррес, Л. и Кроу, Дж. П. Покрытие зондов АСМ водным гуминовым и негуминовым НОМ для изучения их адгезионных свойств. Water Res.
47 , 3109–3119 (2013).
CAS
Статья
PubMed
Google Scholar
Мерфи, Э.М., Захара, Дж. М., Смит, С. К., Филлипс, Дж. Л. и Виетсма, Т. В. Взаимодействие гидрофобных органических соединений с гуминовыми веществами, связанными с минералами. Environ. Sci. Technol.
28 , 1291–1299 (2002).
ADS
Статья
Google Scholar
Sposito, G. Химия почв 2-е изд. (Oxford University Press, 2008).
Майзик, А.& Tombácz, E. Взаимодействие между гуминовой кислотой и монтмориллонитом в присутствии ионов кальция I. Равновесия межфазной и водной фаз: адсорбция и комплексообразование. Org. Геохим.
38 , 1319–1329 (2007).
CAS
Статья
Google Scholar
Cao, Y. et al. Преимущественная адсорбция внеклеточных полимерных веществ бактерий на глинистые минералы и оксид железа. Colloids Surf. B Биоинтерфейсы
83 , 122–127 (2011).
CAS
Статья
PubMed
Google Scholar
Chen, C. & Sparks, D. L. Многоэлементная сканирующая просвечивающая рентгеновская микроскопия — ближняя рентгеновская абсорбционная спектроскопия тонкой структуры органо-минеральных ассоциаций в почвах из восстановленных сред. Environ. Chem.
12 , 64–73 (2015).
Артикул
Google Scholar
Везенов, Д. В., Ной, А., Розняй, Л. Ф. и Либер, К. М. Силовое титрование и визуализация функциональных групп в водных растворах, чувствительных к состоянию ионизации, с помощью химической силовой микроскопии. J. Am. Chem. Soc . 119 , 2006–2015 (1997).
Артикул
Google Scholar
Гранбуа, М., Бейер, М., Риф, М., Клаузен-Шауман, Х. и Гауб, Х. Э. Насколько прочна ковалентная связь? Наука
283 , 1727–1730 (1999).
ADS
CAS
Статья
PubMed
Google Scholar
Кубики, Дж. Д., Ито, М. Дж. И Шрётер, Л. М. Механизмы связывания салициловой кислоты, адсорбированной на иллитовой глине: ATR — FTIR и исследование молекулярных орбиталей. Environ. Sci. Technol.
31 , 1151–1156 (1997).
ADS
CAS
Статья
Google Scholar
Boily, J.-F., Persson, P. & Sjöberg, S. Поверхностное комплексообразование бензенкарбоксилата на границе гетита (α-FeOOH) / воды: II. Связь ИК-спектроскопических наблюдений с механистическими моделями поверхностного комплексообразования для фталата, тримеллитата и пиромеллитата. Геохим. Космохим. Acta
64 , 3453–3470 (2000).
ADS
CAS
Статья
Google Scholar
Гу Б., Шмитт Дж., Чен З., Лян Л. и Маккарти Дж. Ф. Адсорбция и десорбция природного органического вещества на оксиде железа: механизмы и модели. Environ. Sci. Technol.
28 , 38–46 (1994).
ADS
CAS
Статья
PubMed
Google Scholar
Канг, С., Амарасиривардена, Д. и Син, Б. Влияние дегидратации на координацию дикарбоновой кислоты на границе гетита / воды. Colloids Surf. Physicochem. Англ. Asp.
318 , 275–284 (2008).
CAS
Статья
Google Scholar
Chassé, A. W. & Ohno, T. Молекулы органических веществ с более высокой молекулярной массой конкурируют с ортофосфатом за адсорбцию на (окси) гидроксиде железа. Environ. Sci. Technol.
50 , 7461–7469 (2016).
ADS
Статья
PubMed
Google Scholar
Шенг, X., Юнг, Т., Вессон, Дж. А. и Уорд, М. Д. Адгезия на поверхности кристаллов оксалата кальция и влияние компонентов мочи. Proc. Natl Acad. Sci. США
102 , 267–272 (2005).
ADS
CAS
Статья
PubMed
Google Scholar
Бектел, Х. А., Мюллер, Э. А., Олмон, Р. Л., Мартин, М. К. и Рашке, М. Б. Сверхширокополосная инфракрасная наноспектроскопическая визуализация. Proc. Natl Acad. Sci. США
111 , 7191–7196 (2014).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Штёкле, Р. М., Сух, Ю. Д., Декерт, В. и Зеноби, Р. Наноразмерный химический анализ с помощью спектроскопии комбинационного рассеяния света с зондом. Chem. Phys. Lett.
318 , 131–136 (2000).
ADS
Статья
Google Scholar
Майер, Л. М. Степень покрытия минеральных поверхностей органическим веществом в морских отложениях. Геохим. Космохим. Acta
63 , 207–215 (1999).
ADS
CAS
Статья
Google Scholar
Vogel, C. et al. Субмикронные структуры обеспечивают предпочтительные места для связывания углерода и азота в почвах. Нат. Commun.
5 , 2947 (2014).
Артикул
PubMed
PubMed Central
Google Scholar
Сульман, Б. Н., Филлипс, Р. П., Оиши, А. К., Шевлякова, Э. и Пакала, С. В. Оборот, вызванный микробами, компенсирует опосредованное минералами накопление углерода в почве при повышенном уровне CO2. Нат. Клим. Чанг.
4 , 1099–1102 (2014).
ADS
CAS
Статья
Google Scholar
Wang, G., Mayes, M. A., Gu, L. & Schadt, C. W. Представление динамики спящих и активных микробов для моделирования экосистем. PLoS ONE
9 , e89252 (2014).
ADS
Статья
PubMed
PubMed Central
Google Scholar
Тан, Дж. И Райли, У. Дж. Более слабая обратная связь между углеродом почвы и климатом в результате микробных и абиотических взаимодействий. Нат. Клим.Чанг.
5 , 56–60 (2015).
ADS
CAS
Статья
Google Scholar
Чжу, К., Райли, У. Дж., Танг, Дж. И Ковен, С. Д. Множественная конкуренция питательных веществ в почве между растениями, микробами и минеральными поверхностями: разработка моделей, параметризация и примеры применения в нескольких тропических лесах. Biogeosci. Обсудить . 13 , 341–363 (2015).
ADS
Статья
Google Scholar
Burnham, N.A. et al. Сравнение методов калибровки кантилеверов для атомно-силовой микроскопии. Нанотехнологии
14 , 1 (2003).
ADS
CAS
Статья
Google Scholar
II — Образование, модификация и сохранение органических соединений в Солнечной системе, 2 Межзвездная химия | Изучение органических сред Солнечной системы
7.E.L. Гибб, округ Колумбия Whittet, A.C.A. Бугерт, А.Г.Г.М. Тиленс, «Межзвездный лед: наследие инфракрасной космической обсерватории», серия дополнений к астрофизическому журналу , серия 151: 35G, 2004.
8. T.J. Миллар, Э. Хербст и С. Чарнли, «Образование кислородсодержащих органических молекул в компактном хребте Ориона», Astrophysical Journal 369: 147, 1991.
9. A.G.G.M. Тиленс и С. Чарнли, «Околозвездный и межзвездный синтез органических молекул», Origins of Life and Evolution of the Biosphere 27: 23-51, 1997.
10. R.J.A. Грим, Ф. Баас, Т. Гебалле, Дж. М. Гринберг и В. Шутте, «Обнаружение твердого метанола в направлении W33A», Astronomy и Astrophysics 243: 473, 1997.
11. В.К. Agarwal, W. Schutte, J.M. Greenberg, J.P. Ferris, R. Briggs, S. Conner, C.P.E.M. Ван де Булт и Ф. Басс, «Фотохимические реакции в межзвездных зернах, фотолиз CO, NH 3 и H 2 O», Origins of Life 16: 21-40, 1985.
12.Р. Бриггс, Г. Эртем, Дж. П. Феррис, Дж. М. Гринберг, П. Дж. Маккейн, C.X. Мендоса-Гомес и В. Шутте, «Комета Галлея как совокупность межзвездной пыли и дальнейшие доказательства фотохимического образования органических веществ в межзвездной среде», Origins of Life и Evolution of the Biosphere 22: 287-307 , 1992.
13. М.П. Бернштейн, Дж.П. Дворкин, С.А.Сэндфорд, Г.В. Купер и Л. Дж. Алламандола, «Рацемические аминокислоты из ультрафиолетового фотолиза аналогов межзвездного льда», Nature 416: 401-403, 2002.
14. G.M. Муньос Каро, U.J. Meierhenrich, W.A Schutte, B. Barbier, A. Arcones Segovia, H. Rosenbauer, W.H.P. Тиманн, А. Брак и Дж. М. Гринберг, «Аминокислоты от ультрафиолетового облучения аналогов межзвездного льда», Nature 416: 403-406, 2002.
15. Г.М. Муньос Каро, U.J. Meierhenrich, W.A Schutte, B. Barbier, A. Arcones Segovia, H. Rosenbauer, W.H.P. Тиманн, А. Брак и Дж. М. Гринберг, «Аминокислоты от ультрафиолетового облучения аналогов межзвездного льда», Nature 416: 403-406, 2002.
16. М.П. Бернштейн, Дж.П. Дворкин, С.А.Сэндфорд, Г.В. Купер и Л. Дж. Алламандола, «Рацемические аминокислоты из ультрафиолетового фотолиза аналогов межзвездного льда», Nature 416: 401-403, 2002.
17. Для обзора см. Y.J. Pendleton and L.J. Allamandola, «Органический тугоплавкий материал в диффузной межзвездной среде: спектроскопические ограничения в среднем инфракрасном диапазоне», Astrophysical Journal Supplement Series 138: 75-98, 2002.
18.В. Мэннингс, А.П. Босс и С.С. Рассел, ред., Protostars and Planets IV, University of Arizona Press, Tucson, Ariz., 2002.
19. Й. Айкава и Э. Хербст, «Химические модели околозвездных дисков», стр. 425-434 в книге «Астрохимия : от молекулярных облаков к ». Симпозиум 197, Тихоокеанское астрономическое общество, Сан-Франциско, Калифорния, 2000.
20. Недавний обзор см., Например, в P.М. Хоппе и Э. Зиннер, «Пресолнечные частицы пыли из метеоритов и их звездных источников», журнал Journal of Geophysical Research, 105: 10371-10386, 2000.
21. D.E. Браунли, «Космическая пыль: сбор и исследование», Annual Review of Earth and Planetary Science 13: 147-173, 1985.
22. Л.П. Келлер, К.Л. Томас и Д.С. Маккей, «Частица межпланетной пыли со связями с хондритами КИ», Geochimica et Cosmochimica Acta 56: 1409-1412, 1992.
23. K.L. Thomas, L.P. Keller, G.E. Бланфорд и Д. С. Маккей, «Количественный анализ углерода в безводных и гидратированных частицах межпланетной пыли», стр. 165-172 в статье «Анализ межпланетной пыли » (М. Е. Золенский, Т. Л. Уилсон, Ф. Дж. М. Ритмейер и Г. Дж. Флинн, ред.), Материалы конференции AIP 310, Американский институт физики, Вудбери, штат Нью-Йорк, 1994.
24. G.J. Флинн, Л.П. Келлер, К. Якобсен, С. Вирик и М.А. Миллер, «Органический углерод в частицах межпланетной пыли», стр.191-194 в A Новая эра в биоастрономии , ASP Conference Series, Vol. 213, Astronomical Society of the Pacific Press, Сан-Франциско, Калифорния, 2000.
25. Л.П. Келлер, С. Мессенджер, Г.Дж. Флинн, С. Клеметт, С. Вирик и К. Якобсен, «Природа молекулярного облачного материала в межпланетной пыли», Geochimica et Cosmochimica Acta 68 (11): 2577-2589, 2004.
26. G.J. Флинн, Л.П. Келлер, М. Фезер, С. Вирик и К. Якобсен, «Происхождение органического вещества в Солнечной системе: свидетельства межпланетных пылевых частиц», Geochimica et Cosmochimica Acta 67 (24): 4791- 4806, 2003.
27. Дж. Алеон, Ф. Роберт, М. Чауссидон и Б. Марти, «Изотопный состав азота высокомолекулярного органического вещества в частицах межпланетной пыли», Geochimica et Cosmochimica Acta 67: 3773-3783, 2003.
28. Л.П. Келлер, С. Мессенджер, Г.Дж. Флинн, С. Клеметт, С. Вирик и К. Якобсен, «Природа молекулярного облачного материала в межпланетной пыли», Geochimica et Cosmochimica Acta 68 (11): 2577-2589, 2004.
29. Л.П. Келлер, С.Посланник, Г.Дж. Флинн, С. Клеметт, С. Вирик и К. Якобсен, «Природа молекулярного облачного материала в межпланетной пыли», Geochimica et Cosmochimica Acta 68 (11): 2577-2589, 2004.
30. Дж. Алеон, К. Энгранд, Ф. Роберт и М. Чауссидон, «Ключ к разгадке происхождения частиц межпланетной пыли на основе изотопного исследования их водородсодержащих фаз», Geochimica et Cosmochimica Acta 65: 4399- 4412, 2001.
31. Дж. Алеон, Ф. Роберт, М. Чауссидон и Б.Марти, «Изотопный состав азота высокомолекулярного органического вещества в частицах межпланетной пыли», Geochimica et Cosmochimica Acta 67: 3773-3783, 2003.
32. G.J. Флинн, Л.П. Келлер, М. Фезер, С. Вирик и К. Якобсен, «Происхождение органического вещества в Солнечной системе: свидетельства межпланетных пылевых частиц», с. 275 в Биоастрономия 2002: жизнь среди звезд , симпозиум МАС 213 (Р. Норрис и Ф. Стутман, ред.), Тихоокеанское астрономическое общество, Сан-Франциско, Калифорния., 2003.
33. Л.П. Келлер, С. Мессенджер, Г.Дж. Флинн, С. Клеметт, С. Вирик и К. Якобсен, «Природа молекулярного облачного материала в межпланетной пыли», Geochimica et Cosmochimica Acta 68 (11): 2577-2589, 2004.
34. G.J. Флинн, Л.П. Келлер, М. Фезер, С. Вирик и К. Якобсен, «Происхождение органического вещества в Солнечной системе: свидетельства межпланетных пылевых частиц», Geochimica et Cosmochimica Acta 67 (24): 4791- 4806, 2003.
35.Дж. Алеон, К. Энгранд, Ф. Роберт и М. Чауссидон, «Ключ к разгадке происхождения частиц межпланетной пыли на основе изотопного исследования их водородсодержащих фаз», Geochimica et Cosmochimica Acta 65: 4399-4412, 2001
Органическое вещество — обзор
6.04.2.5 Растворенное органическое вещество
РОВ не изучалось так интенсивно, как другие аспекты биологического насоса, возможно, потому, что РОВ не тонет. Однако DOM действительно играет активную роль в биологическом насосе по крайней мере тремя способами.Большая часть РОВ пригодна для биологического использования и может напрямую обеспечивать P и N для первичной продукции (Clark et al. , 1998; Zehr and Ward, 2002). РОВ может собираться в коллоидный и мелкодисперсный материал, который может тонуть, а также поглощать другой материал с образованием морского снега (Alldredge et al. , 1993; Kepkay, 1994; Chin et al. , 1998). РОВ также является крупным резервуаром углерода в океане, содержащим по крайней мере на порядок больше углерода, чем другие резервуары морского органического углерода (Kepkay, 1994).
Хотя происхождение РОВ не было полностью детализировано, считается, что фитопланктон служит основным источником РОВ в океан. Активно растущий фитопланктон выделяет РОВ (Biddanda, Benner, 1997; Soendergaard et al. , 2000; Teira et al. , 2001), а полисахаридный состав экссудатов фитопланктона напоминает высокомолекулярную фракцию РОВ ( Aluwihare and Repeta, 1999). РОВ фитопланктона также выделяется зоопланктоном во время выпаса скота (Strom et al., 1997). Органические вещества, такие как слизь, на поверхности клеток фитопланктона также могут гидролизоваться бактериями и выделяться в виде РОВ (Smith et al. , 1995).
Точный состав морского РОВ неизвестен. До сих пор было показано, что он содержит нейтральные сахара (такие как глюкоза, фукоза, манноза и арабиноза), полисахариды, аминокислоты, амиды (такие как хитин), сложные эфиры фосфора и фосфонаты (Benner et al. , 1992; Маккарти и др. , 1997; Кларк и др., 1998; Amon et al. , 2001). Считается, что микробная деградация играет роль в определении состава РОВ в океане (Amon et al. , 2001).
Одна интересная особенность DOM, по крайней мере, в отношении углеродного цикла, — это его обогащение углеродом по отношению к коэффициенту Редфилда. Соотношение C: N: P высокомолекулярного РОВ составляет примерно 350: 20: 1 (Kolowith et al. , 2001). C-обогащение также наблюдается для объемного РОВ (Kaehler and Koeve, 2001). Частично это обогащение C может быть связано с усиленной реминерализацией P и N из РОВ (Clark et al., 1998; Kolowith et al. , 2001), о чем свидетельствует увеличение отношения C / P РОВ с глубиной (Kolowith et al. , 2001). DOM также можно просто производить с высокими отношениями C / N и C / P. Например, TEP, который образуется из предшественников DOM (Alldredge et al. , 1993; Chin et al. , 1998), имеет высокие отношения C / N (Engel and Passow, 2001; Mari et al. , 2001). ). Полисахариды, которые в конечном итоге образуют TEP, выделяются фитопланктоном и могут представлять собой избыток фотосинтата, который представляет собой углеводы, и липиды, образующиеся в отсутствие питательных веществ, таких как N, которые необходимы для синтеза соединений, таких как белки (Morris, 1981).
Важность пула РОВ, обогащенного углеродом, в углеродном цикле зависит от размера и времени оборачиваемости коллектора. Недавняя оценка растворенного органического углерода (DOC) в океане составляет 200 пг C (Kepkay, 1994), что более сопоставимо с 750 пг углерода, присутствующим в атмосфере, чем с глубоководным резервуаром 36 000 пг C в DIC. (Сандквист, 1993). Средний возраст морского РОВ составляет ~ 6000 лет (Williams and Druffel, 1987), хотя время оборота различных фракций пула РОВ варьируется от десятилетий до почти 20 000 лет (Loh et al., 2004). Основная масса (~ 70%) РОВ имеет низкий молекулярный вес (Benner et al. , 1992) и относительно устойчив к микробной деградации (Bauer et al. , 1992; Amon and Benner, 1994). Высокомолекулярные соединения, которые быстро превращаются в бактериальное разложение (Amon and Benner, 1994), составляют оставшиеся 30% пула РОВ.
Примеры органических соединений в повседневной жизни
Повседневная жизнь полна примеров органических соединений.
В повседневной жизни существует множество примеров органических соединений.Органические соединения содержат углерод и водород, часто с кислородом, азотом, серой, фосфором и другими элементами. Вот список знакомых продуктов и некоторых органических соединений, которые они содержат:
Продукты, содержащие органические соединения
Большинство продуктов содержат органические соединения. Исключения (неорганические соединения) включают воду, воздух, стекло, камни, соли и металлы.
- Асфальт (нефтяные углеводороды)
- Свечи (воск, жир)
- Уголь (смешанные углеводороды)
- Моющее средство (алкилбензолсульфонаты)
- Лекарства (эл.г., ацетаминофен, кофеин, пенициллин)
- Красители (соединения растений или нефтехимии)
- Ферменты (папаин, каталаза, амилаза)
- Ткани [хлопок и лен (целлюлоза), шерсть (кератин) , шелк (серицин и фиброин), нейлон, полиэстер, вискоза)
- Пищевые и многие пищевые добавки (мясо, овощи, зерно)
- Бензин (смесь углеводородов)
- Кожа (кератин)
- Лосьон (масла, спирт, ароматизаторы, глицерин)
- Нафталин (нафталин)
- Лак для ногтей (нитроцеллюлоза, бутилацетат)
- Жидкость для снятия лака (ацетон, толуол)
- Природный газ ( в основном метан)
- Краска (неорганические пигменты в смолах и органических растворителях)
- Бумага (целлюлоза)
- Духи (спирт, смешанный гидро углерода)
- Пластмассы (углеводороды)
- Веревка (целлюлоза, нейлон)
- Шампунь (лауретсульфат натрия, лаурилсульфат натрия, кокамидопропилбетаин, полиэтиленгликоль)
- Мыло (соль жирной кислоты)
- Растворители (этанол, толуол, бутанол, ксилол)
- Витамины
- Дерево (целлюлоза)
Другие примеры органических соединений
- Спирт
- Картон (целлюлоза)
- Ковровое покрытие , акрил)
- Перья (кератин)
- Люди (многочисленные соединения)
- Домашние животные (многочисленные соединения)
- Растения (многочисленные соединения)
- Кожа (кератин)
- Сахар (сахароза, фруктоза)
- Растительное масло (смешанное липидов)
Четыре основных класса органических соединений — это углеводы (сахара и крахмалы), липиды (жирные кислоты, жиры и масла. ls), белки (аминокислоты, пептиды, белки, ферменты) и нуклеиновые кислоты (РНК и ДНК).Многие органические соединения представляют собой полимеры, что означает, что они образованы путем соединения множества субъединиц вместе.
Как распознать органические соединения
Большинство соединений, содержащих как углерод, так и водород, являются органическими соединениями. Почти все соединения, полученные из растений или животных, являются органическими. Однако живые организмы также содержат некоторые неорганические молекулы (в основном воду и компоненты скелета). Вероятно, самый простой способ определить, является ли что-то органическим, — это исключить его неорганическое происхождение.Это произошло от растения или животного? Скорее всего, органический. Это было сделано из нефти? Наверное, органический. Он состоит только из металлов, солей или минералов? Наверное, неорганический.
Органический или химический — Advanced BioTech
Если мы заглянем в словарь, мы обнаружим, что слово химический означает: произведено или используется в химии; изготовлены с использованием химикатов или управляются ими; или любое вещество, используемое или полученное в результате химического процесса. Химический элемент — это любое вещество, которое нельзя разделить на разные вещества, кроме как с помощью радиоактивного распада.Вся материя состоит из таких веществ. Материя не может быть создана или разрушена, но может изменить свою форму, например, в химическом процессе.
Химический процесс может происходить внутри живых организмов или из неживых источников. В начале 1700-х годов считалось, что химический синтез может происходить только в живых организмах, и органические соединения определялись как происходящие из живых организмов, тогда как неорганические соединения происходят из неживых источников. Это убеждение было названо «витализмом», и некоторые до сих пор его придерживаются.Однако сегодня мы знаем, что химический синтез может происходить вне живых организмов.
Органические соединения — это соединения, состоящие из химического элемента углерода. Неорганические соединения не содержат углерода. К неорганическим химическим веществам относятся сера, кислород, азот, серебро, медь и т. Д. Живые существа состоят в основном из органических соединений, но в органических соединениях также содержится много водорода и кислорода с небольшими количествами других неорганических элементов — серы, меди, магния и т. Д. живые существа умирают, эти органические соединения могут изменить форму, превратившись в компост, а еще со временем — в нефть.
Все, что происходит от живых существ, является органическим, но все, что содержит углерод, также является органическим. Пища, которую мы едим, древесина, из которой мы строим дома, одежда, которую мы носим (будь то натуральный хлопок или полиэстер), бензин, пропан, резина, пластмассы, лекарства, пестициды, гербициды — все это сделано из органических соединений. Человек использовал органические соединения на протяжении тысячелетий, начиная с древних египтян и финикийцев, которые использовали химические вещества, полученные от живых организмов, для окрашивания тканей. Производство вина было известно в библейские времена и требовало воздействия живого организма, бактерий, которые использовались в качестве химического вещества, производимого виноградом, сахара, для синтеза алкоголя.Чтобы заставить вино пить, требуется физическое вмешательство человека, чтобы соединить виноград и нужные бактерии.
Синтетическое вещество — это нечто, полученное путем химического синтеза, а не природного происхождения. Неорганический кислород необходим человеку, но когда кислород вступает в химические реакции в нашем организме или в нашем растении, образуются новые формы кислорода, которые являются токсичными. Наши тела обрабатывают азот, чтобы синтезировать мочевину, и кислород, чтобы синтезировать перекись водорода. Это естественные процессы, но оба соединения могут синтезироваться в химических реакциях вне нашего тела.
В начале 1800-х годов Фридрих Велер обнаружил, что мочевину можно получить простым испарением водного раствора цианата аммония. Можно утверждать, что в этот процесс вмешался жизненно важный источник, с физической точки зрения «созданный руками человека». Тем не менее, как бы ни синтезировались мочевина и перекись водорода, они все равно остаются мочевиной и перекисью водорода. Оба имеют полезные цели при химическом синтезе (созданном человеком). Мочевина используется как удобрение, а перекись водорода как антисептик.
Мы не можем утверждать, что «натуральный» витамин С, полученный из цитрусовых, полезнее, чем идентичный «синтетический» витамин С. Алкоголь в вине может иметь приятный вкус, но имеет серьезные последствия для здоровья. Лекарства полезны, если используются по назначению, но вредны, если используются ненадлежащим образом.
Итак, органические соединения, независимо от того, синтезированы ли они «природными» или «искусственными», могут иметь хорошие или плохие эффекты. Наша задача — узнать, как мы используем любые химические вещества, природные или созданные человеком, для защиты окружающей среды и самих себя, но при этом обеспечиваем жизнь в изобилии.Поэтому, когда вы слышите слова, синтетические, органические, искусственные, натуральные и / или химические, пожалуйста, найдите время, чтобы определить, что на самом деле говорится.
ХИМИЧЕСКИЕ УДОБРЕНИЯ: ДЫХАНИЕ ЖИЗНИ
Звук надуманный? Нисколько! Несмотря на все жалобы активистов-экологов на химические удобрения, они могут быть удивлены (и более чем немного просветлены), узнав, какое отношение эти так называемые проклятия человечества имеют к их продолжительному и здоровому существованию.Подумайте: на каждую тонну CO2, которую вдыхает растение кукурузы, три четверти тонны кислорода выбрасываются обратно в атмосферу. В 1992 году урожай кукурузы размером 9,2 миллиарда бушелей выдохнул обратно в воздух 593 миллиона метрических тонн кислорода, чего достаточно, чтобы поддерживать каждого мужчину, женщину и ребенка на этом растении в течение года! Вдумайтесь… Что за урожай, какое кислородное пополнение мы имели бы без химических удобрений? Вместо того, чтобы осуждать химические удобрения, защитникам окружающей среды, возможно, следует посмотреть в зеркало, кто действительно виноват.Ведь они, в отличие от растений, выращиваемых химическими удобрениями, выдыхают СО2, а не кислород. Используя их логику, мы должны уничтожить людей и спасти планету. В этом выпуске Fluid Journal вы также узнаете, насколько эффективно кукуруза и другие культуры удаляют CO2 из воздуха, чтобы уравновесить количество, вносимое ископаемым топливом и природой. Вам будет показано, как увеличение количества химических удобрений сверх текущих уровней может повысить средние урожаи, что поможет улавливать еще больше CO2, который способствует глобальному потеплению.

