Содержание
Органические вещества — урок. Химия, 8–9 класс.
Все известные вещества можно разделить на две группы: органические и неорганические (минеральные).
Органические вещества — соединения углерода.
Исключения: оксиды углерода, угольная кислота и её соли (относятся к неорганическим).
Все органические соединения обязательно содержат углерод и водород. В их состав могут входить атомы кислорода, азота, галогенов, серы.
Органические вещества составляют основную часть всех живых организмов. Белки, жиры, углеводы являются органическими соединениями.
Природный газ, нефть, каменный уголь, торф также состоят из органических веществ.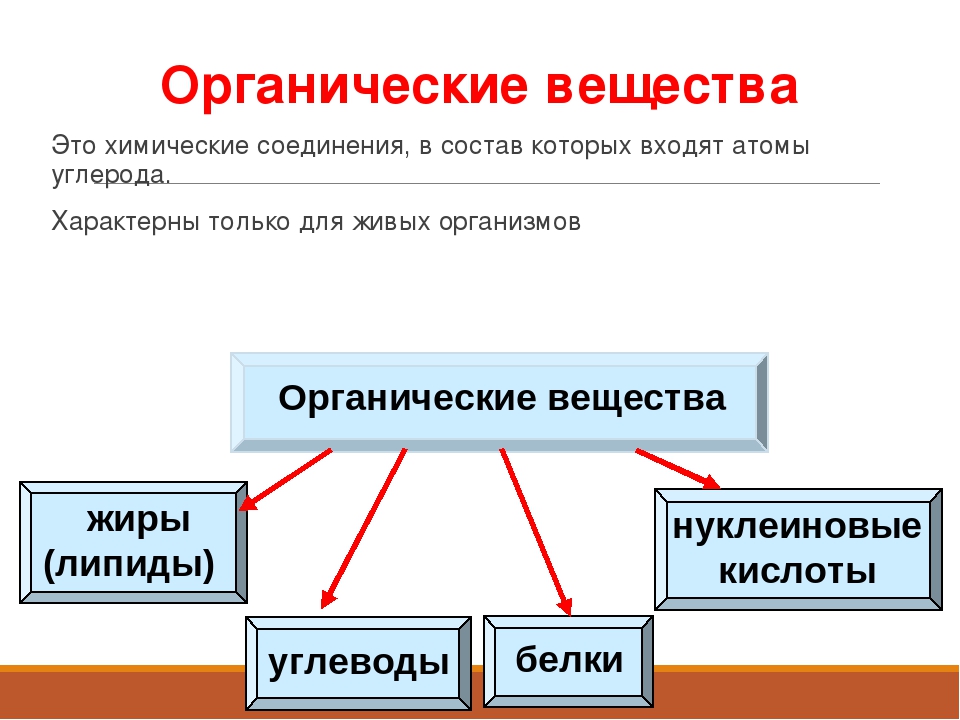
Примеры природных органических веществ, которые использует человек: сахар, крахмал, уксусная кислота, каучук, жиры, древесина.
Мы используем огромное количество синтетических органических веществ, которые в природе никогда не существовали (полиэтилен, капрон, лавсан и многие другие).
В быту мы постоянно применяем моющие средства, лекарства, косметику.
Машины не могут передвигаться без резиновых шин.
Наша одежда состоит из волокон, которые тоже представляют собой органические соединения.
Обрати внимание!
Органические вещества:
- имеют молекулярное строение;
- легкоплавкие и летучие;
- разлагаются при нагревании с образованием угля;
- горят на воздухе и образуют при этом углекислый газ и воду.
Плавление и горение парафина
Источники:
Габриелян О. С. Химия. 9 класс. Учебник для общеобразовательных учреждений. М.: Дрофа, 2011. — 193 с.
Органические вещества
Органические вещества, в отличие от неорганических, образуют ткани и органы живых организмов. К ним относятся белки, жиры, углеводы, нукленовые кислоты и другие.
Состав органических веществ клетки растений
Данные вещества представляют собой химические соединения, в состав которых входит углерод. Редкие исключения из этого правила – карбиды, угольная кислота, цианиды, оксиды углерода, карбонаты. Органические соединения образуются при связи углерода с любым из элементов таблицы Менделеева. Чаще всего в составе этих веществ присутствуют кислород, фосфор, азот, водород.
Чаще всего в составе этих веществ присутствуют кислород, фосфор, азот, водород.
Каждая клетка любого из растений на нашей планете состоит из органических веществ, которые условно можно разделить на четыре класса. Это углеводы, жиры (липиды), белки (протеины), нуклеиновые кислоты. Данные соединения являются биологическими полимерами. Они принимают участие в метаболических процессах в организме как растений, так и животных на клеточном уровне.
Четыре класса органических веществ
1. Белки (протеины) – это соединения, основными структурными элементами которых являются аминокислоты. В организме растений белки выполняют различные важные функции, основная из которых – структурная. Они входят в состав разнообразных клеточных образований, регулируют процессы жизнедеятельности и откладываются про запас.
2. Жиры (липиды) также входят в состав абсолютно всех живых клеток. Они состоят из простейших биологических молекул. Это сложные эфиры карбоновых кислот и спиртов. Главная роль жиров в жизнедеятельности клеток – энергетическая. Жиры откладываются в семенах и других частях растений. Вследствие их расщепления высвобождается необходимая для жизни организма энергия. Зимой многие кустарники и деревья питаются, расходуя запасы жиров и масел, которые они накопили за лето. Также следует отметить важную роль липидов в построении мембран клеток — как растительных, так и животных.
Главная роль жиров в жизнедеятельности клеток – энергетическая. Жиры откладываются в семенах и других частях растений. Вследствие их расщепления высвобождается необходимая для жизни организма энергия. Зимой многие кустарники и деревья питаются, расходуя запасы жиров и масел, которые они накопили за лето. Также следует отметить важную роль липидов в построении мембран клеток — как растительных, так и животных.
3. Углеводы являются основной группой органических веществ, благодаря расщеплению которых организмы получают необходимую энергию для жизни. Их название говорит само за себя. В структуре молекул углеводов наряду с углеродом присутствуют кислород и водород. Самым распространенным запасным углеводом, который образуется в клетках в процессе фотосинтеза, является крахмал. Большое количество этого вещества откладывается, например, в клетках клубней картофеля либо семян злаков. Другие углеводы придают сладкий привкус плодам растений.
4. Нуклеиновые кислоты (ДНК, РНК) представляют собой фосфорсодержащие биополимеры, имеющиеся в клеточных ядрах всех без исключения живых существ. Их основное предназначение – сохранение наследственной информации и передача ее потомкам.
Их основное предназначение – сохранение наследственной информации и передача ее потомкам.
Таким образом, клетка растения является маленькой «природной лабораторией», где синтезируются и преобразуются разнообразные химические органические вещества.
Похожие материалы:
Органические вещества в воде. Чем они опасны и как очистить воду?
Сегодня мы рассказываем все, что вы хотели знать об органических загрязнителях воды.
Органические загрязнители воды
Помимо неорганических веществ (железо, марганец, фториды) в воде содержатся и органические вещества. В нашем блоге вы узнаете о видах органических загрязнителей и о том, как обнаружить их превышение.
Источники загрязнения воды:
Выделяют 3 основных вида источников загрязнения воды:
- Населенные пункты. Канализационные стоки являются в данном случае основным местом скопления бытовых отходов. Ежедневно люди используют огромное количество воды для употребления, приготовления пищи, гигиенических процедур и уборки, после чего эта вода вместе с моющими средствами и пищевыми отходами попадает в канализацию.
 Затем происходит очистка коммунальными сооружениями, и вода возвращается на повторное использование.
Затем происходит очистка коммунальными сооружениями, и вода возвращается на повторное использование. - Промышленность. Является основным загрязнителем в развитых странах с огромным количеством предприятий. Количество выбрасываемых ими сточных вод в три раза превышает коммунально-бытовые стоки.
- Сельское хозяйство. В этой области интенсивно загрязняет водоемы растениеводство, благодаря применению удобрений и пестицидов. Около четверти азотных удобрений, треть калийных и 4 % фосфорных удобрений попадает в водоемы.
Влияние органических загрязнителей на здоровье человека
Существует множество заболеваний, вызванных загрязнением воды. Например, умываясь зараженной водой, можно заболеть коньюктивитом. Моллюски и водоросли, живущие в воде, могут вызвать шистосоматоз(лихорадка, боли в печени).
Как определить количество органических веществ в воде
Величина, характеризующая содержание в воде органических и минеральных веществ называется окисляемостью.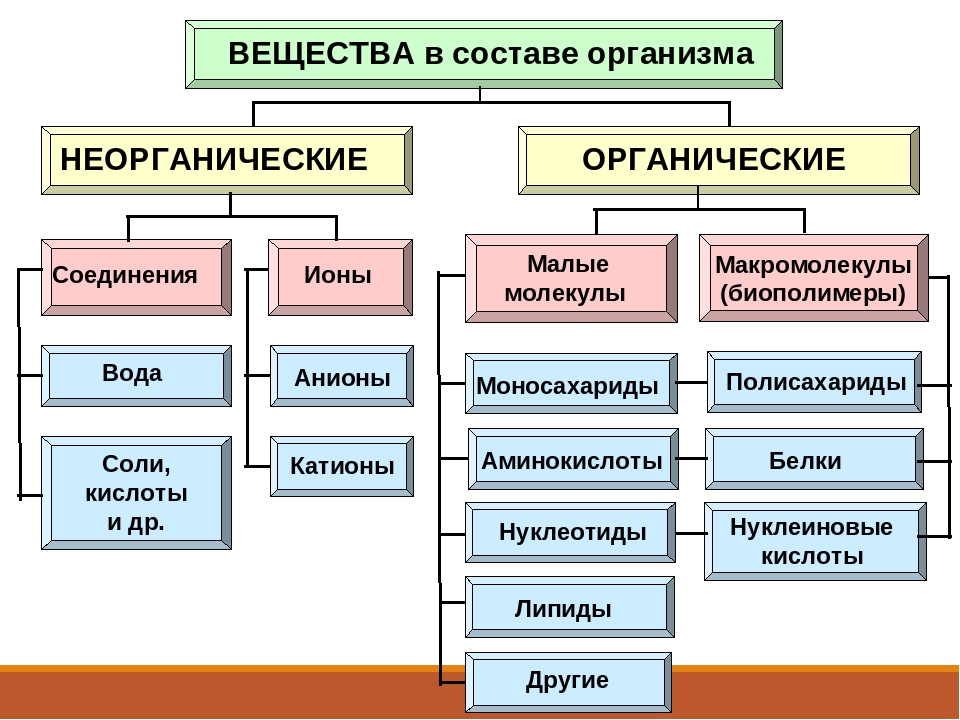 Для оценки химического потребления кислорода, т.е. окисляемости воды, используют бихроматный и перманганатный метод. Определение бихроматной окисляемости требует довольно продолжительного времени, поэтому для массового контроля работы очистных сооружений он малоудобен. Именно перманганатная окисляемость регламентирует качество питьевой воды согласно СанПиН.
Для оценки химического потребления кислорода, т.е. окисляемости воды, используют бихроматный и перманганатный метод. Определение бихроматной окисляемости требует довольно продолжительного времени, поэтому для массового контроля работы очистных сооружений он малоудобен. Именно перманганатная окисляемость регламентирует качество питьевой воды согласно СанПиН.
Что такое перманганатная окисляемость?
Перманганатная окисляемость — показатель, получаемый для оценки ХПК перманганатным методом, иными словами, это показатель общего количества органических веществ в воде. Перманганатная окисляемость выражается в миллиграммах кислорода, пошедшего на окисление этих веществ, содержащихся в 1 дм3 воды. Данный показатель не называет органические вещества, содержащиеся в воде, а говорит лишь о превышении их количества.
Признаки превышения пермаганатной окисляемости
Первым признаком переизбытка органики являются водоросли. Их можно обнаружить на внутренних стенках унитаза, на ощупь они напоминают слизь. Если вы чувствуете гнилой запах, исходящий из раковины или другой сантехники, наверняка перманганатная окисляемость превышена.
Если вы чувствуете гнилой запах, исходящий из раковины или другой сантехники, наверняка перманганатная окисляемость превышена.
Передельно допустимая концентрация
Согласно СанПиН ПДК питьевой воды по перманганатной окисляемости 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» составляет 5,0-7,0 мг/дм3. Чтобы узнать пермаганатную окисляемость воды в вашем доме, рекомендуем сделать анализ, который вы можете заказать на нашем сайте vodalab. Если в результате анализа пробы воды этот показатель превышает ПДК, то такая вода требует очистки.
Вы можете заказать анализ воды на перманганатную окисляемость, заполнив соответствующую форму здесь или позвонив по телефону +7(495)150-15-93.
Исследование на перманагантную окисляемость проводится в каждом из анализов, начиная с «базового», среди представленных на нашем сайте vodalab
Органические вещества входящие в состав клетки — какие основные соединения
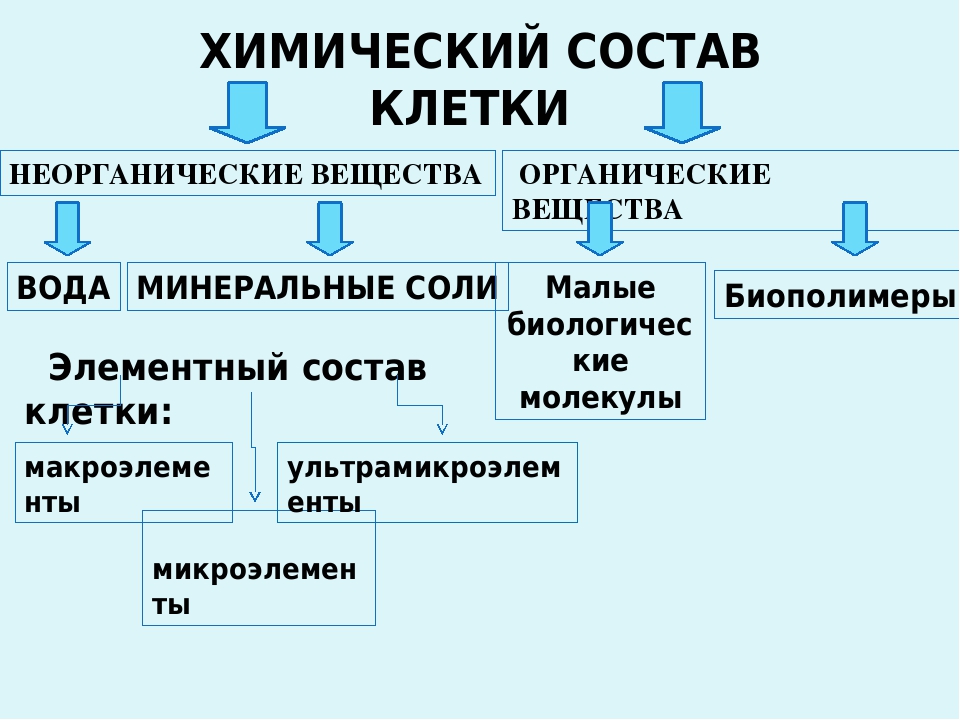
Живая клетка любого организма состоит из органических компонентов на 25–30%.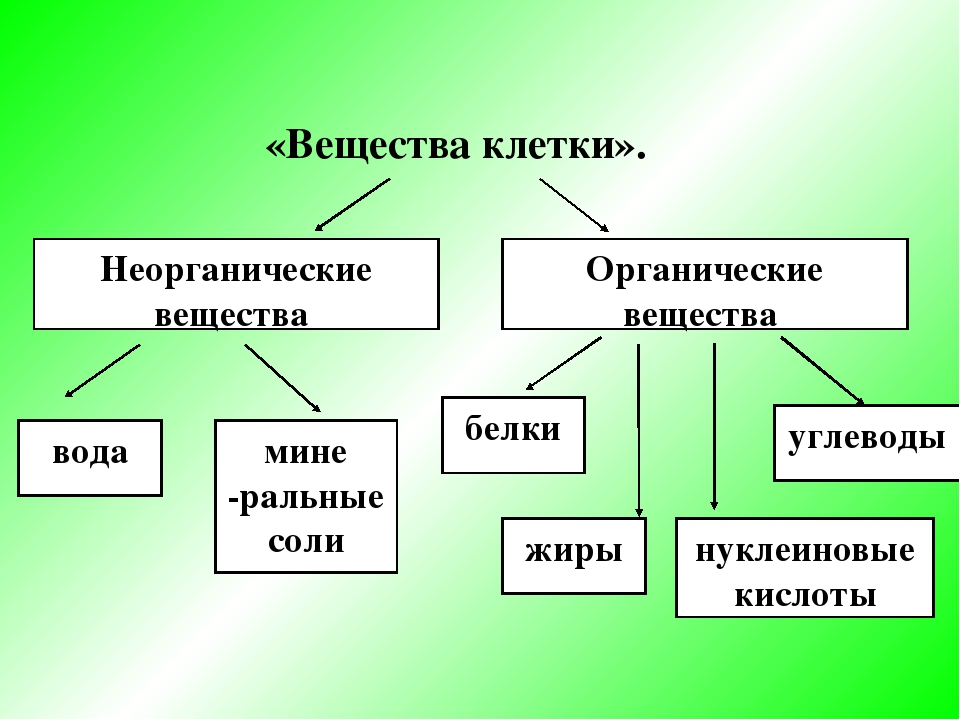
К органическим составляющим относятся как полимеры, так и сравнительно некрупные молекулы – пигменты, гормоны, АТФ и пр.
Клетки живых организмов различаются между собой по структуре, функциям и по своему биохимическому составу. Однако каждая группа органических веществ имеет сходное определение в курсе биологии и выполняет одни и те же функции в любом типе клеток. Основные составляющие компоненты — это жиры, белки, углеводы и нуклеиновые кислоты.
…
Вконтакте
Google+
Мой мир
Липиды
Липидами называются жиры и жироподобные вещества. Эта биохимическая группа отличается хорошей растворимостью в органических веществах, но при этом нерастворима в воде.
Жиры могут иметь твёрдую или жидкую консистенцию. Первая более характерна для животных жиров, вторая – для растительных.
Это интересно: атф это что за вещество — состав, функции и роль в организме.
Функции жиров заключаются в следующем:
- Структурная – фосфолипиды являются основной структурной составляющей клеточных мембран.
- Энергетическая – значительная часть энергии, которую использует клетка в процессе своей жизнедеятельности, получается в результате окисления жиров. Кроме того, в результате окисления липидов клетка получает воду.
- Защитная функция липидов заключается в том, что подкожный жировой слой защищает ткани от температурных воздействий и механических повреждений. Кроме того, у птиц и животных имеется жировая смазка на перьях, шерсти и коже. А листья большинства растений покрыты восковым налётом.
- Изоляционная функция жиров – миелин служит изоляционным слоем для нейронов, это служит ускорению передачи нервных импульсов.
- Из компонентов жировой ткани образуется ряд желчных кислот и витамин Д.
- Гормональная функция заключается в том, что многие гормоны имеют липидную природу.
Углеводы
Углеводы – это органические мономерные и полимерные вещества, которые в своём составе содержат углерод, водород и кислород. При их расщеплении клетка получает значительное количество энергии.
По химическому составу различают следующие классы углеводов:
- Простые углеводы или моносахариды. В зависимости от количества атомов углерода в молекуле такие вещества подразделяют на триозы, пентозы, гексозы и пр. К пентозам относятся вещества рибоза и дезоксирибоза — составляющие компоненты РНК и ДНК. Наиболее известная гексоза – это глюкоза, которая служит основным источником энергии для живых клеток.
- Олигосахариды – соединения, включающие в себя 2 или несколько мономеров гексозы. Наиболее известные дисахариды – лактоза и сахароза.
- Сложные углеводы или полисахариды — это полимеры, в состав которых входят несколько мономеров гексозы. К полисахаридам растительного происхождения относится целлюлоза. Углеводы, входящие в состав клеточной мембраны, представлены в основном сложными соединениями — гликолипидами и гликопротеидами. В животных клетках такую функцию выполняет гликоген. Крахмал – полисахарид, который содержится как в растительных, так и животных клетках.

По сравнению с животными клетками, растительные содержат в своём составе большее количество углеводов. Это объясняется способностью растительных клеток воспроизводить углеводы в процессе фотосинтеза.
Основными функциями углеводов в живой клетке являются энергетическая и структурная.
Энергетическая функция углеводов сводится к накоплению запасов энергии и высвобождению их по мере необходимости. Растительные клетки накапливают в вегетационный период крахмал, который откладывается в клубнях и луковицах. В организмах животных такую роль выполняет полисахарид гликоген, который синтезируется и накапливается в печени.
Структурную функцию углевод выполняют в растительных клетках. Практически вся клеточная стенка растений состоит из полисахарида целлюлозы.
Белки
Белки – органические полимерные вещества, которые занимают ведущее место как по количеству в живой клетке, так и по своему значению в биологии. Вся сухая масса животной клетки состоит из белка примерно наполовину. Этот класс органических соединений отличается поразительным многообразием. Только в организме человека насчитывается около 5 млн различных белков. Они не только отличаются между собой, но и имеют различия с белками других организмов. И все это колоссальное многообразие белковых молекул строится всего из 20 разновидностей аминокислот.
Вся сухая масса животной клетки состоит из белка примерно наполовину. Этот класс органических соединений отличается поразительным многообразием. Только в организме человека насчитывается около 5 млн различных белков. Они не только отличаются между собой, но и имеют различия с белками других организмов. И все это колоссальное многообразие белковых молекул строится всего из 20 разновидностей аминокислот.
Если на белок воздействуют термические или химические факторы, в молекулах происходит разрушение водородных и бисульфидных связей. Это приводит к денатурации белка и изменению структуры и функций клеточной мембраны.
Все белки можно условно разделить на два класса: глобулярные (к ним относятся ферменты, гормоны и антитела), и фибриллярные – коллаген, эластин, кератин.
Функции белка в живой клетке:
- Каталитическая функция. Большая часть биохимических реакций в клетке протекает довольно медленно. Это связано с низким уровнем химической активности многих органических веществ в клетке и их низкой концентрацией в живом организме.
 В этом случае белки исполняют роль катализаторов химических реакций, благодаря чему все процессы в значительной степени ускоряются и активизируются. Природные белковые биокатализаторы называются ферментами или энзимами. Каждый фермент отвечает за определённую химическую реакцию.
В этом случае белки исполняют роль катализаторов химических реакций, благодаря чему все процессы в значительной степени ускоряются и активизируются. Природные белковые биокатализаторы называются ферментами или энзимами. Каждый фермент отвечает за определённую химическую реакцию. - Строительная функция. Многие белки участвуют в строительстве клеточной мембраны и оболочек всех органелл.
- Сигнальная функция. По данным проведённых исследований, все внешние факторы вызывают в молекуле белка обратимые изменения. Такие обратимые изменения лежат в основе важного свойства живых организмов – раздражимости. Под влиянием физических, химических или термических раздражителей происходит изменение пространственной упаковки молекулы белка с изменением её функциональных особенностей.
- Транспортная функция заключается в способности некоторых белков обратимо связываться с органическими и неорганическими веществами и переносить их к различным органам и тканям. Наиболее характерна такая функция для белков крови.
 Примером таких белков может считаться гемоглобин, который способен связываться с молекулами кислорода и углекислого газа. Сывороточные белки альбумины могут транспортировать гормоны и некоторые липиды.
Примером таких белков может считаться гемоглобин, который способен связываться с молекулами кислорода и углекислого газа. Сывороточные белки альбумины могут транспортировать гормоны и некоторые липиды. - Защитная функция белков заключается в выработке в организме в ответ на внедрение чужеродного агента антител. Эти белковые компоненты способны связывать чужеродные компоненты и обезвреживать их.
- В меньшей степени белки могут также служить и источником энергии. При их распаде до аминокислот и дальше до воды, углекислого газа и азотистых соединений, выделяется некоторое количество энергии, необходимой для поддержания нормальной жизнедеятельности клетки.
Нуклеиновые кислоты
Нуклеиновые кислоты имеют важное значение в структуре и правильном функционировании клеток. Химическое строение этих веществ таково, что позволяет сохранять и передавать по наследству информацию о белковой структуре клеток. Эта информация передаётся дочерним клеткам и на каждом этапе их развития формируется определённый вид белков.
Поскольку подавляющее большинство структурных и функциональных особенностей клетки обусловлено их белковой составляющей, очень важна стабильность, которой отличаются нуклеиновые кислоты. В свою очередь, от стабильности структуры и функций отдельных клеток зависит развитие и состояние организма в целом.
Различают две разновидности нуклеиновых кислот – рибонуклеиновая (РНК) и дезоксирибонуклеиновая (ДНК).
ДНК представляет собой полимерную молекулу, которая состоит из пары спиралей нуклеотидов. Каждый мономер молекулы ДНК представлен в виде нуклеотида. В состав нуклеотидов входят азотистые основания (аденин, цитозин, тимин, гуанин), углевод (дезоксирибоза) и остаток фосфорной кислоты.
Все азотистые основания соединяются между собой строго определённым образом. Аденин всегда располагается всегда против тимина, а гуанин – против цитозина. Такое избирательное соединение называется комплементарностью и играет очень важное значение в формировании структуры белка.
Все соседние нуклеотиды между собой связываются остатком фосфорной кислоты и дезоксирибозой.
Рибонуклеиновая кислота имеет большое сходство с дезоксирибонуклеиновой. Различие заключается в том, что вместо тимина в структуре молекулы присутствует азотистое основание урацил. Вместо дезоксирибозы это соединение содержит углевод рибозу.
Все нуклеотиды в цепочке РНК соединяются через фосфорный остаток и рибозу.
По своей структуре РНК может быть одно— и двухцепочечным. У ряда вирусов двухцепочечные РНК выполняют функции хромосом – они являются носителями генетической информации. С помощью одноцепочечной РНК происходит перенос информации о составе белковой молекулы.
Зависимость теплопроводности газонаполненных утеплителей PIR от температурных условий эксплуатации
Шалимов В. Н., Борисов А. А., Нагаев И. Ф. «ТехноНИКОЛЬ-Строительные Системы»
Введение
Теплопроводность утеплителя является одной из ключевых характеристик, свидетельствующих о его эффективности. Температурозависимые физические процессы, протекающие в строительных материалах на макро- и микроуровнях, могут повлечь изменения, влияющие на физико-механические характеристики этих материалов, в целом. Это является одной из основных причин существования ряда «гостовских» измерений λ при разных температурах, например, при 100С, 250С и т.д. Следовательно, получение достоверных сведений о теплопроводности материалов в различных условиях особенно важно. Это позволяет исключить любые спекуляции в нечестной конкурентной борьбе, основанные на недостоверных домыслах, способных дискредитировать в глазах потребителя новые виды утеплителей. Данная статья посвящена таким материалам на основе вспененных полиуретанов (PUR/PIR), занявшим значительную долю зарубежного и отечественного рынков общестроительной изоляции и изоляции холодильных установок.
Температурозависимые физические процессы, протекающие в строительных материалах на макро- и микроуровнях, могут повлечь изменения, влияющие на физико-механические характеристики этих материалов, в целом. Это является одной из основных причин существования ряда «гостовских» измерений λ при разных температурах, например, при 100С, 250С и т.д. Следовательно, получение достоверных сведений о теплопроводности материалов в различных условиях особенно важно. Это позволяет исключить любые спекуляции в нечестной конкурентной борьбе, основанные на недостоверных домыслах, способных дискредитировать в глазах потребителя новые виды утеплителей. Данная статья посвящена таким материалам на основе вспененных полиуретанов (PUR/PIR), занявшим значительную долю зарубежного и отечественного рынков общестроительной изоляции и изоляции холодильных установок.
Особенности PIR
В сравнении с «классическими» утеплителями, существующими на строительном рынке продолжительное время, PIR является относительно новым и, благодаря некоторым отличительным особенностям химического и физического строения, его можно назвать инновационным продуктом. Наибольший интерес для данного исследования представляют именно особенности физического строения, требующие более подробного рассмотрения.
Наибольший интерес для данного исследования представляют именно особенности физического строения, требующие более подробного рассмотрения.
Структурная организации PIR осложнена тем, что он не является монокомпонентным: в его состав, помимо твердого вещества, входит специальный газ. В процессе вспенивания в присутствии специально подобранного для требуемых условий работы пенообразующего агента и последующего отверждения, создается пористая мелкоячеистая структура, в которой объём герметично замкнутых пор (ячеек) составляет более 96 %, что делает материал объёмным и сверхлегким. В ячейках остается инертный газ, имеющий чрезвычайно низкий коэффициент теплопроводности (менее 0,015 Вт/(м*К).
В настоящее время вспенивающие агенты подразделяют на химические («муравьиная» кислота, вода) и физические (фреоны, пентаны и др. низкокипящие инертные органические вещества). Химические вспениватели реагируют с полимерным компонентом и образуют углекислый газ. В случае физических вспенивателей используется их фазовый переход из жидкого состояния в газообразное. Применение того или иного типа вспенивающих агентов позволяет корректировать/подбирать физико-механические характеристики готового продукта, поскольку характеристики газа и его стабильность в ячейках PIR напрямую влияют на долговечность утеплителя. Для справки приведём данные о результатах испытаний в НИИМОССТРОЙ [1], подтверждающие стойкость PIR к периодическому воздействию знакопеременных температур от минус 30°С до 50°С и повышенной влажности. По оценке специалистов, срок службы плит утеплителя из жесткого PIR составляет более 50 лет.
В случае физических вспенивателей используется их фазовый переход из жидкого состояния в газообразное. Применение того или иного типа вспенивающих агентов позволяет корректировать/подбирать физико-механические характеристики готового продукта, поскольку характеристики газа и его стабильность в ячейках PIR напрямую влияют на долговечность утеплителя. Для справки приведём данные о результатах испытаний в НИИМОССТРОЙ [1], подтверждающие стойкость PIR к периодическому воздействию знакопеременных температур от минус 30°С до 50°С и повышенной влажности. По оценке специалистов, срок службы плит утеплителя из жесткого PIR составляет более 50 лет.
Теоретические аспекты теплопроводности PIR при различных температурах
Актуальность исследуемому вопросу добавляет тот факт, что в типовом кровельном «пироге» зона отрицательных температур занимает практически половину его толщины (см. рис 2.1). Поэтому любая ошибка в теплопроводности может существенно исказить весь теплотехнический расчет.
В ходе исследования особое внимание было обращено на работу [2], опубликованную несколько лет назад на сайте зарубежной ассоциации BSC. Особый интерес общественности вызвал график (Рис. 2.2), якобы свидетельствующий о том, что что при определенных температурах происходит критическое изменение коэффициента теплопроводности (λ) одной из модификаций PIR (на графике выделено коричневым цветом), не характерное для традиционных утеплителей, чья величина теплопроводности имела линейную зависимость. Согласно представленным данным наблюдается резкое увеличение λ PIR-изоляции при температурах ниже 150С до значений, превышающих теплопроводности всех известных утеплителей. Столь необычное поведение теплоизолирующей способности пенополиизоцианурата вызвало интерес и желание разобраться в данном вопросе.
В процессе анализа представленных материалов были выявлены некоторые недостатки работы [2], которые заключаются в простой констатации наблюдаемых экспериментальных данных без каких-либо глубоких научных обоснований. Нехватка сведений о химическом составе используемых полимеров, их характеристик, сырьевого состава и примененных вспенивающих агентах дало широкое поле для собственных трактовок отечественным специалистам в работе [3]. В частности, по их мнению, причина наблюдаемого резкого ухудшения λ кроется в возможной конденсации вспенивающего агента, находящегося в ячейках материала, т.е. переходе его из газообразного состояния в жидкое. А жидкая фаза вспенивающего агента, согласно представленным данным, имеет большую теплопроводность.
Нехватка сведений о химическом составе используемых полимеров, их характеристик, сырьевого состава и примененных вспенивающих агентах дало широкое поле для собственных трактовок отечественным специалистам в работе [3]. В частности, по их мнению, причина наблюдаемого резкого ухудшения λ кроется в возможной конденсации вспенивающего агента, находящегося в ячейках материала, т.е. переходе его из газообразного состояния в жидкое. А жидкая фаза вспенивающего агента, согласно представленным данным, имеет большую теплопроводность.
Отметим, что можно сколь угодно долго рассуждать о теоретических аспектах поведения неидентифицированного материала, однако наиболее объективную картину можно получить лишь эмпирическим методом с помощью высокоточного оборудования.
Независимые практические исследования PIR-изоляции
С точки зрения минимальной достаточности данных, позволяющих судить о температурных метаморфозах теплопроводности PIR в пределах существующих нормальных рабочих условий эксплуатации (-600С; +1100С), полезными являются работы [4], [5], [6], [7]. В них экспериментальным путем доказано, что тенденция к резкому увеличению коэффициента теплопроводности при понижении средней температуры (в частности, ниже 15°С), отсутствует, а результаты ранее опубликованной работы [2] не соответствуют действительности и вызывают некоторые сомнения.
В них экспериментальным путем доказано, что тенденция к резкому увеличению коэффициента теплопроводности при понижении средней температуры (в частности, ниже 15°С), отсутствует, а результаты ранее опубликованной работы [2] не соответствуют действительности и вызывают некоторые сомнения.
Однако принципиальная позиция авторов данной статьи заключается в установлении целостной картины поведения материала в условиях, превосходящих по сложности нормальную эксплуатацию в строительстве и холодильных установках. Необходимость получения всесторонних и максимально объективных данных о изменениях теплопроводности заставили провести масштабное исследование с использованием сверхвысокоточного оборудования (рис. 3.1).
Рис. 3.1 Лабораторное измерительное оборудование ВНИИФТРИ
Данное исследование является уникальным и беспрецедентным. С уверенностью можно сказать, что при испытании теплопроводности до некоторых пор не удавалось «заглянуть» за отметку минус 900С – предельный порог для оборудования во ВНИИМ им. Д.И. Менделеева [5]. Осуществленные эксперименты позволили определить поведение материала при рекордных температурах до минус 1800С. Испытания были проведены в лаборатории №310 НИО-3 сектора эталонов и научных исследований в области измерений теплофизических величин ФГУП ВНИИФТРИ. Три серии из 106 измерений проводились в атмосфере воздуха при комнатной температуре 295 К, и в атмосфере азота в диапазоне температур 80-360 К.
Д.И. Менделеева [5]. Осуществленные эксперименты позволили определить поведение материала при рекордных температурах до минус 1800С. Испытания были проведены в лаборатории №310 НИО-3 сектора эталонов и научных исследований в области измерений теплофизических величин ФГУП ВНИИФТРИ. Три серии из 106 измерений проводились в атмосфере воздуха при комнатной температуре 295 К, и в атмосфере азота в диапазоне температур 80-360 К.
Данные результатов измерений оформлены в отчете [8] и сведены в графики (Рис. 3.2, 3.3). Особый интерес вызывает поведения материала в температурном диапазоне наиболее часто встречающихся отрицательных температур, начинающихся левее вертикальной красной линии. Укрупненный график 3.3 говорит том, что даже наличие потенциальной опасности ухудшения λ из-за конденсации газа, визуально заметное как спрямление и небольшой рост кривой теплопроводности, не означает, что ухудшение теплотехнических характеристик будет неизбежным. В частности, внутри материала контакт теплопроводной жидкой фазы с поверхностью пор, может быть незначительным, в отличие от газа, контактирующего со всей внутренней поверхностью пор. Образовавшийся в порах PIR при конденсации вакуум обладает хорошей компенсаторной функцией, позволяющей не только не допустить роста количества передаваемого тепла, но и способствует его существенному снижению. Как мы видим, данный процесс не выражен ярко, что свидетельствует о качестве и стабильности теплоизоляционного материала во всём исследуемом диапазоне температур.
Образовавшийся в порах PIR при конденсации вакуум обладает хорошей компенсаторной функцией, позволяющей не только не допустить роста количества передаваемого тепла, но и способствует его существенному снижению. Как мы видим, данный процесс не выражен ярко, что свидетельствует о качестве и стабильности теплоизоляционного материала во всём исследуемом диапазоне температур.
Представленные данные из лаборатории ВНИИФТРИ практически совпадают с академическим представлением зарубежной лаборатории классических данных (см. рис. 3.4) о поведении газонаполненных полиуретановых материалов при изменении температуры [9].
Практической реализацией данного исследования стали рекомендации по использованию PIR в экстремальных арктических условиях заполярья на нефтегазодобывающем месторождении полуострова Ямал, где был изолирован участок вечной мерзлоты, находящийся непосредственно под факелом утилизации попутного газа, с целью предотвращения разрушения конструкции из-за оттаивания грунта при воздействии тепла от пламени горелки.
Рис 3.5 – Факел утилизации попутного газа с изолированной площадкой грунта.
Основные выводы
Подытоживая проделанную экспериментальную работу, можно сделать ряд основных утверждений:
- Любой современный материал требует глубокого всестороннего изучения. Исследование его поведения, в том числе, в более широком диапазоне температур, чем подразумевает массовое применение, позволяет гарантированно избежать ошибок в проектировании, дискредитации материала в конкурентной борьбе и проблем в эксплуатации.
- Температурная зависимость теплопроводности PIR носит не гладкий характер, несколько затрудняющий интерпретацию результатов. Однако детальный анализ графиков и сравнение с академическими данными дает хорошее понимание происходящих в материале физических процессов.
- Наличие перелома графика свидетельствует о конденсации тяжелого газа, находящегося в ячейках-порах материала.
 Однако увеличение теплопроводности незначительно и больше напоминает стабилизацию значения λ при понижении температуры.
Однако увеличение теплопроводности незначительно и больше напоминает стабилизацию значения λ при понижении температуры. - Можно утверждать о значительном повышении эффективности PIR в зоне отрицательных температур, в которой ранее не было представления о поведении материала. Об этом свидетельствует снижение коэффициента λ, принимающее характер стремительного падения.
- Столь стремительное снижение теплопроводности объясняется очень малым пятном контакта образовавшейся в порах жидкой фазы тяжёлого инертного газа с твёрдым веществом стенок. Факторы увеличения за счёт этого доли лёгких молекул в газовой фазе, а также образование вакуума, замещающего газовую фазу вспенивающего агента, не участвуют в передаче тепла. Как оказалось, вакуум надёжно выполняет компенсаторную функцию.
- Дальнейшее стабильное падение теплопроводности при понижении температуры говорит о герметичности ячеек. Это косвенно может свидетельствовать о чрезвычайно длительном процессе замещения инертного газа в ячейках, сопоставимом со сроком эксплуатации материала, превышающем 50 лет.
- Что касается работы [2], указанный в ней вид полиизоциануратов является одним из архаичных поколений PIR, имеющих весьма отдаленное отношение к современным его видам. Наиболее вероятно использование устаревших вспенивающих агентов (фторпроизводных углеводородов, а также диоксидуглерода СО2), имеющих гораздо более высокую склонность к возможной конденсации в ячейках полимера при более высоких температурах. Поэтому результаты их испытаний нельзя рассматривать применительно к российским материалам.
Список использованных источников
- Заключение № 174 по результатам работы по теме: «Проведение ускоренных испытаний на стойкость к климатическим воздействиям по методике ОАО «НИИМосстрой» сроком на 50 лет образцов пенополиизоцианурата (PIR)»
- Building Science Corporation (BSC) «In Cold climates, R-5 Foam beats R-6». Режим доступа: http://www.greenbuildingadvisor.com/blogs/dept/musings/cold-climates-r-5-foam-beats-r-6.
- Воронин А.
 Анализируй теплопроводность Режим доступа: http://vseokrovle.ru/analizirujj-teploprovodnost.html.
Анализируй теплопроводность Режим доступа: http://vseokrovle.ru/analizirujj-teploprovodnost.html. - Стукань Е. Исследование теплоизоляционных свойств пенополиизоциануратных (ПИР) сэндвич-панелей при пониженных температурах. Режим доступа: http://www.nappan.ru/upload/images/PIR-value.pdf.
- Протокол измерения теплопроводности №2413/02, ВНИИМ им. Д.И. Менделеева, Санкт Петербург, 2017.
- Протокол ООО «Сертификационно-исследовательский центр «Теплоизоляция» при МГУ им. М.В. Ломоносова №0109/14-01 от 16.09.14.
- Мельников В.С., Ванин С.А., Мельников М.В. Суперпозиция факторов теплопроводности строительных пенополиуретанов и пенополиизоциануратов // Интернет-журнал «НАУКОВЕДЕНИЕ» Том 9, №3 (2017).
- Протокол испытаний №3/310-234.17, ФГУП «ВНИИФТРИ», Москва, 2017.
- Sparks, LL; “Thermal Conductivity of a Polyurethane Foam from 95 K to 340 L”, NBSIR 82-1664, March 1982.
Оригинальная версия статьи размещена на vseokrovle. ru
ru
Органическое вещество почвы как фактор, определяющий её плодородие
Гумусовые вещества и их роль в составе почвы
Как избежать снижения плодородия почвы
Растительные и животные остатки
Что является основой плодородия почв
О важности оптимальных условий для накопления и минерализации органического вещества
Органическое вещество почвы — это фактор плодородия почвы, источник энергии для развития и формирования почвы, это то, что отличает плодородную почву от материнской породы.
Органическое вещество почвы представляет собой комплекс органических соединений, входящих в состав почвы. Эти вещества разделены на две группы:
1) подавляющее группа гумусовых веществ;
2) группа растительных и животных остатков различной степени разложения и промежуточных продуктов разложения (негумифицированные органические вещества).
Гумусовые вещества и их роль в составе почвы
Органическое вещество почвы представлено на 85-90% гумусовыми веществами (фульвокислоты, гуминовые кислоты и гумин). По своей природе это устойчивые к разложению, консервированные органические вещества, на 50-60% состоят из углерода, 30-45% кислорода и только на 2.5-5% из азота.
По своей природе это устойчивые к разложению, консервированные органические вещества, на 50-60% состоят из углерода, 30-45% кислорода и только на 2.5-5% из азота.
Так же в их состав входят сера, фосфор и др. Гуминовые кислоты и фульвокислоты, а также образующаяся в почве при разложении органических веществ углекислота, которая растворяет минеральные соединения фосфора, калия, кальция, магния, в результате чего, эти элементы переходят в доступную для растений форму.
Подвижные питательные элементы гумуса в меньшей степени участвуют в питании растений, чем негумифицированные вещества, так как медленно минерализуются, но создают для разложения органических остатков благоприятную среду. Однако при длительном выращивании сельскохозяйственных культур без внесения удобрений, может происходить постепенное разложение и использования гуминовых веществ.
Как избежать снижения плодородия почвы
Это приводит к значительному уменьшению общего количества органического вещества почвы и снижению ее плодородия. Систематическое применение органических и минеральных удобрений, обеспечивая повышение урожайности сельскохозяйственных культур, способствует сохранению и накоплению запасов гумуса и азота в почве, так как с ростом урожая увеличивается количество поступающих в почву корневых и пожнивных остатков и усиливаются процессы гумусообразования.
Систематическое применение органических и минеральных удобрений, обеспечивая повышение урожайности сельскохозяйственных культур, способствует сохранению и накоплению запасов гумуса и азота в почве, так как с ростом урожая увеличивается количество поступающих в почву корневых и пожнивных остатков и усиливаются процессы гумусообразования.
Накопление гумуса в почве способствует созданию благоприятных условий для развития и деятельности микроорганизмов. Микроорганизмы активизируют многие биохимические процессы в почве, участвующих в процессе минерализации органического вещества, увеличивают доступность питательных веществ почвы и удобрений для растений. Поэтому почвы, богатые микроорганизмами, более плодородные и обеспечивают получение более высоких урожаев сельскохозяйственных культур.
Растительные и животные остатки
Вторая группа органических соединений, хотя и является количественно меньше, но по своему значению в чем-то даже и превосходит гумус. В эту группу входят растительные и животные остатки разной степени разложения, промежуточные продукты разложения (жиры, белки, смолы, клетчатка, органические кислоты и др. ).
).
Негумифицированные органические вещества составляют 10-20% от общего количества органики в почве, они являются непосредственным источником элементов питания для растений и животных, некоторые из них влияют на трансформацию питательных элементов почвы и удобрений с недоступной для растений формы в доступную и наоборот. В них содержатся все макро- и микроэлементы, необходимые растениям и животным.
Что является основой плодородия почв
Содержание органического вещества в почвах колеблется от 1-3% (в подзолистых почвах и серозёмах) до 8-10% и более в плодородных черноземах. В нашей практике встречались образцы почвы с содержанием общего органического вещества от 0.5-0.7% до 5-6%, среднее содержание органического вещества в образцах почвы — 2.0-3.5%. Данная статистика говорит о снижении плодородия наших почв и нерациональном их использовании.
Органическое вещество является основой плодородия почв, оно служит своеобразным резервом необходимых растениям питательных веществ, оказывает огромное влияние на структуру почвы, является источником энергии для многих полезных микроорганизмов.
В органическом веществе содержится 98% азота, от 30 до 40% фосфора, до 90% серы (от общего их содержания в почве). Вот почему нам так важно знать при анализе почв и расчета доз удобрений под культуру содержание общего органического вещества, так как это как раз те вещества, которые растения потребляют в большом количестве, и они могут быть получены ими из почвы.
О важности оптимальных условий для накопления и минерализации органического вещества
В почве происходят одновременно два противоположно процесса: синтез, накопление органического вещества, и его разрушение (минерализация). При минерализации азот, фосфор и сера переходят в усвояемую для растений минеральную форму. На интенсивность минерализации влияет культура и технология ее выращивания (система обработки почвы и минерального питания).
Поэтому так важно создавать оптимальные условия для накопления и минерализации органического вещества в почве. Лучшие условия создаются в структурных, рыхлых, культурных почвах, где происходит пополнение растительных и животных остатков, создается оптимальное значение рН.
Вывод
В конечном итоге хотелось бы отметить, что значение такого показателя плодородия почвы как органическое вещество, в процессе разработки компетентных и полных рекомендаций по внесению минеральных удобрений, особенно актуален для расчета доз азотных, фосфорных удобрений и удобрений серы, а также он влияет на нормы внесения гербицидов.
Органические вещества, входящие в состав клетки. Биология 9 класс Мамонтов
Вопрос 1. Назовите основные группы органических веществ, входящих в состав клетки.
Органические соединения составляют в среднем 20–30 % массы клетки живого организма. К ним относятся биологические полимеры – белки, нуклеиновые кислоты и углеводы, а также жиры и ряд небольших молекул – гормоны, пигменты, аминокислоты, простые сахара, нуклеотиды и т. д. Разные типы клеток содержат разные количества органических соединений.
Вопрос 2. Из каких простых органических соединений состоят белки?
Белки – это высокомолекулярные полимерные соединения, мономером которых служат аминокислоты.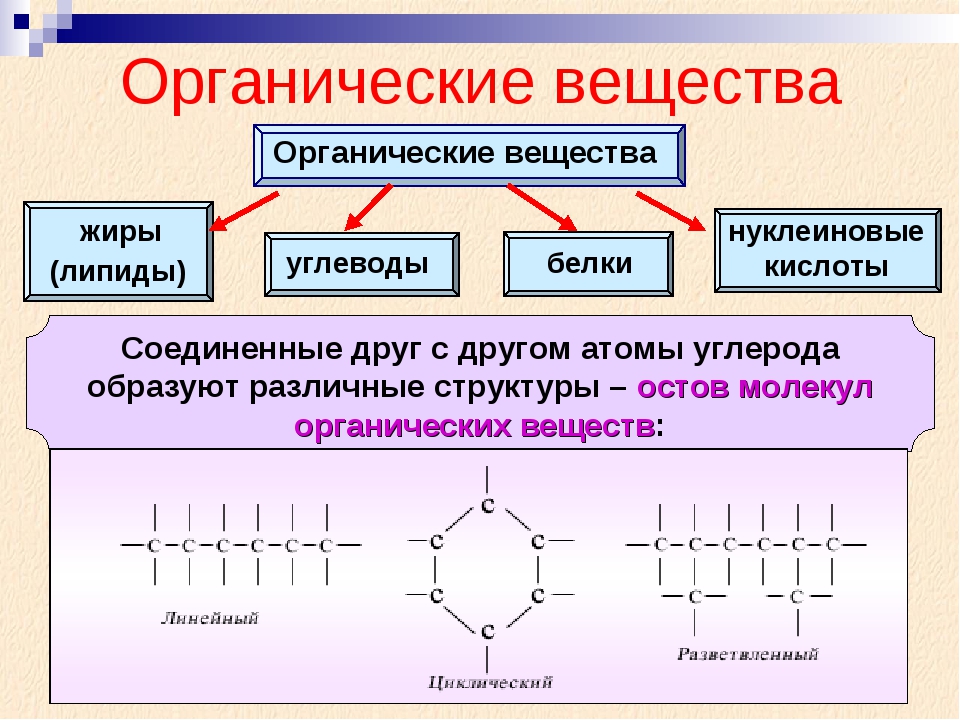
Вопрос 3. Составьте схему «Функции белков в клетке».
Функции белков в клетке многообразны. Одна из важнейших — строительная функция: белки входят в состав всех клеточных мембран и органоидов клетки, а также внеклеточных структур. Для обеспечения жизнедеятельности клетки исключительно важное значение имеет каталитическая, или. ферментативная, роль белков. Биологические катализаторы, или ферменты, — это вещества белковой природы, ускоряющие химические реакции в десятки и сотни тысяч раз.
Ферментам свойственны некоторые черты, отличающие их от катализаторов неорганической природы. Во-первых, один фермент катализирует только одну реакцию или один тип реакций, т. е. биологический катализ специфичен. Во-вторых, активность ферментов ограничена довольно узкими температурными рамками (35— 45 °С), за пределами которых их активность снижается или исчезает. В-третьих, ферменты активны при физиологических значениях рН, т. е. в слабощелочной среде. Еще одно важное отличие ферментов от неорганических катализаторов: биологический катализ протекает при нормальном атмосферном давлении.
Еще одно важное отличие ферментов от неорганических катализаторов: биологический катализ протекает при нормальном атмосферном давлении.
Все это определяет ту важную роль, которую ферменты играют в живом организме. Практически все химические реакции в клетке протекают с участием ферментов. Двигательная функция живых организмов обеспечивается специальными сократительными белками. Эти белки участвуют во всех видах движения, к которым способны клетки и организмы: мерцание ресничек и биение жгутиков у простейших, сокращение мышц у многоклеточных животных и пр. Транспортная функция белков заключается в присоединении химических элементов (например, кислорода) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела.
При поступлении в организм чужеродных белков или микроорганизмов белые кровяные тельца лейкоциты— образуют особые белки — антитела. Они связывают и обезвреживают не свойственные организму вещества — это защитная функция белков. Белки служат также источником энергии в клетке, т. е. выполняют энергетическую функцию. При полном расщеплении 1 г белка выделяется 17,6 кДж энергии.
Белки служат также источником энергии в клетке, т. е. выполняют энергетическую функцию. При полном расщеплении 1 г белка выделяется 17,6 кДж энергии.
Вопрос 4. Какие химические соединения называют углеводами?
Углеводы, обширная группа природных органических соединений, химическая структура которых часто отвечает общей формуле Cm(h3O)n (т. е. углерод вода, отсюда название).
Вопрос 5. Назовите основные функции углеводов. Какие клетки и почему наиболее богаты углеводами?
Углеводы выполняют две основные функции: строительную и энергетическую. Например, целлюлоза образует стенки растительных клеток; сложный полисахарид хитин — главный структурный компонент наружного скелета членистоногих. Строительную функцию хитин выполняет и у грибов. Углеводы играют роль основного источника энергии в клетке. В процессе окисления 1 г углеводов освобождается 17,6 кДж энергии. Крахмал у растений и гликоген у животных, откладываясь в клетках, служит энергетическим резервом.
Вопрос 6. Вспомните из предыдущих курсов биологии, какую функцию выполняет глюкоза в организме человека. Какое количество глюкозы в крови является нормой? Чем опасно резкое снижение концентрации глюкозы в плазме крови?
Глюкоза крови является непосредственным источником энергии в организме. Быстрота ее распада и окисления, а также возможность быстрого извлечения из депо обеспечивают экстренную мобилизацию энергетических ресурсов при стремительно нарастающих затратах энергии в случаях эмоционального возбуждения, при интенсивных мышечных нагрузках и др.
Уровень глюкозы в крови составляет 3,3—5,5 ммоль/л и является важнейшей гомеостатической константой организма. Особенно чувствительной к понижению уровня глюкозы в крови (гипогликемия) является ЦНС. Незначительная гипогликемия проявляется общей слабостью и быстрой утомляемостью. При снижении уровня глюкозы в крови до 2,2—1,7 ммоль/л (40— 30 мг%) развиваются судороги, бред, потеря сознания, а также вегетативные реакции: усиленное потоотделение, изменение просвета кожных сосудов и др. Это состояние получило название «гипогликемическая кома». Введение в кровь глюкозы быстро устраняет данные расстройства.
Это состояние получило название «гипогликемическая кома». Введение в кровь глюкозы быстро устраняет данные расстройства.
Вопрос 7. Объясните, почему термины «жиры» и «липиды» не являются синонимами.
Липиды — разнородная группа углеводород-содержащих органических веществ. Сложные природные и синтетические соединения, объединяемых общим свойством — хорошей растворимостью в неполярных органических растворителях (таких, как эфир и хлороформ) и очень малой растворимостью в воде. Липидам отводится важная роль в формировании биологических мембран, других сторонах жизнедеятельности организмов.
Не следует путать понятия, считая липиды синонимом слова жир, жиры (триглицериды) — лишь один из важных подклассов липидов.
Вопрос 8. Какие функции выполняют липиды? В каких клетках и тканях их особенно много?
Основная функция жиров – служить энергетическим резервуаром. Калорийность липидов выше энергетической ценности углеводов. В ходе расщепления 1 г жиров до СO2 и Н2O освобождается 38,9 кДж энергии. Содержание жира в клетке колеблется в пределах 5–15 % от массы сухого вещества. В клетках жировой ткани количество жира возрастает до 90 %. В организме животных, впадающих в спячку, накапливается избыток жира, у позвоночных животных жир откладывается ещё и под кожей – в так называемой подкожной клетчатке, где он служит для теплоизоляции. Одним из продуктов окисления жиров является вода. Эта метаболическая вода очень важна для обитателей пустынь. Так, жир, которым заполнен горб верблюда, служит в первую очередь не источником энергии (как часто ошибочно полагают), а источником воды.
В ходе расщепления 1 г жиров до СO2 и Н2O освобождается 38,9 кДж энергии. Содержание жира в клетке колеблется в пределах 5–15 % от массы сухого вещества. В клетках жировой ткани количество жира возрастает до 90 %. В организме животных, впадающих в спячку, накапливается избыток жира, у позвоночных животных жир откладывается ещё и под кожей – в так называемой подкожной клетчатке, где он служит для теплоизоляции. Одним из продуктов окисления жиров является вода. Эта метаболическая вода очень важна для обитателей пустынь. Так, жир, которым заполнен горб верблюда, служит в первую очередь не источником энергии (как часто ошибочно полагают), а источником воды.
Очень важную роль для живых организмов играют фосфолипиды, являющиеся компонентами мембран, т. е. выполняющие строительную функцию.
Из липидов можно отметить также воск, который используется у растений и животных в качестве водоотталкивающего покрытия. Из воска пчёлы строят соты. Широко представлены в животном и растительном мире стероиды – это желчные кислоты и их соли, половые гормоны, витамин D, холестерол, гормоны коры надпочечников и т. д. Они выполняют ряд важных биохимических и физиологических функций.
д. Они выполняют ряд важных биохимических и физиологических функций.
Вопрос 9. Откуда в организме берётся метаболическая вода?
Метаболическая, или эндогенная, вода образуется в организме в результате большого количества биохимических превращений. Наибольшее ее количество образуется при окислении углеводов и жиров. Например, при расщеплении 100 г жира выделяется не только значительное количество энергии, но и 134 мл эндогенной воды. Такое свойство жиров позволяет многим животным (амфибиям, рептилиям и млекопитающим) в неблагоприятный сезон года впадать в спячку и не вести активный образ жизни. Это же качество жира делает возможным трансокеанские перелеты некоторых бабочек (махаон).
Вопрос 10. Что такое нуклеиновые кислоты? Какие типы нуклеиновых кислот вы знаете? Чем отличаются РНК и ДНК?
Нуклеиновые кислоты – это полимеры, построенные из огромного числа мономерных единиц, называемых нуклеотидами.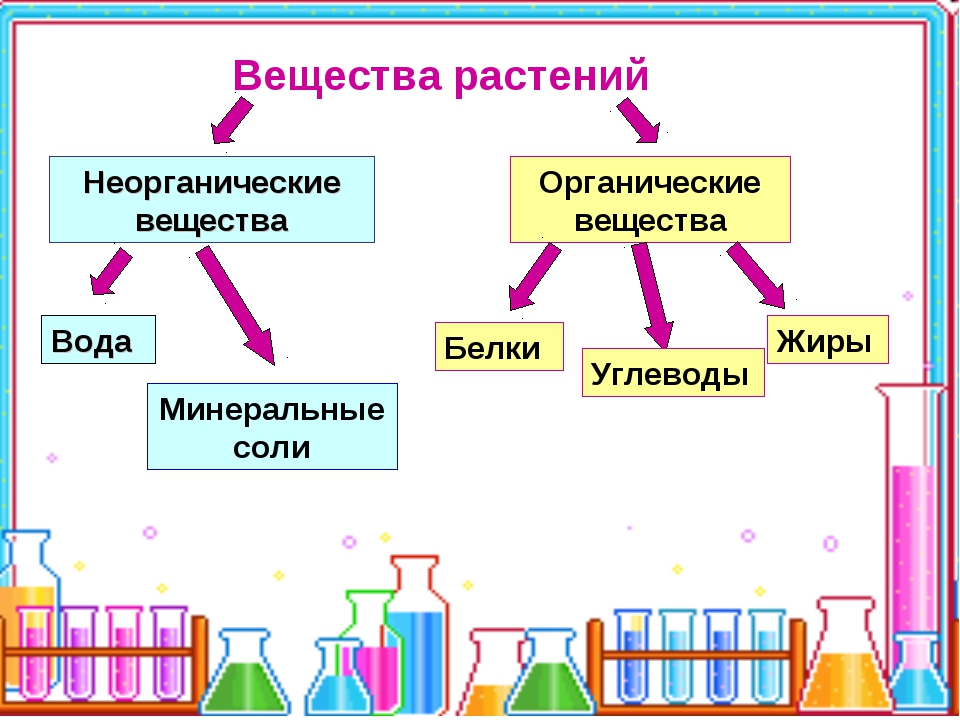
Различают два типа нуклеиновых кислот. Дезоксирибонуклеиновая кислота (ДНК) – двуцепочечный полимер с очень большой молекулярной массой. В одну молекулу могут входить 108 и более нуклеотидов. ДНК несёт в себе закодированную информацию о последовательности аминокислот в белках, синтезируемых клеткой, и обладает способностью к воспроизведению.
Рибонуклеиновая кислота (РНК), в отличие от ДНК, бывает в большинстве случаев одноцепочечной. Существует несколько видов РНК: информационные (иРНК), транспортные (тРНК) и рибосомальные (рРНК). Они различаются по структуре, величине молекул, расположению в клетке и выполняемым функциям.
Вопрос 11. Сравните химический состав живых организмов и тел неживой природы. Какие выводы можно сделать на основе этого сравнения?
Тела живой и неживой природы состоят из одинаковых химических элементов. В состав живых организмов входят неорганические вещества — вода и минеральные соли.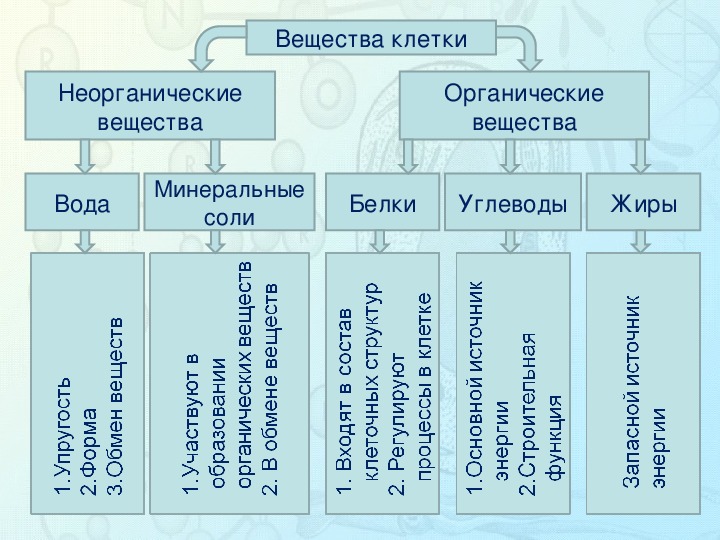 Жизненно важные многочисленные функции воды в клетке обусловлены особенностями ее молекул: их полярностью, способностью образовывать водородные связи. Все это говори об общности и единстве живой и неживом природы.
Жизненно важные многочисленные функции воды в клетке обусловлены особенностями ее молекул: их полярностью, способностью образовывать водородные связи. Все это говори об общности и единстве живой и неживом природы.
Вопрос 12. Какие особенности строения атома углерода обусловливают его ключевую роль в формировании молекул органических веществ?
Большинство окружающих нас веществ — органические соединения. Это ткани животных и растений, наша пища, лекарства, одежда (хлопчатобумажные, шерстяные и синтетические волокна), топливо (нефть и природный газ), резина и пластмассы, моющие средства. В настоящее время известно более 10 млн. таких веществ, и число их каждый год значительно возрастает благодаря тому, что учёные выделяют неизвестные вещества из природных объектов и создают новые, не существующие в природе соединения.
Такое многообразие органических соединений связано с уникальной особенностью атомов углерода образовывать прочные ковалентные связи, как между собой, так и с другими атомами. Атомы углерода, соединяясь друг с другом как простыми, так и кратными связями, могут образовывать цепочки практически любой длины и циклы. Большое разнообразие органических соединений связано также с существованием явления изомерии.
Атомы углерода, соединяясь друг с другом как простыми, так и кратными связями, могут образовывать цепочки практически любой длины и циклы. Большое разнообразие органических соединений связано также с существованием явления изомерии.
Органическое вещество — обзор
3.1.3 ОРГАНИЧЕСКИЙ СОСТАВ СОСТАВНЫХ ОТЛОЖЕНИЙ
Органическое вещество может иметь очень большое влияние на образование хлопьев грязи и стабильность морского дна, c.q. приливные зоны; последний более подробно рассматривается в главе 10. Органическое вещество состоит в основном из органических полимеров. Литература о взаимодействии между полимерами и коллоидами огромна, так как это важный вопрос, например, в обрабатывающей промышленности и сантехнике (например,г Берди, 2003; и Хантер, 2001). Однако литературы о роли органических полимеров в окружающей среде очень мало. Ван Леуссен (1988, 1994) дает краткий обзор литературы, доступной в то время.
Органическое вещество в иле состоит из твердых частиц (pom) и растворенного органического вещества (doc). Органическое вещество может происходить извне зоны отложения или образовываться в отложениях в результате биологических процессов. Органическое вещество аллохтона разлагается во время транспортировки и может состоять в основном из стойкого материала, такого как лигнин.Автохтонный органический материал используется и вырабатывается в метаболических процессах организмов. Образовавшийся органический материал вне организмов обозначается как eps (внеклеточные вещества).
Органическое вещество может происходить извне зоны отложения или образовываться в отложениях в результате биологических процессов. Органическое вещество аллохтона разлагается во время транспортировки и может состоять в основном из стойкого материала, такого как лигнин.Автохтонный органический материал используется и вырабатывается в метаболических процессах организмов. Образовавшийся органический материал вне организмов обозначается как eps (внеклеточные вещества).
Основными органическими веществами, встречающимися в морских илах, являются (Berner, 1980):
- •
Полисахариды и белки, состоящие из пептидов и аминокислот,
- •
Липиды, углеводороды, такие как целлюлоза, лигнин, состоящий из углеводороды алифатические и ароматические,
- •
Гуминовые кислоты.
Первую группу органических веществ можно отнести к флокулянтам, к второй группе относятся нейтральные, а к третьей группе относятся диспергенты (дефлокулянты). Земельный перегной содержит больше лигнина, в то время как морской гумус содержит больше аминокислот, пептидов и полисахаридов.
Земельный перегной содержит больше лигнина, в то время как морской гумус содержит больше аминокислот, пептидов и полисахаридов.
Полимеры встречаются в виде заряженных или нейтральных частиц. Заряженные частицы называются полиэлектролитами и не играют большой роли в естественной окружающей среде. С другой стороны, неионогенные полимеры очень важны.Например, полисахариды, которые продуцируются множеством организмов (бактериями, водорослями, фильтраторами и т. Д.), Относятся к классу неионных полимеров. Эти неионные полимеры могут адсорбироваться на частицы глины посредством трех процессов:
- •
силы Ван-дер-Ваальса,
- •
биполярных сил и
- •
водородных связей.
Биполярные силы намного сильнее, чем силы Ван-дер-Ваальса, и весьма эффективны, поскольку на взаимодействие частиц полимера и глины не влияет электростатическое отталкивание (например,грамм. Раздел 3.2.1), поскольку полимер в целом электрически нейтрален.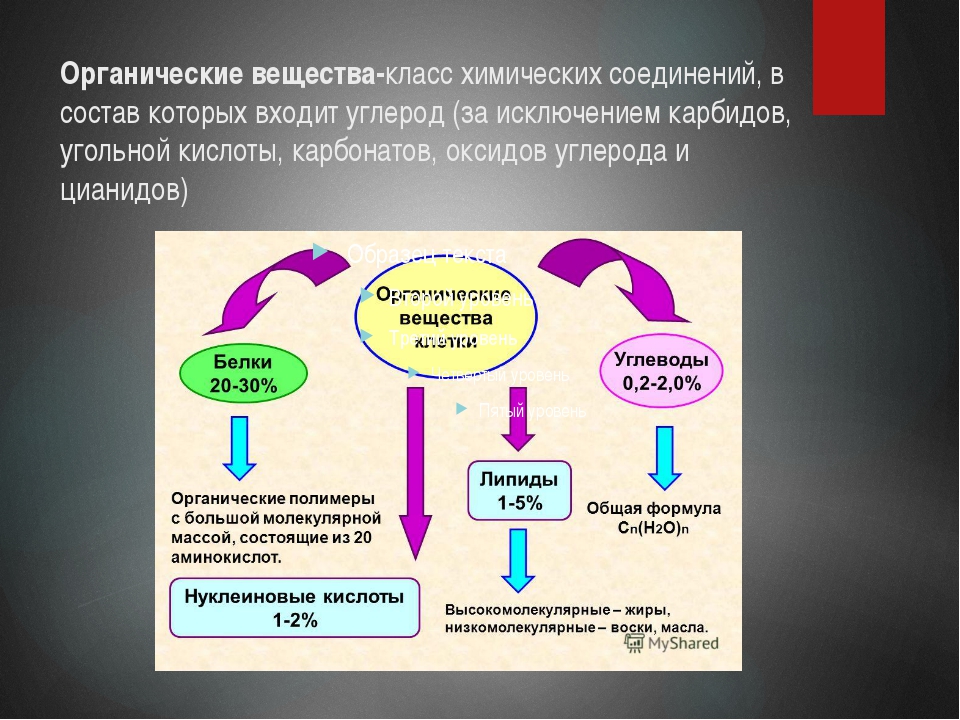 Длинная полимерная нить может прилипать к частице глины в нескольких местах, образуя так называемые петли и один или два хвоста, как показано на рис. 3.8 (например, Hunter, 2001). Когда другая частица глины прикрепляется к петлям и / или хвостам этой полимерной нити, образуется прочная пара частиц. Этот эффект известен как закупоривание и может привести к образованию крупных неорганических / органических хлопьев с прочностью от 10 до 100 раз больше, чем у чистого неорганического материала (Gregory, 1985).Поскольку вода биполярна, глино-полимерные структуры также могут связывать большие количества воды.
Длинная полимерная нить может прилипать к частице глины в нескольких местах, образуя так называемые петли и один или два хвоста, как показано на рис. 3.8 (например, Hunter, 2001). Когда другая частица глины прикрепляется к петлям и / или хвостам этой полимерной нити, образуется прочная пара частиц. Этот эффект известен как закупоривание и может привести к образованию крупных неорганических / органических хлопьев с прочностью от 10 до 100 раз больше, чем у чистого неорганического материала (Gregory, 1985).Поскольку вода биполярна, глино-полимерные структуры также могут связывать большие количества воды.
Рис. 3.8. Набросок полимера, адсорбированного на частице глины.
(заимствовано из Hunter, 2001)
Органический полимер, встречающийся в природе, часто является гетеродисперсным. Полимеры меньшего размера быстро прилипают к частицам глины, и существует меньше возможностей для прилипания более длинных нитей. В результате в этом случае полимеры не могут образовывать большие хлопья (Lyklema, 1988).
Органическое вещество часто содержит гуминовые кислоты с карбоксильными группами (cooh) и фенол-гидроксильными группами с плотностью заряда намного выше, чем у глинистых минералов (Hayes et al., 1990): 3–6 мэкв / г для гуминовых кислот и 0,01–0,2 мэкв / г для глинистых минералов (см. Таблицу 3.3). Карбоксильные группы могут легко образовывать водородные связи при pH = 8, что типично для морской среды. Однако эти связи быстро ослабевают, когда концентрация одновалентных ионов увеличивается, как в морской воде (Weaver, 1989). Следовательно, можно ожидать, что водородные связи не слишком важны в эстуариях и прибрежных морях.
Органический материал в толще воды обычно (частично) окислен. Однако после осаждения он будет восстанавливаться в последовательном порядке нитратом, марганцем, железом и сульфатом (Aller, 1982).Если эти восстановители исчерпаны, происходит анаэробная ферментация (см. Рис. 3.7) с образованием метана и диоксида углерода, что приводит к образованию газа в слое (см. Главу 11). Порядок восстановления определяется энергетическим каскадом, известным как «окислительно-восстановительная башня». Читателю отсылаем к Sigg and Stumm (1994) или Wiedemeyer and Schwamborn (1996) для получения более подробной информации. Обратите внимание, что временной масштаб химических процессов зависит как от скорости осаждения, так и от диффузии в слое.
Главу 11). Порядок восстановления определяется энергетическим каскадом, известным как «окислительно-восстановительная башня». Читателю отсылаем к Sigg and Stumm (1994) или Wiedemeyer and Schwamborn (1996) для получения более подробной информации. Обратите внимание, что временной масштаб химических процессов зависит как от скорости осаждения, так и от диффузии в слое.
Редукция происходит в верхней части пласта, т.е.е. от нескольких миллиметров до не более 1 см. Это изображено на рис. 3.9 по Фенчелу и Ридлу (1970). Ближе к поверхности образуется окисленный слой, в котором присутствует свободный кислород, хотя его количество ниже в слое уменьшается. Этот слой обычно желтый, желто-коричневый или желто-охристый из-за присутствия трехвалентного железа. Другие цвета обнаруживаются из-за различий в кристаллической структуре и следов других компонентов. Глубже в восстановленном слое осадок имеет черный цвет из-за присутствия сульфида железа (FeS).Другие типичные цвета: ржавчина (Fe 2 O 3 ) темно-коричневая, а болотная руда (Fe (OH) 3 ) красно-коричневая.
Рис. 3.9. Характерные профили различных химических параметров в верхней части пласта.
(Fenchel and Riedl, 1970)
Состояние органического материала в слое характеризуется окислительно-восстановительным потенциалом E h и pH (см. Рис. 3.9). Отрицательные значения E h характерны для донных отложений, богатых органическим веществом и состоящих в основном из мелких отложений.Таким образом, ожидается, что в отложениях связных отложений, которые, как правило, содержат (некоторые) органические соединения, положительные значения E h будут обнаружены только в небольшом слое вблизи поверхности слоя.
Процессы обмена водного дна в морской среде в значительной степени регулируются эродируемостью верхних нескольких миллиметров на см слоя (например, Глава 9). Следовательно, градиенты химико-биологического состава, изображенные на рис. 3.9, очень важны, поскольку достоверность почвы в значительной степени зависит от ее химико-биологического состава (главы 9 и 10).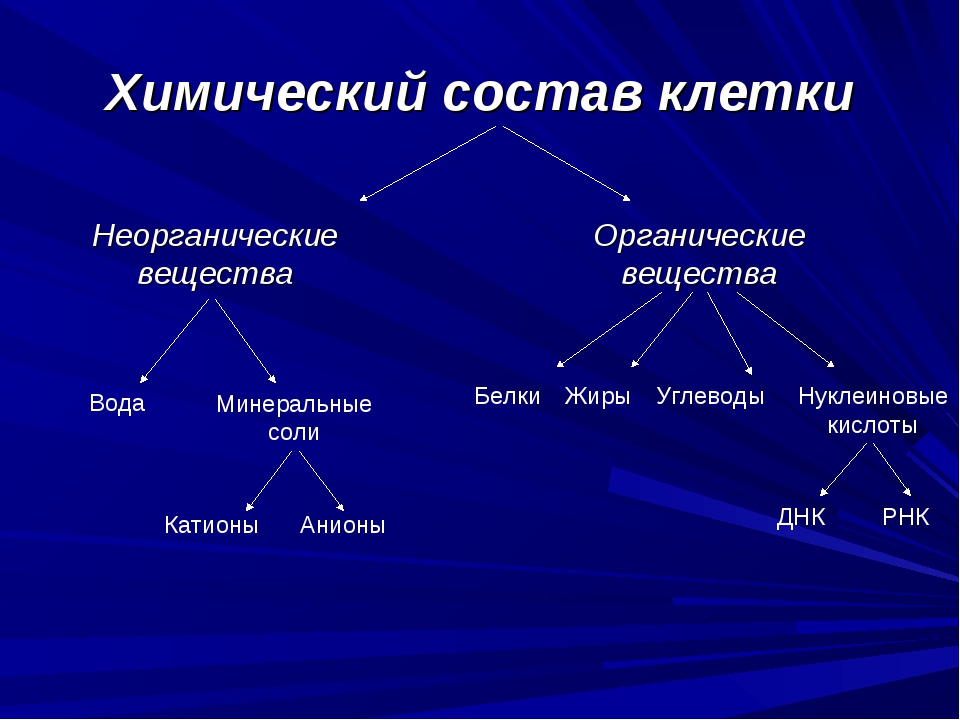
Какие пять распространенных веществ считаются органическими химическими веществами?
Обновлено 25 апреля 2017 г.
Автор: Дэвид Х. Нгуен, Ph.D.
Органические химические вещества — это молекулы, содержащие углерод, водород, кислород, азот, фосфор и серу. Не все органические молекулы должны иметь все шесть этих элементов, но они должны иметь как минимум углерод и водород. Органические химические вещества составляют обычные вещества, которые можно найти в доме. Оливковое масло, используемое для приготовления пищи, является органическим химическим веществом.Так же как и спирт этанол, который содержится в дезинфицирующих средствах для рук и в вине. Повара добавляют в пищу химическое вещество под названием глутамат натрия, чтобы сделать ее вкуснее. Сахар — это органическая молекула. Кофеин в кофе заставляет людей бодрствовать.
Оливковое масло
Кулинарное масло, такое как оливковое масло и кукурузное масло, представляет собой органические молекулы, известные как жирные кислоты. Жирные кислоты представляют собой длинные цепочки атомов углерода, длина которых может составлять от 10 до 30 атомов углерода. Атом углерода на одном конце присоединен к атомам кислорода, но остальные атомы углерода в цепи присоединены к атомам водорода.Оливковое масло является жидкостью при комнатной температуре, потому что его цепь имеет перегиб посередине, из-за чего молекула изгибается в форме буквы L. Если бы он был прямым, то при комнатной температуре был бы твердым, как масло.
Жирные кислоты представляют собой длинные цепочки атомов углерода, длина которых может составлять от 10 до 30 атомов углерода. Атом углерода на одном конце присоединен к атомам кислорода, но остальные атомы углерода в цепи присоединены к атомам водорода.Оливковое масло является жидкостью при комнатной температуре, потому что его цепь имеет перегиб посередине, из-за чего молекула изгибается в форме буквы L. Если бы он был прямым, то при комнатной температуре был бы твердым, как масло.
Этанол
Этанол — это обычный спирт, который можно найти в домашних условиях. Это алкоголь в пиве, вине и других алкогольных напитках. Он состоит из двух атомов углерода, одного атома кислорода и шести атомов водорода. Спирт легко испаряется при комнатной температуре, поэтому вы можете почувствовать запах алкоголя, когда бутылка открыта.В высоких концентрациях этанол является дезинфицирующим средством, убивающим бактерии. Его часто используют в качестве дезинфицирующего средства для рук при смешивании с водой для приготовления раствора, состоящего на 70 процентов из этанола и на 30 процентов из воды.
MSG
Глутамат натрия (MSG) — это органическое соединение, которое добавляют в пищу для улучшения вкуса. Он часто используется в китайской еде, но также встречается в консервированных овощах и консервированных супах. Есть некоторые опасения, что глутамат натрия может вызвать проблемы со здоровьем, такие как головные боли, тошнота и аномальная сердечная деятельность, но исследования не нашли определенных доказательств того, что это так.MSG состоит из глутамата аминокислоты и натриевой соли. Аминокислоты — это строительные блоки, которые клетки используют для производства белков.
Сахар с кофе?
Кофе — любимый напиток многих людей, поскольку в нем есть химическое вещество, которое их будит и заставляет бодрствовать. Это химическое вещество называется кофеином. Форма кофеина — два многоугольных кольца, которые имеют общую сторону. Один из них представляет собой шестиугольник с шестью углами, а другой — пятиугольник с пятью углами. В углах расположены атомы углерода или азота.Столовый сахар, который называют сахарозой, часто добавляют в кофе в качестве подсластителя. Сахароза — это органическая молекула, которая на самом деле состоит из двух более мелких сахаров, которые были соединены вместе, глюкозы и фруктозы.
В углах расположены атомы углерода или азота.Столовый сахар, который называют сахарозой, часто добавляют в кофе в качестве подсластителя. Сахароза — это органическая молекула, которая на самом деле состоит из двух более мелких сахаров, которые были соединены вместе, глюкозы и фруктозы.
Органические соединения
Химические соединения живых существ известны как органических соединений из-за их связи с организмами и потому, что они являются углеродсодержащими соединениями. Органические соединения, которые представляют собой соединения, связанные с жизненными процессами, являются предметом органической химии.Среди многочисленных типов органических соединений во всем живом есть четыре основные категории: углеводы, липиды, белки и нуклеиновые кислоты.
Углеводы
Почти все организмы используют углеводов в качестве источников энергии. Кроме того, некоторые углеводы служат конструкционными материалами. Углеводы — это молекулы, состоящие из углерода, водорода и кислорода; отношение атомов водорода к атомам кислорода и углерода составляет 2: 1.
Простые углеводы, обычно называемые сахарами , могут быть моносахаридами, , если они состоят из одиночных молекул, или дисахаридами, , если они состоят из двух молекул.Наиболее важным моносахаридом является глюкоза, углевод с молекулярной формулой C 6 H 12 O 6 . Глюкоза — это основная форма топлива для живых существ. В многоклеточных организмах он растворим и транспортируется жидкостями организма ко всем клеткам, где метаболизируется с высвобождением своей энергии. Глюкоза является исходным материалом для клеточного дыхания и основным продуктом фотосинтеза (см. Главы 5 и 6).
Три важных дисахарида также содержатся в живых организмах: мальтоза, сахароза и лактоза.Мальтоза представляет собой комбинацию двух ковалентно связанных единиц глюкозы. Сахароза столового сахара образуется путем связывания глюкозы с другим моносахаридом, называемым фруктозой. (Рисунок 2-2 показывает, что при синтезе сахарозы образуется молекула воды. Поэтому этот процесс называется реакцией дегидратации . Обратный процесс — это гидролиз , процесс, в котором молекула расщепляется и добавляется вода.) Лактоза состоит из единиц глюкозы и галактозы.
Поэтому этот процесс называется реакцией дегидратации . Обратный процесс — это гидролиз , процесс, в котором молекула расщепляется и добавляется вода.) Лактоза состоит из единиц глюкозы и галактозы.
Рисунок 2-2 Молекулы глюкозы и фруктозы объединяются, образуя дисахарид сахарозу.
Сложные углеводы известны как полисахариды . Полисахариды образуются путем связывания бесчисленных моносахаридов. Среди наиболее важных полисахаридов — крахмал, который состоит из сотен или тысяч единиц глюкозы, связанных друг с другом. Крахмал служит формой хранения углеводов. Большая часть населения мира удовлетворяет свои потребности в энергии с помощью крахмала в виде риса, пшеницы, кукурузы и картофеля.
Два других важных полисахарида — это гликоген и целлюлоза. Гликоген также состоит из тысяч единиц глюкозы, но эти единицы связаны другим образом, чем в крахмале. Гликоген — это форма, в которой глюкоза хранится в печени человека. Целлюлоза используется в основном как структурный углевод. Он также состоит из единиц глюкозы, но единицы не могут высвобождаться одна из другой, за исключением нескольких видов организмов. Древесина состоит в основном из целлюлозы, как и стенки растительных клеток. Хлопчатобумажная ткань и бумага — это товарные целлюлозные продукты.
Целлюлоза используется в основном как структурный углевод. Он также состоит из единиц глюкозы, но единицы не могут высвобождаться одна из другой, за исключением нескольких видов организмов. Древесина состоит в основном из целлюлозы, как и стенки растительных клеток. Хлопчатобумажная ткань и бумага — это товарные целлюлозные продукты.
Липиды
Липиды — это органические молекулы, состоящие из атомов углерода, водорода и кислорода. Отношение атомов водорода к атомам кислорода в липидах намного выше, чем в углеводах. Липиды включают стероиды (материал, из которого состоят многие гормоны), воски и 90-115 жиров.
Молекулы жира состоят из молекулы глицерина и одной, двух или трех молекул жирных кислот (см. Рис. 2-3). Молекула глицерина содержит три гидроксильные (–ОН) группы.Жирная кислота представляет собой длинную цепочку атомов углерода (от 4 до 24) с карбоксильной (–COOH) группой на одном конце. Все жирные кислоты в жире могут быть одинаковыми или разными. Они связаны с молекулой глицерина в процессе удаления воды.
Все жирные кислоты в жире могут быть одинаковыми или разными. Они связаны с молекулой глицерина в процессе удаления воды.
Некоторые жирные кислоты имеют в своих молекулах одну или несколько двойных связей. Жиры, в состав которых входят эти молекулы, представляют собой ненасыщенных жиров. Другие жирные кислоты не имеют двойных связей. Жиры, в состав которых входят эти жирные кислоты, представляют собой насыщенных жиров. В большинстве случаев, связанных со здоровьем человека, потребление ненасыщенных жиров предпочтительнее насыщенных жиров.
Жиры, хранящиеся в клетках, обычно образуют прозрачные масляные капли, называемые глобулами , потому что жиры не растворяются в воде. Растения часто хранят жиры в своих семенах, а животные — в больших прозрачных шариках в клетках жировой ткани. Жиры в жировой ткани содержат много концентрированной энергии. Следовательно, они служат резервным источником энергии для организма.Фермент липаза расщепляет жиры на жирные кислоты и глицерин в пищеварительной системе человека.
Рис. 2-3 Молекула жира создается путем объединения молекулы глицерина с тремя молекулами жирных кислот. (Две насыщенные жирные кислоты и одна ненасыщенная жирная кислота показаны для сравнения.) Сконструированная молекула находится внизу.
Белки
Белки, среди самых сложных из всех органических соединений, состоят из аминокислот (см. Рис. 2-4), которые содержат атомы углерода, водорода, кислорода и азота.Некоторые аминокислоты также содержат атомы серы, фосфора или других микроэлементов, таких как железо или медь.
Рисунок 2-4 Структура и химический состав аминокислот. Когда две аминокислоты соединяются в дипептид, –OH одной аминокислоты удаляется, а –H второй удаляется. Итак, вода удалена. Дипептидная связь (справа) образует соединение аминокислот вместе.
Многие белки огромны и чрезвычайно сложны. Однако все белки состоят из длинных цепочек относительно простых аминокислот. Есть 20 видов аминокислот. Каждая аминокислота (см. Левую иллюстрацию на рис. 2-4) имеет амино (–NH 2 ) группу, карбоксильную (–COOH) группу и группу атомов, называемую –R группой (где R обозначает радикал ). Аминокислоты различаются в зависимости от природы группы –R, как показано на средней иллюстрации рисунка 2-4. Примерами аминокислот являются аланин, валин, глутаминовая кислота, триптофан, тирозин и гистидин.
Есть 20 видов аминокислот. Каждая аминокислота (см. Левую иллюстрацию на рис. 2-4) имеет амино (–NH 2 ) группу, карбоксильную (–COOH) группу и группу атомов, называемую –R группой (где R обозначает радикал ). Аминокислоты различаются в зависимости от природы группы –R, как показано на средней иллюстрации рисунка 2-4. Примерами аминокислот являются аланин, валин, глутаминовая кислота, триптофан, тирозин и гистидин.
Удаление молекул воды связывает аминокислоты с образованием белка.Процесс называется дегидратационным синтезом , и побочным продуктом синтеза является вода. Связи между аминокислотами составляют пептидных связей, и небольшие белки, часто называемые пептидами .
Все живые существа зависят от белков. Белки — это основные молекулы, из которых построены живые существа. Некоторые белки растворены или взвешены в водянистом веществе клеток, а другие включены в различные структуры клеток.Белки также являются поддерживающими и укрепляющими материалами в тканях вне клеток. Кости, хрящи, сухожилия и связки состоят из белков.
Кости, хрящи, сухожилия и связки состоят из белков.
Одна из важнейших функций белков — это фермент. Ферменты катализируют химические реакции, происходящие в клетках. Они не расходуются в реакции; скорее, они остаются доступными для катализа последующих реакций.
Каждый вид производит белки, уникальные для этого вида. Информация для синтеза уникальных белков находится в ядре клетки.Так называемый генетический код определяет аминокислотную последовательность в белках. Следовательно, генетический код регулирует химию, происходящую внутри клетки. Белки также могут служить резервным источником энергии для клетки. Когда аминогруппа удаляется из аминокислоты, полученное соединение богато энергией.
Нуклеиновые кислоты
Подобно белкам, нуклеиновых кислот представляют собой очень большие молекулы. Нуклеиновые кислоты состоят из более мелких единиц, называемых 90–115 нуклеотидами. Каждый нуклеотид содержит молекулу углевода (сахар), фосфатную группу и азотсодержащую молекулу, которая в силу своих свойств является азотистым основанием .
У живых организмов есть две важные нуклеиновые кислоты. Один тип — это дезоксирибонуклеиновая кислота, или ДНК. Другой — это рибонуклеиновая кислота, или РНК. ДНК находится в основном в ядре клетки, в то время как РНК обнаруживается как в ядре, так и в цитоплазме , — полужидкое вещество, составляющее объем клетки (см. Главу 3).
ДНК и РНК
отличаются друг от друга по своим компонентам. ДНК содержит углевод дезоксирибозу, а РНК — рибозу. Кроме того, ДНК содержит тимин, а РНК — урацил. Структура ДНК и ее значение в жизни клеток рассматриваются в главе 10.
Разберитесь между органическими и неорганическими веществами
Слово «органический» в химии означает нечто совершенно иное, чем когда вы говорите о продуктах и продуктах питания.Органические соединения и неорганические соединения составляют основу химии.
Основное различие между органическими и неорганическими соединениями состоит в том, что органические соединения всегда содержат углерод, в то время как большинство неорганических соединений не содержат углерода.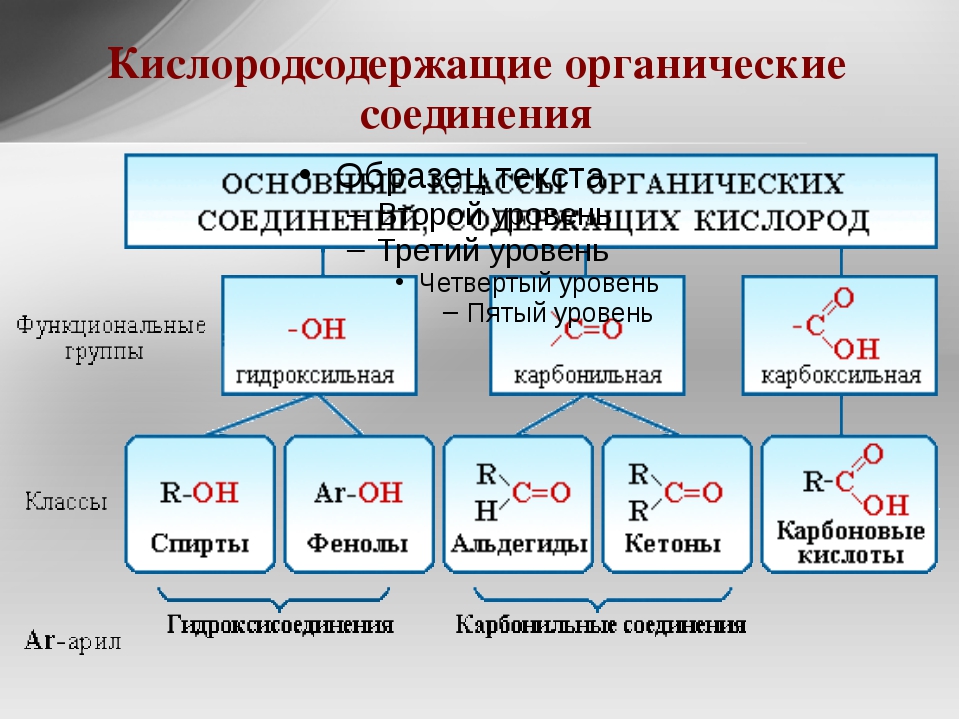
Кроме того, почти все органические соединения содержат связи углерод-водород или C-H. Обратите внимание, что , содержащее углерод, недостаточно для того, чтобы соединение считалось органическим. Ищите и углерод, и водород.
Вы знали?
Органическая и неорганическая химия — две основные дисциплины химии.Химик-органик изучает органические молекулы и реакции, а неорганическая химия занимается неорганическими реакциями.
Примеры органических соединений или молекул
Молекулы, связанные с живыми организмами, являются органическими. К ним относятся нуклеиновые кислоты, жиры, сахара, белки, ферменты и углеводородное топливо. Все органические молекулы содержат углерод, почти все содержат водород, а многие также содержат кислород.
- ДНК
- столовый сахар или сахароза, C 12 H 22 O 11
- бензол, C 6 H 6
- метан, CH 4
- этанол или зерновой спирт, C 2 H 6 O
Примеры неорганических соединений
Неорганические вещества включают соли, металлы, вещества, состоящие из отдельных элементов, и любые другие соединения, не содержащие углерод, связанный с водородом. Некоторые неорганические молекулы действительно содержат углерод.
Некоторые неорганические молекулы действительно содержат углерод.
- поваренная соль или хлорид натрия, NaCl
- диоксид углерода, CO 2
- алмаз (чистый углерод)
- серебро
- сера
Органические соединения без связей C-H
Некоторые органические соединения не содержат углерод-водородных связей. Примеры этих исключений включают
- четыреххлористый углерод (CCl 4 )
- мочевина [CO (NH 2 ) 2 ]
Органические соединения и жизнь
В то время как большинство органических соединений, встречающихся в химии, производятся живыми организмами, молекулы могут образовываться посредством других процессов.
Например, когда ученые говорят об органических молекулах, обнаруженных на Плутоне, это не означает, что в мире есть инопланетяне. Солнечное излучение может дать энергию для производства органических соединений из неорганических углеродных соединений.
органических соединений — биология, видео от Brightstorm
Органические соединения — это соединения, состоящие из углерода, водорода и часто кислорода или азота. Органические соединения названы так, потому что они связаны с живыми организмами.Несколько важных типов органических соединений включают углеводы, липиды, нуклеиновые кислоты и белки.
Одна из основных идей в биологической химии — это идея органических соединений. Теперь название «органический» буквально означает «живой». Ученые выяснили, что многие молекулы живых существ на самом деле основаны на углероде.Итак, теперь мы называем эти углеродные молекулы органическими молекулами.
Почему так много используется углерод? Углерод — очень полезный атом, потому что он может образовывать четыре связи, и практически большинство связей, которые он образует, ковалентны, потому что он довольно сильный, но не слишком сильный с точки зрения его электоральной негативности. Итак, в этом примере здесь он связан с четырьмя разными элементами, и каждая из этих связей ковалентна или полярно-ковалентна.
Итак, в этом примере здесь он связан с четырьмя разными элементами, и каждая из этих связей ковалентна или полярно-ковалентна.
В большой группе органических соединений, пожалуй, наиболее полезными из них являются органические полимеры.Теперь я сразу перейду к тому, что такое полимеры, но четыре основные группы — это липиды, которые представляют собой такие вещества, как жиры и воски. Есть белки, из которых состоят такие вещи, как ваши мышцы, волосы, ногти, передняя часть глаза. Углеводы, из которых состоят сахара и крахмалы, которые мы любим есть, и нуклеиновые кислоты, из которых состоят очень важные молекулы, называемые ДНК и РНК.
Итак, полимер, как я упоминал ранее, представляет собой длинную молекулу, состоящую из группы более мелких молекул, называемых мономерами.Это похоже на то, как поезд на самом деле представляет собой длинную цепочку сцепленных вместе железнодорожных вагонов. Мы называем отдельные вагоны из полимерных мономеров, как я уже сказал. И внутри липидов у них есть разные мономеры, тогда есть белки, которые имеют разные мономеры, углеводы и нуклеиновые кислоты.
Теперь я собираюсь продолжить и посмотреть, как мы можем связать эти мономеры вместе? Вот я нарисовал пару мономеров. Это будут моносахариды, которые представляют собой отдельные мономеры углеводов, которые, когда вы связываете их вместе, два моносахарида образуют дисахарид.Вы начинаете получать больше двух, вам все равно, сколько их, поэтому вы просто называете их многими из сахаридов или полисахаридов. Итак, вот один моносахарид или сахар, вот еще один моносахарид. Чтобы собрать их вместе, я собираюсь собрать группу OH отсюда. И я просто отложу это в сторону. Теперь здесь есть связь, которая открыта для присоединения к этому кислороду, но у него уже есть две связи, которые обычно необходимы. Так что я просто сниму этот водород, и теперь этот кислород легко свяжется с этим углеродом, и теперь у меня есть дисахарид или диммер в целом.Теперь вы заметили, что я вытащил из него воду. Как мы называем этот процесс? Ну, как вы это называете, когда с чего-то удаляете воду? Это называется обезвоживанием.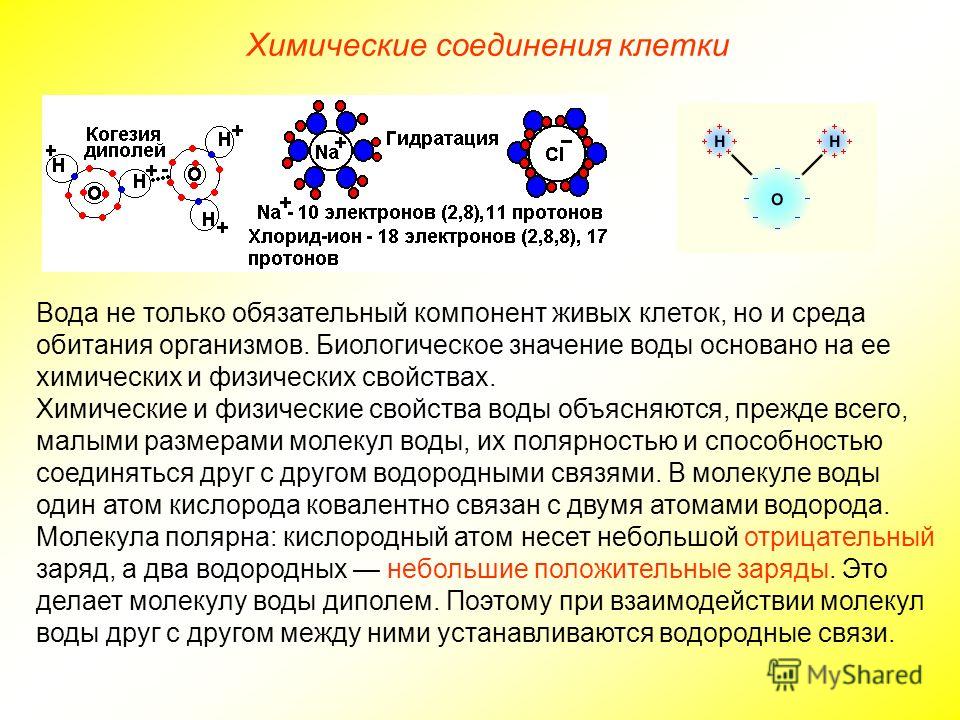 Эта ручка умирает, до свидания. Обезвоживание, поэтому мы слили воду. А зачем мы вытаскивали воду? Мы вытаскивали воду, чтобы что-то сделать. Теперь ученые не любят использовать термин «сделать», поэтому вместо этого они используют термин «синтез», потому что он звучит круче и дороже. Это называется «синтез обезвоживания», хорошо? И все ваши органические полимеры производятся с помощью одного и того же основного процесса.Вы извлекаете водород из одного мономера, вы извлекаете группу ОН из другого, и они соединяются вместе вот так. Итак, как мне запустить это в обратном порядке?
Эта ручка умирает, до свидания. Обезвоживание, поэтому мы слили воду. А зачем мы вытаскивали воду? Мы вытаскивали воду, чтобы что-то сделать. Теперь ученые не любят использовать термин «сделать», поэтому вместо этого они используют термин «синтез», потому что он звучит круче и дороже. Это называется «синтез обезвоживания», хорошо? И все ваши органические полимеры производятся с помощью одного и того же основного процесса.Вы извлекаете водород из одного мономера, вы извлекаете группу ОН из другого, и они соединяются вместе вот так. Итак, как мне запустить это в обратном порядке?
Ну, помните, у меня раньше была эта молекула воды. Если бы я только мог сломать это и положить туда водород, позвольте мне сделать это. Я, нет, позволь мне заключить здесь действительно долгую связь. Итак, я разорвал это, это означает, что эта связь здесь разорвется, но этот углерод сейчас нестабилен. Что, если я добавлю это туда. Вот и все. Что мне нужно было сделать, чтобы это произошло? Пришлось разбить эту воду пополам. Какое слово правила означает воду, гидро, и есть еще одно слово правила, называемое lys, которое означает разрыв или расщепление. Уберите их в сторону, и я просто превратил это в название процесса, которое называется «гидролиз». Итак, гидролиз — это то, как нам снова разделить наши полимеры на мономеры, с которых мы начали. А это органические молекулы.
Какое слово правила означает воду, гидро, и есть еще одно слово правила, называемое lys, которое означает разрыв или расщепление. Уберите их в сторону, и я просто превратил это в название процесса, которое называется «гидролиз». Итак, гидролиз — это то, как нам снова разделить наши полимеры на мономеры, с которых мы начали. А это органические молекулы.
Примеры органических соединений
Органические соединения
Органические соединения — это просто любая молекула, содержащая атомы углерода.Некоторые определения также включают необходимость содержать атомы водорода, поскольку углерод и водород являются компонентами, необходимыми для живых существ. Это определение справедливо для молекул, независимо от того, в каком состоянии вещества они находятся. Исторически существует несколько углеродсодержащих молекул, таких как карбиды, которые не считались органическими.
Целая область науки, также известная как органическая химия, развивалась для изучения углеродсодержащих веществ. Органическая химия на самом деле родилась из очень старого, еще в первом веке, понимания первопричин и требований жизни, называемого «витализмом».«
Органическая химия на самом деле родилась из очень старого, еще в первом веке, понимания первопричин и требований жизни, называемого «витализмом».«
Примеры органических соединений:
1. Натуральное против синтетического
Некоторые органические соединения встречаются в естественных условиях в растениях и животных, а другие создаются. Ученые далее классифицировали тот факт, что некоторые синтетические органические соединения — это именно то, что, как вы могли подумать, означает это слово: созданные искусственно, например, в лабораторных условиях. Но исследователи также обнаружили, что некоторые синтетические органические соединения производятся в качестве побочного продукта внутри растений или животных.Они по-прежнему являются органическими соединениями, потому что содержат углерод, но они также остаются синтетическими, поскольку «производятся» организмом. Одним из примеров может быть метан, так как это побочный продукт пищеварения.
2. Сахариды
Существует несколько основных типов сахаридов — моносахариды, дисахариды и полисахариды, и это лишь некоторые из них, — и они представляют собой органические соединения, состоящие из углеводов и цепочек простых сахаров.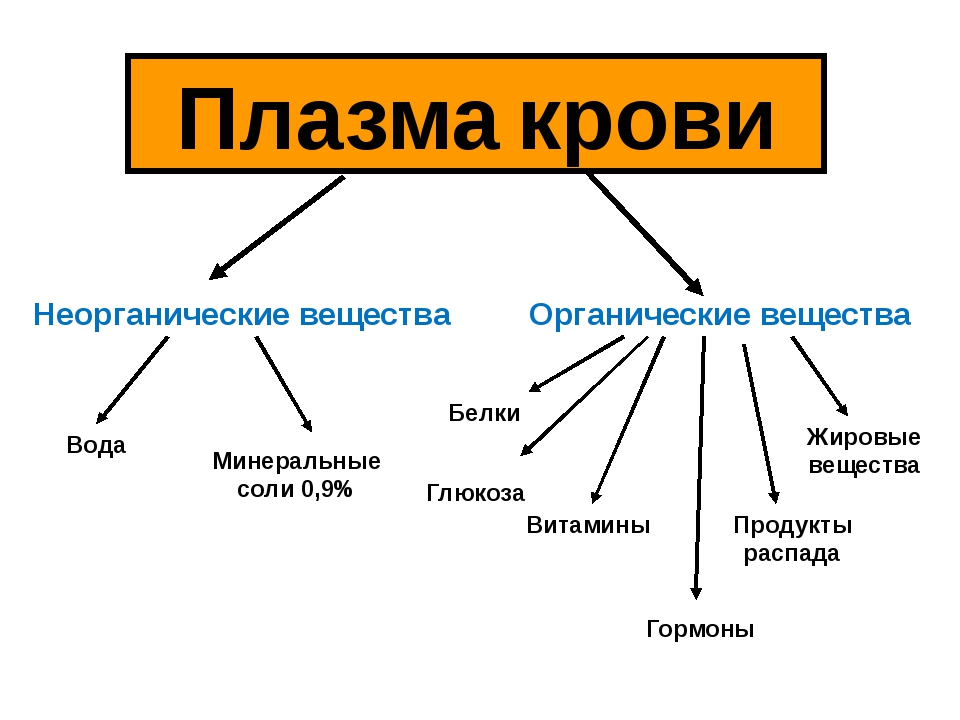 Некоторые из них включают целлюлозу, карбоксиметилцеллюлозу, гемицеллюлозу, арабиноксилан, сахарозу, мальтозу, лактозу, фруктозу, галактозу, глюкозу и рибозу.
Некоторые из них включают целлюлозу, карбоксиметилцеллюлозу, гемицеллюлозу, арабиноксилан, сахарозу, мальтозу, лактозу, фруктозу, галактозу, глюкозу и рибозу.
3. Липиды
Липиды классифицируются как органические соединения из-за присутствия в их составе молекул углерода. Липиды — это жирные или воскообразные вещества, которые естественным образом вырабатываются в клетках растений и животных и выполняют множество функций. Эти функции включают создание защитного слоя на чувствительных участках, таких как покрытие снаружи листьев или слуховых проходов человека, а также в транспортировке веществ по клетке. Некоторые из наиболее известных липидов — это ненасыщенные и насыщенные жиры, транс-жиры и глицериды, хотя их гораздо больше.
4. Другие органические соединения
Есть много других категорий органических соединений, включая белки, гормоны, такие как эстроген, клеточные компоненты, такие как рецепторы Т-клеток, различные спирты и сахарные спирты и многие другие.
Свойства органических соединений
Сравнение органических соединений и неорганических соединений
Тест по клеточным функциям органических соединений
Примеры соединений
Примеры неорганических соединений
Насыщенные и ненасыщенные углеводороды
Примеры углеводородов
Фактов органической химии
Примеры: грамматические и научные примеры для детей
Что такое органическое соединение? [Видео]
Органические соединения
Привет, и добро пожаловать в это видео о органических и неорганических соединениях.Сегодня мы рассмотрим как исторические, так и современные определения и попутно представим несколько примеров каждого из них.
Первоначальная классификация органических и неорганических соединений была сделана много веков назад, но с тех пор изменилась. Испытывая трепет перед живыми организмами, ранние ученые предположили, что между живыми и неживыми существами должна быть фундаментальная разница. Это было основано на теории витализма , которая утверждала, что живые организмы приводятся в движение жизненной силой, которая делает их по своей сути отличными от их неодушевленных собратьев.Таким образом, ученые-виталисты классифицировали химические соединения живых организмов как органические, а соединения неживых вещей как неорганические. Считая, что люди не могут создавать или манипулировать жизненной силой живых организмов, химики считали невозможным синтезировать органические вещества из безжизненных неорганических соединений.
Это было основано на теории витализма , которая утверждала, что живые организмы приводятся в движение жизненной силой, которая делает их по своей сути отличными от их неодушевленных собратьев.Таким образом, ученые-виталисты классифицировали химические соединения живых организмов как органические, а соединения неживых вещей как неорганические. Считая, что люди не могут создавать или манипулировать жизненной силой живых организмов, химики считали невозможным синтезировать органические вещества из безжизненных неорганических соединений.
Лишь в начале 1800-х годов химики развенчали эту виталистическую теорию. Фридрих Велер синтезировал мочевину, основное азотсодержащее соединение в моче и, следовательно, органическое соединение, используя цианат калия и хлорид аммония, два неорганических соединения.При этом он продемонстрировал, что никакая жизненная сила не отделяет органические соединения от неорганических, и что последние могут быть использованы для создания первых.
Однако, хотя витализм был полностью опровергнут, номенклатура органического и неорганического продолжает жить в современной химии, но с обновленными определениями.
В широком смысле, по сегодняшнему определению, органические соединения — это вещества на основе углерода . На самом деле это соответствует первоначальному виталистскому определению, потому что земные формы жизни фактически основаны на углероде.Следовательно, большинство химических соединений в организмах являются органическими по сегодняшнему определению. Например, ДНК, , белки, , жиры и углеводы — все это органические соединения.
Однако, в отличие от определения виталистов, органические соединения не обязательно должны быть получены из живого организма, но могут быть синтезированы в лаборатории. Например, нейлон, полезный и популярный полимер, представляет собой синтетическое органическое соединение.
От простых углеродных цепочек, называемых алканами , насыщенных только водородом, до длинных сложных молекул, наполненных различными функциональными группами, есть миллионы органических соединений.Функциональные группы состоят из элементов в правом верхнем углу периодической таблицы (кислород, азот, сера, фосфор, кремний и галогены).
Органические соединения обычно представляют собой молекулярные твердые вещества, что означает, что они образуют автономные молекулярные единицы за счет ковалентной связи. В твердой и жидкой фазах эти звенья удерживаются вместе за счет слабых межмолекулярных взаимодействий, что приводит к более низким температурам плавления и кипения по сравнению со многими неорганическими соединениями.
Неорганические соединения обычно можно определить как соединения, не содержащие углерода.Очевидно, что это большая часть таблицы Менделеева, поэтому физические характеристики неорганических соединений сильно различаются, и их трудно резюмировать. Мы ежедневно сталкиваемся с множеством неорганических соединений, например, ионных соединений, таких как хлорид натрия; кварц в ваших часах — диоксид кремния; и вода, наиболее известное неорганическое соединение.
Может быть, в этот момент вы думаете про себя: «Ну, если в соединении есть углерод, я буду считать его органическим». К сожалению, хотя все органические соединения содержат углерод, не все углеродсодержащие соединения являются органическими.
К сожалению, хотя все органические соединения содержат углерод, не все углеродсодержащие соединения являются органическими.
Например, сплавы, содержащие углерод, считаются неорганическими. Сюда входит сталь, сплав железа и углерода. А аллотропы углерода, такие как графит и алмаз, не считаются органическими соединениями, потому что они просто один элемент, а не соединение элементов. Кроме того, простые оксиды, такие как монооксид углерода и диоксид углерода, также часто определяют как неорганические. На самом деле это может быть пережитком витализма, который считал углекислый газ неорганическим, потому что он был произведен из неодушевленных источников, таких как вулканы и минералы.
Таким образом, более строгое и, возможно, более полезное определение органических соединений требует, чтобы соединение имело углерод-водородные связи. Хотя даже у этого определения есть заметные исключения, такие как мочевина и четыреххлористый углерод, которые не содержат углерод-водородных связей, но считаются органическими.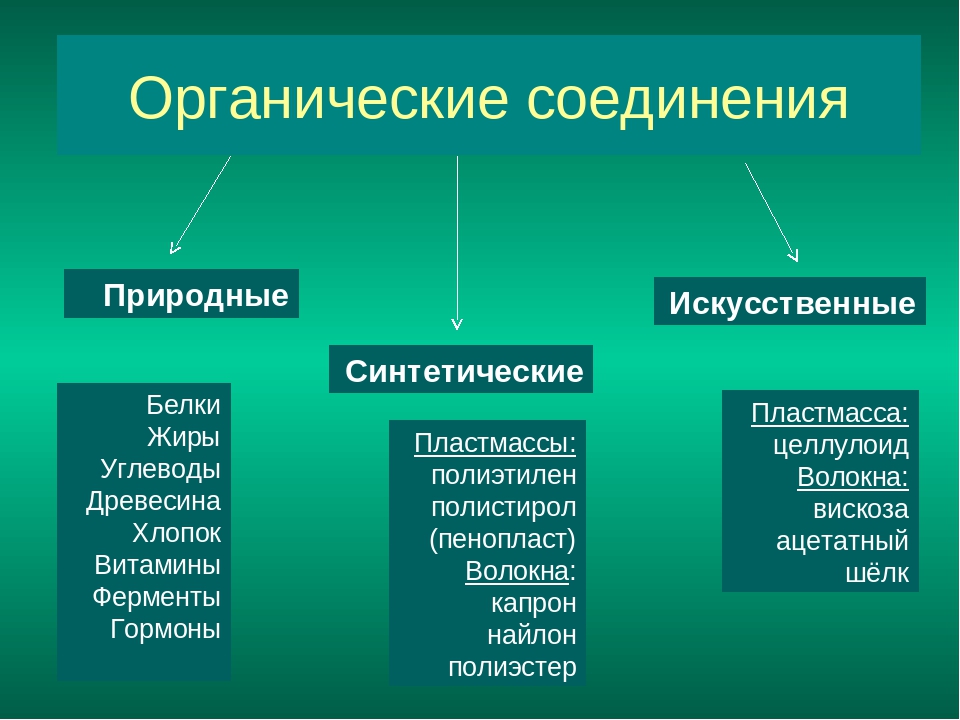 Кроме того, некоторые органические соединения образуют комплексы с металлами, которые обычно находятся в центре внимания химиков-неоргаников. Это дает начало промежуточным классификациям, таким как металлоорганические соединения и металлопротеины.Здесь, в геме, металлопротеине в гемоглобине, вы можете увидеть органическую структуру, сосредоточенную вокруг атома железа.
Кроме того, некоторые органические соединения образуют комплексы с металлами, которые обычно находятся в центре внимания химиков-неоргаников. Это дает начало промежуточным классификациям, таким как металлоорганические соединения и металлопротеины.Здесь, в геме, металлопротеине в гемоглобине, вы можете увидеть органическую структуру, сосредоточенную вокруг атома железа.
Если все это кажется произвольным, это понятно, но на самом деле не существует идеальных определений для органических и неорганических соединений. Даже ИЮПАК не дает конкретных определений.
Однако, несмотря на это, все же практично признать разницу между органическими и неорганическими веществами. Химия органических и неорганических соединений настолько различна, что имеет смысл преподавать их отдельно, а химикам — специализироваться на одном или другом.Например, поведение более крупных атомов металла может сильно отличаться от поведения более мелких атомов в органических соединениях, а синтетические методы, используемые для создания сложных органических молекул, требуют глубоких знаний, которые могут не иметь отношения к химикам-неорганикам.
