Содержание
Кислотные оксиды — получение и химические свойства » HimEge.ru
Кислотными называются оксиды, взаимодействующие с основаниями (или основными оксидами) с образованием солей.
Кислотные оксиды представляют собой оксиды неметаллов или переходных металлов в высоких степенях окисления, им соответствуют кислотные гидроксиды, обладающие свойствами кислот.
Например, S+6O3 → H2S+6O4; N2+5O5 → HN+5O3, причем степень окисления элемента не изменяется при переходе от оксида к гидроксиду.
Получение кислотных оксидов
1. Окисление кислородом
4Р + 5О2 = 2Р2О5,
2. Горение сложных веществ
СН4 + 2О2 → СО2 + 2 Н2О;
2ZnS + 3O2 = 2ZnO + 2SO2,
Химические свойства кислотных оксидов
1. Большинство кислотных оксидов непосредственно взаимодействуют с водой с образованием кислот:
SO3 + H2O = H2SO4,
CO2 + H2O = H2CO3,
P2O5 + H2O = 2HPO3,
P2O5 + 3H2O = 2H3PO4.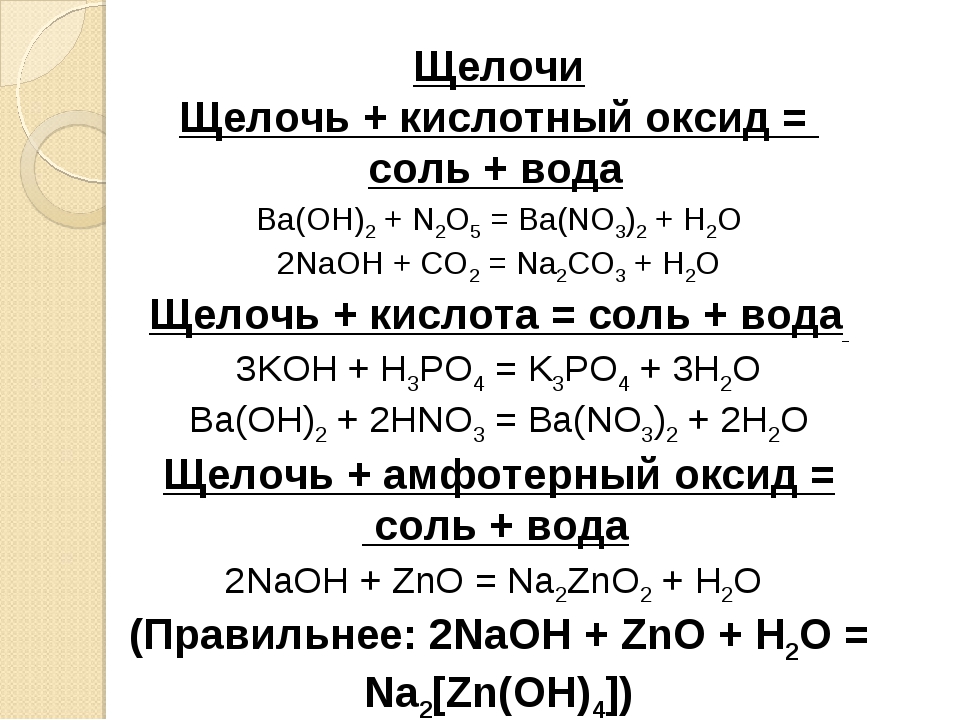
2. Наиболее типичными для кислотных оксидов являются их следующие реакции с образованием солей:
| с основными оксидами: | SO3 + Na2O = Na2SO4 |
| с амфотерными оксидами: | P2O5 + Al2O3 = 2AlPO4 |
| со щелочами: | CO2 + 2KOH = K2CO3 + H2O |
3. Кислотные оксиды могут вступать в многочисленные окислительно-восстановительные реакции, например,
СO2 + C = 2CO,
2SO2 + O2 = 2SO3,
SO2 +2H2S = 3S + 2H2O,
4CrO3 + C2H5OH = 2Cr2O3 + 2CO2 + 3H2O
4. Менее летучие кислотные оксиды вытесняют более летучие кислотные оксиды из их солей (сплавление):
Менее летучие кислотные оксиды вытесняют более летучие кислотные оксиды из их солей (сплавление):
Na2CO3 + SiO2 → Na2SiO3 + CO2↑
Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение. Химия. 8 класс. Конспект урока
УМК «Химия. 8 класс» О. С. Габриеляна.
Тип урока: урок изучения нового материала (урок-исследование).
Цели:
- образовательная: повторить, углубить и обобщить знания учащихся о химических свойствах, получении и применении основных и кислотных оксидов;
- воспитательная: развивать коммуникабельность, интерес к предмету;
- развивающая: формировать способность к самостоятельному приобретению знаний; развивать умения анализировать, синтезировать, обобщать, делать выводы, устанавливать причинно – следственные связи ( состав – строение – свойства).
Задачи: организация проблемно-поисковой деятельности. Работа в группах. Проведение самостоятельной работы по вариантам. Эксперимент. Обсуждение результатов. Формулирование выводов.
Использованные источники:
- Химия. 8 класс: учеб. для общеобразоват. учреждений / О.С.Габриелян. – 12-е изд., стереотип. – М. : Дрофа, 2007. – 267, [5 с. : ил.]
- Химия. 8 класс. Тетрадь для лабораторных опытов и практических работ. Вертикаль О.С.Габриелян. – М. : Дрофа, 2013. – 96.
- Химия. 8 класс. Рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 8 класс» (с тестовыми заданиями ЕГЭ). Вертикаль О.С.Габриелян, Сладков С.А. – М. : Дрофа,2013. – 208.
- Химия. 8–9 классы. Электронное приложение к учебникам О.С.Габриеляна. http: //www.drofa.ru
Урок-исследование
Оборудование. На демонстрационном столе: оксид бария, оксид фосфора (V), оксид меди (II), оксид железа (III), растворы гидроксида натрия, хлороводородной (соляной) кислоты, лакмуса, фенолфталеина, четыре химических стакана (50 мл), подъемный столик, черно-белый экран для демонстрационных опытов;
Ход урока
Ι.
 Изучение нового материала
Изучение нового материала
Организация проблемно-поисковой деятельности. Работа в группах.
Задание 1-й группе (Оксиды. Классификация. Номенклатура.)
1) Пользуясь представленной на столах коллекцией оксидов и статьёй «Физические свойства оксидов» с. 218, опишите их физические свойства, отметьте агрегатное состояние, цвет. Сделайте вывод. Попытайтесь объяснить подобное многообразие.
Предполагаемый ответ: Исследование представленных оксидов показало, что они бывают твердые – оксид меди (П) СuО, оксид кальция СаО, жидкие оксид cepы(VI) SO3 и газообразные- оксид углерода(IV) СO2. Цвет их также чрезвычайно разнообразен: СuО черного цвета, оксид кальция СаО белого цвета, оксид углерода(IV) СO2 – бесцветный. Можно предположить, что причины в различном строении этих оксидов.
2) Выберите из перечня слов ключевые слова, которые, по вашему мнению характеризуют оксиды: простые вещества, сложные вещества, летучие, не имеющие окраски, окрашенные, бинарные соединения, содержат кислород, неметаллы, металлы.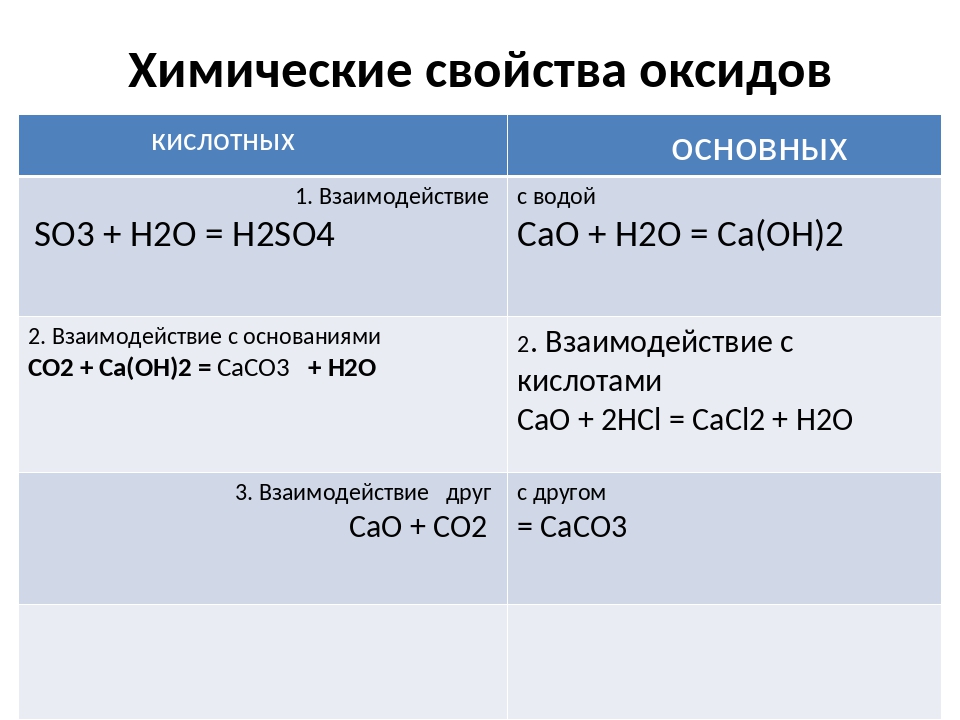
На основании ключевых слов сформулируйте определение оксидов. Запишите его. Проверьте по учебнику с. 91.
3) Классификация. Выделите признаки, на основании которых можно оксиды разделить на группы.
Предполагаемый ответ:
Ι. по принадлежности элемента, образующего оксид, к металлам и неметаллам:
а) оксиды металлов;
б) оксиды неметаллов.
ΙΙ. по способности образовывать гидроксиды определённого класса: основания (щёлочи), кислоты:
а) основные оксиды;
б) кислотные оксиды.
ΙΙΙ. по химическим свойствам:
а) несолеобразующие
б) солеобразующие.
4) Номенклатура. Работа с книгой. С помощью инструкции учебника с.89-90 назовите предложенные оксиды. Сформулируйте правило названия оксидов.
Задание 2-й группе
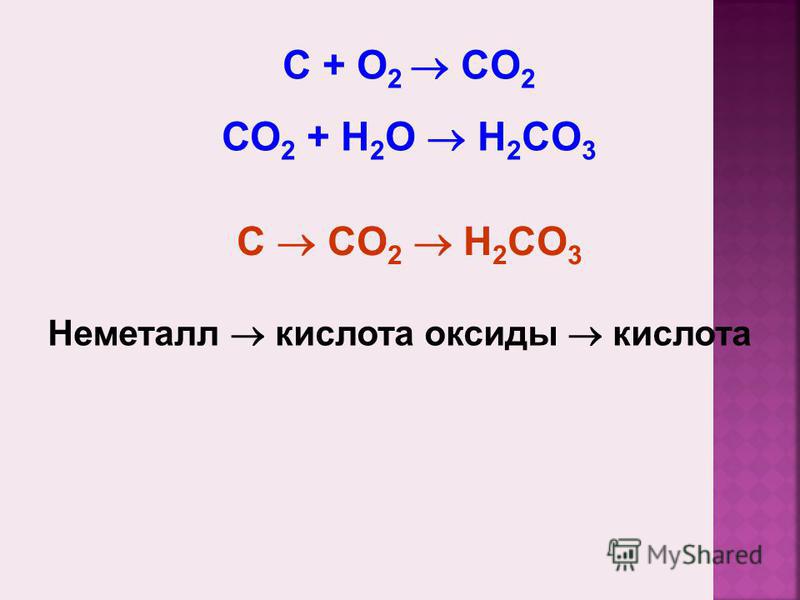
1) свойства кислотных оксидов.
Осуществите превращения:
Углерод (C) → оксид углерода (CO2) → угольная кислота (H2CO3) → карбонат кальция (CaCO3) → силикат кальция (CaSiO3).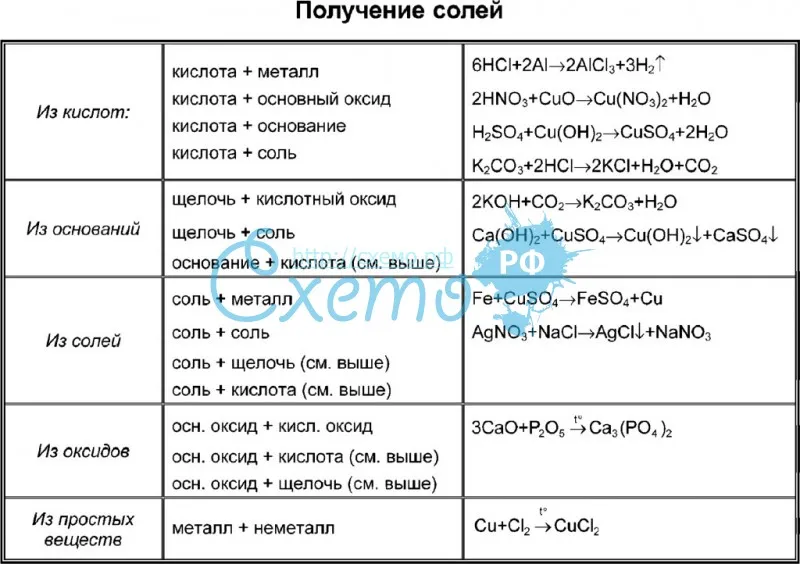
Сделайте вывод о химических свойствах кислотных оксидов. Проверьте своё заключение, сверив его с данными учебника с. 220.
2) свойства основных оксидов.
Осуществите превращения:
|
|
|
|
|
|
|
|
|
Сделайте вывод о химических свойствах основных оксидов. Проверьте своё заключение, сверив его с с данными учебника с. 219.
Задание 3-й группе.

1) Получение оксидов.
а) Получите P2O5, CO2 реакцией горения.
б) Получите Al2O3, SO3, CaO разложением сложных веществ.
Сделайте вывод о способах получения оксидов.
Предполагаемый ответ: оксиды образуются:
1) при горении простых и сложных веществ;
2) при разложении сложных веществ: а) нерастворимых оснований; б) кислот; в) солей.
Задание 4-й группе
Применение.
1) Докажите или опровергните утверждение:
- Песок не имеет применения в промышленности
- Углекислый газ – продукт фотосинтеза
- Из руд, состоящих из оксидов железа Fe2O3 и Fe3O4 получают чугун и сталь
ΙΙ. Закрепление знаний, умений, навыков
Проведение самостоятельной работы по вариантам:
Вариант I
1) С какими из перечисленных веществ, формулы которых приведены ниже, будет вступать в реакцию оксид кальция: НС1, NaOH, H2O, H2SO4, KС1? Составьте уравнения возможных реакций.
2) Составьте формулы оснований, соответствующих оксидам натрия, кальция, алюминия, магния.
Вариант 2
1) С какими из перечисленных веществ, формулы которых приведены ниже, будет вступать в реакцию оксид серы (VI): НС1, NaOH, H2O, Ca(OH)2, KC1? Составьте уравнения возможных реакций.
2) Составьте формулы кислот, соответствующих оксидам серы (VI), фосфора (V), азота (V), углерода (IV).
Вариант 3 (экспериментальное)
Задача I. Как доказать, что оксид бария —основный оксид?
Беседа о порядке решения экспериментальной задачи. Выполнение опыта учащимся у доски, растворение оксида бария в воде и обнаружение индикатором образующейся щелочи. Другой учащийся растворяет оксид бария в хлороводородной (соляной) кислоте, предварительно «подкрашенной» лакмусом. Далее они составляют уравнения реакций.
Вариант 4 (экспериментальное)
Задача 2. Как доказать, что оксид фосфора (V) — кислотный оксид?
Как доказать, что оксид фосфора (V) — кислотный оксид?
Обсуждение решения задачи всем классом. Опыты выполняет учитель. Учащиеся составляют уравнения реакций и отвечают на вопросы:
1) Какой кислотный оксид не взаимодействует с водой?
2) Может ли оксид фосфора (V) находиться в природных условиях?
В целях обобщения химических свойств оксидов составляется сравнительная таблица и используется Электронное приложение к учебникам О.С.Габриеляна Химия. 8-9классы.
http: //www.drofa.ru «Основные классы неорганических соединений. Оксиды» фото и видеоролики.
Домашнее задание
§ 30. Знать определение оксидов, уметь писать уравнения реакций, характеризующие свойства оксидов. Выполните упражнения 1–3 с. 221, решить задачи 4,5 с.221. Повторить §18.
Экспериментальная часть Опыт 1. Свойства основных и кислотных оксидов
а) Взаимодействие
основного оксида с водой.
Поместить в пробирку
микрошпатель оксида кальция и добавить
немного воды. Размешать стеклянной
палочкой. Добавить две капли фенолфталеина.
Объяснить все наблюдаемые явления,
написать уравнения реакций, сделать
вывод.
б) Взаимодействие
основного оксида с кислотой.
В пробирку поместить
микрошпатель оксида меди (II) и добавить
5-6 капель серной кислоты. Нагреть до
кипения. Что наблюдается? Объяснить,
написать уравнения реакции, сделать
вывод.
в) Взаимодействие
кислотного оксида с основанием (с
получением средней и кислой соли).
Налить в пробирку
5 капель гидроксида кальция и через
стеклянную трубочку (конец её протереть
ватой, смоченной спиртом), опущенную в
раствор, выдувать ртом выдыхаемый воздух
до появления в пробирке помутнения.
Объяснить это. Пропустить ещё воздух
до исчезновения помутнения. Написать
уравнение реакции, сделать вывод.
Опыт 2.
 Свойства оснований и кислот.
Свойства оснований и кислот.
а) Реакция
нейтрализации.
В пробирку поместить
5 капель гидроксида натрия и 2 капли
фенолфталеина. Добавить по каплям
разбавленный раствор хлорово-дородной
кислоты, встряхнуть пробирку. Как и
почему изменилась окраска фенолфталеина?
Объясните наблюдения. Напишите уравнение
реакции, сделайте вывод.
б) Взаимодействие
кислот с солями.
В пробирку налить
4-5 капель разбавленной серной кислоты
и добавить туда 2-3 кристаллика ацетата
натрия, встряхнуть. Осторожно понюхать.
Объяснить происходящую реакцию. Написать
уравнение реакции, сделать вывод.
в) Свойства
амфотерных оснований.
В три пробирки
поместить по 8-10 капель (порознь) раствора
солей: ZnSO4,
MgSO4,
Al2(SO4)3.
Прибавить во все пробирки по каплям
раствор гидроксида натрия до образования
осадков гидроксидов. Каждый из полученных
Каждый из полученных
осадков разделите вместе с жидкостью
на две части. На одну часть подействуйте
раствором хлороводородной кислоты (4-5
капель), на другую — раствором щёлочи
(4-5 капель). Обратите внимание на
растворимость осадков в кислоте и в
щёлочи и установите, какие из полученных
оснований являются амфотерными, какие
основными. Результаты опыта занесите
в таблицу №2.
Таблица №2
Свойства оснований
Основания | Растворимость | Характер оснований | |
в | в | ||
Напишите уравнения
реакций, сделайте вывод.
Опыт 3. Способы получения солей
а) Взаимодействие
солей между собой.
В
пробирку поместить несколько капель
нитрата свинца и добавить 3-4 капли йодида
калия. Описать наблюдения. Написать
уравнение реакции, сделать вывод.
б) Взаимодействие
солей с металлами.
В пробирку поместить
5 капель сульфата меди и опустить в неё
кусочек цинка. Через 5-6 минут, слив
раствор из пробирки, достать кусочек
цинка и положить на фильтровальную
бумагу. Что произошло при реакции?
Написать уравнение реакции, сделать
вывод.
Вопросы для самоконтроля
1. Из предложенных
оксидов: BaO, SiO2,
Al2O3,
Mo2O3,
Cl2O7,
NiO, ZnO, BeO, Mn2O7
выберите: а) основные, б) кислотные, в)
амфотерные.
2. Допишите
предложенные уравнения:
BaO+SiO2
? Cr2O3+HCl
?
Cr2O3+NaOH
? CO2+Ba(OH)2
?
BeO+NaOH
? MnO+H2SO4
?
Na2O+H2O
?
3. Допишите
Допишите
уравнения химических реакций:
HCl+Fe2O3
? HNO3+Sr(OH)2
? H2SO4+Ba(NO3)2
?
4. Из предложенных
соединений выберите: а) основания, б)
щёлочи.
Ba(OH)2,
Cu(OH)2,
RbOH, Ca(OH)2,
NaOH.
5. Допишите уравнения
реакций:
Ni(OH)2+H2SO4
? BaO+CO2
?
Zn(OH)2+NaOH
? HCl+Al
?
состав, номенклатура, химические свойства и получения»
Урок химии в 8 классе «Оксиды: состав, номенклатура, химические свойства и получения»
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Структура урока:
1. Организационный этап – 2 мин.
Организационный этап – 2 мин.
2.Подготовительный этап – 5 мин
3. Основной этап:
* усвоение новых знаний и способов деятельности;
* первичной проверки понимания изученного;
* закрепление новых знаний и способов деятельности – 25 мин
4.Информация о домашнем задании – 3 мин.
5. Подведение итогов учебного занятия. Рефлексия. – 5 мин.
Ход урока
1.Организационный этап.
Учитель приветствует учащихся. Учащиеся проверяют наличие необходимого инструментария для урока.
2.Подготовительный этап
Вводное слово учителя:
Изучая химию, мы неоднократно встречались с различными классами неорганических соединений: оксидами.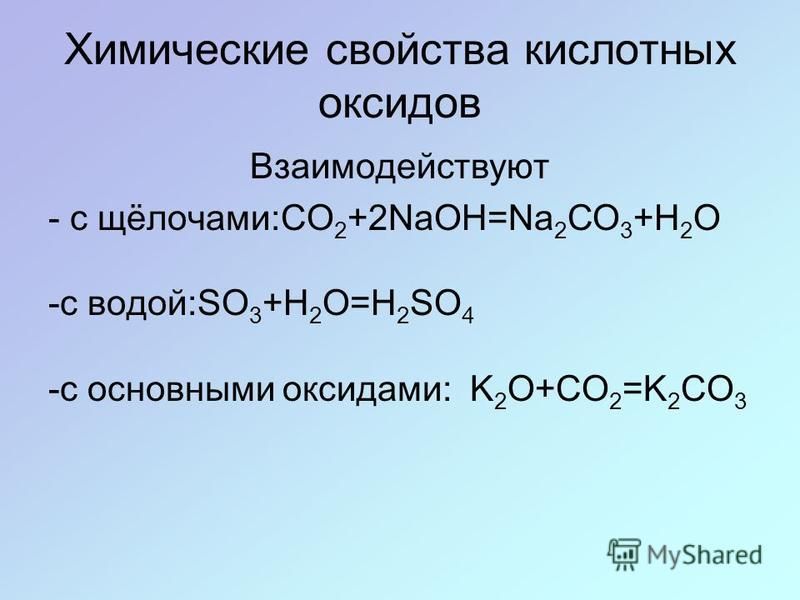 Основаниями. Кислотами и солями. Настало время расширить и привести в систему знания об этих значительных классах веществ
Основаниями. Кислотами и солями. Настало время расширить и привести в систему знания об этих значительных классах веществ
Выставка предметов ( оксидов) стакан с водой, бутылка с газированной водой. Кусок железной руды – гематита, глиняная ваза.
Почему все предметы собраны вместе?
Тема урока «Оксиды: состав, номенклатура, химические свойства и получения»
Понятие «оксиды» включает бесконечное разнообразие веществ:
Оксид водорода ( вода ) – жидкое вещество;
Оксид кремния ( песок ) SiO2- кварцевый песок, кремнезем, минерал горного хрусталя, оксид алюминия (глинозем) Al2O3 2Sio2- глина состоит из оксидов алюминия и кремния – твердые вещества.
Оксиды могут быть газами, как, например оксид углерода (4 ) – углекислый газ и оксид углерода ( 2)- угарный газ.
Таким образом среди оксидов есть твердые, газообразные и жидкие вещества
ИКТ стр.1 Классификация оксидов ЦВЕТ (Cuo, MqO, CaO, Al2O3).
Написать несколько примеров оксидов ( используют ПСХЭ 1 2 3 групп). Дать им названия по международной номенклатуре. Согласно номенклатуре любой оксид называют оксидом с указанием названия элемента в родительном падеже, указывая валентность в скобках соответствующую римскую цифру.
Особенности номенклатуры для оксидов. Названия оксидов зависят от числа атомов кислорода в формуле.
CO — монооксид углерода ( приставка моно обозначает один) или оксид углерода (2) , угарный газ.
CO2 – диоксид углерода или оксид углерода (4) всем известный углекислый газ
Еще существуют тривиальные названия, например – углекислый газ. Угарный газ. До сих пор в химической литературе встречаются названия – закись ( для более низких) , окись ( для более высоких с.о.) степеней окисления.
Угарный газ. До сих пор в химической литературе встречаются названия – закись ( для более низких) , окись ( для более высоких с.о.) степеней окисления.
N2O– закись азота или оксид азота (1)
NO –окись азота или оксид азота (2)
Задание : Дать названия оксидам по международной номенклатуре
PbO, SO2, SO3, K2O, FeO, Fe2O3
По составу все оксиды характеризуются тремя общими признаками:
· Любой оксид является сложным веществом
· Состоит из атомов двух элементов
· Один из элементов кислород
Получение оксидов.
Оксиды могут быть получены в результате следующих реакций
1.Реакция соединения (учащиеся пишут уравнения самостоятельно)
2.Реакция разложения
3.Реакции замещения
ИКТ стр.2 Получение оксидов
3. Основной этап
По химическим свойствам оксиды делятся на несолеобразующие ( СО , NO,N2O,h3O) и солеобразующие ( MgO, S2O3, Al2o3 ).
Солеобразующие оксиды подразделяются на основные – CaO, CuO, амфотерные — ZnO Al2O3 и кислотные- SO3
.
Данные о химических свойствах оксидов в виде шпаргалки ( табличка каждому учащемуся)
Обозначение О.О. — основные оксиды
К. О.- кислотные оксиды
О.- кислотные оксиды
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Учебник химия 8 класс Г.Е. Рудзитис параграф 30 стр. 92 таблица 9.
|
|
|
|
|
|
|
|
|
|
|
|
Презентация слайд № 1-5
ИКТ. Прочитайте, прослушайте
*Оксиды это сложные вещества, состоящие из атомов двух химических элементов, один из которых кислород. Оксиды делятся на оксиды металлов и оксиды неметаллов.
* Оксиды неметаллов, взаимодействуя с водой, образуют кислоты. Оксиды неметаллов , которым соответствуют кислоты, называются кислотными оксидами.
* Оксиды металлов взаимодействуют с водой, образуют основания. Оксиды металлов, которым соответствуют основаниям, называются основными оксидами
Подведение итогов. Рефлексия.
1.Что узнали? Чему научились?
2.Какие характеристики классов оксидов нам уже известны?
Домашнее задание: параграф 30 стр.89-92 упр.1 стр.92
МКОУ « Чеботарихинская СОШ»
Урок химии по теме
«Оксиды: состав, номенклатура. Химические свойства и получения»
Учитель : Колокольцева Н. В.
2011 -2012 г
Оксиды их классификация, способы получения и химические свойства (таблица, схема)
Оксиды — это бинарные соединения кислорода, то есть сложные вещества, состоящие из двух элементов, один из которых является кислород.
Э2+nOn-2 — общая формула оксидов, где
n — степень окисления элемента
-2 — степень окисления кислорода
Названия оксидов составляется из слова «оксид» и названия элемента образующего оксид в родительном падеже (CaO — оксид кальция).
Схема классификация оксидов
Таблица классификация оксидов с примерами
|
Классификация оксидов
|
Определение
|
Примеры реакций
|
Типичные взаимодействия
|
|
Нормальные
|
Оксиды, в которых есть только связи между кислородом и каким-нибудь элементом
|
MgO, SO3, SiO2
|
Смотрите свойства кислотных и основных оксидов
|
|
Пероксиды
|
Те, в которых есть связи между двумя атомами кислорода
|
Na2O2, H2O2
|
Смотрите таблицу свойства пероксида водорода
|
|
Смешанные оксиды
|
Те, которые представляют собой смесь двух оксидов одного элемента в разных степенях окисления
|
Pb3O4 = 2РbО · PbO2 Fe3O4 = FeO · Fe2O3
|
Обладают теми же свойствами, что и входящие в их составы оксиды
|
|
Кислотные или ангидриды
|
Оксиды, которые реагируют с водой, образуя кислоты; с основаниями и основными оксидами — образуют соли
|
SO3, SO2, Mn2O7
|
С водой:
SO2 + Н2O → Н2SO3
С основаниями и основными оксидами: Мn2O7 + 2КOН → 2КМnO4 + Н2O
|
|
Основные оксиды
|
Те, которые реагируют с водой, образуя основания; с кислотами и кислотными оксидами образуют соли
|
CaO, Na2O
|
С водой:
СаО + Н2O → Са(ОН)2
С кислотами и кислотными оксидами:
Na2O + СО2 → Na2CO3
|
|
Амфотерные оксиды
|
Те, которые в зависимости от условий проявляют свойства и кислотных, и основных оксидов
|
ZnO, Al2O3
|
С кислотами:
ZnO + 2НСl → ZnCl2 + Н2O
С щелочами:
ZnO + 2NaOH + H2O → Na2[Zn(OH)4]
|
|
Безразличные (несолеобразующие)
|
Оксиды, которые не реагируют ни с кислотами, ни с основаниями. Солей не образуют
|
NO, N2O
|
NO + Н2O -/-> N2O + NaOH
|
Способы получения оксидов таблица
Почти все хим. элементы образуют оксиды. На данный момент не получены оксиды гелия, неона и аргона.
|
Способы получения оксидов
|
Примеры
|
Примечание
|
|
Взаимодействие простых веществ с кислородом
|
S + O2 → SO2
4Аl + 3O2 → 2Аl203
|
Так получают преимущественно оксиды неметаллов
|
|
Термическое разложение оснований, солей, кислот
|
СаСО3t→ CaO + CO2↑
2H3BO3 t→ Bg2O3 + H2O↑
Mg(OH)2 t→ MgO + H20
|
Так получают преимущественно оксиды металлов
|
|
Взаимодействие простых веществ и солей с кислотами-окислителями
|
C + 4HNO3(p-p) → CO2 + 4N02 + H2O
Сu + 4HNO3(конд.) → Cu(NO3)2 + 2NO2 + 2H2O
Na2SO3 + 2H2SO4 → 2NaHS04 + SO2↑ + H2O
|
Способ получения преимущественно оксидов неметаллов
|
Химические свойства оксидов таблица
|
Классификация оксидов
|
Химические свойства оксидов
|
Примеры реакции
|
|
Основные оксиды
|
1. Основной оксид* + вода —> щелочь
|
К2О + Н2О → 2КОН,
ВаО + Н2O → Ва(ОН)2
|
|
2. Основной оксид + кислота —> соль + вода
|
CuO + H2SO4 → CuSO4 + Н2О
| |
|
3. Основной оксид + кислотный оксид —> соль
|
MgO + СО2 → MgCO3,
ЗСаО + P2O5 → Ca3(PO4)2
| |
|
Кислотные оксиды
|
1. Кислотный оксид + вода —> кислота
|
SO3+ Н2O → H2SO4
Сl2O7 + Н2О → 2НСlO4
SiO2 + Н2O -/-> нет реакции (исключение)
|
|
2. Кислотный оксид + щелочь —> соль + вода
|
SO3 + 2NaOH → Na2SO4+ Н2O
| |
|
3. Кислотный оксид + основной оксид —> соль
|
SiO2 + CaO t→ CaSiO3,
Р2O4 + ЗК2O → 2К3РО4
| |
|
Амфотерные оксиды
|
1. С кислотами реагируют как основные оксиды
|
ZnO + H2SO4 → ZnSO4 + Н2O
|
|
2. С основаниями (щелочами) реагируют как кислотные оксиды
|
ZnO + 2NaOH → Na2ZnO2 + Н2O
|
_______________
Источник информации: Насонова А.Е. Химия, школьная программа в таблицах и формулах, 1998
Удаление оксида азота при производстве азотной кислоты
Тиан, Х., Чен, Г., Лу, К., Сюй, X., Рен, В., Чжан, Б., Бангер, К., Тао, Б., Пан, С., Лю, М., Чжан, К., Брювилер, Л., и Вофси, С., Здоровье и устойчивость экосистемы , 2014 г., т. 1, вып. 4, стр. 1.
Статья
Google Scholar
Такетт Р., Парниковые газы / Справочный модуль по химии, молекулярным наукам и химической инженерии, Амстердам: Elsevier, 2018.https://doi.org/10.1016/B978-0-12-409547-2.14031-4
Google Scholar
Равишанкара А.Р., Дэниел Дж.С., Портманн Р.В., Science , 2009, т. 326, стр. 123.
CAS
PubMed
Статья
Google Scholar
Linak, W.P. и Kramlich, J.C., Stud. Environ. Sci ., 1998, т. 72, стр. 265.
CAS
Статья
Google Scholar
Отчет, подготовленный для DGXI / Варианты сокращения выбросов оксида азота — Заключительный отчет, 1998, т.3.
Kapteijn, F., Rodriguez-Mirasol, J., and Moulijn, J.A., Appl. Катал., В , 1996, т. 9, стр. 25.
CAS
Статья
Google Scholar
Перес-Рамирес, Дж., Каптейн, Ф., Мулб, Г., Шуб, X., и Мулиджн, Дж. А., Catal. Сегодня , 2002 г., т. 76, стр. 55.
Статья
Google Scholar
Справочник инженера-азотного химика , Москва: Химия, 1987, т.2.
Бруштейн Е.А., Ванчурин В.И., Ященко А.В., Катал. Пром-сти. , 2012, т. 4, стр. 292.
Google Scholar
Perez-Ramırez, J., Kapteijn, F., Schoffel, K., and Moulijn, J.A., Appl. Катал., В , 2003, т. 44, стр. 117.
Статья
CAS
Google Scholar
Швефер, М., Маурер Р., Гровс М., Азот , Вена, 2000.
Гигиенические стандарты ГН 2.1.6.695-98, М .: Минздрав России, 1998.
Li, Y. and Armor, JN, Appl. Катал., В , 1993, т. 3, стр. 55.
CAS
Статья
Google Scholar
Шутилов Р.А., Шутилов А.А., Зенковец Г.А., Матер. Сегодня: Учеб. , 2017, т. 4, стр. 11490.
CAS
Google Scholar
Санкар, С., Putluru, R., Schill, L., Godiksen, A., Poreddy, R., Mossin, S., Jensen, A.D., and Fehrmann, R., Appl. Катал., В , 2016, т. 183, стр. 282.
Статья
CAS
Google Scholar
Huang, X., Zhang, S., Chen, H., Zhong, Q., and Huang, X., J. Mol. Struct. , 2015, т. 1098, стр. 289.
CAS
Статья
Google Scholar
Гржибек Т.and Papp, H., Appl. Катал., В , 1992, т. 1, стр. 271.
CAS
Статья
Google Scholar
Groves, M.C.E. и Sasonow, A., J. Integrative Environ. Sci ., 2010, т. 7, вып. S1, стр. 211.
Статья
Google Scholar
Perbandt, C., Bacher, V., Groves, M., Schwefer, M., Siefert, R., and Turek, T., Chem. Ing. Тех ., 2013, т. 585, стр. 705.
Статья
CAS
Google Scholar
Овчинникова Е.В., Чумаченко В.А., Пирютко Л.В., Харитонов А.С., Носков А.С., Катал. Пром-сти ., 2009, т. 1, стр. 76.
Google Scholar
Лю Н., Чжан Р., Чен Б. и Ли Ю., J. Catal ., 2012, т. 294, стр. 99.
CAS
Статья
Google Scholar
Ю., Х.and Wang, X., Catal. Commun ., 2018, т. 106, стр. 40.
CAS
Статья
Google Scholar
Zasada, F., Piskorz, W., Janas, J., Grybos, J., Indyka, P., and Sojka, Z., ACS Catal. , 2015, т. 5, стр. 6879.
CAS
Статья
Google Scholar
Kaczmarczyk, J., Zasada, F., Janas, J., Indyka, P.A., Piskorz, W., Kotarba, A., and Sojka, Z., ACS Catal. , 2016, т. 6, стр. 1235.
CAS
Статья
Google Scholar
Dandl, H. and Emig, G., Appl. Катал., А , 1998, т. 168, стр. 261.
Piskorz, W., Zasada, F., Stelmachowski, P., Kotarba, A., and Sojka, Z., Catal. Сегодня . 2008, т. 137, стр. 418.
CAS
Статья
Google Scholar
Ямасита Т.и Vannice, A., J. Catal., 1996, vol. 161, стр. 254.
CAS
Статья
Google Scholar
Raj, S.L. and Srinivasan, V., J. Catal., 1980, vol. 65, нет. 1, стр. 121.
CAS
Статья
Google Scholar
Winter, E.R.S., J. Chem. Soc. А , 1968, т. 0, п. 2889.
CAS
Статья
Google Scholar
Сазонов, Л.А., Москвина З.В., Артамонов Е.В. Кинетика и катализ .1974. 15, вып. 1, стр. 120.
CAS
Google Scholar
Иванов Д.В., Садовская Е.М., Пинаева Л.Г., Исупова Л.А., J. Catal., 2009, т. 267, стр. 5.
CAS
Статья
Google Scholar
Ли, Г.Н., Пидко, Э.А., Филот, И.А.У., ван Сантен, Р.А., Ли, К., и Хенсен, E.J.M., J. Catal., 2013, т. 308, стр. 386.
CAS
Статья
Google Scholar
Guesmi, H., Berthomieu, D., and Kiwi-Minsker, L., J. Phys. Chem , 2008, т. 112, нет. 51, стр. 20319.
CAS
Google Scholar
Guesmi, H., Berthomieu, D., Bromley, B., Coqa, B., and Kiwi-Minsker, L., Phys. Chem. Chem.Физ ., 2010, т. 12, стр. 2873.
CAS
PubMed
Статья
Google Scholar
Катализ с помощью церия и родственных материалов , Catalytic Science Series, Trovarelli, A. и Fornasiero, P., Eds., London: Imperial College, 2013, vol. 12.
Google Scholar
Паша, Н., Лингайаха, Н., Сешу Бабуа, Н., Шива Санкар Реддья, П., и Саи Прасад, П.С., Катал. Commun ., 2008, т. 10, стр. 132.
CAS
Статья
Google Scholar
Гжибек, Г., Стельмаховски, П., Гудыка, С., Индика, П., Сойка, З., Гильен-Уртадо, Н., Рико-Перес, В., Буэно-Лопес, А. , and Kotarba, A., Appl. Катал., В , 2016, т. 180, стр. 622.
CAS
Статья
Google Scholar
Ю, Чанг, Х., Ma, L., Guo, L., Qin, X., Li, J., and Li, J., Chem. Англ. J. , 2018, т. 347, стр. 184.
CAS
Статья
Google Scholar
Забильский М., Джинови П., Чернычева Е., Пинтар А., Заявл. Катал., В , 2016, т. 197, стр. 146.
CAS
Статья
Google Scholar
Иванек, Э., Кравчик, К., Петрик, Дж., Собчак, Дж.W., and Kaszkur, Z., Appl. Катал., В , 2011, т. 106, стр. 416.
CAS
Статья
Google Scholar
Parres-Esclapez, S., Illán-Gómez, M.J., Salinas-Martínez de Lecea, C., and Bueno-López, A., Appl. Катал., В, 2010, т. 96, стр. 370.
CAS
Статья
Google Scholar
Паррес-Эсклапес, С., Суч-Басанез, И., Иллан-Гомес, М.J., Салинас-Мартинес де Лесеа, К., и Буэно-Лопес, А., J. Catal., 2010, vol. 276, стр. 390.
CAS
Статья
Google Scholar
Нобукава, Т., Танака, С., Ито, С., Томисигэ, К., Камеока, С., и Кунимори, К., Catal. Lett . 2002, т. 83, №№ 1–2, с. 5.
CAS
Статья
Google Scholar
Лю С., Тан, Н., Шан, К., Wu, C., Xu, G., and Cong, Y., Chin. J. Catal., 2018, т. 39, стр. 1189.
CAS
Статья
Google Scholar
Иванов Д.В., Пинаева Л.Г., Исупова Л.А., Садовская Е.М., Просвирин И.П., Герасимов Е.Ю., Яковлева И.С. Катал., А , 2013, т. 457, стр. 42.
Иванов Д.В., Пинаева Л.Г., Садовская Е.М., Исупова Л.А., J. Mol. Катал. А: Chem ., 2016, т. 412, стр. 34.
CAS
Статья
Google Scholar
Франкен Т. и Палковиц Р., Заявл. Catal., B, 2015, т. 176–177, с. 298.
Статья
CAS
Google Scholar
Амрусс Р., Цуцуми А., Бачар А. и Лахсен Д., Appl. Катал., А , 2013, т. 450, стр. 253.
Асано, К., Ohnishi, C., Iwamoto, S., Shioya, Y., and Inoue, M., Appl. Катал., В , 2008, т. 78, стр. 242.
CAS
Статья
Google Scholar
Марнеллос Г.Е., Эфтимиадис Е.А., Васалос И.А., Appl. Катал., В , 2003, т. 46, стр. 523.
CAS
Статья
Google Scholar
Имамура, С., Шоно, М., Окамото, Н., Хамада, Р., and Ishida, S., Appl. Катал., А , 1996, т. 142, стр. 279.
Xue, L., Zhang, C., He, H., and Teraoka, Y., Appl. Катал., В , 2007, т. 75, стр. 167.
CAS
Статья
Google Scholar
Сюэ, Л., Хэ, Х., Лю, К., Чжан, К., и Чжан, Б., Env. Sci. Технол ., 2009, т. 43, нет. 3, стр. 890.
CAS
Статья
Google Scholar
Забильский, М., Erjavec, B., Djinovic, P., and Pintar, A., Chem. Англ. J. , 2014, т. 254, стр. 153.
CAS
Статья
Google Scholar
Liu, Z., He, C., Chen, B., and Liu, H., Catal. Сегодня , 2017, т. 297, стр. 78.
CAS
Статья
Google Scholar
Дои, К., Ву, Ю.Ю., Такеда, Р., Мацунами, А., Араи, Н., Тагава, Т., и Гото, С., заявл. Катал., В, 2001, т. 35, стр. 43.
CAS
Статья
Google Scholar
Huang, C., Ma, Z., Xie, P., Yue, Y., Hua, W., and Gao, Z., J. Mol. Катал. А: Chem ., 2015, т. 400, стр. 90.
CAS
Статья
Google Scholar
Хуанг, К., Ма, З., Мяо, К., Юэ, Ю., Хуа, В., и Гао, З., RSC Adv ., 2017, т.7, стр. 4243.
CAS
Статья
Google Scholar
Хуан, К., Цзян, Ю., Ма, З., Се, П., Линь, Ю., Мэн, Т., Мяо, К., Юэ, Ю., Хуа, В., and Gao, Z., J. Mol. Катал. А: Химия, 2016, т. 420, стр. 73.
CAS
Статья
Google Scholar
Oi, J., Obuchi, A., Bamwenda, G.R., Ogata, A., Yagita, H., Kushiyama, S., and Mizuno, K., Appl.Катал., В , 1997, т. 12, стр. 277.
CAS
Статья
Google Scholar
Sui, C., Zhang, T., Dong, Y., Yuan, F., Niu, X., and Zhu, Y., Mol. Катал ., 2017, т. 435, стр. 174.
CAS
Статья
Google Scholar
Wood, B.R., Reimer, J.A., and Bell, A.T., J. Catal. , 2002, т. 209, стр. 151.
CAS
Статья
Google Scholar
Лю, З., He, C., Chen, B., and Liu, H., Catal. Сегодня , 2017, т. 297, стр. 78.
CAS
Статья
Google Scholar
Xue, Z., Shen, Y., Shen, S., Li, C., and Zhu, S., J. Ind. Eng. Chem. , 2015, т. 30, стр. 98.
CAS
Статья
Google Scholar
Adamski, A., Zaj, W., Zasada, F., and Sojka, Z., Catal. Сегодня , 2012 г., т.191, стр. 129.
CAS
Статья
Google Scholar
Abu-Zied, B.M., Bawaked, S.M., Kosa, S.A., Ali, T.T., and Schwieger, W., Catalysts , 2016, vol. 6, стр. 70.
Статья
CAS
Google Scholar
Abu-Zied, B.M., Bawaked, S.M., Kosa, S.A., Ali, T.T., Schwieger, W., and Aqlan, F.M., Appl. Серфинг. Sci ., 2017, т. 419, стр.399.
CAS
Статья
Google Scholar
Abu-Zied, B.M., Bawaked, S.M., Kosa, S.A., Ali, T.T., and Schwieger, W., Int. J. Electrochem. Sci. , 2016, т. 11, стр. 1568.
CAS
Google Scholar
Abu-Zied, B.M., Bawaked, S.M., Kosa, S.A., Ali, T.T., and Schwieger, W., I nt. J. Electrochem. Sci ., 2016, т. 11, стр. 2230.
CAS
Google Scholar
Xu, X., Xu, H., Kapteijn, F., and Moulijn, J.A., Appl. Катал., В, 2004, т. 53, стр. 265.
CAS
Статья
Google Scholar
Li, Y. and Armor, J.N., Appl. Catal., B, 1992, т. л, п. 21.
Статья
Google Scholar
Руссо, Н., Фино Д., Саракко Г. и Спеккиа В., Catal. Сегодня . 2007, т. 119, стр. 228.
CAS
Статья
Google Scholar
Abu-Zied, B.M. and Soliman, S.A., Catal. Lett ., 2009, т. 132, стр. 299.
CAS
Статья
Google Scholar
Абу-Зиед, Б.М., Чин . J. Catal., 2011, т. 32, стр. 264.
CAS
Статья
Google Scholar
Абу-Зиед, Б.М., Солиман С.А. и Абделлах С.Е., Чин . J. Catal., 2014, т. 35, стр. 1105.
CAS
Google Scholar
Abu-Zied, B.M., Soliman, S.A., and Abdellah, S.E., J. Ind. Eng. Chem ., 2015, т. 21, стр. 814.
CAS
Статья
Google Scholar
Abu-Zied, B.M., Soliman, S.A., and Abdellah, S.E., Mod.Res. Катал ., 2017, т. 6, стр. 47.
CAS
Статья
Google Scholar
Li, Z., Cang-cang, W., and Xiu-feng, X., J. Fuel Chem. Технол ., 2016, т. 44, нет. 12. 1494.
Статья
Google Scholar
Франкен Т. и Палковиц Р., , заявл. Катал., В , 2015, т. 176–177, с. 298.
Статья
CAS
Google Scholar
Хромчакова, З., Обалова, Л., Кованда, Ф., Легут, Д., Титов, А., Ритц, М., Фридрихова, Д., Михалик, С., Кустровски, П., и Джиратова, К., Catal. Сегодня , 2015, т. 257, стр. 18.
CAS
Статья
Google Scholar
Клюшина, А., Пакультова, К., Крейцова, С., Словик, Г., Жиратова, К., Кованда, Ф., Рычковски, Дж., И Обалова, Л., Catal. Сегодня , 2015, т. 257, стр. 2.
CAS
Статья
Google Scholar
Обалова, Л., Караскова К., Джиратова К., Кованда Ф., , заявл. Катал., В , 2009, т. 90, стр. 132.
CAS
Статья
Google Scholar
Обалова Л., Джиратова К., Караскова К., Кованда Ф., Чин. J. Catal., 2011, т. 32, стр. 816.
CAS
Статья
Google Scholar
Пакультова К., Караскова К., Стракосова Ю., Джиратова К., и Обалова, Л., C. R. Chim. , 2015, т. 18, стр. 1114.
CAS
Статья
Google Scholar
Kim, M.-J., Lee, S.-J., Ryu, I.-S., Jeon, M.-W., Moon, S.-H., Roh, H.- S., and Jeon, SG, Mol. Катал. , 2017, т. 442, стр. 202.
CAS
Статья
Google Scholar
Ян, Л., Рен, Т., Ван, X., Гао, К., Цзи, Д., и Суо, Дж., Catal. Commun ., 2003, т. 4, стр. 505.
CAS
Статья
Google Scholar
Ян, Л., Рен, Т., Ван, X., Цзи, Д., и Суо, Дж., Appl. Катал., В , 2003, т. 45, стр. 85.
CAS
Статья
Google Scholar
Котарба А., Крук И. и Сойка З., J. Catal., 2002, т. 211, стр. 265.
CAS
Статья
Google Scholar
Стельмаховски, П., Maniak, G., Kotarba, A., and Sojka, Z., Catal. Commun ., 2009, т. 10, стр. 1062.
CAS
Статья
Google Scholar
Maniak, G., Stelmachowski, P., Zasada, F., Piskorz, W., Kotarba, A., and Sojka, Z., Catal. Сегодня , 2011 г., т. 176, стр. 369.
CAS
Статья
Google Scholar
Маняк, Г., Стельмаховски, П., Котарба, А., Сойка, З., Рико-Перес, В., и Буэно-Лопес, А., Appl. Катал., В , 2013, т. 136–137, с. 302.
Статья
CAS
Google Scholar
Maniak, G., Stelmachowski, P., Stanek, J.J., Kotarba, A., and Sojka, Z., Catal. Commun ., 2011, т. 15, стр. 127.
CAS
Статья
Google Scholar
Стельмаховски П., Маняк Г., Kaczmarczyk, J., Zasada, F., Piskorz, W., Kotarba, A., and Sojka, Z., Appl. Катал., В , 2014, т. 146, стр. 105.
CAS
Статья
Google Scholar
Гжибек, Г., Войчик, С., Чура, К., Грибос, Дж., Индика, П., Ошайка, М., Стельмаховски, П., Витковски, С., Ингер, М., Wilk, M., Kotarba, A., and Sojka, Z., Appl. Катал., В , 2017, т. 210, стр. 34.
CAS
Статья
Google Scholar
Гудыка, С., Гжибек, Г., Грибос, Дж., Индика, П., Лещинский, Б., Котарба, А., и Сойка, З., Appl. Катал., В , 2017, т. 201, стр. 339.
CAS
Статья
Google Scholar
Tursun, M., Wang, X., Zhang, F., and Yu, H., Catal. Commun ., 2015, т. 65, стр. 1.
CAS
Статья
Google Scholar
Pietrogiacomi, D., Campa, M.C., Карбоне, Л.Р., Тути, С., и Окчиуцци, М., Appl. Катал., В, 2016, т. 187, стр. 218.
CAS
Статья
Google Scholar
Grzybek, G., Wójcik, S., Legutko, P., Grybos, J., Indyka, P., Leszczynski, B., Kotarba, A., and Sojka, Z., Appl. Катал., В , 2017, т. 205, стр. 597.
CAS
Статья
Google Scholar
Войчик, С., Гжибек Г., Грибос Дж., Котарба А. и Сойка З., Catal. Commun ., 2018, т. 110, стр. 64.
CAS
Статья
Google Scholar
Wojcik, S., Ercolino, G., Gajewska, M., Moncada Quintero, C.W., Specchia, S., and Kotarba, A., Chem. Англ. J. , 2019. https://doi.org/10.1016/j.cej.2018.10.025
Артикул
CAS
Google Scholar
Си-сюань, Л., Xia, L., Li, J., Liu, X., Sun, J., Wang, H., Chi, Y., Li, C., and Song, Y., J. Fuel Chem. Технол ., 2018, т. 46, нет. 11, стр. 1377.
Статья
Google Scholar
Yu, H., Tursun, M., Wang, X., and Wu, X., Appl. Катал., В , 2016, т. 185, стр. 110.
CAS
Статья
Google Scholar
Ю, Х., Ван, X. и Ву, X., Мол. Катал. , 2018, т. 460, стр. 69.
CAS
Статья
Google Scholar
Yu, H., Wang, X., Wu, X., and Chen, Y., Chem. Англ. J. , 2018, т. 334, стр. 800.
CAS
Статья
Google Scholar
Yu, H., Wang, X., and Li, Y., Catal. Сегодня , 2019. https://doi.org/10.1016/j.cattod.2018.10.036
CAS
Статья
Google Scholar
Ю., Х.and Wang, X., Catal. Commun ., 2018, т. 106, стр. 40.
CAS
Статья
Google Scholar
Ван, Ю., Ху, X., Чжэн, К., Вэй, X., и Чжао, Ю., Catal. Commun ., 2018, т. 111, стр. 70.
CAS
Статья
Google Scholar
Иванова Ю.А., Сутормина Е.Ф., Исупова Л.А., Вовк Е.И., Кинет. Катал ., 2017, т. 58, нет. 6, стр. 793.
CAS
Статья
Google Scholar
Иванова Ю.А., Сутормина Е.Ф., Исупова Л.А., Рогов В.А. Кинет. Катал ., 2018, т. 59, нет. 3, стр. 357.
CAS
Статья
Google Scholar
Шен, К., Ли, Л., Ли, Дж., Тиан, Х., и Хао, З., Хазард, Дж., J. Hazardous Mater. , 2009, т. 163, стр.1332.
CAS
Статья
Google Scholar
Пападатос К. и Шелстад К.А., J. Catal., 1973, т. 28, стр. 116.
CAS
Статья
Google Scholar
Сан, К., Ся, Х., Хенсен, Э., ван Сантен, Р., и Ли, К., J. Catal., 2006, т. 238, стр. 186.
CAS
Статья
Google Scholar
Соболев, В.И., Панов Г.И., Харитонов А.С., Романников В.Н., Володин А.М., Ионе К.Г., J. Catal., 1993, т. 139, стр. 435.
CAS
Статья
Google Scholar
Дубков К.А., Ованесян Н.С., Штейнмаан А.А., Староконь Е.В., Панов Г.И., J. Catal., 2002, т. 207, стр. 341.
CAS
Статья
Google Scholar
Рой, П.K., Prins, R., and Pirngruber, G.D., Appl. Катал., В , 2008, т. 80, стр. 226.
CAS
Статья
Google Scholar
Аренс М., Мари О., Базен П. и Датури М., J. Catal., 2010, т. 271, стр. 1.
CAS
Статья
Google Scholar
Се, П., Ло, Ю., Ма, З., Хуан, К., Мяо, К., Юэ, Ю., Хуа, В., и Гао, З., J. Catal., 2015, т. 330, стр. 311.
CAS
Статья
Google Scholar
Чжан Б., Лю Ф., Хэ Х. и Сюэ Л., Чин. J. Catal., 2014, т. 35, стр. 1972 г.
CAS
Статья
Google Scholar
Abu-Zied, B.M. and Asiri, A.M., Chin. J. Catal., 2015, т. 36, стр. 1837.
Статья
CAS
Google Scholar
Рутковская, М., Piwowarska, Z., Micek, E., и Chmielarz, L., Microporous Mesoporous Mater ., 2015, т. 209, стр. 54.
CAS
Статья
Google Scholar
Zhang, F., Wang, X., Zhang, X., Turxun, M., Yu, H., and Zhao, J., Chem. Англ. J. , 2014, т. 256, с. 365.
CAS
Статья
Google Scholar
Чжан Ф., Ван Х., Чжан Х., Tursun, M., and Yu, H., Chin. J. Catal., 2015, т. 36, стр. 344.
Статья
CAS
Google Scholar
Basahel, S.N., Abd El-Maksod, I.H., Abu-Zied, B.M., and Mokhtar, M., J. Alloys Compd. , 2010, т. 493, стр. 630.
CAS
Статья
Google Scholar
Ладавос А. и Бакас Т., React. Кинет. Катал. Lett ., 2001, т. 73, нет. 2, стр. 229.
CAS
Статья
Google Scholar
Перес-Алонсо, Ф.Дж., Мелиан-Кабрера, И., Лопес Гранадос, М., Каптейн, Ф., и Фиерро, J.L.G., J. Catal., 2006, vol. 239, стр. 340.
CAS
Статья
Google Scholar
Huanga, C., Zhuc, Y., Wang, X., Liu, X., Wang, J., and Zhang, T., J. Catal. , 2017, т.347, стр. 9.
Статья
CAS
Google Scholar
Alini, S., Basile, F., Blasioli, S., Rinaldi, C., and Vaccari, A., Appl. Катал., В , 2007, т. 70, стр. 323.
CAS
Статья
Google Scholar
Кави, С., Лю, С.Й., и Шен, С.-К., Catal. Сегодня , 2001 г., т. 68, стр. 237.
CAS
Статья
Google Scholar
Хабер, Дж., Machej, T., Janas, J., and Nattich, M., Catal. Сегодня , 2004 г., т. 90, стр. 15.
CAS
Статья
Google Scholar
Haber, J., Nattich, M., and Machej, T., Appl. Катал., В , 2008, т. 77, стр. 278.
CAS
Статья
Google Scholar
Komvokis, V.G., Marnellos, G.E., Vasalos, I.A., and Triantafyllidis, K.S., Appl.Катал., В, 2009, т. 89, стр. 627.
CAS
Статья
Google Scholar
Ким, С.С., Ли, С.Дж., и Хонг, С.С., J. Ind. Eng. Chem ., 2012, том 18, с. 1263.
CAS
Статья
Google Scholar
Ким, С.С., Ли, С.Дж., и Хонг, С.С., Chem. Англ. J. , 2011, т. 169, стр. 173.
CAS
Статья
Google Scholar
Ангелидис Т.N. and Tzitzios, V., Appl. Катал., В , 2003, т. 41, стр. 357.
CAS
Статья
Google Scholar
Лю, Х. и Ма, З., Чин. J. Chem. Eng ., 2018, т. 26, стр. 109.
CAS
Статья
Google Scholar
Kogel, M., Abu-Zied, B.M., Schwefer, M., and Turek, T., Catal. Commun ., 2001, т. 2, стр. 273.
CAS
Статья
Google Scholar
ван ден Бринк, Р.W., Booneveld, S., Pels, J.R., Bakker, D.F., and Verhaak, M.J.F.M., Appl. Катал., В, 2001, т. 32, стр. 73.
CAS
Статья
Google Scholar
Булушев Д.А., Киви-Минскер Л., Ренкен А., J. Catal., 2004, т. 222, стр. 389.
CAS
Статья
Google Scholar
Киви-Минскер Л., Булушев Д.А., Ренкен А., J. Catal., 2003, т. 219, стр. 273.
CAS
Статья
Google Scholar
Пирнгрубер Г.Д., J. Catal., 2003, т. 219, стр. 456.
CAS
Статья
Google Scholar
Берриер Э., Овсицер О., Кондратенко Э. В., Швиддер М., Грюнерт В., Брюкнер А., J. Catal., 2007, т. 249, стр. 67.
CAS
Статья
Google Scholar
Парк, Дж.-H., Choung, J.-H., Nam, I.-S., and Ham, S.-W., Appl. Катал., В , 2008, т. 78, стр. 342.
CAS
Статья
Google Scholar
Xia, H., Sun, K., Liu, Z., Feng, Z., Ying, P., and Li, C., J. Catal. , 2010, т. 270, стр. 103.
CAS
Статья
Google Scholar
Шен, К., Ву, М., Ван, Х., Сунь, Н., Хе, К., и Вэй, В., заявл. Серфинг. Науки ., 2018, т. 441, стр. 474.
CAS
Статья
Google Scholar
Садовска Г., Бернауэр М., Бернауэр Б., Табор Э., Вондрова А. и Собалик З., Catal. Commun ., 2018, т. 112, стр. 58.
CAS
Статья
Google Scholar
Табора, Э., Садовская, Г., Бернауэра, М., Сазама, П., Новакова, Дж., Филаб, В., Kmjecc, T., Kohout, J., Zaveta, K., and Sobalik, Z., Appl. Катал., В , 2019, т. 240, стр. 358.
Статья
CAS
Google Scholar
Лим, Дж. Б., Ча, С. Х. и Хонг, С. Б., Прил. Катал., В , 2019, т. 243, стр. 750.
CAS
Статья
Google Scholar
Фэнсон, П.Т., Страдт, М.В., Лаутербах, Дж., И Делгасс, В.Н., заявл. Катал., В , 2002, т. 38, стр. 331.
CAS
Статья
Google Scholar
Meng, T., Ren, N., and Ma, Z., J. Mol. Катал. А: Chem., 2015, т. 404–405, с. 233.
Статья
CAS
Google Scholar
Meng, T., Ren, N., and Ma, Z., Chin. J. Chem. Eng ., 2018, т. 26, стр. 1051.
CAS
Статья
Google Scholar
Палелла, Б.I., Cadoni, M., Frache, A., Pastore, H.O., Pirone, R., Russo, G., Coluccia, S., and Marchese, L., J. Catal., 2003, vol. 217, стр. 100.
CAS
Google Scholar
Zou, W., Xie, P., Hua, W., Wang, Y., Kong, D., Yue, Y., Ma, Z., Yang, W., и Gao, Z. , J. Mol. Катал. A: Chem. , 2014, т. 394, стр. 83.
CAS
Статья
Google Scholar
Лю X., Янг, З., Чжан, Р., Ли, К., и Ли, Ю., J. Phys. Chem , 2012, т. 116, стр. 20262.
CAS
Google Scholar
Лю X., Ян З., Ли Ю. и Чжан Ф., J. Mol. Катал. А: Химия, 2015, т. 396, стр. 181.
CAS
Статья
Google Scholar
Горювода М., Янч У., Краус М. и Лунд Дж. Патент ФРГ 102 004 024 026, 2004.
Jantsch, U., Lund, J., Gorywoda, M., and Kraus, M., Патент США 20 050 202 966, 2005 г.
Jantsch, U., Lund, J., Gorywoda, M., and Kraus, M., RU Patent 2 304 465, 2005.
Nirisen, O., Schoffel, K., Waller, D., and Ovrebo, D., WO Patent 0 202 230 , 2002.
Nirisen, O., Schoffel, K., Waller, D., and Ovrebo, D., WO Patent 02/02230, 2002.
Nirisen, O., Schoffel, K. ., Waller, D., и Ovrebo, D., Патент США 2004/0023796, 2004.
Schumacher, V., Bűrger, G., Fetzer, T., Baier, M., and Hesse, M. , WO Patent 99/55621, 1999.
Schumacher, V., Bűrger, G., Fetzer, T., Baier, M., and Hesse, M., Патент США 6743404, 2004.
Абё, К.М., Исследование катализатора разложения закиси азота Yara 58-Y1, Магистерская диссертация , Тронхейм: Норвежский университет науки и технологий, 2014.https://ntnuopen.ntnu.no/ntnu-xmlui/bitstream/handle/11250/2351725/10844_FULLTEXT.pdf?sequence= 1 & isAllowed = y
Google Scholar
Burckhardt, W., Froehlich, F., and Seifert, F., Key Eng. Материалы ., 1997, т. 132–136, с. 775.
Статья
Google Scholar
Буркхардт В., Зайферт Ф. и Винтерстайн Г., Патент WO 00/13789, 2000.
Neveu, G., WO Patent 99/64139, 1999.
Sermon, PA, US Patent 4 088 604, 1978.
Vernooy, PD, US Patent 2002/0123424, 2002.
Vernooy, PD, патент США 6429168, 2002.
Hamon, C. and Duclos, D., WO Patent 2004/052512, 2004.
Schwefer, M., Маурер Р. и Турек Т., патент WO 01/51415, 2001.
Jantsch, U., Лунд, Дж., Горивода, М., Краус, М., Патент США 2009/0130010, 2009.
Нойман Дж., Исупова Л., Пинаева Л., Куликовская Н., and Zolotarskii, I., WO Patent 2007/104403, 2007.
Jantzen, S., Neumann, J., and Novel, A., Семейство многофункциональных продуктов концепции MKS Umicore: помимо простого решения для N 2 O Abatement, Uhde Fertilizer Symposium , Dortmund, 2006.
Перес-Рамирес, Дж. И Сантьяго, М., Chem. Commun. , 2007, т. 6, стр. 619.
Статья
Google Scholar
Axon, S., Coupland, D., Foy, J., Ridland, J., and Wishart, I., WO Patent 2004/096703, 2004.
Machida, M., Eguchi , K., and Arai, H., J. Catal. , 1990, т. 123, стр. 477.
CAS
Статья
Google Scholar
Гроппи, Г., Cristiani, C., and Forzatti, P., J. Catal. , 1997, т. 168, стр. 95.
CAS
Статья
Google Scholar
Кикучи, Р., Иваса, Ю., Такегучи, Т., и Егучи, К., , заявл. Катал., А , 2005, т. 281, стр. 61.
Консолакис М., ACS Catal ., 2015, т. 5, вып. 11, стр. 6397.
CAS
Статья
Google Scholar
Чжан, Ю., Ван, X., Чжу, Y., и Zhang, T., Appl. Катал., В , 2013, т. 129, стр. 382.
CAS
Статья
Google Scholar
Байер, М., Фетцер, Т., Хофштадт, О., Гессе, М., Бюргер, Г., Харт, К., Шумахер, В., Вистуба, Х., и Отто, Б. , WO Patent 0 023 176, 2000.
Пинаева Л.Г., Исупова Л.А., Куликовская Н.А., Марчук А.А. Патент RU 28. 2430781, 2011.
Садыков В.А., Исупова Л.А., Золотарский И.А., Боброва Л.Н., Носков А.С., Пармон В.Н., Бруштейн Е.А., Телятникова Т.В., Чернышев В.И., Лунин В.В., Прил. Катал., А , 2000, т. 204, стр. 59.
Пинаева Л.Г., Просвирин И.П., Довлитова Л.С., Данилова И.Г., Садовская Е.М., Исупова Л.А., Catal. Sci. Технол ., 2016, т. 6, стр. 2150.
CAS
Статья
Google Scholar
Пинаева, Л.Г., Довлитова Л.С., Исупова Л.А. Кинет. Катал. , 2017, т. 58, нет. 2. п. 167.
CAS
Статья
Google Scholar
Giecko, G., Borowiecki, T., Gac, W., and Kruk, J., Catal. Сегодня , 2008 г., т. 137, стр. 403.
CAS
Статья
Google Scholar
Wu, Y., Ni, X., Beaurain, A., Dujardin, C., and Granger, P., Appl.Катал., В , 2012, т. 125, стр. 149.
CAS
Статья
Google Scholar
Wu, Y., Cordier, C., Berrier, E., Nuns, N., Dujardin, C., and Granger, P., Appl. Катал., В , 2013, т. 140–141, с. 151.
Статья
CAS
Google Scholar
EP Patent 2 616 165, 2011.
Granger, P., Esteves, P., Kieger, S., Navascues, L., and Leclercq, G., Appl. Катал., В , 2006, т. 62, стр. 236.
CAS
Статья
Google Scholar
Esteves, P., Wu, Y., Dujardin, C., Dongare, M.K., and Granger, P., Catal. Сегодня , 2011 г., т. 176, стр. 453.
CAS
Статья
Google Scholar
Крук, Дж., Столецкий, К., Михальска, К., Конкол, М., и Ковалик, П., Catal. Сегодня , 2012 г., т. 191, стр. 125.
CAS
Статья
Google Scholar
Кондратенко Е.В., Гелден В., Соколов С., ChemCatChem. , 2010, т. 2, стр. 633.
CAS
Статья
Google Scholar
Модуляция производства и активности оксида азота эндотелия с помощью таурина и таурин-конъюгированных желчных кислот
Основные моменты
- •
Таурин и таурин-конъюгированные желчные кислоты (ТВК) регулируют продукцию и активность NO.
- •
Сигнал TBA от рецепторов FXR, TGR5, M3 и S1PR2 на эндотелиальных клетках.
- •
Таурин и ТВА — потенциальные стратегии профилактики сосудистых заболеваний.
Abstract
Таурин — это полуосновная аминокислота, обнаруженная в высоких концентрациях в плазме и клетках млекопитающих, где она регулирует клеточные функции, такие как поток ионов, контролирует объем клеток и служит субстратом для конъюгированных желчных кислот (БК).Экзогенное введение как таурина, так и таурин-конъюгированных БА также вовлечено в модуляцию сердечно-сосудистых функций. В этом кратком обзоре суммируется роль таурина и конъюгированных с таурином ЖК в сосудистой релаксации за счет модуляции оксида азота (NO), производного эндотелия. Влияние таурина на здоровье сосудов противоречиво. Однако при наличии кардиометаболических факторов риска было высказано предположение, что таурин может повышать уровни NO в сосудах за счет увеличения экспрессии eNOS, фосфорилирования eNOS на Ser1177, биодоступности NO, уровня антиоксидантной защиты и асимметричного диметиларгинина ингибитора l-аргинина / NOS. (ADMA) соотношение.Также сообщалось, что опосредованная таурином BA-опосредованная активация рецептора Фарнезоида X (FXR), рецептора BA, связанного с G-белком (TGR5) и / или мускаринового рецептора 3 (M3), также увеличивает продукцию NO в сосудах. Активация FXR увеличивает экспрессию eNOS и может снизить образование ADMA, в то время как TGR5 увеличивает мобилизацию Ca 2+ и фосфорилирование eNOS и Akt в эндотелиальных клетках. Кроме того, таурин и конъюгированные с таурином БА могут регулировать синтез и активность NO, увеличивая образование H 2 S.Несколько исследований продемонстрировали положительное влияние таурина и таурин-конъюгированных БА на изменение эндотелиальной дисфункции, связанной с диабетом, атеросклерозом, гипертонией, ожирением, недоеданием и курением. Кроме того, БА, конъюгированные с таурином, стали потенциальным средством лечения портальной гипертензии. Несмотря на эти благоприятные результаты, существует необходимость в дальнейшем изучении механизмов и сигнальных путей, лежащих в основе эндотелиальных эффектов таурина и таурин-конъюгированных БА.Здесь мы суммируем основные результаты, касающиеся влияния таурина и таурин-конъюгированных БА на эндотелиальную дисфункцию, связанную с измененным метаболизмом NO при сердечно-сосудистых заболеваниях.
Ключевые слова
Оксид азота
Таурин
Таурин-конъюгированные желчные кислоты
Эндотелий
Расширение сосудов
Рекомендуемые статьи Цитирующие статьи (0)
Полный текст
© 2019 Elsevier Inc. Все права защищены.
Рекомендуемые статьи
Ссылки на статьи
Оксид азота | DermNet NZ
Автор: Д-р Шарника Абейакирти, дерматолог, Коломбо, Шри-Ланка, 2009 г.Пересмотрено в октябре 2020 г.
Что такое оксид азота?
Оксид азота — это небольшая газообразная молекула, также известная как окись азота, с химической формулой NO.
Молекула оксида азота синтезируется из молекулярного азота и кислорода при очень высоких температурах> 10 000 ° C. Это происходит естественным образом в окружающей среде во время молнии.
В лаборатории оксид азота можно получить восстановлением азотной или азотистой кислоты. Оксид азота имеет температуру плавления -163.6 ° C (109,6 K) и температуре кипения -151,7 ° C (121,4 K).
Оксид азота называется свободным радикалом, потому что он содержит в своей молекуле отдельные неспаренные электроны. Следовательно, он является реактивным и имеет период полураспада всего несколько секунд.
Считается загрязнителем воздуха, ответственным за разрушение озонового слоя. Оксид азота реагирует с кислородом (O2) и озоном (O3) с образованием диоксида азота (NO 2 ), коричневого дыма и загрязнителя окружающей среды. Оксид азота, образующийся в автомобильных двигателях, на промышленных предприятиях и на электростанциях, является причиной кислотных дождей и смога.
Однако было показано, что этот токсичный загрязнитель окружающей среды является очень важной сигнальной молекулой в живых организмах, включая организм человека.
Какую роль играет оксид азота в организме?
Некоторые из известных функций оксида азота перечислены в таблице ниже.
| Сердечно-сосудистая система |
|
| Нервная система |
|
| Легкие |
|
| Желудочно-кишечный тракт |
|
| Почечная система |
|
| Иммунная система |
|
Какова роль оксида азота в коже?
Оксид азота контролирует кожную микроциркуляцию. Оксид азота:
- Модулирует сосудорасширяющую реакцию кожи на местное нагревание и ультрафиолет-B (UVB)
- Опосредует кожный отек и воспаление
- Участвует в пигментации кожи за счет меланогенеза, индуцированного ультрафиолетом
- Может способствовать нарушению барьерной функции
- Способствует заживлению ран за счет клеточной пролиферации и ангиогенеза.
Оксид азота обладает антимикробными свойствами в отношении микроорганизмов.
- Бактерии — Staphylococcus aureus
- Дерматофиты — Trichophyton rubrum , Trichophyton mentagrophytes
- Дрожжи — Candida albicans
Оксид азота также играет важную роль в заболеваниях кожи, опосредованных Т-клетками, и он обладает как про, так и антиапоптотическими свойствами в зависимости от его концентрации, типа клеток и доступности других субстратов.
Как в организме человека образуется оксид азота?
Люди производят оксид азота по нескольким механизмам.
- Из аминокислоты L-аргинин с помощью фермента синтазы оксида азота (NOS)
- Из неорганических нитратов в зеленых листовых овощах, фруктах, злаках и вяленом мясе
Синтаза оксида азота имеет 3 изоформы:
- Нейрональная БДУ — nNOS или БДУ I
- Inducible NOS — iNOS или NOS II
- Эндотелиальная БДУ — eNOS или БДУ III
Нейрональная БДУ и эндотелиальная БДУ являются конститутивными ферментами.Их уровни в организме человека относительно стабильны. Они обнаружены в эндотелиальных клетках, нейронах, скелетных мышцах, эпителиальных клетках и многих других тканях.
NOS II индуцируется и стимулируется специфическими цитокинами. Большинство клеток человеческого тела синтезируют iNOS в ответ на воспалительные процессы.
Как кожа производит оксид азота?
Поскольку все 3 изоформы NOS присутствуют либо в клетках эпидермиса, либо в клетках дермы, либо в обоих, кожа может производить оксид азота по ферментно-зависимому механизму.
Кожа человека может выделять оксид азота независимо от ферментов за счет фотолиза запасов оксида азота УФА.
Оксид азота также образуется путем снижения нитрата пота комменсальными бактериями кожи, в частности стафилококками.
Как оксид азота хранится в организме человека?
Оксид азота обычно не существует в организме в свободной форме из-за своей нестабильной природы, но вступает в реакцию с другими молекулами с образованием более стабильных продуктов.
- В крови оксид азота имеет очень короткий период полураспада и быстро окисляется до нитрита.Затем он дополнительно окисляется оксигемоглобином с образованием нитрата. Оксид азота также напрямую реагирует с оксигемоглобином с образованием метгемоглобина и нитрата.
- Реакции с остатками цистеина в белках приводят к образованию нитрозилированных продуктов. Из-за своего высокого сродства к сульфгидрильным группам (тиолам) S-нитрозотиолы (RSNO) являются наиболее распространенным нитрозилированным продуктом в плазме.
Нитрат — это основная форма хранения оксида азота. Он очень стабилен по сравнению с другими формами хранения, такими как нитриты и RSNO, которые являются важными переносчиками и донорными молекулами оксида азота.
Как можно проверить на оксид азота?
Тесты на сам оксид азота отсутствуют, так как он слишком нестабилен. Вместо этого нитраты, нитриты и нитрозилированные соединения можно измерить с помощью следующих тестов.
- Анализ Грисса
- Анализ Сэвилла
- Спектроскопия электронного парамагнитного резонанса (ЭПР)
- Хемилюминесцентный метод
Дефицит оксида азота
Предполагается, что дефицит оксида азота играет роль в нескольких расстройствах.
- Эссенциальная гипертензия (высокое кровяное давление)
- Врожденные аномалии, включая ахалазию кардии, гипертрофический пилорический стеноз и болезнь Гиршпрунга
- Хроническая болезнь почек
Недостаток оксида азота в коже может привести к псориазу, способствуя пролиферации клеток и уменьшая дифференцировку клеток кожи.
- Считается, что пониженные уровни eNOS в эндотелиальных клетках, выстилающих кровеносные сосуды кожи, способствуют развитию системного склероза и морфеи (локализованной склеродермии).
Избыточный оксид азота
Употребление пищи, богатой нитратами и нитритами, увеличивает уровень оксида азота и его форму хранения. Так же, как дефицит оксида азота может привести к болезням, слишком большое количество также может вызвать болезнь.
Оксид азота выделяется из сосудистой сети головного мозга, тканей мозга и нервных окончаний.
- Может вызывать головную боль при мигрени.
- Он может повредить клетки мозга, что приведет к нейродегенеративным заболеваниям, таким как болезнь Паркинсона, болезнь Альцгеймера, болезнь Хантингтона и боковой амиотрофический склероз.
Оксид азота, продуцируемый β-клетками поджелудочной железы, может повреждать клетки (апоптоз), вызывая диабет 1 типа.
В коже ультрафиолетовое облучение может привести к чрезмерному производству оксида азота посредством ферментно-зависимых и независимых механизмов. Оксид азота играет роль в стимулировании и росте меланомы посредством множества механизмов.
Лечебный потенциал оксида азота
Благодаря своим антимикробным свойствам гелевый состав, высвобождающий оксид азота, бердазимер натрия (SB206, SB207, Novan), проходит оценку для лечения дерматофитных грибковых инфекций, таких как дерматофития стопы и вирусных кожных инфекций. включая остроконечные кондиломы и контагиозный моллюск.
исследований проливают новый свет на то, как образуется оксид азота | VUMC Reporter
Исследования, начатые в рамках исследовательского сотрудничества Джуди Ашнер, доктора медицины, приняли неожиданный поворот и привели к совершенно новому пониманию того, как образуется оксид азота — важная сигнальная молекула в организме.
«Наши результаты удивили всех», — сказала Ашнер, профессор педиатрии Джулии Карелл Штадлер и директор отделения неонатологии Университета Вандербильта.
В декабрьском выпуске Nature Medicine Ашнер и его коллеги из Медицинского колледжа Бейлора сообщают, что фермент под названием ASL (аргининосукцинатлиаза) — часть цикла мочевины, которая удаляет аммиак из организма, — играет ранее неизвестную и ключевую роль в производство оксида азота.
Среди множества видов биологической активности оксид азота расслабляет кровеносные сосуды и увеличивает кровоток (это основа для использования нитроглицерина при лечении сердечной стенокардии).
Интерес Ашнер к молекуле проистекает из ее клинического опыта в отделении интенсивной терапии новорожденных, где у младенцев часто возникают заболевания легких, сопровождающиеся легочной гипертензией (высокое кровяное давление в легочных артериях). По словам Ашнера, оксид азота, газ, является одним из немногих вариантов лечения легочной гипертензии у новорожденных, но он дорог и сложен в применении.
Джуди Ашнер
«В течение многих лет мы концентрировались на пути оксида азота, чтобы найти новые методы лечения, которые могут улучшить результаты у детей с легочной гипертензией», — сказал Ашнер.
В организме фермент синтаза оксида азота (NOS) производит оксид азота из аминокислоты аргинина. Ашнер и его коллеги обнаружили, что NOS присутствует в мультибелковом комплексе, который важен для активации NOS и производства оксида азота.
Фермент ASL также присутствует в комплексе, и текущие исследования показывают, что ASL необходим для образования комплекса. Исследователи демонстрируют, что мыши со сниженной экспрессией ASL не собирают мультибелковый комплекс и не производят достаточного количества оксида азота.
Открытие также дает новое понимание научной загадки — так называемого «аргининового парадокса» — что добавление в клетки дополнительного количества аргинина увеличивает производство оксида азота, даже если в клетке более чем достаточно аргинина для насыщения фермента NOS.
Теперь, сказал Ашнер, похоже, что «NOS не может использовать любую молекулу аргинина, которая есть поблизости; аргинин должен быть доставлен непосредственно в NOS через этот мультибелковый комплекс ».
Ашнер особенно взволнован последствиями результатов исследования для младенцев с легочной гипертензией.По ее словам, у недоношенных детей есть «биохимическая незрелость» многих ферментных систем, включая ферменты цикла мочевины, такие как ASL, которые могут увеличить риск хронических заболеваний легких и легочной гипертензии за счет снижения выработки оксида азота.
В рамках нового гранта Национального института здравоохранения для Ашнер ее команда набирает недоношенных новорожденных для изучения биомаркеров в пути цикла оксид азота-мочевина (включая аминокислоты аргинин и цитруллин).
«Если окажется, что у младенцев, у которых развиваются хронические заболевания легких, наблюдается дефицит аргинина или цитруллина, то введение этих аминокислот будет представлять собой диетическую терапию, которая должна быть безопасной и потенциально может изменить правила игры для недоношенных детей.”
Она и ее коллеги уже продемонстрировали на двух моделях животных, что диетические добавки с цитруллином обращают вспять болезнь легких у новорожденных.
Идея цитруллина в качестве терапии (он тестируется для предотвращения легочной гипертензии у детей, перенесших операцию на сердце) родилась в Вандербильте в исследованиях, проведенных Риком Барром, доктором медицины, и Маршаллом Саммаром, доктором медицины. понимание действия цитруллина как части цикла производства оксида азота.
«Я думаю, что мы находимся на пороге чего-то, что может изменить представление о том, как мы лечим младенцев с риском хронических заболеваний легких или с хроническими формами легочной гипертензии», — сказал Ашнер. «Я очень рад этому, потому что в настоящее время у нас нет хороших профилактических или лечебных стратегий для младенцев с этими состояниями».
Исследование поддержано грантами Национальных институтов здравоохранения.
Катализатор на основе оксида металла, модифицированного карбоновой кислотой, для аэробного аммоксидирования с регулируемой селективностью
Альфонсо, И. и Готор, В. Биокаталитические и биомиметические реакции аминолиза: полезные инструменты для селективных преобразований на полифункциональных субстратах. Chem. Soc. Ред. 33 , 201–209 (2004).
CAS
Статья
PubMed
Google Scholar
Ohshima, T., Iwasaki, T., Maegawa, Y., Yoshiyama, A. & Mashima, K. Ферментоподобное хемоселективное ацилирование спиртов в присутствии аминов, катализируемое четырехъядерным цинковым кластером. J. Am. Chem. Soc. 130 , 2944–2945 (2008).
CAS
Статья
PubMed
Google Scholar
Де Саркар, С., Гримм, С. и Студер, А. Катализируемое NHC окисление альдегидов до сложных эфиров: хемоселективное ацилирование спиртов в присутствии аминов. J. Am. Chem. Soc. 132 , 1190–1191 (2010).
Артикул
PubMed
Google Scholar
Sasano, Y. et al. Высокохемоселективное аэробное окисление аминоспиртов до аминокарбонильных соединений. Angew. Chem. Int. Эд. 53 , 3236–3240 (2014).
CAS
Статья
Google Scholar
Корма А. и Серна П. Хемоселективное гидрирование нитросоединений с использованием золотых катализаторов на носителе. Наука 313 , 332–334 (2006).
ADS
CAS
Статья
PubMed
Google Scholar
Tan, Y. et al. Нанокластеры Au 25 на основе ZnAl-гидроталькита в качестве предварительных катализаторов для хемоселективного гидрирования 3-нитростирола. Angew. Chem. Int. Эд. 56 , 2709–2713 (2017).
CAS
Статья
Google Scholar
Zhang, J. et al. Углеродные нанотрубки с модифицированной поверхностью катализируют окислительное дегидрирование н-бутана. Science 322 , 73–77 (2008).
ADS
CAS
Статья
PubMed
Google Scholar
Studt, F. et al. О роли поверхностных модификаций палладиевых катализаторов в селективном гидрировании ацетилена. Angew. Chem. Int. Эд. 47 , 9299–9302 (2008).
CAS
Статья
Google Scholar
Vang, R. T. et al. Управление селективностью разрыва каталитических связей на поверхностях Ni с помощью ступенчатой блокировки. Nat. Матер. 4 , 160–162 (2005).
ADS
CAS
Статья
PubMed
Google Scholar
Хьюз М. Д., Йи-Джун X., Дженкинс П. и Макморн П. Настраиваемые золотые катализаторы для селективного окисления углеводородов в мягких условиях. Природа 437 , 1132–1135 (2005).
ADS
CAS
Статья
PubMed
Google Scholar
Шенбаум, К. А., Шварц, Д. К. и Медлин, Дж. У. Управление поверхностной средой гетерогенных катализаторов с помощью самоорганизующихся монослоев. В соотв.Chem. Res. 47 , 1438–1445 (2014).
CAS
Статья
PubMed
Google Scholar
Альмора-Барриос, Н., Кано, И., ван Левен, П. В. и Лопес, Н. Согласованное хемоселективное гидрирование акролеина на наночастицах золота, украшенных вторичным оксидом фосфина. ACS Catal. 7 , 3949–3954 (2017).
CAS
Статья
Google Scholar
Marshall, S.T. et al. Контролируемая селективность для палладиевых катализаторов с использованием самоорганизующихся монослоев. Nat. Матер. 9 , 853–858 (2010).
ADS
CAS
Статья
PubMed
Google Scholar
Makosch, M. et al. Модифицированные органическими тиолами катализаторы Pt / TiO 2 для контроля хемоселективного гидрирования замещенных нитроаренов. ACS Catal. 2 , 2079–2081 (2012).
CAS
Статья
Google Scholar
Wu, B., Huang, H., Yang, J., Zheng, N. & Fu, G. Селективное гидрирование α, β-ненасыщенных альдегидов, катализируемое нанокристаллами платины и кобальта с аминовыми группами. Angew. Chem. Int. Эд. 51 , 3440–3499 (2012).
CAS
Статья
Google Scholar
Кахсар, К. Р., Шварц, Д. К.И Медлин, Дж. У. Контроль селективности металлического катализатора посредством специфических нековалентных молекулярных взаимодействий. J. Am. Chem. Soc. 136 , 520–526 (2013).
Артикул
PubMed
Google Scholar
Панг, С. Х., Шенбаум, К. А., Шварц, Д. К. и Медлин, Дж. У. Направление путей реакции путем выбора активного центра катализатора с использованием самоорганизующихся монослоев. Nat. Commun. 4 , 2448 (2013).
ADS
PubMed
Google Scholar
Jeong, H., Kim, C., Yang, S. & Lee, H. Селективное гидрирование фурановых альдегидов с использованием катализаторов из наночастиц Ni, покрытых органическими молекулами. J. Catal. 344 , 609–615 (2016).
CAS
Статья
Google Scholar
Кумар, Г., Лиен, К. Х., Яник, М. Дж. И Медлин, Дж.W. Выбор сайта катализатора через контроль над нековалентными взаимодействиями в самоорганизующихся монослоях. ACS Catal. 6 , 5086–5094 (2016).
CAS
Статья
Google Scholar
Шредер И., Варнеке Дж., Бакенкёлер Дж. И Кунц С. Функционализация наночастиц платины L-пролином: одновременное повышение каталитической активности и селективности. J. Am. Chem. Soc. 137 , 905–912 (2015).
CAS
Статья
PubMed
Google Scholar
Лю П., Цинь Р., Фу Г. и Чжэн Н. Координационная химия поверхности металлических наноматериалов. J. Am. Chem. Soc. 139 , 2122–2131 (2017).
CAS
Статья
PubMed
Google Scholar
Tamura, M., Kishi, R., Nakagawa, Y. & Tomishige, K. Самособирающиеся гибридные катализаторы на основе оксидов металлов, полученные простым смешиванием с органическими модификаторами. Nat. Commun. 6 , 8580 (2015).
ADS
CAS
Статья
PubMed
PubMed Central
Google Scholar
Эллис, Л. Д., Тротье, Р. М., Масгрейв, К. Б., Шварц, Д. К. и Медлин, Дж. У. Управление реакционной способностью поверхности диоксида титана с помощью электронной настройки самоорганизующихся монослоев. ACS Catal. 7 , 8351–8357 (2017).
CAS
Статья
Google Scholar
Эртль, Г. Элементарные этапы гетерогенного катализа. Angew. Chem. Int. Эд. 29 , 1219–1227 (1990).
Артикул
Google Scholar
Лоффреда Д., Дельбек Ф., Винье Ф. и Сотет П. Каталитическое гидрирование ненасыщенных альдегидов на Pt (111): понимание селективности из расчетов из первых принципов. Angew. Chem. Int. Эд. 44 , 5279–5282 (2005).
CAS
Статья
Google Scholar
Chen, C. et al. Супергидрофобный нанокомпозит на основе SiO 2 , модифицированный органическими группами в качестве катализатора селективного окисления этилбензола. J. Mater. Chem. А 2 , 8126–8134 (2014).
CAS
Статья
Google Scholar
Wang, M. et al. Понимание смачиваемости носителя при настройке каталитических характеристик при окислении алифатических спиртов до кислот. Chem. Commun. 49 , 6623–6625 (2013).
CAS
Статья
Google Scholar
Chen, C. et al. Супергидрофобные материалы как эффективные катализаторы селективного окисления углеводородов. Chem. Commun. 47 , 1336–1338 (2011).
CAS
Статья
Google Scholar
Jia, X. et al. Щелочной α-MnO 2 / Na x MnO 2 совместно катализирует тандемную реакцию аммоксидирования – Пиннера альдегидов. Catal. Sci. Technol. 6 , 7429–7436 (2016).
CAS
Статья
Google Scholar
Jia, X. et al. Каталитическое превращение 5-гидроксиметилфурфурола в дигидрохлорид 2,5-фурандиамидина. Green Chem. 18 , 974–978 (2016).
CAS
Статья
Google Scholar
Li, X. et al. Каталитическое амидирование 5-гидроксиметилфурфурола до 2,5-фурандикарбоксамида над щелочными оксидами марганца. Подбородок. J. Chem. 35 , 984–990 (2017).
CAS
Статья
Google Scholar
Тамура М. и Томишиге К. Редокс-свойства CeO 2 при низкой температуре: прямой синтез иминов из спирта и амина. Angew. Chem. Int. Эд. 54 , 864–867 (2015).
CAS
Статья
Google Scholar
Бадри А., Бине К. и Лавелли Дж. С. Использование метанола в качестве ИК-молекулярного зонда для исследования поверхности поликристаллического церия. J. Chem. Soc., Faraday Trans. 93 , 1159–1168 (1997).
CAS
Статья
Google Scholar
Барто, М. А. Требования к участку реакций на оксидных поверхностях. J. Vac. Sci. Technol. A. 11 , 2162–2168 (1993).
ADS
CAS
Статья
Google Scholar
Гершер В. А., Кокс Д. Ф. и Темлин Дж. М. Химия с контролируемыми кислородными вакансиями на поверхности оксида металла: диссоциация и окисление метанола на SnO 2 (110). Прибой. Sci. 306 , 279–293 (1994).
ADS
CAS
Статья
Google Scholar
Аллара Д. Л. и Нуццо Р. Г. Спонтанно организованные молекулярные сборки. 1. Образование, динамика и физические свойства н-алкановых кислот, адсорбированных из раствора на окисленной поверхности алюминия. Langmuir 1 , 45–52 (1985).
CAS
Статья
Google Scholar
Аллара Д. Л. и Нуццо Р. Г. Спонтанно организованные молекулярные сборки. 2. Количественное инфракрасное спектроскопическое определение равновесных структур адсорбированных в растворе н-алкановых кислот на окисленной поверхности алюминия. Langmuir 1 , 52–66 (1985).
CAS
Статья
Google Scholar
Пуджари, С. П., Шерес, Л., Марселис, А., Зуилхоф, Х. Ковалентная модификация поверхности оксидов. Angew. Chem. Int. Эд. 53 , 6322–6356 (2014).
CAS
Статья
Google Scholar
Накамото, К. Инфракрасные и рамановские спектры неорганических и координационных соединений, Часть B, Приложения в координации, металлоорганической и биоинорганической химии 6-е изд. (Wiley, 2009).
Persson, P., Karlsson, M. & Öhman, L.O. Координация ацетата с Al (III) в водном растворе и на границе раздела вода-гидроксид алюминия: исследование FTIR потенциометрического и ослабленного полного отражения. Геохим. Космохим. Acta 62 , 3657–3668 (1998).
ADS
CAS
Статья
Google Scholar
Оямяэ, Л., Аулин, К., Педерсен, Х. и Келл, П. О. ИК и квантово-химические исследования адсорбции карбоновой кислоты и глицина на наночастицах рутилового TiO 2 . J. Colloid Interface Sci. 296 , 71–78 (2006).
ADS
Статья
PubMed
Google Scholar
Biswas, S. et al. Легкий доступ к универсальным функциональным группам из спирта с помощью единственного многофункционального многоразового катализатора. заявл. Катал. B-Environ. 203 , 607–614 (2017).
CAS
Статья
Google Scholar
Ямагути, К., Кобаяши, Х., Оиши, Т. и Мизуно, Н. Гетерогенно катализируемый синтез первичных амидов непосредственно из первичных спиртов и водного раствора аммиака. Angew. Chem. Int. Эд. 51 , 544–547 (2012).
CAS
Статья
Google Scholar
Ishida, T. et al. Катализируемое оксидом металла аммоксидирование спиртов в нитрилы и промотирующий эффект наночастиц золота для однореакторного синтеза амида. заявл. Катал. A-Gen. 425 , 85–90 (2012).
Артикул
Google Scholar
van Putten, R. -J. и другие. Гидроксиметилфурфурол — универсальный химический продукт, производимый из возобновляемых источников. Chem. Ред. 113 , 1499–1597 (2013).
Артикул
PubMed
Google Scholar
Nicolaou, K., Pavia, M. & Seitz, S.Углеводы в органическом синтезе. Синтез макролидных антибиотиков с 16-членным кольцом. 5. Полный синтез O-мицинозилтилонолида: синтез ключевых промежуточных продуктов. J. Am. Chem. Soc. 104 , 2027–2029 (1982).
CAS
Статья
Google Scholar
Трост Б. М., Сюй Дж. И Райхл М. Энантиоселективный синтез α-третичных гидроксиальдегидов путем катализируемого палладием асимметричного аллильного алкилирования енолятов. J. Am. Chem. Soc. 129 , 282–283 (2007).
CAS
Статья
PubMed
PubMed Central
Google Scholar
Лепенис, Б., Инь, Дж. И Сибергер, П. Х. Применение синтетических углеводов в химической биологии. Curr. Opin. Chem. Биол. 14 , 404–411 (2010).
CAS
Статья
PubMed
Google Scholar
Tattersall, D. B. et al. Устойчивость к травоядным животным благодаря искусственному синтезу цианогенных глюкозидов. Наука 293 , 1826–1828 (2001).
ADS
CAS
Статья
PubMed
Google Scholar
Bjarnholt, N. & Møller, B.L. Гидроксинитрилглюкозиды. Фитохимия 69 , 1947–1961 (2008).
CAS
Статья
PubMed
Google Scholar
Bjarnholt et al. Разнообразие древней темы: гидроксинитрилглюкозиды. Фитохимия 69 , 1507–1516 (2008).
CAS
Статья
PubMed
Google Scholar
Салициловая кислота активирует синтез оксида азота у арабидопсиса | Журнал экспериментальной ботаники
Аннотация
Взаимосвязь между оксидом азота (NO) и салициловой кислотой (SA) была исследована на Arabidopsis thaliana .Здесь показано, что SA способна индуцировать синтез NO дозозависимым образом в Arabidopsis . Продукция NO была обнаружена с помощью конфокального микроскопического анализа и спектрофлуориметрического анализа в корнях растений и культивируемых клетках. Чтобы идентифицировать метаболические пути, участвующие в SA-индуцированном синтезе NO, были приняты генетические и фармакологические подходы. Анализ мутанта nia1, nia2 показал, что активность нитратредуктазы не требуется для SA-индуцированной продукции NO. Эксперименты, проведенные в присутствии ингибитора синтазы оксида азота (NOS), предположили участие NOS-подобной ферментативной активности в этом метаболическом пути.Более того, продукция NO при обработке SA мутантных растений Atnos1 была сильно снижена по сравнению с растениями дикого типа. Были идентифицированы компоненты сигнального пути SA, приводящие к продукции NO, и было продемонстрировано участие как кальция, так и казеинкиназы 2 (CK2). Взятые вместе, эти результаты предполагают, что SA индуцирует продукцию NO, по крайней мере, частично за счет активности NOS-подобного фермента и что активность кальция и CK2 являются важными компонентами сигнального каскада.
Введение
Салициловая кислота (СК) — это фенольное соединение, влияющее на ряд физиологических процессов в растениях, включая термогенез, синтез этилена и созревание плодов (Rhoads and McIntosh, 1992). Он также играет роль в реакции растений на различные абиотические стрессы, такие как УФ-излучение и воздействие озона (Rao and Davis, 1999; Senaratna et al., 2000), в различных условиях развития или в ответ на различные биологические стимулы, например, во время нодуляция (Stacey et al., 2006). Роль SA во время атаки патогена особенно важна (Yang et al. , 1997) как в стимулировании местного ответа, так и в системной приобретенной устойчивости (SAR) (Alvarez, 2000). Фактически, при инфильтрации SA в листьев Arabidopsis индуцируется тот же набор генов, активированных инфекцией патогена (Uknes et al. , 1992). Также сообщалось, что после инокуляции листьев микроорганизмом, способным индуцировать SAR, СК накапливается в очень высоких концентрациях не только в листьях и в стебле, но и в корнях, где СК достигает концентраций выше, чем у растений. ткани, расположенные рядом с местом заражения (Kubota and Nishia 2006).
Оксид азота (NO) — это высокоактивная газообразная молекула, участвующая в различных патофизиологических процессах (Neill et al. , 2003; Grün et al. , 2006). Важным достижением в понимании функций NO у растений стало определение различных путей биосинтеза NO (Lamotte et al. , 2005), и, фактически, NO может образовываться цитоплазматической нитратредуктазой (cNR), нитрит-NO редуктазой. (NI-NOR) или неидентифицированными белками, проявляющими активность NOS (синтазы оксида азота).cNR, по-видимому, действует в анаэробных условиях в присутствии высоких концентраций нитритов (Yamasaki, 2000; Yamasaki and Sakihama, 2000), чаще в корнях, чем в листьях (Stöhr, 1999). В корнях NO также может образовываться NI-NOR, который использует нитрит в качестве субстрата (Stöhr et al. , 2001). Недавно был выделен мутант Arabidopsis с измененной продукцией NO (Atnos1 ) (Guo et al. , 2003). Первоначально считалось, что он изменен в активности NOS, локализованной на митохондриальном уровне (Guo and Crawford, 2005).Однако недавно было исключено, что белок AtNOS1 обладает активностью NOS (Zemojtel et al. , 2006), но этот мутант по-прежнему полезен из-за своего фенотипа, который показывает пониженные уровни NO (He et al. , 2004; Zeidler et al., 2004; Bright et al. , 2006).
При гиперчувствительной реакции, активируемой патогенами, NO и активные формы кислорода (ROS) действуют как сигнальные молекулы (Delledonne, 2005). АФК и NO также участвуют в регуляции биосинтеза SA (Durner et al., 1998). Некоторые модели подтверждают, что передача сигналов окислительно-восстановительного потенциала посредством NO и ROS усиливается с помощью SA в процессе самоусиливания (Klessig et al. , 2000). Тем не менее, взаимосвязь между NO, SA и ROS в активации защитных генов и / или индукции гибели клетки-хозяина четко не определена.
В этом отчете представлены экспериментальные доказательства того, что SA активирует синтез NO как в корнях Arabidopsis , так и в культивируемых клетках, и что это производство NO происходит, по крайней мере, частично, посредством NOS-зависимого пути.
Материалы и методы
Материалы
Ингибитор NOS N G -монометил-L-аргинин (L-NMMA) был от Alexis (Винчи, Италия). Специфический для казеинкиназы 2 (CK2) ингибитор 4,5,6,7-тетрабромбензотриазол (TBB) использовали в конечной концентрации 30 мкМ (Ruzzene et al. , 2002). Все остальные химические вещества были от Sigma-Aldrich (Милан, Италия). Салицилат натрия растворяли в воде. Ингибиторы киназ растворяли в диметилсульфоксиде (ДМСО) в указанных концентрациях, и такое же количество растворителя использовали для контрольных экспериментов.
Клеточные культуры и растительный материал
Клеточная линия Arabidopsis была получена, как описано в Carimi et al. (2005). Опыты на проростках растений проводили на Arabidopsis дикого типа, nia1, nia2 (Nottingham Arabidopsis Stock Center) и Atnos1 мутантов экотипа Columbia-0. Поверхность семян стерилизовали погружением в 4% гипохлорид натрия (об. / Об.) И пять раз промывали дистиллированной стерильной водой перед переносом в отвержденную среду MS (Murashige and Skoog, 1962) (7 г на агар типа M -1 ).Все эксперименты проводились на проростках 5-дневного возраста.
НЕТ количественного определения
Флуорометрический анализ:
Проницаемое для клеток производное диацетата диаминофлуоресцеин-FM (DAF-FM DA; Alexis Biochemicals, Cod 620-071-M001) использовали в качестве специфического флуоресцентного зонда для обнаружения внутриклеточного NO (Gould et al. , 2003).
Пятидневные проростки Arabidopsis инкубировали в течение 15 мин в загрузочном буфере (5 мМ MES-KOH, pH 5.7, 0,25 мМ KCl, 1 мМ CaCl 2 ) с или без ингибитора NOS (1 мМ L-NMMA), ингибиторов протеинкиназы (2 мкМ K252a, 30 мкМ TBB) или акцептора NO cPTIO [0,5 мМ, 2- ( 4-карбоксифенил) -4,4,5,5-тетраметилимидазолин-1-оксил-3-оксид]. Затем проростки инкубировали в течение 15 минут в том же загрузочном буфере, содержащем 15 мкМ DAF-FM DA, после чего 20 минут промывали загрузочным буфером для удаления избытка флуоресцентного зонда. Затем проростки инкубировали в буфере с SA или без нее в течение разного времени в присутствии или в отсутствие различных ингибиторов.В экспериментах без кальция кальций удаляли из буферов после загрузки DAF.
Флуоресценцию DAF-FM оценивали с помощью конфокальной лазерной сканирующей микроскопии (возбуждение 488 нм, эмиссия 515–530 нм; Nikon PCM2000). Интенсивность пикселей флуоресцентных изображений, полученных с помощью конфокального микроскопа, определяли с помощью программного обеспечения ImageJ (NIH, США). Значения были скорректированы на фон.
Представленные конфокальные изображения представляют три различных эксперимента, в которых по меньшей мере пять проростков были проанализированы для каждой обработки ( n = 15).
Спектрофотометрический анализ:
Концентрацию NO измеряли путем мониторинга превращения оксигемоглобина (HbO 2 ) в метгемоглобин (metHb) в среде культивируемых клеток, как описано Мерфи и Ноак (1994). Для анализа NO 1 мл суспензии клеток Arabidopsis инкубировали с 100 ед. Мл -1 каталазы (Sigma) и 100 ед. Мл -1 супероксиддисмутазы (Sigma) в течение 5 минут для удаления ROS перед добавлением HbO 2 (конечная концентрация 10 мкМ, гемоглобин-A 0 человек, Sigma).Затем клетки разделяли фильтрацией через хроматографические колонки (Bio-Rad, 731-1550) и собирали 0,8 мл среды для определения NO. NO определяли количественно путем измерения спектрофотометрически (лямбда-спектрофотометр Perkin-Elmer) после преобразования HbO 2 в metHb при 401 нм и 421 нм, используя коэффициент экстинкции 77 мМ -1 см -1 ( A 401 HbO 2 — A 421 metHb). Приведенные значения были скорректированы на базальное содержание NO в необработанных клетках.
Для этих экспериментов использовался рандомизированный полный блок-дизайн с тремя повторностями (отдельные колбы Эрленмейера). Каждый эксперимент повторяли трижды ( n = 9).
Анализ активности СК2
Эндогенную активность СК2 измеряли на белковых экстрактах, полученных из 5-дневных проростков Arabidopsis , согласно Zottini et al. (2002). Аликвоту экстрактов белков 2,5–5 мкг инкубировали в течение 10 мин при 30 ° C с CK2-специфическим пептидом RRRADDSDDDDD (0.5 мМ) в присутствии смеси фосфорилирования, состоящей из 50 мМ ТРИС-HCl pH 7,5, 100 мМ MgCl 2 , 50 мМ АТФ, [γ- 33 P] АТФ (удельная активность 3000-6000 имп / мин пмоль — 1 ), 100 мМ NaCl, 10 мМ NaF и 1 мМ окадаиновой кислоты. Образцы наносили на фосфоцеллюлозные фильтры, промывали и считали сцинтилляцией, как описано (Ruzzene et al. , 2002). Пустое значение, полученное в контрольных экспериментах, проведенных в тех же условиях, но в присутствии 4 мкМ TBB, предотвращая, таким образом, фосфорилирование СК2, вычитали из каждого значения.Концентрацию белка определяли методом Брэдфорда (1976) и нормализовали вестерн-блоттингом с антителами против β-субъединицы АТФазы, загружая 2,5 мкг белка. Каждый эксперимент повторяли трижды. Для каждого эксперимента использовали сто проростков, и ферментативный анализ повторяли четыре раза.
Результаты
SA индуцирует продукцию NO дозозависимым образом
Чтобы оценить способность СК вызывать выброс NO, продуцирование NO анализировали в проростках Arabidopsis с использованием проницаемого для клеток флуоресцентного зонда DAF-FM DA в сочетании с конфокальной лазерной сканирующей микроскопией.На рис. 1А показано получение в реальном времени изображения продукции NO в проростках Arabidopsis , предварительно загруженных 15 мкМ DAF-FM DA и впоследствии обработанных SA (1 мМ). SA в концентрации 1 мМ не токсичен для проростков Arabidopsis (данные не представлены).
Рис. 1.
SA стимулирует продукцию NO в Arabidopsis . (A) Динамика SA-индуцированного выброса NO, обнаруженного с помощью конфокальной лазерной сканирующей микроскопии. Arabidopsis 5-дневные проростки загружали 15 мкМ DAF-FM DA и обрабатывали водой (вверху) или 1 мМ SA (внизу).(B) Флуоресцентная визуализация проростков, нагруженных DAF-FM, обработанных в течение 2 часов SA с 0,5 мМ cPTIO или без него. (C) Флуоресцентная визуализация проростков, нагруженных DAF-FM, обработанных в течение 2 часов водой (CNT) или 1 мМ гидроксибензоатом (4-HB).
Рис. 1.
SA стимулирует продукцию NO в Arabidopsis . (A) Динамика SA-индуцированного выброса NO, обнаруженного с помощью конфокальной лазерной сканирующей микроскопии. Arabidopsis 5-дневные проростки загружали 15 мкМ DAF-FM DA и обрабатывали водой (вверху) или 1 мМ SA (внизу).(B) Флуоресцентная визуализация проростков, нагруженных DAF-FM, обработанных в течение 2 часов SA с 0,5 мМ cPTIO или без него. (C) Флуоресцентная визуализация проростков, нагруженных DAF-FM, обработанных в течение 2 часов водой (CNT) или 1 мМ гидроксибензоатом (4-HB).
Обработка SA привела к сильному увеличению флуоресценции, что свидетельствует о продукции NO. Чтобы убедиться, что сигнал флуоресценции обусловлен только NO, были проведены контрольные эксперименты. Сначала была протестирована эффективность cPTIO, широко используемого поглотителя NO. Как видно на рис.1B, обработка 0,5 мМ cPTIO предотвращала увеличение флуоресценции в корнях проростков Arabidopsis , инкубированных с 0,75 и 1 мМ СК. На рис. 1C показан контрольный эксперимент, проведенный при обработке проростков неактивным аналогом SA (1 мМ гидроксибензоат; Norman и др. , 2004), при этом изменений флуоресценции DAF-FM не наблюдалось.
На рис. 2А представлена кинетика накопления NO в проростках, нагруженных DAF, обработанных возрастающими концентрациями СК (0,5, 0,75 и 1 мМ).Наблюдалась четкая дозовая зависимость накопления NO с максимальным откликом в течение 2 ч.
Рис. 2.
(A) Динамика SA-индуцированной продукции NO у проростков, нагруженных DAF-FM, обработанных различными концентрациями SA. Флуоресценция DAF-FM указывается в произвольных единицах интенсивности пикселей (A.U.). (B) Динамика индуцированного SA продукции NO в культивируемых клетках, оцененная спектрофотометрически после превращения оксигемоглобина в метгемоглобин.Значения представляют собой среднее значение ± стандартное отклонение.
Рис. 2.
(A) Временной ход SA-индуцированной продукции NO у проростков, нагруженных DAF-FM, обработанных различными концентрациями SA. Флуоресценция DAF-FM указывается в произвольных единицах интенсивности пикселей (A.U.). (B) Динамика индуцированного SA продукции NO в культивируемых клетках, оцененная спектрофотометрически после превращения оксигемоглобина в метгемоглобин. Значения представляют собой среднее значение ± стандартное отклонение.
Для обнаружения NO настоятельно рекомендуется использовать более одного метода (Zeidler et al., 2004). По этой причине NO также определяли спектрофотометрически путем измерения превращения HbO 2 в metHb в культивируемых клетках Arabidopsis . Этот метод является количественным и дает возможность определить точное количество NO, продуцируемого по-разному обработанными образцами. На фиг. 2В показана кинетика накопления NO в культивируемых клетках, обработанных повышенными концентрациями СК. Последние данные подтверждают дозовую зависимость продукции NO, индуцированной СК, и хорошо коррелируют с данными, полученными в корнях с помощью флуорометрического анализа.
Источники синтеза NO, индуцированного СК
Чтобы идентифицировать метаболические пути, участвующие в синтезе NO, был принят генетический подход. Сначала оценивали вклад активности нитратредуктазы (NR). В Arabidopsis NR кодируется двумя генами ( NIA1 и NIA2 ), а двойной мутант nia1, nia2 показывает <1% активности NR дикого типа (Wilkinson and Crawford, 1993).
Низкие уровни флуоресценции наблюдались у необработанных мутантов дикого типа и nia1, nia2 (рис.3). Мутант nia1, nia2 не выделял NO при инкубации в присутствии 1 мМ нитрита, как ожидалось, в то время как корни дикого типа демонстрировали> 3-кратное повышение уровней флуоресценции в тех же экспериментальных условиях. Проростки, обработанные 1 мМ СК в течение 2 ч, показали аналогичную индукцию продукции NO как в корнях дикого типа, так и в мутантных корнях nia1, nia2 (рис. 2). Эти результаты указывают на независимый от NR путь для SA-индуцированного синтеза NO.
Рис.3.
SA-индуцированная продукция NO в проростках дикого типа и nia1, nia2 мутантных проростков. (A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ нитритом, 1 мМ СК и 1 мМ L-NMMA + 1 мМ СК. (B) Интенсивность пикселей DAF-FM флуоресценции корней. Столбцы соответствуют средним значениям ± стандартное отклонение.
Рис. 3.
SA-индуцированная продукция NO в проростках дикого типа и nia1, nia2 мутантных проростков. (A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ нитритом, 1 мМ СК и 1 мМ L-NMMA + 1 мМ СК.(B) Интенсивность пикселей DAF-FM флуоресценции корней. Столбцы соответствуют средним значениям ± стандартное отклонение.
Чтобы определить, происходит ли индуцированный SA синтез NO посредством NOS-подобной активности, эксперименты были повторены с SA после предварительной обработки проростков L-NMMA, ингибитором NOS на основе аргинина, широко используемым в системах растений (Zeidler et al. , 2004). Как показано на фиг. 3, предварительная обработка 1 мМ L-NMMA снижала продукцию NO как в корнях дикого типа, так и в мутантных корнях, инкубированных с 1 мМ SA. Результаты показали снижение сигнала DAF-FM в обоих образцах, которое, однако, не было полностью устранено; фактически, аналогичный сигнал флуоресценции оставался в корнях дикого типа и мутантных корнях.Это говорит о том, что, помимо участия NOS-активности, второстепенный NOS-независимый путь вносит вклад в общую продукцию NO в корнях.
Участвует ли AtNOS1 в SA-индуцированном производстве NO?
Недавно был охарактеризован мутант Arabidopsis ( Atnos1 ), у которого нарушена продукция NO (Guo et al. , 2003). Чтобы оценить, будет ли мутация Atnos1 участвовать в SA-индуцированной продукции NO, были проведены эксперименты на проростках дикого типа и мутантных проростках Atnos1 .
На фиг. 4 можно видеть, что обработка SA (1 мМ) в течение 2 ч увеличивала продукцию NO как в корнях дикого типа, так и в мутантных корнях Atnos1 , хотя и не в такой степени. В мутантных корнях, обработанных SA, сигнал флуоресценции DAF-FM составлял ~ 60% от сигнала, обнаруженного в корнях дикого типа. Затем эксперименты повторяли в присутствии ингибитора NOS L-NMMA (1 мМ). Результаты показали снижение сигнала DAF-FM в обоих образцах, которое, однако, не было полностью устранено, в то время как аналогичный сигнал флуоресценции оставался в корнях дикого типа и мутантных корнях.Этот результат предполагает, что AtNOS1, несмотря на то, что сам по себе не обладает определенной активностью NOS (Guo, 2006; Zemojtel et al. , 2006), тем не менее, участвует в активности, подобной NOS.
Рис. 4.
SA-индуцированная продукция NO в проростках дикого типа и Atnos1 мутантных проростков. (A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ SA, 1 мМ L-NMMA или обоими. (B) Интенсивность пикселей DAF-FM флуоресценции корней.Столбцы соответствуют средним значениям ± стандартное отклонение.
Рис. 4.
SA-индуцированная продукция NO в проростках дикого типа и Atnos1 мутантных проростков. (A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ SA, 1 мМ L-NMMA или обоими. (B) Интенсивность пикселей DAF-FM флуоресценции корней. Столбцы соответствуют средним значениям ± стандартное отклонение.
Компоненты пути передачи сигнала, индуцированного SA
Для исследования сигнальных компонентов, участвующих в SA-повышенном синтезе NO, была изучена роль фосфорилирования кальция и белков.
Поскольку роль кальция была обнаружена в других NO-индуцированных элиситорных путях (Lamotte et al. , 2004), эксперименты были выполнены на проростках Arabidopsis , инкубированных в среде, не содержащей кальция. Как показано на рис. 5, отсутствие ионов кальция в среде полностью предотвращает SA-индуцированный синтез NO, демонстрируя, что кальций строго необходим в этом сигнальном пути. Эти данные подтверждаются экспериментами, проведенными в присутствии хелатора кальция EGTA (2.5 мМ; данные не показаны).
Рис. 5.
Синтез NO зависит от фосфорилирования кальция и белков. (A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ СК, или в комбинации с 2 мкМ K252a или 30 мкМ TBB, или в среде, не содержащей кальция. (B) Интенсивность пикселей DAF-FM флуоресценции корней. Столбцы соответствуют средним значениям ± стандартное отклонение.
Рис. 5.
Синтез NO зависит от фосфорилирования кальция и белков.(A) Продукция NO (показана как флуоресценция DAF-FM) в 5-дневных проростках после обработки в течение 2 часов 1 мМ СК, или в комбинации с 2 мкМ K252a или 30 мкМ TBB, или в среде, не содержащей кальция. (B) Интенсивность пикселей DAF-FM флуоресценции корней. Столбцы соответствуют средним значениям ± стандартное отклонение.
Протеинкиназы были указаны как критические компоненты передачи сигналов SA. Чтобы понять, может ли киназная активность участвовать в SA-индуцированной продукции NO, уровень NO был определен в проростках Arabidopsis , обработанных различными ингибиторами протеинкиназ.Как показано на фиг. 5, общий ингибитор серин / треонинкиназы K252a не предотвращал продукцию NO при обработке SA. Недавно сообщалось, что CK2 участвует в SA-индуцированном фосфорилировании специфических белков, участвующих в передаче сигналов SA (Hidalgo et al. , 2001). Таким образом, был протестирован эффект TBB, специфического ингибитора CK2 (Ruzzene et al. , 2002), на индуцированную SA продукцию NO. Как показано на фиг. 5, значительное ингибирование наблюдалось у проростков, предварительно подвергнутых воздействию 30 мкМ TBB.Были проведены контрольные эксперименты с ДМСО и СК, показавшие, что ДМСО не оказывает никакого влияния на ответ СК (данные не показаны).
Чтобы лучше понять, как эта специфическая протеинкиназа участвует в передаче сигналов SA, ведущих к продукции NO, был проведен анализ активности CK2. Как показано на фиг. 6, активность СК2 уже присутствует в необработанных проростках и на нее не влияет обработка СК. Активность CK2 сильно ингибируется 30 мкМ TBB даже в присутствии SA, в то время как на нее не влияет предварительная обработка K252a.Более того, неэффективность K252a также оценивалась с помощью анализа in vitro , выполненного с использованием рекомбинантной формы CK2. Используя этот анализ, активность CK2 не ингибировалась K252a при концентрациях до 5 мкМ (данные не показаны).
Рис. 6.
Эндогенную активность СК2 измеряли по отношению к конкретному пептиду (см. Материалы и методы), используя 2,5–5 мкг белковых экстрактов из проростков Arabidopsis , обработанных, как указано. Столбцы соответствуют средним значениям ± стандартное отклонение.
Рис. 6.
Эндогенную активность СК2 измеряли по отношению к конкретному пептиду (см. Материалы и методы), используя 2,5–5 мкг белковых экстрактов из проростков Arabidopsis , обработанных, как указано. Столбцы соответствуют средним значениям ± стандартное отклонение.
Обсуждение
В этом отчете показано, что СК способна запускать синтез NO у проростков Arabidopsis . Изучая кинетику накопления NO, наблюдали четкую реакцию, которая зависела от концентрации SA.Чтобы подтвердить этот результат, были приняты два различных метода для специфического обнаружения NO: флуорометрический анализ, который оценивает продукцию NO на клеточном уровне в корнях Arabidopsis , и спектрофотометрический анализ, который определяет количество NO, выделяемого культивируемыми клетками. Между этими двумя методами и двумя разными биологическими системами (клетки и проростки) наблюдалась хорошая корреляция. Этот момент усиливает достоверность результатов, предполагая более широкое распространение индуцированной СК продукции NO, не ограничивающейся конкретными тканями или органами.
Для определения метаболических путей, участвующих в этом процессе, использовались как генетические, так и фармакологические подходы. Вероятно, что у растений есть несколько ферментных систем для производства NO, хотя наиболее интенсивно изучаемые основаны на NR и предполагаемой NOS. В предыдущем отчете Klepper (1991) показал, что СК индуцирует выделение NO из листьев сои в присутствии гербицидов, ингибирующих фотосинтез, предполагая, что выработка NO происходит из-за стимулирующего действия активности NR в сочетании с неэффективным фотосинтетическим процессом.По этой причине была сделана первая попытка определить роль активности NR в индукции NO с помощью генетического подхода с использованием NR-дефицитного мутанта Arabidopsis ( nia1, nia2 ). Когда проростки дикого типа и мутантные проростки инкубировали в присутствии SA, синтез NO явно индуцировался в обеих линиях, показывая, что активность NR не участвовала в этом процессе.
Для оценки участия ферментативной активности NOS-типа в SA-индуцированной продукции NO, проростки дикого типа и nia1, nia2 инкубировали с ингибитором NOS L-NMMA перед добавлением SA.Этот эксперимент определяет важную роль активности NOS, так как продукция NO была сильно снижена этой предварительной обработкой. SA-индуцированная продукция NO была также обнаружена у мутанта Atnos1 , но не в такой степени, как у дикого типа, поскольку сигнал флуоресценции у мутанта составлял ~ 60% от сигнала, обнаруженного у дикого типа. Эти данные позволяют предположить, что AtNOS1 участвует в этом процессе, хотя и не исключительным образом. При комбинированной обработке (SA + L-NMMA) Atnos1 , а также проростков дикого типа, SA-индуцированная продукция NO дополнительно снижалась.Эти результаты предполагают, что вызванная SA продукция NO включает AtNOS1 посредством активности, подобной NOS. Даже если задействованный молекулярный механизм все еще неизвестен, данные согласуются с данными других авторов, показывающими сильное нарушение продукции NO у мутанта Atnos1 в ответ на различные биологические стимулы (например, абсцизовую кислоту, липополисахарид и т. Д.) (Guo et al., 2003; Zeidler et al., 2004; Bright et al., 2006).
При комбинированной обработке (SA + L-NMMA) аналогичный сигнал флуоресценции, более высокий, чем у контролей, наблюдался у дикого типа и у мутантов nia1, nia2 и Atnos1 .Этот остаточный сигнал флуоресценции можно отнести к NO, синтезируемому другим путем, например, недавно обнаруженным NI-NOR, связанным с плазматической мембраной. Было показано, что эта активность индуцирует синтез NO из нитрита, и, как известно, она специфически экспрессируется в корнях растений (Stöhr et al. , 2001).
В предыдущем отчете (Song and Goodman, 2001) было показано, что индукция SAR значительно уменьшалась, когда растения табака вводили одновременно с ингибиторами SA и NOS.Настоящие данные ясно демонстрируют, что NO является сигналом нижестоящего в SA-индуцированном ответе у растений и что это производство NO происходит в основном по NOS-зависимому пути.
Фармакологический подход был принят для исследования сигнальных компонентов, участвующих в синтезе NO при лечении СК. Используя ингибиторы протеинкиназы, были получены доказательства того, что события фосфорилирования участвуют в индуцированном SA сигнальном каскаде, ведущем к продукции NO. В частности, результаты показывают, что продукция NO полностью зависит от активности конкретного CK2, поскольку только специфический ингибитор CK2 (TBB) был эффективен как на продукцию NO, так и на активность CK2.Напротив, общий ингибитор серин / треонинкиназы (K252a), совершенно неэффективный в отношении продукции NO, также не мог влиять на активность CK2. Эти данные согласуются с предыдущими результатами, показывающими участие CK2 в SA-индуцированной активности (Kang and Klessig, 2005). В этих экспериментах активность CK2 не увеличивалась обработкой SA, в отличие от того, что наблюдалось в листьях табака Kang and Klessig (2005). Обнаружение того, что активность CK2 уже высока в проростках, независимо от обработки SA, полностью согласуется с текущим взглядом на эту киназу как на конститутивно активный фермент, на который не влияют внешние раздражители (Pinna, 2002).Более того, результаты согласуются с недавним отчетом Salinas et al. (2006), где не было обнаружено изменений в экспрессии генов CK2 после обработки СК. Несмотря на его немодифицированную активность, участие CK2 в ответе на СК четко указывается в настоящих данных, предполагая, что некоторые изменения, вызванные лечением СК, абсолютно требуют, чтобы события CK2-зависимого фосфорилирования были эффективными: всякий раз, когда активность СК2 низкая, СК недостаточно. сам по себе, чтобы вызвать производство NO.Потребуются дальнейшие исследования, чтобы выяснить, на каком уровне и на каких субстратах CK2 оказывает свое фундаментальное влияние.
Следует также учитывать, что SA-индуцированная продукция NO, вероятно, контролируется несколькими механизмами, как предполагают эксперименты по передаче сигналов кальция. Появляется все больше доказательств существования перекрестных помех между системами передачи сигналов NO и кальция у растений (Lamotte et al. , 2004). Чтобы изучить участие кальция в SA-индуцированном синтезе NO, были проведены эксперименты в среде, не содержащей кальция, что показало, что этот компонент имеет решающее значение для сигнального пути SA.Роль, которую играет кальций в синтезе NO, индуцированном СК, может быть ролью сигнальной молекулы и / или ферментативного кофактора.
В заключение, настоящие результаты ясно демонстрируют, что по крайней мере часть SA-индуцированного синтеза NO происходит через NOS-зависимый путь; Передача сигналов кальция и фосфорилирование белков через CK2 являются ранними и важными компонентами SA-индуцированного пути, опосредующего синтез NO. Данные, которые демонстрируют существование SA-зависимой продукции NO в растениях, представляют интерес, поскольку они предполагают наличие регуляторной петли, способной усиливать сигнал с участием NO и SA.Более того, благодаря лучшему определению взаимосвязи между SA и NO эти результаты способствуют более детальному пониманию метаболических путей, в которых участвуют эти молекулы.
Сокращения
CK2
cNR
цитоплазматическая нитратредуктаза
cPTIO
2- (4-карбоксифенил) 3-оксид 3-оксидазолин 1-тетраметилим
DAF-FM DA
диаминофлуоресцеин-FM диацетат
ДМСО
HbO 2
K252a
K252a
- 9000 9000 9000 9000 9000 9000 9000 9000 9000 NM000 9000 9000
NO
NOS
NR
ROS
SA
SAR
Системная устойчивость 9000,6 9000 3 тетрабромбензотриазол
Сокращения
Мы хотели бы поблагодарить Найджела Кроуфорда и Фэн-Цин Го (Калифорнийский университет, Сан-Диего, США) за предоставление Atno s1 мутантных семян и профессора Марио Терци за полезные обсуждения.Работа поддержана программой PRIN Министерства научных исследований Италии.
Список литературы
.
Салициловая кислота в механизме гибели гиперчувствительных клеток и устойчивости к болезням
,
Молекулярная биология растений
,
2000
, vol.
44
(стр.
429
—
442
).
Быстрый и чувствительный метод количественного определения количества белка в микрограммах, использующий принцип связывания белок-краситель
,
Analytical Biochemistry
,
1976
, vol.
72
(стр.
248
—
254
),,,,.
АБК-индуцированная генерация NO и закрытие устьиц у Arabidopsis зависят от синтеза H 2 O 2
,
The Plant Journal
,
2006
, vol.
45
(стр.
113
—
122
),,,,,,.
Передача сигналов NO в цитокинин-индуцированной программируемой гибели клеток
,
Plant, Cell and Environment
,
2005
, vol.
28
(стр.
1171
—
1178
).
НЕТ новостей — хорошие новости для растений
,
Текущее мнение по биологии растений
,
2005
, vol.
8
(стр.
390
—
396
),,.
Индукция защитного гена в табаке оксидом азота, циклическим GMP и циклической ADP-рибозой
,
Proceedings of the National Academy of Sciences, USA
,
1998
, vol.
95
(стр.
10328
—
10333
),,,,.
Производство оксида азота в клетках листьев табака: обобщенная реакция на стресс?
,
Завод, клетки и окружающая среда
,
2003
, т.
26
(стр.
1851
—
1862
),,,.
Оксид азота и регуляция генов у растений
,
Journal of Experimental Botany
,
2006
, vol.
57
(стр.
507
—
516
).
Ответ Zemojtel et al.: Синтаза оксида азота растений: AtNOS1 — это только начало
,
Тенденции в науке о растениях
,
2006
, vol.
11
(стр.
527
—
528
),.
Arabidopsis синтаза оксида азота1 нацелена на митохондрии и защищает от окислительного повреждения и темнового старения
,
The Plant Cell
,
2005
, vol.
17
(стр.
3436
—
3450
),,.
Идентификация гена синтазы оксида азота растений, участвующего в гормональной передаче сигналов
,
Science
,
2003
, vol.
302
(стр.
100
—
103
),,, и др.
Оксид азота подавляет переход цветков Arabidopsis
,
Science
,
2004
, vol.
305
(стр.
1968
—
1971
),,,,,.
Активность ядерной казеинкиназы 2 участвует в ранних событиях активации транскрипции, вызванной салициловой кислотой в табаке
,
Plant Physiology
,
2001
, vol.
125
(стр.
396
—
405
),.
Салициловая кислота, индуцируемая Arabidopsis CK2-подобная активность фосфорилирует TGA2
,
Plant Molecular Biology
,
2005
, vol.
57
(стр.
541
—
557
).
Выделение NOx листьями сои, обработанными салициловой кислотой и выбранными производными
,
Pesticide Biochemistry and Physiology
,
1991
, vol.
39
(стр.
43
—
48
),,, и др.
Передача сигналов оксида азота и салициловой кислоты в защите растений
,
Proceedings of the National Academy of Sciences, USA
,
2000
, vol.
97
(стр.
8849
—
8855
),.
Салициловая кислота накапливается в корнях и гипокотиле после инокуляции листьев огурца Colletotrichum lagenarium
,
Journal of Plant Physiology
,
2006
, vol.
163
(стр.
1111
—
1117
),,,,.
Оксид азота в растениях: биосинтез и клеточные сигнальные свойства удивительной молекулы
,
Planta
,
2005
, vol.
221
(стр.
1
—
4
),,,,,,,.
Анализ сигнальных функций оксида азота в клетках табака, зараженных элиситором cryptogein
,
Plant Physiology
,
2004
, vol.
135
(стр.
516
—
529
),.
Обновленная среда для быстрого роста и биологических анализов с культурами тканей табака
,
Physiologia Plantarum
,
1962
, vol.
15
(стр.
473
—
497
),.
Определение оксида азота с использованием метода гемоглобина
,
Методы энзимологии
,
1994
, vol.
233
(стр.
240
—
250
),,.
Передача сигналов оксида азота в растениях
,
New Phytologist
,
2003
, vol.
159
(стр.
11
—
35
),,,,.
Салициловая кислота является разобщителем и ингибитором митохондриального транспорта электронов
,
Plant Physiology
,
2004
, vol.
134
(стр.
1
—
10
).
Протеинкиназа CK2: вызов канонам
,
Journal of Cell Science
,
2002
, vol.
115
(стр.
3873
—
3878
),.
Озон-индуцированная гибель клеток в Arabidopsis происходит посредством двух различных механизмов: роль салициловой кислоты
,
The Plant Journal
,
1999
, vol.
17
(стр.
603
—
614
),.
Регуляция дыхания у высших растений салициловой кислотой: альтернативная экспрессия оксидазы
,
The Plant Cell
,
1992
, vol.
4
(стр.
1131
—
1139
),,.
Ингибитор протеинкиназы CK2 4,5,6,7-тетрабромбензотриазол (TBB) индуцирует апоптоз и каспазозависимую деградацию гематопоэтического клеточно-специфического белка 1 (HS1) в клетках Jurkat
,
Biochemical Journal
,
2002
, vol. .
364
(стр.
41
—
47
),,,,,.
Обширный обзор α- и β-субъединиц CK2 в Arabidopsis : множественные изоформы обнаруживают дифференциальную субклеточную локализацию
,
Plant and Cell Physiology
,
2006
, vol.
47
(стр.
1295
—
1308
),,,.
Ацетилсалициловая кислота (аспирин) и салициловая кислота вызывают множественную стрессоустойчивость у растений фасоли и томатов
,
Регулирование роста растений
,
2000
, vol.
30
(стр.
157
—
161
),.
Активность оксида азота зависит от функции салициловой кислоты в сигнальном пути системной приобретенной устойчивости табака, но частично требуется.
14
(стр.
1458
—
1462
),,,,.
Влияние эндогенной салициловой кислоты на клубеньки в модельных бобовых Lotus japonicus и Medicago truncatula
,
Физиология растений
,
2006
, vol.
141
(стр.
1473
—
1481
).
Взаимосвязь поступления нитратов со скоростью роста, связанной с плазматической мембраной и цитозольной нитратредуктазы и содержанием нитратов в тканях растений табака
,
Растения, клетки и окружающая среда
,
1999
, vol.
22
(стр.
169
—
177
),,,,.
Связанный с плазматической мембраной фермент корней табака катализирует образование оксида азота из нитрита
,
Planta
,
2001
, vol.
212
(стр.
835
—
841
),,,,,,,,,.
Приобретенная устойчивость у Arabidopsis
,
The Plant Cell
,
1992
, vol.
4
(стр.
645
—
656
),.
Идентификация и характеристика хлорат-устойчивого мутанта Arabidopsis thaliana с мутациями в обоих структурных генах нитратредуктазы NIA1 и NIA2
,
Molecular and General Genetics
,
1993
, vol.
239
(стр.
289
—
297
).
Нитрит-зависимый путь образования оксида азота: значение для участия активных форм азота в фотоингибировании in vivo
,
Philosophical Transactions of the Royal Society B: Biological Sciences
,
2000
, vol.
355
(стр.
1477
—
1488
),.
Одновременное производство оксида азота и пероксинитрита растительной нитратредуктазой: in vitro свидетельство NR-зависимого образования активных форм азота
,
FEBS Letters
,
2000
, vol.
468
(стр.
89
—
92
),,.
Восприятие и передача сигналов в защитных реакциях растений
,
Gene Development
,
1997
, vol.
11
(стр.
1621
—
1639
),,,,,,,.
Врожденный иммунитет у Arabidopsis thaliana : липополисахариды активируют синтазу оксида азота (NOS) и индуцируют защитные гены
,
Proceedings of the National Academy of Sciences, USA
,
2004
, vol.
101
(стр.
15811
—
15816
),,, и др.
Завод синтазы оксида азота: бесконечная история?
,
Тенденции в растениеводстве
,
2006
, т.
11
(стр.
524
—
525
),,,,,.
Оксид азота влияет на функциональность митохондрий растений in vivo
,
FEBS Letters
,
2002
, vol.
515
(стр.
75
—
78
)
© Автор [2007].Опубликовано Oxford University Press [от имени Общества экспериментальной биологии]. Все права защищены. Для получения разрешений обращайтесь по электронной почте: [email protected]
.
трансжирных кислот вызывают воспаление сосудов и снижают продукцию оксида азота в эндотелиальных клетках
Abstract
Потребление трансжирных кислот (ТЖК), которые потребляются при употреблении в пищу продуктов, приготовленных из частично гидрогенизированных растительных масел, связано с более высоким риском сердечно-сосудистых заболеваний.Эта связь может быть объяснена многими факторами, включая отрицательное влияние TFA на функцию эндотелия и снижение биодоступности оксида азота (NO). В этом исследовании мы исследовали влияние трех различных TFA (2 общих изомера C18, обнаруженных в частично гидрогенизированном растительном масле, и изомер C18, обнаруженный в молочных продуктах и мясе жвачных животных) на активацию эндотелия NF-κB и оксид азота (NO) производство. Эндотелиальные клетки человека обрабатывали увеличивающимися концентрациями элаидика ( транс, -C18: 1 (9 транс)), линоэлаидика ( транс, -C18: 2 (9 транс, 12 транс)) и трансвацина ( транс, -C18). : 1 (11 транс)) в течение 3 часов.И элаидовая, и линоэлаидовая кислоты были связаны с увеличением активации NF-κB, измеряемой по уровням IL-6 и фосфорилированию IκBα, а также с нарушением передачи сигналов эндотелиальным инсулином и продукции NO, тогда как трансвакценовая кислота не была связана с этими ответами. Мы также измерили производство супероксида, которое, как предполагалось, необходимо для зависимой от жирных кислот активации NF-κB. И элаидиновая кислота, и линоэлаидовая кислота связаны с повышенным образованием супероксида, тогда как трансвакценовая кислота (которая не вызывает воспалительных реакций) не увеличивает выработку супероксида.Мы наблюдали дифференциальную активацию продукции эндотелиального супероксида, активацию NF-κB и снижение продукции NO различными изомерами C18, предполагая, что расположение и количество двойных транс-связей влияют на активацию эндотелиального NF-κB.
Образец цитирования: Ивата Н.Г., Фам М., Риццо Н.О., Ченг А.М., Мэлони Э., Ким Ф. (2011) Трансжирные кислоты вызывают воспаление сосудов и снижают продукцию оксида азота в эндотелиальных клетках. PLoS ONE 6 (12):
e29600.
https: // doi.org / 10.1371 / journal.pone.0029600
Редактор: Массимо Федеричи, Университет Тор Вергата, Италия
Поступила: 30 августа 2011 г .; Принято: 1 декабря 2011 г .; Опубликовано: 28 декабря 2011 г.
Авторские права: © 2011 Iwata et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Финансирование: Грантовая поддержка: Национальный институт здравоохранения RO1 DK073878, Благотворительный фонд Джона Локка-младшего и докторская степень по профилактической кардиологии Кеннета Х. Купера. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили, что конкурирующих интересов не существует.
Введение
Трансжирные кислоты (TFA) включают мононенасыщенные жирные кислоты или полиненасыщенные жирные кислоты, которые содержат по крайней мере одну транс-двойную связь углерод-углерод.Большинство диетических ТЖК получают в результате частичной гидрогенизации растительного масла или из пищевых продуктов жвачных животных (молочные продукты и мясо). ТЖК широко используются в пищевой промышленности при производстве хлебобулочных изделий, продуктов, жаренных во фритюре, и упакованных закусок. Подсчитано, что на долю ТЖК приходится до 4–12% общего количества жиров, поступающих с пищей, среди населения США [1]. В течение последних 20 лет эпидемиологические исследования определили, что потребление ТЖК является важным изменяемым фактором риска развития сердечно-сосудистых заболеваний [2], [3].В последнее время использование и присутствие ТЖК в рационе стало предметом многочисленных дискуссий в области общественного здравоохранения.
Потребление TFA повышает уровень холестерина ЛПНП и снижает уровень холестерина ЛПВП в большей степени по сравнению с потреблением равного количества энергии из насыщенных, моно- или полиненасыщенных жиров. Однако взаимосвязь между потреблением TFA и частотой сердечно-сосудистых заболеваний была больше, чем предсказывали только изменения липидов сыворотки, что позволяет предположить, что TFA влияют на другие факторы риска сердечно-сосудистых заболеваний.
Известно, что потребление
TFA влияет на множество факторов риска, помимо изменений липидов / липопротеинов, включая усиление системного воспаления [4], усиление тромбообразования и снижение функции эндотелия [5], все из которых в сочетании или по отдельности способствуют увеличению риска сердечно-сосудистых заболеваний. Экспериментальные исследования показывают, что TFA проявляют свои многочисленные эффекты, влияя на метаболические и сигнальные пути в гепатоцитах, моноцитах, адипоцитах и эндотелиальных клетках. Точные молекулярные пути, посредством которых TFA влияют на эти типы клеток, неизвестны.
Эндотелиальная дисфункция может быть описана как нарушение образования и функции оксида азота (NO) как сосудорасширяющего и сосудистого гомеостатического средства. Снижение биодоступности NO значительно увеличивает риск развития атеросклероза и гипертонии. Эндотелиальная синтаза оксида азота (eNOS) синтезирует NO в ответ на многие агонисты, включая напряжение сдвига жидкости, брадикинин и инсулин, что увеличивает выработку NO в эндотелиальных клетках через субстрат рецептора инсулина-1 (IRS-1) и фосфатидилинозитол-3-киназу (PI3). -киназа) зависимый путь, который приводит к фосфорилированию эндотелиальной синтазы оксида азота (eNOS) с помощью Akt кальций-независимым образом [6], [7].Ранее мы показали, что пищевой насыщенный жир, пальмитат, ослабляет передачу сигналов эндотелиального инсулина и продукцию NO, сначала активируя передачу сигналов NF-κB, что приводит к снижению передачи сигналов IRS-1 / pAkt / peNOS. Основываясь на этих результатах, мы спросили, будет ли TFA снижать уровни эндотелиального NO, сначала активируя NF-κB.
Было показано, что в эндотелиальных клетках TFA увеличивает маркеры эндотелиальной дисфункции, включая E-селектин, ICAM, и нарушает опосредованную потоком вазодилатацию (мера продукции NO в сосудах) у людей [5], [8].В этом исследовании мы выбрали три различных TFA, все изомеры C18 — транс, -C18: 1 (9 транс), транс, -C18: 2 (9 транс, 12 транс), транс, -C18: 1 (11 транс). Транс -C18: 1 (транс 9), также известная как элаидовая кислота, представляет собой обычную TFA, образованную частичной гидрогенизацией растительного масла, транс -C18: 2, также известная как линоэлаидовая кислота, обычно обнаруживается во время процесса. нагревания растительных масел (для жарки или запекания пищи в растительном масле), приводящего к образованию двух двойных транс-связей, транс -C18: 1 (транс11), также известного как трансваценовая кислота, представляет собой модель TFA, полученных из жвачных животных, которые являются продуцируется бактериями в желудке жвачных.TFA, полученная из жвачных животных, содержится в молочных продуктах или в мясных тканях, однако потребление TFA, полученного из жвачных животных, обычно невелико из-за низкой концентрации (1%). Все эти TFA имеют 18 атомов углерода, однако различаются расположением двойных транс-связей. Мы спросили, связаны ли эти разные TFA с дифференциальным действием на эндотелиальную передачу сигналов NF-κB и NO.
Методы
Материалы
Антитела против фосфо-IκBα были получены от Cell Signaling (Беверли, Массачусетс), наборов ELISA для человеческого IL-6 от R and D Systems (Миннеаполис, Миннесота) и фосфо-IκBα Case ™ Cellular Activation of Signaling ELISA SuperArray Bioscience Corporation (Frederick , Д.м.н.).Наборы для ELISA Total Akt и pAkt (серин 473) были получены от Biosource (Камарилло, Калифорния). Спиновая ловушка 1-гидрокси-3-метоксикарбонил-2,2,5,5-тетраметилпирролидин (CMH) была приобретена у Alexis Biochemical (Lausen, Switzerland). Натрий DETC был получен от Alexis Biochemical (Лаузен, Швейцария). FeSO 4 7h3O был приобретен у Sigma (Сент-Луис, Миссури). Супероксиддисмутаза (PEG-SOD), дифениленидоний (DPI) и LPS были получены от Sigma-Aldrich. Дигидроэтидий (DHE) был приобретен у (Molecular Probes / Invitrogen, Eugene Oregon).
пальмитиновый (C 16: 0), C18: 1T или 11-транс-октадеценовый (трансвакценовый), C 18: 1T или 9-транс-октадеценовый (элаидовый), C18: 2 (линолевый), C18: 2 линоэлаидный (9- транс-12 (транс-октадекадиеновая) жирные кислоты были получены от Nu-Chek Prep, Inc. (Elysian, MN), а BSA (без FFA) был приобретен у Roche (Индианаполис, Индиана). FFA растворяли в 0,1 М NaOH при 70 ° C, а затем образовывали комплекс с 10% BSA при 55 ° C в течение 10 мин для достижения конечной концентрации жирных кислот 100 мкМ, как описано ранее [9]. Исходные растворы 5 мМ FFA с 10% BSA и 10% BSA контрольные растворы готовили за 1 день до экспериментов.Препараты жирных кислот оценивали на загрязнение LPS с помощью теста на лизат амебоцитов (Biowhittaker).
Культура клеток
Эндотелиальные клетки микрососудов человека (HMEC) были приобретены у (Invitrogen-Cascade Biological) и культивированы в RPMI 1640 с добавлением 10% фетальной бычьей сыворотки (Hyclone Laboratories, Logan, UT) и 12 мкг / мл экстракта бычьего мозга (Clonetics, Walkersville, MD), L-глутамин (2 мМ), пируват натрия (1 мМ) и заменимые аминокислоты в присутствии пенициллина (100 единиц / мл) и поддерживаются при 37 ° C в 5% CO 2 .Все западные боты выполнялись, как описано [10], с использованием равных количеств общего белка для каждого условия и каждого эксперимента. Электрофорез в геле с SDS проводили с использованием градиентного геля 4% на 20%. Тотальную РНК экстрагировали с помощью набора RNeasy Mini Kit (Qiagen), а пары праймеров TNFα человека, ICAM и iNOS были приобретены в Applied Biosystems.
Измерение супероксида
Эндотелиальный супероксидный радикал был измерен с помощью спектроскопии электронного парамагнитного резонанса (ЭПР) с использованием спиновой ловушки (CMH) [11], [12], [13].HMEC обрабатывали однократной промывкой ледяным PBS и удаляли ломом. После центрифугирования клетки ресуспендировали в буфере Krebs-HEPES и использовали 0,1 мМ диэтилентриаминпентауксусную кислоту (DTPA) для ингибирования катализируемого железом окисления ловушки CMH. Спектроскопию электронного парамагнитного резонанса (ЭПР) проводили на настольном спектрометре Х-диапазона Miniscope (Magnettech, Германия). Записи производились при комнатной температуре с использованием небольшой капиллярной трубки. Настройки прибора: биополе 3350, развертка 60 G, частота микроволн 9.78 ГГц, мощность микроволн 20 мВт, кинетическое время 10 мин.
Измерение оксида азота
Оксид азота измеряли с помощью спиновой ловушки Fe (DETC) 2 , о которой впервые сообщили и подтвердили Клещев и др. [14]. Получение коллоида Fe (DETC) 2 : Натрий DETC (3,6 мг) и FeSO 4 7h30 (2,25 мг) растворяли в атмосфере аргона в 10 мл ледяного буфера Кребса-Хепеса [15] (состоящего из, в мМ: NaCl 99, KCl 4,7, MgSO 4 1,2, KH 2 PO 4 1.0, CaCl 2 1,9, NaHCO 3 25, глюкоза 11,1 и Na-Hepes 20, pH 7,4). Их быстро перемешивали с получением раствора Fe (DETC) 2 бледно-желто-коричневого цвета, который использовали немедленно. После удаления среды для культивирования клеток эндотелиальные клетки один раз промывали PBS и в планшеты для культивирования клеток добавляли 100 мкл буфера Krebs-hepes. Затем добавляли коллоид Fe (DETC) 2 до конечной концентрации 286 мкМ и инкубировали при 37 ° C в течение 90 минут. Спектроскопию электронного парамагнитного резонанса (ЭПР) проводили на настольном спектрометре Х-диапазона Miniscope (Magnettech, Германия).Запись производилась при 77 К с использованием колбы Дьюара. Настройки прибора составляли 10 мВт микроволновой мощности, 1 мТл амплитудной модуляции, 100 кГц частоты модуляции, 20 с времени развертки и 10 сканирований.
Статистика
Во всех экспериментах измерения денситометрии / ELISA были нормализованы для контролей, инкубированных с носителем, и было рассчитано процентное изменение относительно контрольных условий. Анализ результатов проводился с использованием статистического пакета STATA8. Данные выражены как среднее ± стандартная ошибка среднего, а значения p <0.05 считались статистически значимыми. Двусторонний тест t использовался для сравнения средних значений исследований с участием двух экспериментальных групп. Данные были проанализированы с помощью двухфакторного дисперсионного анализа с использованием сравнительного теста Бонферони-post-hoc, когда это было необходимо.
Результаты
Трансжирные кислоты индуцируют ответы NF-κB в эндотелиальных клетках человека
Сначала мы спросили, связаны ли TFA, содержащиеся в западной диете, с повышенной активацией эндотелиального NF-κB.Мы протестировали три различных TFA: транс, -C18: 1 (11 транс), транс, -C18: 2 (9 транс, 12 транс) и транс, -C18: 1T (9 транс), все различные изомеры C18. Мы использовали пальмитат в качестве контроля, поскольку ранее показали, что пальмитиновая кислота увеличивает активацию эндотелиального NF-κB дозозависимым образом [16]. C18: 2 в цис-конфигурации (линолевая) также использовался в качестве отрицательного контроля, поскольку этот полиненасыщенный жир не усиливает эндотелиальную передачу сигналов NF-κB. Мы выбрали 3-часовой инкубационный период с жирами, входящими в состав BSA, поскольку предыдущие исследования продемонстрировали апоптотический эффект в эндотелиальных клетках в течение периодов времени более 6-8 часов.Чтобы оценить активацию NF-κB в эндотелиальных клетках, мы измерили фосфорилирование IκBα и продукцию IL-6 (цитокин, зависимый от NF-κB). И транс, -C18: 2 (9 транс, 12 транс), и транс, -C18: 1 (9 транс) увеличивали уровни фосфо-IκBα и IL-6 дозозависимым образом, тогда как C18: 2 (линолевая) и транс -C18: 1 (11 транс) (трансваценовая кислота) не увеличивал уровни фосфо-IκBα или IL-6 (рис. 1A, B). Как и ожидалось, пальмитат увеличивал передачу сигналов NF-κB дозозависимым образом (Рисунок 1).Как элаидик ( транс, -C18: 1 (9 транс)), так и линоэлаидик (транс-C18: 2 (9 транс, 12 транс)) в концентрации 100 мкМ увеличивали экспрессию NF-κB-зависимого гена (TNFα, ICAM, и iNOS), что не наблюдалось при использовании линолевой или трансвакценовой кислоты (рис. 1C). Таким образом, обычные «промышленные TFA» связаны с усилением эндотелиального воспаления, тогда как TFA (трансваценовая кислота), полученная из жвачных животных, нет. Кроме того, расположение транс-двойной связи оказывает различное воспалительное действие на эндотелиальные клетки.
Рисунок 1. Влияние TFA на эндотелиальную передачу сигналов NF-κB.
Эндотелиальные клетки человека обрабатывали возрастающими концентрациями пальмитата, линолевой кислоты, трансвакценовой ( транс, -C18: 1 (11 транс)), линоэлаидовой ( транс, -C18: 2 (9 транс, 12 транс)) и элаидик ( транс -C18: 1 (9 транс)) в течение 3 часов. Все жирные кислоты изначально образовывали комплекс с BSA, и в контрольных условиях клетки обрабатывали одним BSA в течение 3 часов. А . Уровни фосфо-IκBα измеряли с помощью анализа ELISA.Было рассчитано кратное увеличение по сравнению с контролем (только BSA). (n = 3, * p <0,05). Б . Уровни IL-6, измеренные с помощью ELISA. (n = 3, * p <0,05). С . Уровни экспрессии TNFα, ICAM и iNOS в ответ на 100 мкМ жира. (n = 3, * p <0,05).
https://doi.org/10.1371/journal.pone.0029600.g001
Влияние трансжиров на передачу сигналов эндотелиального инсулина
Мы ранее показали, что в эндотелиальных клетках опосредованная пальмитатом активация передачи сигналов NF-κB связана со сниженной опосредованной инсулином передачей сигналов Akt и eNOS в эндотелиальных клетках [16].Затем мы исследовали, может ли TFA также снижать передачу сигналов эндотелиального инсулина. Эндотелиальные клетки обрабатывали 100 мкМ TFA в течение 3 часов, и инсулино-опосредованную передачу сигналов оценивали после обработки носителем или 100 нМ инсулина в течение 15 минут. Как ожидалось и согласуется с опубликованными результатами, предварительная обработка 100 мкМ пальмитата приводила к снижению опосредованного инсулином фосфорилирования Akt и eNOS при отсутствии каких-либо изменений общих уровней eNOS или Akt. Хотя стимуляция инсулином увеличивает фосфорилирование серина 473 Akt и серина 1177 eNOS, предварительная обработка транс -C18: 2 (9 транс 12 транс) и транс -C18: 1 (транс 9) связана с нарушением передачи сигналов эндотелиального инсулина, однако мы не наблюдали ингибирующего эффекта с транс, -C18: 1 (11 транс) (трансвацениновая кислота) или с линолевой кислотой (рис. 2A и 2B).TFA, которые связаны с повышенной активацией NF-κB, также связаны со снижением передачи сигналов эндотелиального инсулина.
Рисунок 2. Влияние TFA на передачу сигналов эндотелиального инсулина.
Эндотелиальные клетки человека обрабатывали либо 100 мкМ пальмитата, линолевой кислоты, трансвакценовой ( транс, -C18: 1 (11 транс)), линоэлаидной ( транс, -C18: 2 (9 транс, 12 транс)), и элаидик ( транс, -C18: 1 (9 транс)) в течение 3 часов, а затем стимулировали инсулином 100 нМ или носителем в течение 15 минут. А . Готовили клеточные лизаты и анализировали инсулино-опосредованное фосфорилирование серина 473 Akt и общего Akt с помощью ELISA. Было рассчитано увеличение кратности по сравнению с состоянием автомобиля. (n = 3, * p <0,05) B . Лизаты клеток анализировали на инсулино-опосредованное фосфорилирование eNOS серина 1177 и общего eNOS с помощью вестерн-блоттинга. Показаны репрезентативные вестерн-блоты фосфо-eNOS. Было рассчитано увеличение кратности по сравнению с состоянием транспортного средства (n = 3, * p <0,05). С . Инсулино-опосредованное производство оксида азота измеряли по СОЭ с использованием спиновой ловушки Fe (DETC) 2 (n = 3, * p <0.05).
https://doi.org/10.1371/journal.pone.0029600.g002
Влияние TFA на продукцию NO
Затем мы определили эффект TFA на продукцию NO эндотелием, измеренный с помощью ESR с использованием спиновой ловушки Fe (DETC) 2 , признанного и чувствительного метода обнаружения NO [17], [18]. Как и ожидалось, предварительная обработка пальмитатом связана со снижением инсулино-опосредованной продукции NO (фиг. 2C), тогда как предварительная обработка линолевой кислотой (C18: 2) или трансвакценовой кислотой не снижает опосредованную инсулином продукцию NO.TFA, связанная с повышенной активацией эндотелиального NF-κB ( транс -C18: 2 и транс -C18: 1), также связана со снижением опосредованной инсулином продукции NO, что является ожидаемым результатом, поскольку мы ранее связывали активацию NF-κB с сокращение производства NO.
Влияние TFA на образование супероксида
В предыдущих исследованиях пальмитат увеличивает активацию NF-κB посредством механизма, зависящего от продукции супероксида, производного НАДФН-оксидазы [19]. Затем мы спросили, будет ли TFA также увеличивать производство активных форм кислорода (ROS).Эндотелиальные клетки обрабатывали 100 мкМ TFA, и продукцию ROS измеряли с помощью ESR и спиновой ловушки CMH. Как и ожидалось, 100 мкМ пальмитата увеличивали продукцию ROS в 2 раза, тогда как линолевая кислота и трансвакценовая кислота не увеличивали продукцию ROS. Транс -C18: 1 (9 транс) и транс -C18: 2 (9 транс, 12 транс) были связаны с 2-кратным увеличением продукции ROS, как измерено с помощью ESR. TFA, которые связаны с увеличением эндотелиального NF-κB, также связаны с увеличением продукции ROS.Предварительная обработка супероксиддисмутазой (SOD) или инкубация с дифенилен-йоднием (DPI) ослабляет пальмитат-зависимую активацию эндотелиального воспаления [19] и, как и ожидалось, аналогичная предварительная обработка ослабляет активацию эндотелиального NF-κB (на уровне продукции IL-6) в присутствие транс -C18: 1 (9 транс) и транс -C18: 2 (9 транс 12 транс), предполагая, что эти TFA также активируют NF-κB через механизм, зависящий от продукции ROS (Рисунок 3B).
Рисунок 3.Влияние TFA на продукцию супероксида эндотелия.
Эндотелиальные клетки человека обрабатывали либо 100 мкМ пальмитата, линолевой кислоты, трансвакценовой ( транс, -C18: 1 (11 транс)), линоэлаидовой ( транс, -C18: 2 (9 транс, 12 транс)), и элаидик ( транс, -C18: 1 (9 транс)) в течение 3 часов. А . Уровни супероксида измеряли с помощью ESR и спиновой ловушки CMH. Было рассчитано увеличение кратности по сравнению с контрольным условием (только BSA). (n = 3, * p <0,05 по сравнению с контролем BSA). Б . Клетки предварительно обрабатывали одним из двух ингибиторов супероксида (SOD, 100 единиц / мл или DPI 25 мкМ) перед стимуляцией элаидовой или линоэлаидовой кислотой. Уровни IL-6, измеренные с помощью ELISA.
https://doi.org/10.1371/journal.pone.0029600.g003
Обсуждение
Многочисленные эпидемиологические исследования коррелировали повышенное потребление ТЖК с пищей с повышением смертности и заболеваемости сердечно-сосудистыми заболеваниями. В этом исследовании мы исследовали три TFA на предмет их способности активировать эндотелиальный NF-κB и впоследствии снижать продукцию NO.Мы обнаружили, что два из TFA, транс, -C18: 2 (9 транс, 12 транс) (линоэлаидик) и транс, -C18: 1 (9 транс) (элаидик), связаны с повышенной активацией NF-κB и снижают передача сигналов эндотелиального инсулина и продукция NO, тогда как транс, -C18: 1 (11 транс) (трансваценик) не связан ни с одним из этих ответов. Кроме того, как линолеэлаидовая, так и элаидовая кислоты увеличивают продукцию ROS эндотелием, что, как предполагается, необходимо для активации эндотелиального NF-κB.Эти результаты предполагают, что разные изомеры C18 способны оказывать различное действие на функцию эндотелия.
Воздействие на эндотелиальные клетки пальмитата, глюкозы, TNF-α, всех медиаторов инсулинорезистентности, приводит к активации NF-κB и повышенной экспрессии молекул адгезии [20], [21], раннего маркера атеросклероза. Кроме того, мы показали, что эти медиаторы инсулинорезистентности также связаны со снижением продукции NO эндотелием [6], [22]. Повышение системного воспаления путем инъекции S.Вакцина typhi нарушает функцию эндотелия у людей-добровольцев [23], что позволяет предположить, что системное воспаление влияет на биодоступность оксида азота. Следовательно, механизм, лежащий в основе эндотелиальной дисфункции, может включать активацию NF-κB, который, ингибируя передачу сигнала IRS-1 / PI3-киназы, ослабляет продукцию NO. Ослабление эндотелиальной передачи сигналов NF-κB (с использованием мутанта IκBα) в присутствии пальмитата восстанавливает эндотелиальное содержание NO [24], что дополнительно поддерживает механистическую связь между NF-κB и сниженными уровнями NO.В настоящем исследовании TFA, которые связаны с усилением передачи сигналов NF-κB, связаны со снижением передачи сигналов эндотелиального NO. Связь между транс -C18: 1 (Elaidic) и trans -C18: 2 (Linoelaidic) на активацию эндотелиального NF-κB была продемонстрирована ранее [8], и наши исследования подтверждают предыдущее наблюдение. Однако мы расширяем это открытие, связывая активацию NF-κB со снижением передачи сигналов эндотелиальным инсулином и выработкой NO.
Взаимосвязь между общим промышленным потреблением ТЖК (частично гидрогенизированного растительного масла) и сердечно-сосудистыми заболеваниями хорошо изучена.Однако о сосудистых эффектах определенных изомеров TFA известно меньше. Во время частичного гидрирования растительного масла (промышленного TFA), такого как транс -18: 1, расположение двойной связи варьируется от углеродного номера 4 до 16, однако двойные связи в основном сосредоточены на углероде 9 или 10. распределение зависит, во-первых, от исходного растительного масла и, во-вторых, от степени гидрирования. Имеет ли конкретный изомер транс -C18: 1 больший риск сердечно-сосудистых заболеваний, остается вопросом без ответа, однако, возможно, трудно ответить на него с помощью популяционных исследований.Однако наши текущие исследования in vitro подтверждают гипотезу о том, что различные изомеры транс -C18: 1 по-разному влияют на активацию эндотелиального NF-κB и на продукцию NO и супероксида. Кроме того, эти различные эффекты могут служить «механистическим» объяснением дифференциального клинического риска различных изомеров TFA и предполагают, что некоторые изомеры C18: 1 (например, трансваценовая кислота) могут иметь ограниченное действие на эндотелиальные клетки.
Влияние TFA, полученного из жвачных животных (например,Transvaccenic acid) на риск сердечно-сосудистых заболеваний или эндотелиальной дисфункции четко не определены. Tardy et al. недавно были рассмотрены 5 исследований, в которых изучалась связь между потреблением ТЖК, полученных из жвачных животных, и риском сердечно-сосудистых заболеваний [25]. В отличие от промышленных TFA, в настоящее время нет убедительных доказательств связи TFA, полученных из жвачных животных, с риском сердечно-сосудистых заболеваний. TFA, полученная из жвачных животных, может быть менее вредным, особенно при более низком уровне, и потребление молочных жиров может быть допустимым в отношении риска сердечно-сосудистых заболеваний.Кроме того, в небольших обсервационных исследованиях не было выявлено конкретной связи между ТЖК жвачных и системным воспалением или эндотелиальной дисфункцией. Наши текущие исследования in vitro с трансвакценовой кислотой (наша модель TFA, полученного из жвачных животных) подтверждают это наблюдение и согласуются с наблюдаемыми клиническими исследованиями.
Точные молекулярные пути, с помощью которых TFA усиливают передачу сигналов NF-κB, остаются без ответа, однако было предложено несколько возможных механизмов. Во-первых, известно, что многие пищевые жиры включаются в клеточные мембраны и липидные рафты, что может изменять функцию рецепторов клеток.Исследования in vitro на эндотелиальных клетках аорты человека продемонстрировали повышенное включение транс -C18: 2 в клеточную мембрану, что было связано с повышенной экспрессией молекул адгезии [8]. Во-вторых, TFA может изменять метаболизм жирных кислот за счет снижения поглощения и этерификации жирных кислот. В-третьих, наша лаборатория и другие показали роль рецептора врожденного иммунитета, toll-подобного рецептора 4, в опосредовании эффектов насыщенных жиров при активации NF-κB [24]. Возможно, что TFA может активировать TLR4 напрямую или косвенно, изменяя функцию липидного рафта.Наконец, наша лаборатория и другие продемонстрировали потенциальную роль НАДФН-оксидазозависимого образования АФК в опосредовании воспалительных эффектов пищевых жиров [19]. Снижение передачи сигналов NAPDHoxidase или генерации ROS ослабляет способность пальмитата усиливать передачу сигналов NF-κB. В текущем исследовании мы также наблюдали корреляцию с генерацией ROS и активацией эндотелиального NF-κB.
Клинические исследования продемонстрировали сильное влияние FFA на продукцию NO. У здоровых пациентов-добровольцев прием однократного приема пищи с высоким содержанием жиров временно ухудшает функцию эндотелия, что измеряется с помощью вазодилатации плечевой артерии, опосредованной потоком [26].Инфузия высоких доз интралипида плюс гепарин нормальным добровольцам повышает концентрацию циркулирующих FFA от начальной концентрации 350 мкМ до пика 3800 мкМ [27]. Вазодилатация, вызванная метахолином, уменьшилась на 20%, что указывает на то, что повышенные уровни СЖК вызывают эндотелиальную дисфункцию [27]. В другом исследовании повышение уровней FFA приводило к нарушению базальной и инсулино-опосредованной продукции NO [28]. Эти исследования на людях показывают, что производство NO нарушается в присутствии высоких циркулирующих уровней СЖК.
В наших исследованиях in vitro мы использовали дозы отдельных TFA от 25 до 100 мкМ, что выше, чем у людей. Было показано, что диета, богатая различными транс -C18: 1, увеличивает сывороточные уровни всех TFA до 40–120 мМ [29], что позволяет предположить, что дозы TFA в исследовании in vitro могут быть в 2–4 раза выше, чем обнаруженные в человеческая сыворотка. Исследования in vitro ограничены тем, что для наблюдения биологического эффекта необходимы более высокие концентрации, и их необходимо подтверждать в исследованиях питания.
В заключение, настоящие исследования демонстрируют, что два обычных промышленных TFA-изомера C18 увеличивают активацию NF-κB и ухудшают инсулино-опосредованную продукцию NO в эндотелиальных клетках. Эти исследования предполагают дифференциальный эффект изомеров C18 и то, что расположение и количество двойных транс-связей влияют на активацию эндотелиального NF-κB. Кроме того, эти исследования предоставляют механистическое понимание роли TFA в опосредовании эндотелиальной дисфункции, приводящей к сосудистым нарушениям.
Вклад авторов
Задумал и спроектировал эксперименты: NGI MP NOR AMC EM FK.Проведены эксперименты: NGI MP NOR AMC EM. Проанализированы данные: NGI MP NOR AMC EM FK. Предоставленные реагенты / материалы / инструменты анализа: AMC FK. Написал статью: NGI FK.
Ссылки
- 1.
Эллисон Д. Б., Иган С. К., Баррадж Л. М., Когман С., Инфанте М. и др. (1999) Расчетное потребление трансжирных и других жирных кислот населением США. J Am Diet Assoc 99: 166–174; викторина 175–166. - 2.
Lemaitre RN, King IB, Mozaffarian D, Sotoodehnia N, Rea TD, et al.(2006) Трансжирные кислоты фосфолипидов в плазме, смертельная ишемическая болезнь сердца и внезапная сердечная смерть у пожилых людей: исследование здоровья сердечно-сосудистой системы. Тираж 114: 209–215. - 3.
Сан К., Ма Дж., Кампос Х., Хэнкинсон С.Е., Мэнсон Дж. Э. и др. (2007) Проспективное исследование трансжирных кислот в эритроцитах и риска ишемической болезни сердца. Тираж 115: 1858–1865. - 4.
Baer DJ, Judd JT, Clevidence BA, Tracy RP (2004) Диетические жирные кислоты влияют на плазменные маркеры воспаления у здоровых мужчин, получающих контролируемую диету: рандомизированное перекрестное исследование.Am J Clin Nutr 79: 969–973. - 5.
Лопес-Гарсия Э., Шульце М.Б., Мейгс Дж.Б., Мэнсон Дж.Э., Рифаи Н. и др. (2005) Потребление трансжирных кислот связано с плазменными биомаркерами воспаления и эндотелиальной дисфункции. J Nutr 135: 562–566. - 6.
Kim F, Gallis B, Corson MA (2001) TNF-alpha ингибирует поток и передачу сигналов инсулина, приводя к продукции NO в эндотелиальных клетках аорты. Am J Physiol Cell Physiol 280: C1057–1065. - 7.
Montagnani M, Ravichandran LV, Chen H, Esposito DL, Quon MJ (2002) Субстрат-1 рецептора инсулина и фосфоинозитид-зависимая киназа-1 необходимы для стимулированного инсулином производства оксида азота в эндотелиальных клетках.Мол Эндокринол 16: 1931–1942. - 8.
Харви К.А., Арнольд Т., Расул Т., Анталис С., Миллер С.Дж. и др. (2008) Трансжирные кислоты вызывают провоспалительные реакции и дисфункцию эндотелиальных клеток. Br J Nutr 99: 723–731. - 9.
Cousin SP, Hugl SR, Wrede CE, Kajio H, Myers MG и др. (2001) Ингибирование индуцированного свободными жирными кислотами глюкозы и индуцированного инсулиноподобным фактором роста I синтеза дезоксирибонуклеиновой кислоты в линии бета-клеток поджелудочной железы INS-1. Эндокринология 142: 229–240. - 10.
Галлис Б., Корталс Г.Л., Гудлетт Д.Р., Уэба Х., Ким Ф. и др. (1999) Идентификация зависимых от потока участков фосфорилирования эндотелиальной синтазы оксида азота с помощью масс-спектрометрии и регуляции фосфорилирования и продукции оксида азота ингибитором фосфатидилинозитол-3-киназы LY294002. J Biol Chem 274: 30101–30108. - 11.
Ландмессер У., Кай Х., Дикалов С., Макканн Л., Хванг Дж. И др. (2002) Роль p47 (phox) в оксидативном стрессе сосудов и гипертонии, вызванной ангиотензином II.Гипертония 40: 511–515. - 12.
Дикалов С.И., Ли В., Мехранпур П., Ван С.С., Зафари А.М. (2007) Производство внеклеточного супероксида линиями лимфобластных клеток человека: сравнение методов электронного спинового резонанса и анализа восстановления цитохрома С. Biochem Pharmacol 73: 972–980. - 13.
Chalupsky K, Cai H (2005) Эндотелиальная дигидрофолатредуктаза: критически важна для биодоступности оксида азота и роли в разобщении ангиотензином II эндотелиальной синтазы оксида азота.Proc Natl Acad Sci U S A 102: 9056–9061. - 14.
Клещев А.Л., Моллнау Х., Эльзе М., Мейнерц Т., Хуанг Й. и др. (2000) Спиновое улавливание оксида азота в сосудах с использованием коллоидного Fe (II) -диэтилдитиокарбамата. Biochem Biophys Res Commun 275: 672–677. - 15.
Alp NJ, McAteer MA, Khoo J, Choudhury RP, Channon KM (2004) Повышенный синтез эндотелиального тетрагидробиоптерина за счет направленной сверхэкспрессии трансгенной GTP-циклогидролазы I снижает эндотелиальную дисфункцию и атеросклероз у мышей с нокаутом ApoE.Артериосклер Thromb Vasc Biol 24: 445–450. - 16.
Ким Ф., Тисселинг К.А., Райс Дж., Фам М., Хаджи Л. и др. (2005) Нарушение производства оксида азота в эндотелиальных клетках свободными жирными кислотами опосредуется IKKbeta. Артериосклер Thromb Vasc Biol 25: 989–994. - 17.
Cai H, Dikalov S, Griendling KK, Harrison DG (2007) Обнаружение активных форм кислорода и оксида азота в сосудистых клетках и тканях: сравнение чувствительности и специфичности. Методы Mol Med 139: 293–311. - 18.
Клещев А.Л., Мунзель Т. (2002) Усовершенствованное спин-улавливание оксида азота сосудов с использованием диэтилдитиокарбамата коллоидного железа. Методы Enzymol 359: 42–51. - 19.
Мэлони Э., Свит И.Р., Хоккенбери Д.М., Фам М., Риццо Н.О. и др. (2009) Активация NF-kappaB пальмитатом в эндотелиальных клетках: ключевая роль супероксида, производного от НАДФН-оксидазы, в ответ на активацию TLR4. Артериосклер Thromb Vasc Biol 29: 1370–1375. - 20.
Young VM, Toborek M, Yang F, McClain CJ, Hennig B (1998) Эффект линолевой кислоты на медиаторы воспаления эндотелиальных клеток.Метаболизм 47: 566–572. - 21.
Pieper GM, Riaz ul H (1997) Активация ядерного фактора-kappaB в культивируемых эндотелиальных клетках путем повышения концентрации глюкозы: предотвращение с помощью кальфостина C. J Cardiovasc Pharmacol 30: 528–532. - 22.
Ким Ф., Тисселинг К.А., Райс Дж., Галлис Б., Хаджи Л. и др. (2005) Активация IKKbeta глюкозой необходима и достаточна для нарушения передачи сигналов инсулина и выработки оксида азота в эндотелиальных клетках. J Mol Cell Cardiol 39: 327–334. - 23.
Хингорани А.Д., Кросс Дж., Харбанда Р.К., Маллен М.Дж., Бхагат К. и др. (2000) Острое системное воспаление нарушает зависимую от эндотелия дилатацию у людей. Тираж 102: 994–999. - 24.
Ким Ф., Фам М., Латтрелл И., Баннерман Д. Д., Таппер Дж. И др. (2007) Toll-подобный рецептор-4 опосредует сосудистое воспаление и инсулинорезистентность при ожирении, вызванном диетой. Circ Res 100: 1589–1596. - 25.
Tardy AL, Morio B, Chardigny JM, Malpuech-Brugere C (2011) Жвачные животные и промышленные источники трансжиров, сердечно-сосудистых и диабетических заболеваний.Nutr Res Rev 1–7. - 26.
Фогель Р.А., Корретти М.С., Плотник Г.Д. (1997) Влияние однократного приема пищи с высоким содержанием жиров на функцию эндотелия у здоровых субъектов. Am J Cardiol 79: 350–354. - 27.
Steinberg HO, Tarshoby M, Monestel R, Hook G, Cronin J и др. (1997) Повышенный уровень циркулирующих свободных жирных кислот нарушает эндотелий-зависимую вазодилатацию. Дж. Клин Инвест 100: 1230–1239. - 28.
Steinberg HO, Paradisi G, Hook G, Crowder K, Cronin J и др.(2000) Повышение уровня свободных жирных кислот ухудшает опосредованную инсулином вазодилатацию и выработку оксида азота. Диабет 49: 1231–1238. - 29.
Dlouhy P, Kucera P, Kraml P, Pompachova A, Potockova J, et al. (2008) Кратковременное потребление трансжирных кислот C18: 1 с пищей снижает функцию клеточного иммунитета у здоровых молодых мужчин.

 Осмысливания и первичного закрепления информации по теме «Оксиды: состав, номенклатура, химические свойства. Способы получения
Осмысливания и первичного закрепления информации по теме «Оксиды: состав, номенклатура, химические свойства. Способы получения
 О. раств. + вода = щелочь
О. раств. + вода = щелочь