Содержание
Химические свойства кислот
H2SO4 — серная (сульфаты)
HCl — соляная (Хлориды)
HNO3 — азотная (нитраты)
H3PO4 — фосфорная (Фосфаты)
H2SO3 -сернистая (сульфиты)
H2S -сероводород (сульфиды)
H2CO3 — угольная (карбонаты)
H2SiO3 — кремниевая (силикаты)
1. Кислоты реагируют
- с металлами, стоящими в ряду активностм левее водорода с выделением водорода (кроме азотной и концентрированной серной)
- с основными оксидами с образованием соли и воды
- с основаниями с образованием соли и воды
- с солями, образованными более слабыми кислотами с выпадением осадка или выделением газа
2. Азотная кислота реагирует со всеми металлами, кроме Au, Pt, Al, Fe, при этом водород не выделяется, а образуются различные соединения азота (NH4NO3, N2, N2O, NO, NO2) в зависимости от концентрации кислоты и активности металла.
3. Концентрированная серная кислота реагирует со всеми металлами, кроме Au, Pt, Al, Fe, при этом водород не выделяется, а выделяются различные соединения серы (H2S, S, SO2) в зависимости от активности металла.
4. Вытеснительный ряд кислот (по убыванию):
H2SO4 —> HCl и HNO3 —> H3PO4 —> H2SO3 —> H2S —> H2CO3 —> H2SiO3
5. Кислоты (кроме нерастворимой в воде кремниевой кислоты) изменяют окраску индикаторов: фиолетовый лакмус в кислотах краснеет, оранжевый метилоранж становится розовым.
Давайте порассуждаем вместе
1. С разбавленным раствором серной кислоты реагирует
1) медь
2) оксид меди (II)
3) оксид серы (IV)
4) оксид кремния (IV)
Ответ: №2, т.
к. кислоты реагируют с основными оксидами H2SO4 + CuO = CuSO4 + H2O
2. Какая из кислот реагирует и с гидроксидом бария и с хлоридом бария?
1) азотная
2) серная
3) соляная
4) угольная
Ответ: №2, т.к. выпадает нарастворимый в кислотах осадок сульфата бария
Ba(OH)2 + H2SO4 = BaSO4 + 2H2O
BaCl2 + H2SO4 = BaSO4 + 2HCl
3. Какая из перечисленных кислот реагирует с гидроксидом натрия, но не изменяет окраску лакмуса?
1) серная
2) соляная
3) угольная
4) кремниевая
Ответ №4, т.
к. кремниевая кислота не растворяется в воде и не изменяет окраску лакмуса
4. Какая из кислот реагирует с серебром даже в разбавленном растворе?
1) азотная
2) серная
3) фосфорная
4) соляная
Ответ: №1, т.к. азотная кислота сильный окислитель и реагирует даже с металлами, стоящими после водорода, выделяя NO
3Ag + 4HNO3 = 3AgNO3 + NO + 2H2O
5. Какое из веществ не реагирует с азотной кислотой, но реагирует с соляной кислотой с образованием белого осадка?
1) MgCO3
2) Zn
3) AgNO3
4) Cu
Ответ: №3, т.к. AgNO3 + HCl = AgCl + HNO3 выпадает белый осадок хлорида серебра, нерастворимый в азотной кислоте.
6. Какое из веществ не реагирует с азотной кислотой, но реагирует с серной кислотой с образованием белого осадка?
1) CaCO3
2) BaCl2
3) Ag
4) Cu(NO3)2
Ответ: №2, т.к. BaCl2 + H2SO4 = BaSO4 + 2HCl выпадает белый осадок сульфата бария
7. Для серной кислоты справедливо высказывание:
1) плотность серной кислоты примерна равна 1 г/мл
2) серная кислота — легкоподвижная жидкость
3) растворение кислоты в воде — экзотермическая реакция
4) серная кислота не действует на цинк и медь
Ответ: №3, т.к. при растворении концентрированной серной кислоты в воде выделяется большое количество тепла.
Химические свойства гидроксидов и кислот
Дидактический материал
Тренировочные тесты ЕГЭ по химии
Характерные химические свойства оснований, и амфотерных гидроксидов. Характерные химические
свойства кислот.
1. Гидроксид калия взаимодействует с каждым из двух веществ
1) NH3 и HCl 2) CO2 и CuCl2 3) H2SO4 и NaNO3 4) MgO и HNO3
2. Разбавленная хлороводородная кислота взаимодействует с каждым из двух веществ
1) медью и гидроксидом натрия
2) магнием и нитратом серебра
3) железом и оксидом кремния (IV)
4) свинцом и нитратом калия
3. С соляной кислотой взаимодействует
1) NaHCO3 2)Hg 3) SiO2 4) S
4. Реакция нейтрализации происходит при взаимодействии
1) Fe2O3 и HCl
2) Fe(OH)3 и HCl
3) FeCl3 и NaNCS
4) Fe и HCl
5. Гидроксид железа (II) взаимодействует с
Гидроксид железа (II) взаимодействует с
1) азотной кислотой
2) оксидом кальция
3) сульфатом меди
4) аммиаком
6. Разбавленная серная кислота не взаимодействует с
1) гидроксидом кальция
2) оксидом меди (II)
3) цинком
4) оксидом углерода (IV)
7. С гидроксидом калия реагирует каждое из двух веществ
1) AlCl3 и H2S
2) CuO и Ba(OH)2
3) CaCO3 и NH3
4) K2SO4 и AlCl3
8. Гидроксид кальция реагирует с каждым из двух веществ
1) HCl и СО2
2) HNO3 и MgO
3) HCl и KOH
4) BaCl2 и NaOH
9. Гидроксид калия реагирует с
1) водой
2) щелочью
3) кислотой
4) кислотой и щелочью
10. Гидроксид кальция не взаимодействует
1) HCl 2) ZnS 3) CO2 4) HNO3
11. Гидроксид хрома (III) реагирует с каждым из двух веществ
Гидроксид хрома (III) реагирует с каждым из двух веществ
1) СО2 и HCl
2) SiO2 и Cu(OH)2
3) NO и NaNO3
4) H2SO4 и NaOH
12. Реакция нейтрализации происходит между
1) | цинком и соляной кислотой |
2) | серной кислотой и хлоридом бария |
3) | гидроксидом кальция и азотной кислотой |
4) | гидроксидом натрия и сульфатом меди |
13 . С раствором серной кислоты взаимодействует каждое из двух веществ:
1) | хлорид бария и оксид углерода (IV) |
2) | магний и хлорид бария |
3) | хлорид натрия и фосфорная кислота |
4) | медь и гидроксид калия |
14. Гидроксид кальция реагирует с
Гидроксид кальция реагирует с
1) | Ba(NO3)2 | 2) | KCl | 3) | NH3·H2O | 4) | Na3PO4 |
15. Концентрированная азотная кислота в обычных условиях не взаимодействует с
1) | магнием |
2) | гидроксидом натрия |
3) | железом |
4) | оксидом магния |
16. При сливании водных растворов уксусной кислоты и гидроксида калия образуется
При сливании водных растворов уксусной кислоты и гидроксида калия образуется
1) | ацетат калия и водород |
2) | карбонат калия и вода |
3) | ацетат калия и вода |
4) | карбид калия и углекислый газ |
17. Гидроксид натрия не реагирует с
1) | Al(OH)3 | 2) | ZnO | 3) | H2SO4 | 4) | Ba(OH)2 |
18. Разбавленная серная кислота реагирует с каждым из двух веществ:
Разбавленная серная кислота реагирует с каждым из двух веществ:
1) | Na2SiO3 и HNO3 |
2) | Fe2O3 и KNO3 |
3) | Ag и Cu(OH)2 |
4) | Fe и Al2O3 |
19. Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
1) | CuO | 2) | H2SO4 | 3) | CO2 | 4) | NaOH |
20. Соляная кислота не взаимодействует ни с одним из двух веществ:
Соляная кислота не взаимодействует ни с одним из двух веществ:
1) | цинком и гидроксидом натрия |
2) | медью и оксидом меди (II) |
3) | ртутью и оксидом углерода (IV) |
4) | магнием и аммиаком |
21. С каждым из перечисленных веществ: H2S, KOH, Zn
взаимодействует
1) | Pb(NO3)2 | 2) | ZnSO4 | 3) | Na2CO3 | 4) | HCl |
22. Разбавленная серная кислота может реагировать с каждым из двух веществ:
Разбавленная серная кислота может реагировать с каждым из двух веществ:
1) | серой и магнием |
2) | оксидом железа (II) и оксидом кремния (IV) |
3) | гидроксидом калия и хлоридом калия |
4) | нитратом бария и гидроксидом меди (II) |
23. С раствором серной кислоты взаимодействует каждое из двух веществ:
1) | хлорид бария и оксид углерода (IV) |
2) | магний и хлорид бария |
3) | хлорид натрия и фосфорная кислота |
4) | медь и гидроксид калия |
24. Концентрированная азотная кислота в обычных условиях не взаимодействует с
Концентрированная азотная кислота в обычных условиях не взаимодействует с
1) | магнием |
2) | гидроксидом натрия |
3) | железом |
4) | оксидом магния |
25. Раствор гидроксида натрия реагирует с каждым из веществ, указанных попарно
1) | хлоридом железа (III) и углекислым газом |
2) | оксидом железа (II) и соляной кислотой |
3) | серной кислотой и карбонатом кальция |
4) | оксидом цинка и хлоридом калия |
26. Гидроксид натрия не реагирует с
Гидроксид натрия не реагирует с
1) | Al(OH)3 | 2) | ZnO | 3) | H2SO4 | 4) | Ba(OH)2 |
27. Разбавленная серная кислота реагирует с каждым из двух веществ:
1) | Na2SiO3 и HNO3 |
2) | Fe2O3 и KNO3 |
3) | Ag и Cu(OH)2 |
4) | Fe и Al2O3 |
28. Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
1) | CuO | 2) | H2SO4 | 3) | CO2 | 4) | NaOH |
29. Соляная кислота не взаимодействует ни с одним из двух веществ:
1) | цинком и гидроксидом натрия |
2) | медью и оксидом меди (II) |
3) | ртутью и оксидом углерода (IV) |
4) | магнием и аммиаком |
30. Раствор гидроксида натрия не взаимодействует с
Раствор гидроксида натрия не взаимодействует с
1) | СО2 | 2) | HСl | 3) | SO2 | 4) | MgO |
ОТВЕТЫ: 1-2, 2-2, 3-1, 4-2, 5-1, 6-4, 7-1, 8-1, 9-3, 10-2, 11-4, 12-3, 13-2, 14-4, 15-1, 16-3, 17-4, 18-4, 19-4, 20-3, 21-1, 22-4, 23-2, 24-3, 25-3, 26-4, 27-4, 28-4, 29-3, 30-4, 31-1.
Seite nicht gefunden — Портал Продуктов Группы РСС
Сообщите нам свой адрес электронной почты, чтобы подписаться на рассылку новостного бюллетеня. Предоставление адреса электронной почты является добровольным, но, если Вы этого не сделаете, мы не сможем отправить Вам информационный бюллетень. Администратором Ваших персональных данных является Акционерное Общество PCC Rokita, находящееся в Бжег-Дольном (ул. Сенкевича 4, 56-120 Бжег-Дольный, Польша ). Вы можете связаться с нашим инспектором по защите личных данных по электронной почте: .
Администратором Ваших персональных данных является Акционерное Общество PCC Rokita, находящееся в Бжег-Дольном (ул. Сенкевича 4, 56-120 Бжег-Дольный, Польша ). Вы можете связаться с нашим инспектором по защите личных данных по электронной почте: .
Мы обрабатываем Ваши данные для того, чтобы отправить Вам информационный бюллетень — основанием для обработки является реализация нашей законодательно обоснованной заинтересованности или законодательно обоснованная заинтересованность третьей стороны – непосредственный маркетинг наших продуктов / продуктов группы PCC .
Как правило, Ваши данные мы будем обрабатывать до окончания нашего с Вами общения или же до момента, пока Вы не выразите свои возражения, либо если правовые нормы будут обязывать нас продолжать обработку этих данных, либо мы будем сохранять их дольше в случае потенциальных претензий, до истечения срока их хранения, регулируемого законом, в частности Гражданским кодексом.
В любое время Вы имеете право:
- выразить возражение против обработки Ваших данных;
- иметь доступ к Вашим данным и востребовать их копии;
- запросить исправление, ограничение обработки или удаление Ваших данных;
- передать Ваши персональные данные, например другому администратору, за исключением тех случаев, если их обработка регулируется законом и находится в интересах администратора;
- подать жалобу Президенту Управления по защите личных данных.

Получателями Ваших данных могут быть компании, которые поддерживают нас в общении с Вами и помогают нам в ведении веб-сайта, внешние консалтинговые компании (такие как юридические, маркетинговые и бухгалтерские) или внешние специалисты в области IT, включая компанию Группы PCC .
Больше о том, как мы обрабатываем Ваши данные Вы можете узнать из нашего Полиса конфиденциальности.
ВВЕДЕНИЕ
%PDF-1.5
%
1 0 obj
>
/Metadata 2 0 R
/Outlines 3 0 R
/PageLayout /OneColumn
/Pages 4 0 R
/StructTreeRoot 5 0 R
/Type /Catalog
>>
endobj
6 0 obj
/Comments ()
/Company ()
/CreationDate (D:20150227082350+03’00’)
/Creator
/Keywords ()
/ModDate (D:20150227082401+03’00’)
/Producer (Adobe PDF Library 10.0)
/SourceModified (D:20150227051859)
/Subject ()
/Title
>>
endobj
2 0 obj
>
stream
2015-02-27T08:24:01+03:002015-02-27T08:23:50+03:002015-02-27T08:24:01+03:00Acrobat PDFMaker 10.1 для Worduuid:c8f0c946-4918-45cd-9d6b-1bad6009c878uuid:9ca518a8-22ec-4c0b-9cd6-94beb6243623
application/pdf
Adobe PDF Library 10.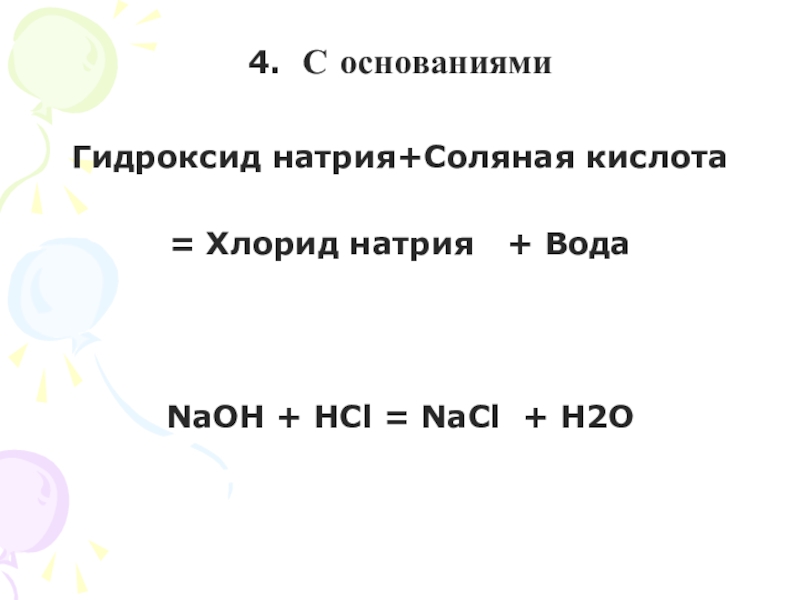 0D:20150227051859
0D:20150227051859
endstream
endobj
3 0 obj
>
endobj
4 0 obj
>
endobj
5 0 obj
>
endobj
7 0 obj
>>
endobj
8 0 obj
>>
endobj
9 0 obj
>
endobj
10 0 obj
>
endobj
11 0 obj
>
endobj
12 0 obj
>
endobj
13 0 obj
>
endobj
14 0 obj
>
endobj
15 0 obj
>
endobj
16 0 obj
>
endobj
17 0 obj
>
endobj
18 0 obj
>
endobj
19 0 obj
>
endobj
20 0 obj
>
endobj
21 0 obj
>
endobj
22 0 obj
>>
endobj
23 0 obj
>
endobj
24 0 obj
>>
endobj
25 0 obj
>
endobj
26 0 obj
>>
endobj
27 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 0
/Type /Page
/Annots [2766 0 R]
>>
endobj
28 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 1
/Type /Page
>>
endobj
29 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 2
/Type /Page
>>
endobj
30 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 3
/Type /Page
>>
endobj
31 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 4
/Type /Page
>>
endobj
32 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 5
/Type /Page
>>
endobj
33 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 6
/Type /Page
>>
endobj
34 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 7
/Type /Page
>>
endobj
35 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 8
/Type /Page
>>
endobj
36 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 9
/Type /Page
>>
endobj
37 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 10
/Type /Page
>>
endobj
38 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 11
/Type /Page
>>
endobj
39 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 12
/Type /Page
>>
endobj
40 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 13
/Type /Page
>>
endobj
41 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 14
/Type /Page
>>
endobj
42 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 15
/Type /Page
>>
endobj
43 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 16
/Type /Page
>>
endobj
44 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 17
/Type /Page
>>
endobj
45 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 18
/Type /Page
>>
endobj
46 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 19
/Type /Page
>>
endobj
47 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 20
/Type /Page
>>
endobj
48 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 21
/Type /Page
>>
endobj
49 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 22
/Type /Page
>>
endobj
50 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 23
/Type /Page
>>
endobj
51 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 24
/Type /Page
>>
endobj
52 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 25
/Type /Page
>>
endobj
53 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 26
/Type /Page
>>
endobj
54 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 27
/Type /Page
>>
endobj
55 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 28
/Type /Page
>>
endobj
56 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 29
/Type /Page
>>
endobj
57 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 30
/Type /Page
>>
endobj
58 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 31
/Type /Page
>>
endobj
59 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 32
/Type /Page
>>
endobj
60 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 33
/Type /Page
>>
endobj
61 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 34
/Type /Page
>>
endobj
62 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 35
/Type /Page
>>
endobj
63 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 36
/Type /Page
>>
endobj
64 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 37
/Type /Page
>>
endobj
65 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 38
/Type /Page
>>
endobj
66 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 39
/Type /Page
>>
endobj
67 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 40
/Type /Page
>>
endobj
68 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 41
/Type /Page
>>
endobj
69 0 obj
>
/ExtGState >
/Font >
/XObject >
>>
/Rotate 0
/StructParents 42
/Type /Page
>>
endobj
70 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 43
/Type /Page
>>
endobj
71 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 44
/Type /Page
>>
endobj
72 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 45
/Type /Page
>>
endobj
73 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 46
/Type /Page
>>
endobj
74 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 47
/Type /Page
>>
endobj
75 0 obj
>
/ExtGState >
/Font >
>>
/Rotate 0
/StructParents 48
/Type /Page
>>
endobj
76 0 obj
>
endobj
77 0 obj
>
endobj
78 0 obj
>
endobj
79 0 obj
>
endobj
80 0 obj
>
endobj
81 0 obj
>
endobj
82 0 obj
>
endobj
83 0 obj
>
endobj
84 0 obj
>
endobj
85 0 obj
>
endobj
86 0 obj
>
endobj
87 0 obj
>
endobj
88 0 obj
>
endobj
89 0 obj
>
endobj
90 0 obj
>
endobj
91 0 obj
>
endobj
92 0 obj
>
endobj
93 0 obj
>
endobj
94 0 obj
>
endobj
95 0 obj
>
endobj
96 0 obj
>
endobj
97 0 obj
>
endobj
98 0 obj
>
endobj
99 0 obj
>
endobj
100 0 obj
>
endobj
101 0 obj
>
endobj
102 0 obj
>
endobj
103 0 obj
>
endobj
104 0 obj
>
endobj
105 0 obj
>
endobj
106 0 obj
>
endobj
107 0 obj
>
endobj
108 0 obj
>
endobj
109 0 obj
>
endobj
110 0 obj
>
endobj
111 0 obj
>
endobj
112 0 obj
>
endobj
113 0 obj
>
endobj
114 0 obj
>
endobj
115 0 obj
>
endobj
116 0 obj
>
endobj
117 0 obj
>
endobj
118 0 obj
>
endobj
119 0 obj
>
endobj
120 0 obj
>
endobj
121 0 obj
>
endobj
122 0 obj
>
endobj
123 0 obj
>
endobj
124 0 obj
>
endobj
125 0 obj
>
endobj
126 0 obj
>
endobj
127 0 obj
>
endobj
128 0 obj
>
endobj
129 0 obj
>
endobj
130 0 obj
>
endobj
131 0 obj
>
endobj
132 0 obj
>
endobj
133 0 obj
>
endobj
134 0 obj
>
endobj
135 0 obj
>
endobj
136 0 obj
>
endobj
137 0 obj
>
endobj
138 0 obj
>
endobj
139 0 obj
>
endobj
140 0 obj
>
endobj
141 0 obj
>
endobj
142 0 obj
>
endobj
143 0 obj
>
endobj
144 0 obj
>
endobj
145 0 obj
>
endobj
146 0 obj
>
endobj
147 0 obj
>
endobj
148 0 obj
>
endobj
149 0 obj
>
endobj
150 0 obj
>
endobj
151 0 obj
>
endobj
152 0 obj
>
endobj
153 0 obj
>
endobj
154 0 obj
>
endobj
155 0 obj
>
endobj
156 0 obj
>
endobj
157 0 obj
>
endobj
158 0 obj
>
endobj
159 0 obj
>
endobj
160 0 obj
>
endobj
161 0 obj
>
endobj
162 0 obj
>
endobj
163 0 obj
>
endobj
164 0 obj
>
endobj
165 0 obj
>
endobj
166 0 obj
>
endobj
167 0 obj
>
endobj
168 0 obj
>
endobj
169 0 obj
>
endobj
170 0 obj
>
endobj
171 0 obj
>
endobj
172 0 obj
>
endobj
173 0 obj
>
endobj
174 0 obj
>
endobj
175 0 obj
>
endobj
176 0 obj
>
endobj
177 0 obj
>
endobj
178 0 obj
>
endobj
179 0 obj
>
endobj
180 0 obj
>
endobj
181 0 obj
>
endobj
182 0 obj
>
endobj
183 0 obj
>
endobj
184 0 obj
>
endobj
185 0 obj
>
endobj
186 0 obj
>
endobj
187 0 obj
>
endobj
188 0 obj
>
endobj
189 0 obj
>
endobj
190 0 obj
>
endobj
191 0 obj
>
endobj
192 0 obj
>
endobj
193 0 obj
>
endobj
194 0 obj
>
endobj
195 0 obj
>
endobj
196 0 obj
>
endobj
197 0 obj
>
endobj
198 0 obj
>
endobj
199 0 obj
>
endobj
200 0 obj
>
endobj
201 0 obj
>
endobj
202 0 obj
>
endobj
203 0 obj
>
endobj
204 0 obj
>
endobj
205 0 obj
>
endobj
206 0 obj
>
endobj
207 0 obj
>
endobj
208 0 obj
>
endobj
209 0 obj
>
endobj
210 0 obj
>
endobj
211 0 obj
>
endobj
212 0 obj
>
endobj
213 0 obj
>
endobj
214 0 obj
>
endobj
215 0 obj
>
endobj
216 0 obj
>
endobj
217 0 obj
>
endobj
218 0 obj
>
endobj
219 0 obj
>
endobj
220 0 obj
>
endobj
221 0 obj
>
endobj
222 0 obj
>
endobj
223 0 obj
>
endobj
224 0 obj
>
endobj
225 0 obj
>
endobj
226 0 obj
>
endobj
227 0 obj
>
endobj
228 0 obj
>
endobj
229 0 obj
>
endobj
230 0 obj
>
endobj
231 0 obj
>
endobj
232 0 obj
>
endobj
233 0 obj
>
endobj
234 0 obj
>
endobj
235 0 obj
>
endobj
236 0 obj
>
endobj
237 0 obj
>
endobj
238 0 obj
>
endobj
239 0 obj
>
endobj
240 0 obj
>
endobj
241 0 obj
>
endobj
242 0 obj
>
endobj
243 0 obj
>
endobj
244 0 obj
>
endobj
245 0 obj
>
endobj
246 0 obj
>
endobj
247 0 obj
>
endobj
248 0 obj
>
endobj
249 0 obj
>
endobj
250 0 obj
>
endobj
251 0 obj
>
endobj
252 0 obj
>
endobj
253 0 obj
>
endobj
254 0 obj
>
endobj
255 0 obj
>
endobj
256 0 obj
>
endobj
257 0 obj
>
endobj
258 0 obj
>
endobj
259 0 obj
>
endobj
260 0 obj
>
endobj
261 0 obj
>
endobj
262 0 obj
>
endobj
263 0 obj
>
endobj
264 0 obj
>
endobj
265 0 obj
>
endobj
266 0 obj
>
endobj
267 0 obj
>
endobj
268 0 obj
>
endobj
269 0 obj
>
endobj
270 0 obj
>
endobj
271 0 obj
>
endobj
272 0 obj
>
endobj
273 0 obj
>
endobj
274 0 obj
>
endobj
275 0 obj
>
endobj
276 0 obj
>
endobj
277 0 obj
>
endobj
278 0 obj
>
endobj
279 0 obj
>
endobj
280 0 obj
>
endobj
281 0 obj
>
endobj
282 0 obj
>
endobj
283 0 obj
>
endobj
284 0 obj
>
endobj
285 0 obj
>
endobj
286 0 obj
>
endobj
287 0 obj
>
endobj
288 0 obj
>
endobj
289 0 obj
>
endobj
290 0 obj
>
endobj
291 0 obj
>
endobj
292 0 obj
>
endobj
293 0 obj
>
endobj
294 0 obj
>
endobj
295 0 obj
>
endobj
296 0 obj
>
endobj
297 0 obj
>
endobj
298 0 obj
>
endobj
299 0 obj
>
endobj
300 0 obj
>
endobj
301 0 obj
>
endobj
302 0 obj
>
endobj
303 0 obj
>
endobj
304 0 obj
>
endobj
305 0 obj
>
endobj
306 0 obj
>
endobj
307 0 obj
>
endobj
308 0 obj
>
endobj
309 0 obj
>
endobj
310 0 obj
>
endobj
311 0 obj
>
endobj
312 0 obj
>
endobj
313 0 obj
>
endobj
314 0 obj
>
endobj
315 0 obj
>
endobj
316 0 obj
>
endobj
317 0 obj
>
endobj
318 0 obj
>
endobj
319 0 obj
>
endobj
320 0 obj
>
endobj
321 0 obj
>
endobj
322 0 obj
>
endobj
323 0 obj
>
endobj
324 0 obj
>
endobj
325 0 obj
>
endobj
326 0 obj
>
endobj
327 0 obj
>
endobj
328 0 obj
>
endobj
329 0 obj
>
endobj
330 0 obj
>
endobj
331 0 obj
>
endobj
332 0 obj
>
endobj
333 0 obj
>
endobj
334 0 obj
>
endobj
335 0 obj
>
endobj
336 0 obj
>
endobj
337 0 obj
>
endobj
338 0 obj
>
endobj
339 0 obj
>
endobj
340 0 obj
>
endobj
341 0 obj
>
endobj
342 0 obj
>
endobj
343 0 obj
>
endobj
344 0 obj
>
endobj
345 0 obj
>
endobj
346 0 obj
>
endobj
347 0 obj
>
endobj
348 0 obj
>
endobj
349 0 obj
>
endobj
350 0 obj
>
endobj
351 0 obj
>
endobj
352 0 obj
>
endobj
353 0 obj
>
endobj
354 0 obj
>
endobj
355 0 obj
>
endobj
356 0 obj
>
endobj
357 0 obj
>
endobj
358 0 obj
>
endobj
359 0 obj
>
endobj
360 0 obj
>
endobj
361 0 obj
>
endobj
362 0 obj
>
endobj
363 0 obj
>
endobj
364 0 obj
>
endobj
365 0 obj
>
endobj
366 0 obj
>
endobj
367 0 obj
>
endobj
368 0 obj
>
endobj
369 0 obj
>
endobj
370 0 obj
>
endobj
371 0 obj
>
endobj
372 0 obj
>
endobj
373 0 obj
>
endobj
374 0 obj
>
endobj
375 0 obj
>
endobj
376 0 obj
>
endobj
377 0 obj
>
endobj
378 0 obj
>
endobj
379 0 obj
>
endobj
380 0 obj
>
endobj
381 0 obj
>
endobj
382 0 obj
>
endobj
383 0 obj
>
endobj
384 0 obj
>
endobj
385 0 obj
>
endobj
386 0 obj
>
endobj
387 0 obj
>
endobj
388 0 obj
>
endobj
389 0 obj
>
endobj
390 0 obj
>
endobj
391 0 obj
>
endobj
392 0 obj
>
endobj
393 0 obj
>
endobj
394 0 obj
>
endobj
395 0 obj
>
endobj
396 0 obj
>
endobj
397 0 obj
>
endobj
398 0 obj
>
endobj
399 0 obj
>
endobj
400 0 obj
>
endobj
401 0 obj
>
endobj
402 0 obj
>
endobj
403 0 obj
>
endobj
404 0 obj
>
endobj
405 0 obj
>
endobj
406 0 obj
>
endobj
407 0 obj
>
endobj
408 0 obj
>
endobj
409 0 obj
>
endobj
410 0 obj
>
endobj
411 0 obj
>
endobj
412 0 obj
>
endobj
413 0 obj
>
endobj
414 0 obj
>
endobj
415 0 obj
>
endobj
416 0 obj
>
endobj
417 0 obj
>
endobj
418 0 obj
>
endobj
419 0 obj
>
endobj
420 0 obj
>
endobj
421 0 obj
>
endobj
422 0 obj
>
endobj
423 0 obj
>
endobj
424 0 obj
>
endobj
425 0 obj
>
endobj
426 0 obj
>
endobj
427 0 obj
>
endobj
428 0 obj
>
endobj
429 0 obj
>
endobj
430 0 obj
>
endobj
431 0 obj
>
endobj
432 0 obj
>
endobj
433 0 obj
>
endobj
434 0 obj
>
endobj
435 0 obj
>
endobj
436 0 obj
>
endobj
437 0 obj
>
endobj
438 0 obj
>
endobj
439 0 obj
>
endobj
440 0 obj
>
endobj
441 0 obj
>
endobj
442 0 obj
>
endobj
443 0 obj
>
endobj
444 0 obj
>
endobj
445 0 obj
>
endobj
446 0 obj
>
endobj
447 0 obj
>
endobj
448 0 obj
>
endobj
449 0 obj
>
endobj
450 0 obj
>
endobj
451 0 obj
>
endobj
452 0 obj
>
endobj
453 0 obj
>
endobj
454 0 obj
>
endobj
455 0 obj
>
endobj
456 0 obj
>
endobj
457 0 obj
>
endobj
458 0 obj
>
endobj
459 0 obj
>
endobj
460 0 obj
>
endobj
461 0 obj
>
endobj
462 0 obj
>
endobj
463 0 obj
>
endobj
464 0 obj
>
endobj
465 0 obj
>
endobj
466 0 obj
>
endobj
467 0 obj
>
endobj
468 0 obj
>
endobj
469 0 obj
>
endobj
470 0 obj
>
endobj
471 0 obj
>
endobj
472 0 obj
>
endobj
473 0 obj
>
endobj
474 0 obj
>
endobj
475 0 obj
>
endobj
476 0 obj
>
endobj
477 0 obj
>
endobj
478 0 obj
>
endobj
479 0 obj
>
endobj
480 0 obj
>
endobj
481 0 obj
>
endobj
482 0 obj
>
endobj
483 0 obj
>
endobj
484 0 obj
>
endobj
485 0 obj
>
endobj
486 0 obj
>
endobj
487 0 obj
>
endobj
488 0 obj
>
endobj
489 0 obj
>
endobj
490 0 obj
>
endobj
491 0 obj
>
endobj
492 0 obj
>
endobj
493 0 obj
>
endobj
494 0 obj
>
endobj
495 0 obj
>
endobj
496 0 obj
>
endobj
497 0 obj
>
endobj
498 0 obj
>
endobj
499 0 obj
>
endobj
500 0 obj
>
endobj
501 0 obj
>
endobj
502 0 obj
>
endobj
503 0 obj
>
endobj
504 0 obj
>
endobj
505 0 obj
>
endobj
506 0 obj
>
endobj
507 0 obj
>
endobj
508 0 obj
>
endobj
509 0 obj
>
endobj
510 0 obj
>
endobj
511 0 obj
>
endobj
512 0 obj
>
endobj
513 0 obj
>
endobj
514 0 obj
>
endobj
515 0 obj
>
endobj
516 0 obj
>
endobj
517 0 obj
>
endobj
518 0 obj
>
endobj
519 0 obj
>
endobj
520 0 obj
>
endobj
521 0 obj
>
endobj
522 0 obj
>
endobj
523 0 obj
>
endobj
524 0 obj
>
endobj
525 0 obj
>
endobj
526 0 obj
>
endobj
527 0 obj
>
endobj
528 0 obj
>
endobj
529 0 obj
>
endobj
530 0 obj
>
endobj
531 0 obj
>
endobj
532 0 obj
>
endobj
533 0 obj
>
endobj
534 0 obj
>
endobj
535 0 obj
>
endobj
536 0 obj
>
endobj
537 0 obj
>
endobj
538 0 obj
>
endobj
539 0 obj
>
endobj
540 0 obj
>
endobj
541 0 obj
>
endobj
542 0 obj
>
endobj
543 0 obj
>
endobj
544 0 obj
>
endobj
545 0 obj
>
endobj
546 0 obj
>
endobj
547 0 obj
>
endobj
548 0 obj
>
endobj
549 0 obj
>
endobj
550 0 obj
>
endobj
551 0 obj
>
endobj
552 0 obj
>
endobj
553 0 obj
>
endobj
554 0 obj
>
endobj
555 0 obj
>
endobj
556 0 obj
>
endobj
557 0 obj
>
endobj
558 0 obj
>
endobj
559 0 obj
>
endobj
560 0 obj
>
endobj
561 0 obj
>
endobj
562 0 obj
>
endobj
563 0 obj
>
endobj
564 0 obj
>
endobj
565 0 obj
>
endobj
566 0 obj
>
endobj
567 0 obj
>
endobj
568 0 obj
>
endobj
569 0 obj
>
endobj
570 0 obj
>
endobj
571 0 obj
>
endobj
572 0 obj
>
endobj
573 0 obj
>
endobj
574 0 obj
>
endobj
575 0 obj
>
endobj
576 0 obj
>
endobj
577 0 obj
>
endobj
578 0 obj
>
endobj
579 0 obj
>
endobj
580 0 obj
>
endobj
581 0 obj
>
endobj
582 0 obj
>
endobj
583 0 obj
>
endobj
584 0 obj
>
endobj
585 0 obj
>
endobj
586 0 obj
>
endobj
587 0 obj
>
endobj
588 0 obj
>
endobj
589 0 obj
>
endobj
590 0 obj
>
endobj
591 0 obj
>
endobj
592 0 obj
>
endobj
593 0 obj
>
endobj
594 0 obj
>
endobj
595 0 obj
>
endobj
596 0 obj
>
endobj
597 0 obj
>
endobj
598 0 obj
>
endobj
599 0 obj
>
endobj
600 0 obj
>
endobj
601 0 obj
>
endobj
602 0 obj
>
endobj
603 0 obj
>
endobj
604 0 obj
>
endobj
605 0 obj
>
endobj
606 0 obj
>
endobj
607 0 obj
>
endobj
608 0 obj
>
endobj
609 0 obj
>
endobj
610 0 obj
>
endobj
611 0 obj
>
endobj
612 0 obj
>
endobj
613 0 obj
>
endobj
614 0 obj
>
endobj
615 0 obj
>
endobj
616 0 obj
>
endobj
617 0 obj
>
endobj
618 0 obj
>
endobj
619 0 obj
>
endobj
620 0 obj
>
endobj
621 0 obj
>
endobj
622 0 obj
>
endobj
623 0 obj
>
endobj
624 0 obj
>
endobj
625 0 obj
>
endobj
626 0 obj
>
endobj
627 0 obj
>
endobj
628 0 obj
>
endobj
629 0 obj
>
endobj
630 0 obj
>
endobj
631 0 obj
>
endobj
632 0 obj
>
endobj
633 0 obj
>
endobj
634 0 obj
>
endobj
635 0 obj
>
endobj
636 0 obj
>
endobj
637 0 obj
>
endobj
638 0 obj
>
endobj
639 0 obj
>
endobj
640 0 obj
>
endobj
641 0 obj
>
endobj
642 0 obj
>
endobj
643 0 obj
>
endobj
644 0 obj
>
endobj
645 0 obj
>
endobj
646 0 obj
>
endobj
647 0 obj
>
endobj
648 0 obj
>
endobj
649 0 obj
>
endobj
650 0 obj
>
endobj
651 0 obj
>
endobj
652 0 obj
>
endobj
653 0 obj
>
endobj
654 0 obj
>
endobj
655 0 obj
>
endobj
656 0 obj
>
endobj
657 0 obj
>
endobj
658 0 obj
>
endobj
659 0 obj
>
endobj
660 0 obj
>
endobj
661 0 obj
>
endobj
662 0 obj
>
endobj
663 0 obj
>
endobj
664 0 obj
>
endobj
665 0 obj
>
endobj
666 0 obj
>
endobj
667 0 obj
>
endobj
668 0 obj
>
endobj
669 0 obj
>
endobj
670 0 obj
>
endobj
671 0 obj
>
endobj
672 0 obj
>
endobj
673 0 obj
>
endobj
674 0 obj
>
endobj
675 0 obj
>
endobj
676 0 obj
>
endobj
677 0 obj
>
endobj
678 0 obj
>
endobj
679 0 obj
>
endobj
680 0 obj
>
endobj
681 0 obj
>
endobj
682 0 obj
>
endobj
683 0 obj
>
endobj
684 0 obj
>
endobj
685 0 obj
>
endobj
686 0 obj
>
endobj
687 0 obj
>
endobj
688 0 obj
>
endobj
689 0 obj
>
endobj
690 0 obj
>
endobj
691 0 obj
>
endobj
692 0 obj
>
endobj
693 0 obj
>
endobj
694 0 obj
>
endobj
695 0 obj
>
endobj
696 0 obj
>
endobj
697 0 obj
>
endobj
698 0 obj
>
endobj
699 0 obj
>
endobj
700 0 obj
>
endobj
701 0 obj
>
endobj
702 0 obj
>
endobj
703 0 obj
>
endobj
704 0 obj
>
endobj
705 0 obj
>
endobj
706 0 obj
>
endobj
707 0 obj
>
endobj
708 0 obj
>
endobj
709 0 obj
>
endobj
710 0 obj
>
endobj
711 0 obj
>
endobj
712 0 obj
>
endobj
713 0 obj
>
endobj
714 0 obj
>
endobj
715 0 obj
>
endobj
716 0 obj
>
endobj
717 0 obj
>
endobj
718 0 obj
>
endobj
719 0 obj
>
endobj
720 0 obj
>
endobj
721 0 obj
>
endobj
722 0 obj
>
endobj
723 0 obj
>
endobj
724 0 obj
>
endobj
725 0 obj
>
endobj
726 0 obj
>
endobj
727 0 obj
>
endobj
728 0 obj
>
endobj
729 0 obj
>
endobj
730 0 obj
>
endobj
731 0 obj
>
endobj
732 0 obj
>
endobj
733 0 obj
>
endobj
734 0 obj
>
endobj
735 0 obj
>
endobj
736 0 obj
>
endobj
737 0 obj
>
endobj
738 0 obj
>
endobj
739 0 obj
>
endobj
740 0 obj
>
endobj
741 0 obj
>
endobj
742 0 obj
>
endobj
743 0 obj
>
endobj
744 0 obj
>
endobj
745 0 obj
>
endobj
746 0 obj
>
endobj
747 0 obj
>
endobj
748 0 obj
>
endobj
749 0 obj
>
endobj
750 0 obj
>
endobj
751 0 obj
>
endobj
752 0 obj
>
endobj
753 0 obj
>
endobj
754 0 obj
>
endobj
755 0 obj
>
endobj
756 0 obj
>
endobj
757 0 obj
>
endobj
758 0 obj
>
endobj
759 0 obj
>
endobj
760 0 obj
>
endobj
761 0 obj
>
endobj
762 0 obj
>
endobj
763 0 obj
>
endobj
764 0 obj
>
endobj
765 0 obj
>
endobj
766 0 obj
>
endobj
767 0 obj
>
endobj
768 0 obj
>
endobj
769 0 obj
>
endobj
770 0 obj
>
endobj
771 0 obj
>
endobj
772 0 obj
>
endobj
773 0 obj
>
endobj
774 0 obj
>
endobj
775 0 obj
>
endobj
776 0 obj
>
endobj
777 0 obj
>
endobj
778 0 obj
>
endobj
779 0 obj
>
endobj
780 0 obj
>
endobj
781 0 obj
>
endobj
782 0 obj
>
endobj
783 0 obj
>
endobj
784 0 obj
>
endobj
785 0 obj
>
endobj
786 0 obj
>
endobj
787 0 obj
>
endobj
788 0 obj
>
endobj
789 0 obj
>
endobj
790 0 obj
>
endobj
791 0 obj
>
endobj
792 0 obj
>
endobj
793 0 obj
>
endobj
794 0 obj
>
endobj
795 0 obj
>
endobj
796 0 obj
>
endobj
797 0 obj
>
endobj
798 0 obj
>
endobj
799 0 obj
>
endobj
800 0 obj
>
endobj
801 0 obj
>
endobj
802 0 obj
>
endobj
803 0 obj
>
endobj
804 0 obj
>
endobj
805 0 obj
>
endobj
806 0 obj
>
endobj
807 0 obj
>
endobj
808 0 obj
>
endobj
809 0 obj
>
endobj
810 0 obj
>
endobj
811 0 obj
>
endobj
812 0 obj
>
endobj
813 0 obj
>
endobj
814 0 obj
>
endobj
815 0 obj
>
endobj
816 0 obj
>
endobj
817 0 obj
>
endobj
818 0 obj
>
endobj
819 0 obj
>
endobj
820 0 obj
>
endobj
821 0 obj
>
endobj
822 0 obj
>
endobj
823 0 obj
>
endobj
824 0 obj
>
endobj
825 0 obj
>
endobj
826 0 obj
>
endobj
827 0 obj
>
endobj
828 0 obj
>
endobj
829 0 obj
>
endobj
830 0 obj
>
endobj
831 0 obj
>
endobj
832 0 obj
>
endobj
833 0 obj
>
endobj
834 0 obj
>
endobj
835 0 obj
>
endobj
836 0 obj
>
endobj
837 0 obj
>
endobj
838 0 obj
>
endobj
839 0 obj
>
endobj
840 0 obj
>
endobj
841 0 obj
>
endobj
842 0 obj
>
endobj
843 0 obj
>
endobj
844 0 obj
>
endobj
845 0 obj
>
endobj
846 0 obj
>
endobj
847 0 obj
>
endobj
848 0 obj
>
endobj
849 0 obj
>
endobj
850 0 obj
>
endobj
851 0 obj
>
endobj
852 0 obj
>
endobj
853 0 obj
>
endobj
854 0 obj
>
endobj
855 0 obj
>
endobj
856 0 obj
>
endobj
857 0 obj
>
endobj
858 0 obj
>
endobj
859 0 obj
>
endobj
860 0 obj
>
endobj
861 0 obj
>
endobj
862 0 obj
>
endobj
863 0 obj
>
endobj
864 0 obj
>
endobj
865 0 obj
>
endobj
866 0 obj
>
endobj
867 0 obj
>
endobj
868 0 obj
>
endobj
869 0 obj
>
endobj
870 0 obj
>
endobj
871 0 obj
>
endobj
872 0 obj
>
endobj
873 0 obj
>
endobj
874 0 obj
>
endobj
875 0 obj
>
endobj
876 0 obj
>
endobj
877 0 obj
>
endobj
878 0 obj
>
endobj
879 0 obj
>
endobj
880 0 obj
>
endobj
881 0 obj
>
endobj
882 0 obj
>
endobj
883 0 obj
>
endobj
884 0 obj
>
endobj
885 0 obj
>
endobj
886 0 obj
>
endobj
887 0 obj
>
endobj
888 0 obj
>
endobj
889 0 obj
>
endobj
890 0 obj
>
endobj
891 0 obj
>
endobj
892 0 obj
>
endobj
893 0 obj
>
endobj
894 0 obj
>
endobj
895 0 obj
>
endobj
896 0 obj
>
endobj
897 0 obj
>
endobj
898 0 obj
>
endobj
899 0 obj
>
endobj
900 0 obj
>
endobj
901 0 obj
>
endobj
902 0 obj
>
endobj
903 0 obj
>
endobj
904 0 obj
>
endobj
905 0 obj
>
endobj
906 0 obj
>
endobj
907 0 obj
>
endobj
908 0 obj
>
endobj
909 0 obj
>
endobj
910 0 obj
>
endobj
911 0 obj
>
endobj
912 0 obj
>
endobj
913 0 obj
>
endobj
914 0 obj
>
endobj
915 0 obj
>
endobj
916 0 obj
>
endobj
917 0 obj
>
endobj
918 0 obj
>
endobj
919 0 obj
>
endobj
920 0 obj
>
endobj
921 0 obj
>
endobj
922 0 obj
>
endobj
923 0 obj
>
endobj
924 0 obj
>
endobj
925 0 obj
>
endobj
926 0 obj
>
endobj
927 0 obj
>
endobj
928 0 obj
>
endobj
929 0 obj
>
endobj
930 0 obj
>
endobj
931 0 obj
>
endobj
932 0 obj
>
endobj
933 0 obj
>
endobj
934 0 obj
>
endobj
935 0 obj
>
endobj
936 0 obj
>
endobj
937 0 obj
>
endobj
938 0 obj
>
endobj
939 0 obj
>
endobj
940 0 obj
>
endobj
941 0 obj
>
endobj
942 0 obj
>
endobj
943 0 obj
>
endobj
944 0 obj
>
endobj
945 0 obj
>
endobj
946 0 obj
>
endobj
947 0 obj
>
endobj
948 0 obj
>
endobj
949 0 obj
>
endobj
950 0 obj
>
endobj
951 0 obj
>
endobj
952 0 obj
>
endobj
953 0 obj
>
endobj
954 0 obj
>
endobj
955 0 obj
>
endobj
956 0 obj
>
endobj
957 0 obj
>
endobj
958 0 obj
>
endobj
959 0 obj
>
endobj
960 0 obj
>
endobj
961 0 obj
>
endobj
962 0 obj
>
endobj
963 0 obj
>
endobj
964 0 obj
>
endobj
965 0 obj
>
endobj
966 0 obj
>
endobj
967 0 obj
>
endobj
968 0 obj
>
endobj
969 0 obj
>
endobj
970 0 obj
>
endobj
971 0 obj
>
endobj
972 0 obj
>
endobj
973 0 obj
>
endobj
974 0 obj
>
endobj
975 0 obj
>
endobj
976 0 obj
>
endobj
977 0 obj
>
endobj
978 0 obj
>
endobj
979 0 obj
>
endobj
980 0 obj
>
endobj
981 0 obj
>
endobj
982 0 obj
>
endobj
983 0 obj
>
endobj
984 0 obj
>
endobj
985 0 obj
>
endobj
986 0 obj
>
endobj
987 0 obj
>
endobj
988 0 obj
>
endobj
989 0 obj
>
endobj
990 0 obj
>
endobj
991 0 obj
>
endobj
992 0 obj
>
endobj
993 0 obj
>
endobj
994 0 obj
>
endobj
995 0 obj
>
endobj
996 0 obj
>
endobj
997 0 obj
>
endobj
998 0 obj
>
endobj
999 0 obj
>
endobj
1000 0 obj
>
endobj
1001 0 obj
>
endobj
1002 0 obj
>
endobj
1003 0 obj
>
endobj
1004 0 obj
>
endobj
1005 0 obj
>
endobj
1006 0 obj
>
endobj
1007 0 obj
>
endobj
1008 0 obj
>
endobj
1009 0 obj
>
endobj
1010 0 obj
>
endobj
1011 0 obj
>
endobj
1012 0 obj
>
endobj
1013 0 obj
>
endobj
1014 0 obj
>
endobj
1015 0 obj
>
endobj
1016 0 obj
>
endobj
1017 0 obj
>
endobj
1018 0 obj
>
endobj
1019 0 obj
>
endobj
1020 0 obj
>
endobj
1021 0 obj
>
endobj
1022 0 obj
>
endobj
1023 0 obj
>
endobj
1024 0 obj
>
endobj
1025 0 obj
>
endobj
1026 0 obj
>
endobj
1027 0 obj
>
endobj
1028 0 obj
>
endobj
1029 0 obj
>
endobj
1030 0 obj
>
endobj
1031 0 obj
>
endobj
1032 0 obj
>
endobj
1033 0 obj
>
endobj
1034 0 obj
>
endobj
1035 0 obj
>
endobj
1036 0 obj
>
endobj
1037 0 obj
>
endobj
1038 0 obj
>
endobj
1039 0 obj
>
endobj
1040 0 obj
>
endobj
1041 0 obj
>
endobj
1042 0 obj
>
endobj
1043 0 obj
>
endobj
1044 0 obj
>
endobj
1045 0 obj
>
endobj
1046 0 obj
>
endobj
1047 0 obj
>
endobj
1048 0 obj
>
endobj
1049 0 obj
>
endobj
1050 0 obj
>
endobj
1051 0 obj
>
endobj
1052 0 obj
>
endobj
1053 0 obj
>
endobj
1054 0 obj
>
endobj
1055 0 obj
>
endobj
1056 0 obj
>
endobj
1057 0 obj
>
endobj
1058 0 obj
>
endobj
1059 0 obj
>
endobj
1060 0 obj
>
endobj
1061 0 obj
>
endobj
1062 0 obj
>
endobj
1063 0 obj
>
endobj
1064 0 obj
>
endobj
1065 0 obj
>
endobj
1066 0 obj
>
endobj
1067 0 obj
>
endobj
1068 0 obj
>
endobj
1069 0 obj
>
endobj
1070 0 obj
>
endobj
1071 0 obj
>
endobj
1072 0 obj
>
endobj
1073 0 obj
>
endobj
1074 0 obj
>
endobj
1075 0 obj
>
endobj
1076 0 obj
>
endobj
1077 0 obj
>
endobj
1078 0 obj
>
endobj
1079 0 obj
>
endobj
1080 0 obj
>
endobj
1081 0 obj
>
endobj
1082 0 obj
>
endobj
1083 0 obj
>
endobj
1084 0 obj
>
endobj
1085 0 obj
>
endobj
1086 0 obj
>
endobj
1087 0 obj
>
endobj
1088 0 obj
>
endobj
1089 0 obj
>
endobj
1090 0 obj
>
endobj
1091 0 obj
>
endobj
1092 0 obj
>
endobj
1093 0 obj
>
endobj
1094 0 obj
>
endobj
1095 0 obj
>
endobj
1096 0 obj
>
endobj
1097 0 obj
>
endobj
1098 0 obj
>
endobj
1099 0 obj
>
endobj
1100 0 obj
>
endobj
1101 0 obj
>
endobj
1102 0 obj
>
endobj
1103 0 obj
>
endobj
1104 0 obj
>
endobj
1105 0 obj
>
endobj
1106 0 obj
>
endobj
1107 0 obj
>
endobj
1108 0 obj
>
endobj
1109 0 obj
>
endobj
1110 0 obj
>
endobj
1111 0 obj
>
endobj
1112 0 obj
>
endobj
1113 0 obj
>
endobj
1114 0 obj
>
endobj
1115 0 obj
>
endobj
1116 0 obj
>
endobj
1117 0 obj
>
endobj
1118 0 obj
>
endobj
1119 0 obj
>
endobj
1120 0 obj
>
endobj
1121 0 obj
>
endobj
1122 0 obj
>
endobj
1123 0 obj
>
endobj
1124 0 obj
>
endobj
1125 0 obj
>
endobj
1126 0 obj
>
endobj
1127 0 obj
>
endobj
1128 0 obj
>
endobj
1129 0 obj
>
endobj
1130 0 obj
>
endobj
1131 0 obj
>
endobj
1132 0 obj
>
endobj
1133 0 obj
>
endobj
1134 0 obj
>
endobj
1135 0 obj
>
endobj
1136 0 obj
>
endobj
1137 0 obj
>
endobj
1138 0 obj
>
endobj
1139 0 obj
>
endobj
1140 0 obj
>
endobj
1141 0 obj
>
endobj
1142 0 obj
>
endobj
1143 0 obj
>
endobj
1144 0 obj
>
endobj
1145 0 obj
>
endobj
1146 0 obj
>
endobj
1147 0 obj
>
endobj
1148 0 obj
>
endobj
1149 0 obj
>
endobj
1150 0 obj
>
endobj
1151 0 obj
>
endobj
1152 0 obj
>
endobj
1153 0 obj
>
endobj
1154 0 obj
>
endobj
1155 0 obj
>
endobj
1156 0 obj
>
endobj
1157 0 obj
>
endobj
1158 0 obj
>
endobj
1159 0 obj
>
endobj
1160 0 obj
>
endobj
1161 0 obj
>
endobj
1162 0 obj
>
endobj
1163 0 obj
>
endobj
1164 0 obj
>
endobj
1165 0 obj
>
endobj
1166 0 obj
>
endobj
1167 0 obj
>
endobj
1168 0 obj
>
endobj
1169 0 obj
>
endobj
1170 0 obj
>
endobj
1171 0 obj
>
endobj
1172 0 obj
>
endobj
1173 0 obj
>
endobj
1174 0 obj
>
endobj
1175 0 obj
>
endobj
1176 0 obj
>
endobj
1177 0 obj
>
endobj
1178 0 obj
>
endobj
1179 0 obj
>
endobj
1180 0 obj
>
endobj
1181 0 obj
>
endobj
1182 0 obj
>
endobj
1183 0 obj
>
endobj
1184 0 obj
>
endobj
1185 0 obj
>
endobj
1186 0 obj
>
endobj
1187 0 obj
>
endobj
1188 0 obj
>
endobj
1189 0 obj
>
endobj
1190 0 obj
>
endobj
1191 0 obj
>
endobj
1192 0 obj
>
endobj
1193 0 obj
>
endobj
1194 0 obj
>
endobj
1195 0 obj
>
endobj
1196 0 obj
>
endobj
1197 0 obj
>
endobj
1198 0 obj
>
endobj
1199 0 obj
>
endobj
1200 0 obj
>
endobj
1201 0 obj
>
endobj
1202 0 obj
>
endobj
1203 0 obj
>
endobj
1204 0 obj
>
endobj
1205 0 obj
>
endobj
1206 0 obj
>
endobj
1207 0 obj
>
endobj
1208 0 obj
>
endobj
1209 0 obj
>
endobj
1210 0 obj
>
endobj
1211 0 obj
>
endobj
1212 0 obj
>
endobj
1213 0 obj
>
endobj
1214 0 obj
>
endobj
1215 0 obj
>
endobj
1216 0 obj
>
endobj
1217 0 obj
>
endobj
1218 0 obj
>
endobj
1219 0 obj
>
endobj
1220 0 obj
>
endobj
1221 0 obj
>
endobj
1222 0 obj
>
endobj
1223 0 obj
>
endobj
1224 0 obj
>
endobj
1225 0 obj
>
endobj
1226 0 obj
>
endobj
1227 0 obj
>
endobj
1228 0 obj
>
endobj
1229 0 obj
>
endobj
1230 0 obj
>
endobj
1231 0 obj
>
endobj
1232 0 obj
>
endobj
1233 0 obj
>
endobj
1234 0 obj
>
endobj
1235 0 obj
>
endobj
1236 0 obj
>
endobj
1237 0 obj
>
endobj
1238 0 obj
>
endobj
1239 0 obj
>
endobj
1240 0 obj
>
endobj
1241 0 obj
>
endobj
1242 0 obj
>
endobj
1243 0 obj
>
endobj
1244 0 obj
>
endobj
1245 0 obj
>
endobj
1246 0 obj
>
endobj
1247 0 obj
>
endobj
1248 0 obj
>
endobj
1249 0 obj
>
endobj
1250 0 obj
>
endobj
1251 0 obj
>
endobj
1252 0 obj
>
endobj
1253 0 obj
>
endobj
1254 0 obj
>
endobj
1255 0 obj
>
endobj
1256 0 obj
>
endobj
1257 0 obj
>
endobj
1258 0 obj
>
endobj
1259 0 obj
>
endobj
1260 0 obj
>
endobj
1261 0 obj
>
endobj
1262 0 obj
>
endobj
1263 0 obj
>
endobj
1264 0 obj
>
endobj
1265 0 obj
>
endobj
1266 0 obj
>
endobj
1267 0 obj
>
endobj
1268 0 obj
>
endobj
1269 0 obj
>
endobj
1270 0 obj
>
endobj
1271 0 obj
>
endobj
1272 0 obj
>
endobj
1273 0 obj
>
endobj
1274 0 obj
>
endobj
1275 0 obj
>
endobj
1276 0 obj
>
endobj
1277 0 obj
>
endobj
1278 0 obj
>
endobj
1279 0 obj
>
endobj
1280 0 obj
>
endobj
1281 0 obj
>
endobj
1282 0 obj
>
endobj
1283 0 obj
>
endobj
1284 0 obj
>
endobj
1285 0 obj
>
endobj
1286 0 obj
>
endobj
1287 0 obj
>
endobj
1288 0 obj
>
endobj
1289 0 obj
>
endobj
1290 0 obj
>
endobj
1291 0 obj
>
endobj
1292 0 obj
>
endobj
1293 0 obj
>
endobj
1294 0 obj
>
endobj
1295 0 obj
>
endobj
1296 0 obj
>
endobj
1297 0 obj
>
endobj
1298 0 obj
>
endobj
1299 0 obj
>
endobj
1300 0 obj
>
endobj
1301 0 obj
>
endobj
1302 0 obj
>
endobj
1303 0 obj
>
endobj
1304 0 obj
>
endobj
1305 0 obj
>
endobj
1306 0 obj
>
endobj
1307 0 obj
>
endobj
1308 0 obj
>
endobj
1309 0 obj
>
endobj
1310 0 obj
>
endobj
1311 0 obj
>
endobj
1312 0 obj
>
endobj
1313 0 obj
>
endobj
1314 0 obj
>
endobj
1315 0 obj
>
endobj
1316 0 obj
>
endobj
1317 0 obj
>
endobj
1318 0 obj
>
endobj
1319 0 obj
>
endobj
1320 0 obj
>
endobj
1321 0 obj
>
endobj
1322 0 obj
>
endobj
1323 0 obj
>
endobj
1324 0 obj
>
endobj
1325 0 obj
>
endobj
1326 0 obj
>
endobj
1327 0 obj
>
endobj
1328 0 obj
>
endobj
1329 0 obj
>
endobj
1330 0 obj
>
endobj
1331 0 obj
>
endobj
1332 0 obj
>
endobj
1333 0 obj
>
endobj
1334 0 obj
>
endobj
1335 0 obj
>
endobj
1336 0 obj
>
endobj
1337 0 obj
>
endobj
1338 0 obj
>
endobj
1339 0 obj
>
endobj
1340 0 obj
>
endobj
1341 0 obj
>
endobj
1342 0 obj
>
endobj
1343 0 obj
>
endobj
1344 0 obj
>
endobj
1345 0 obj
>
endobj
1346 0 obj
>
endobj
1347 0 obj
>
endobj
1348 0 obj
>
endobj
1349 0 obj
>
endobj
1350 0 obj
>
endobj
1351 0 obj
>
endobj
1352 0 obj
>
endobj
1353 0 obj
>
endobj
1354 0 obj
>
endobj
1355 0 obj
>
endobj
1356 0 obj
>
endobj
1357 0 obj
>
endobj
1358 0 obj
>
endobj
1359 0 obj
>
endobj
1360 0 obj
>
endobj
1361 0 obj
>
endobj
1362 0 obj
>
endobj
1363 0 obj
>
endobj
1364 0 obj
>
endobj
1365 0 obj
>
endobj
1366 0 obj
>
endobj
1367 0 obj
>
endobj
1368 0 obj
>
endobj
1369 0 obj
>
endobj
1370 0 obj
>
endobj
1371 0 obj
>
endobj
1372 0 obj
>
endobj
1373 0 obj
>
endobj
1374 0 obj
>
endobj
1375 0 obj
>
endobj
1376 0 obj
>
endobj
1377 0 obj
>
endobj
1378 0 obj
>
endobj
1379 0 obj
>
endobj
1380 0 obj
>
endobj
1381 0 obj
>
endobj
1382 0 obj
>
endobj
1383 0 obj
>
endobj
1384 0 obj
>
endobj
1385 0 obj
>
endobj
1386 0 obj
>
endobj
1387 0 obj
>
endobj
1388 0 obj
>
endobj
1389 0 obj
>
endobj
1390 0 obj
>
endobj
1391 0 obj
>
endobj
1392 0 obj
>
endobj
1393 0 obj
>
endobj
1394 0 obj
>
endobj
1395 0 obj
>
endobj
1396 0 obj
>
endobj
1397 0 obj
>
endobj
1398 0 obj
>
endobj
1399 0 obj
>
endobj
1400 0 obj
>
endobj
1401 0 obj
>
endobj
1402 0 obj
>
endobj
1403 0 obj
>
endobj
1404 0 obj
>
endobj
1405 0 obj
>
endobj
1406 0 obj
>
endobj
1407 0 obj
>
endobj
1408 0 obj
>
endobj
1409 0 obj
>
endobj
1410 0 obj
>
endobj
1411 0 obj
>
endobj
1412 0 obj
>
endobj
1413 0 obj
>
endobj
1414 0 obj
>
endobj
1415 0 obj
>
endobj
1416 0 obj
>
endobj
1417 0 obj
>
endobj
1418 0 obj
>
endobj
1419 0 obj
>
endobj
1420 0 obj
>
endobj
1421 0 obj
>
endobj
1422 0 obj
>
endobj
1423 0 obj
>
endobj
1424 0 obj
>
endobj
1425 0 obj
>
endobj
1426 0 obj
>
endobj
1427 0 obj
>
endobj
1428 0 obj
>
endobj
1429 0 obj
>
endobj
1430 0 obj
>
endobj
1431 0 obj
>
endobj
1432 0 obj
>
endobj
1433 0 obj
>
endobj
1434 0 obj
>
endobj
1435 0 obj
>
endobj
1436 0 obj
>
endobj
1437 0 obj
>
endobj
1438 0 obj
>
endobj
1439 0 obj
>
endobj
1440 0 obj
>
endobj
1441 0 obj
>
endobj
1442 0 obj
>
endobj
1443 0 obj
>
endobj
1444 0 obj
>
endobj
1445 0 obj
>
endobj
1446 0 obj
>
endobj
1447 0 obj
>
endobj
1448 0 obj
>
endobj
1449 0 obj
>
endobj
1450 0 obj
>
endobj
1451 0 obj
>
endobj
1452 0 obj
>
endobj
1453 0 obj
>
endobj
1454 0 obj
>
endobj
1455 0 obj
>
endobj
1456 0 obj
>
endobj
1457 0 obj
>
endobj
1458 0 obj
>
endobj
1459 0 obj
>
endobj
1460 0 obj
>
endobj
1461 0 obj
>
endobj
1462 0 obj
>
endobj
1463 0 obj
>
endobj
1464 0 obj
>
endobj
1465 0 obj
>
endobj
1466 0 obj
>
endobj
1467 0 obj
>
endobj
1468 0 obj
>
endobj
1469 0 obj
>
endobj
1470 0 obj
>
endobj
1471 0 obj
>
endobj
1472 0 obj
>
endobj
1473 0 obj
>
endobj
1474 0 obj
>
endobj
1475 0 obj
>
endobj
1476 0 obj
>
endobj
1477 0 obj
>
endobj
1478 0 obj
>
endobj
1479 0 obj
>
endobj
1480 0 obj
>
endobj
1481 0 obj
>
endobj
1482 0 obj
>
endobj
1483 0 obj
>
endobj
1484 0 obj
>
endobj
1485 0 obj
>
endobj
1486 0 obj
>
endobj
1487 0 obj
>
endobj
1488 0 obj
>
endobj
1489 0 obj
>
endobj
1490 0 obj
>
endobj
1491 0 obj
>
endobj
1492 0 obj
>
endobj
1493 0 obj
>
endobj
1494 0 obj
>
endobj
1495 0 obj
>
endobj
1496 0 obj
>
endobj
1497 0 obj
>
endobj
1498 0 obj
>
endobj
1499 0 obj
>
endobj
1500 0 obj
>
endobj
1501 0 obj
>
endobj
1502 0 obj
>
endobj
1503 0 obj
>
endobj
1504 0 obj
>
endobj
1505 0 obj
>
endobj
1506 0 obj
>
endobj
1507 0 obj
>
endobj
1508 0 obj
>
endobj
1509 0 obj
>
endobj
1510 0 obj
>
endobj
1511 0 obj
>
endobj
1512 0 obj
>
endobj
1513 0 obj
>
endobj
1514 0 obj
>
endobj
1515 0 obj
>
endobj
1516 0 obj
>
endobj
1517 0 obj
>
endobj
1518 0 obj
>
endobj
1519 0 obj
>
endobj
1520 0 obj
>
endobj
1521 0 obj
>
endobj
1522 0 obj
>
endobj
1523 0 obj
>
endobj
1524 0 obj
>
endobj
1525 0 obj
>
endobj
1526 0 obj
>
endobj
1527 0 obj
>
endobj
1528 0 obj
>
endobj
1529 0 obj
>
endobj
1530 0 obj
>
endobj
1531 0 obj
>
endobj
1532 0 obj
>
endobj
1533 0 obj
>
endobj
1534 0 obj
>
endobj
1535 0 obj
>
endobj
1536 0 obj
>
endobj
1537 0 obj
>
endobj
1538 0 obj
>
endobj
1539 0 obj
>
endobj
1540 0 obj
>
endobj
1541 0 obj
>
endobj
1542 0 obj
>
endobj
1543 0 obj
>
endobj
1544 0 obj
>
endobj
1545 0 obj
>
endobj
1546 0 obj
>
endobj
1547 0 obj
>
endobj
1548 0 obj
>
endobj
1549 0 obj
>
endobj
1550 0 obj
>
endobj
1551 0 obj
>
endobj
1552 0 obj
>
endobj
1553 0 obj
>
endobj
1554 0 obj
>
endobj
1555 0 obj
>
endobj
1556 0 obj
>
endobj
1557 0 obj
>
endobj
1558 0 obj
>
endobj
1559 0 obj
>
endobj
1560 0 obj
>
endobj
1561 0 obj
>
endobj
1562 0 obj
>
endobj
1563 0 obj
>
endobj
1564 0 obj
>
endobj
1565 0 obj
>
endobj
1566 0 obj
>
endobj
1567 0 obj
>
endobj
1568 0 obj
>
endobj
1569 0 obj
>
endobj
1570 0 obj
>
endobj
1571 0 obj
>
endobj
1572 0 obj
>
endobj
1573 0 obj
>
endobj
1574 0 obj
>
endobj
1575 0 obj
>
endobj
1576 0 obj
>
endobj
1577 0 obj
>
endobj
1578 0 obj
>
endobj
1579 0 obj
>
endobj
1580 0 obj
>
endobj
1581 0 obj
>
endobj
1582 0 obj
>
endobj
1583 0 obj
>
endobj
1584 0 obj
>
endobj
1585 0 obj
>
endobj
1586 0 obj
>
endobj
1587 0 obj
>
endobj
1588 0 obj
>
endobj
1589 0 obj
>
endobj
1590 0 obj
>
endobj
1591 0 obj
>
endobj
1592 0 obj
>
endobj
1593 0 obj
>
endobj
1594 0 obj
>
endobj
1595 0 obj
>
endobj
1596 0 obj
>
endobj
1597 0 obj
>
endobj
1598 0 obj
>
endobj
1599 0 obj
>
endobj
1600 0 obj
>
endobj
1601 0 obj
>
endobj
1602 0 obj
>
endobj
1603 0 obj
>
endobj
1604 0 obj
>
endobj
1605 0 obj
>
endobj
1606 0 obj
>
endobj
1607 0 obj
>
endobj
1608 0 obj
>
endobj
1609 0 obj
>
endobj
1610 0 obj
>
endobj
1611 0 obj
>
endobj
1612 0 obj
>
endobj
1613 0 obj
>
endobj
1614 0 obj
>
endobj
1615 0 obj
>
endobj
1616 0 obj
>
endobj
1617 0 obj
>
endobj
1618 0 obj
>
endobj
1619 0 obj
>
endobj
1620 0 obj
>
endobj
1621 0 obj
>
endobj
1622 0 obj
>
endobj
1623 0 obj
>
endobj
1624 0 obj
>
endobj
1625 0 obj
>
endobj
1626 0 obj
>
endobj
1627 0 obj
>
endobj
1628 0 obj
>
endobj
1629 0 obj
>
endobj
1630 0 obj
>
endobj
1631 0 obj
>
endobj
1632 0 obj
>
endobj
1633 0 obj
>
endobj
1634 0 obj
>
endobj
1635 0 obj
>
endobj
1636 0 obj
>
endobj
1637 0 obj
>
endobj
1638 0 obj
>
endobj
1639 0 obj
>
endobj
1640 0 obj
>
endobj
1641 0 obj
>
endobj
1642 0 obj
>
endobj
1643 0 obj
>
endobj
1644 0 obj
>
endobj
1645 0 obj
>
endobj
1646 0 obj
>
endobj
1647 0 obj
>
endobj
1648 0 obj
>
endobj
1649 0 obj
>
endobj
1650 0 obj
>
endobj
1651 0 obj
>
endobj
1652 0 obj
>
endobj
1653 0 obj
>
endobj
1654 0 obj
>
endobj
1655 0 obj
>
endobj
1656 0 obj
>
endobj
1657 0 obj
>
endobj
1658 0 obj
>
endobj
1659 0 obj
>
endobj
1660 0 obj
>
endobj
1661 0 obj
>
endobj
1662 0 obj
>
endobj
1663 0 obj
>
endobj
1664 0 obj
>
endobj
1665 0 obj
>
endobj
1666 0 obj
>
endobj
1667 0 obj
>
endobj
1668 0 obj
>
endobj
1669 0 obj
>
endobj
1670 0 obj
>
endobj
1671 0 obj
>
endobj
1672 0 obj
>
endobj
1673 0 obj
>
endobj
1674 0 obj
>
endobj
1675 0 obj
>
endobj
1676 0 obj
>
endobj
1677 0 obj
>
endobj
1678 0 obj
>
endobj
1679 0 obj
>
endobj
1680 0 obj
>
endobj
1681 0 obj
>
endobj
1682 0 obj
>
endobj
1683 0 obj
>
endobj
1684 0 obj
>
endobj
1685 0 obj
>
endobj
1686 0 obj
>
endobj
1687 0 obj
>
endobj
1688 0 obj
>
endobj
1689 0 obj
>
endobj
1690 0 obj
>
endobj
1691 0 obj
>
endobj
1692 0 obj
>
endobj
1693 0 obj
>
endobj
1694 0 obj
>
endobj
1695 0 obj
>
endobj
1696 0 obj
>
endobj
1697 0 obj
>
endobj
1698 0 obj
>
endobj
1699 0 obj
>
endobj
1700 0 obj
>
endobj
1701 0 obj
>
endobj
1702 0 obj
>
endobj
1703 0 obj
>
endobj
1704 0 obj
>
endobj
1705 0 obj
>
endobj
1706 0 obj
>
endobj
1707 0 obj
>
endobj
1708 0 obj
>
endobj
1709 0 obj
>
endobj
1710 0 obj
>
endobj
1711 0 obj
>
endobj
1712 0 obj
>
endobj
1713 0 obj
>
endobj
1714 0 obj
>
endobj
1715 0 obj
>
endobj
1716 0 obj
>
endobj
1717 0 obj
>
endobj
1718 0 obj
>
endobj
1719 0 obj
>
endobj
1720 0 obj
>
endobj
1721 0 obj
>
endobj
1722 0 obj
>
endobj
1723 0 obj
>
endobj
1724 0 obj
>
endobj
1725 0 obj
>
endobj
1726 0 obj
>
endobj
1727 0 obj
>
endobj
1728 0 obj
>
endobj
1729 0 obj
>
endobj
1730 0 obj
>
endobj
1731 0 obj
>
endobj
1732 0 obj
>
endobj
1733 0 obj
>
endobj
1734 0 obj
>
endobj
1735 0 obj
>
endobj
1736 0 obj
>
endobj
1737 0 obj
>
endobj
1738 0 obj
>
endobj
1739 0 obj
>
endobj
1740 0 obj
>
endobj
1741 0 obj
>
endobj
1742 0 obj
>
endobj
1743 0 obj
>
endobj
1744 0 obj
>
endobj
1745 0 obj
>
endobj
1746 0 obj
>
endobj
1747 0 obj
>
endobj
1748 0 obj
>
endobj
1749 0 obj
>
endobj
1750 0 obj
>
endobj
1751 0 obj
>
endobj
1752 0 obj
>
endobj
1753 0 obj
>
endobj
1754 0 obj
>
endobj
1755 0 obj
>
endobj
1756 0 obj
>
endobj
1757 0 obj
>
endobj
1758 0 obj
>
endobj
1759 0 obj
>
endobj
1760 0 obj
>
endobj
1761 0 obj
>
endobj
1762 0 obj
>
endobj
1763 0 obj
>
endobj
1764 0 obj
>
endobj
1765 0 obj
>
endobj
1766 0 obj
>
endobj
1767 0 obj
>
endobj
1768 0 obj
>
endobj
1769 0 obj
>
endobj
1770 0 obj
>
endobj
1771 0 obj
>
endobj
1772 0 obj
>
endobj
1773 0 obj
>
endobj
1774 0 obj
>
endobj
1775 0 obj
>
endobj
1776 0 obj
>
endobj
1777 0 obj
>
endobj
1778 0 obj
>
endobj
1779 0 obj
>
endobj
1780 0 obj
>
endobj
1781 0 obj
>
endobj
1782 0 obj
>
endobj
1783 0 obj
>
endobj
1784 0 obj
>
endobj
1785 0 obj
>
endobj
1786 0 obj
>
endobj
1787 0 obj
>
endobj
1788 0 obj
>
endobj
1789 0 obj
>
endobj
1790 0 obj
>
endobj
1791 0 obj
>
endobj
1792 0 obj
>
endobj
1793 0 obj
>
endobj
1794 0 obj
>
endobj
1795 0 obj
>
endobj
1796 0 obj
>
endobj
1797 0 obj
>
endobj
1798 0 obj
>
endobj
1799 0 obj
>
endobj
1800 0 obj
>
endobj
1801 0 obj
>
endobj
1802 0 obj
>
endobj
1803 0 obj
>
endobj
1804 0 obj
>
endobj
1805 0 obj
>
endobj
1806 0 obj
>
endobj
1807 0 obj
>
endobj
1808 0 obj
>
endobj
1809 0 obj
>
endobj
1810 0 obj
>
endobj
1811 0 obj
>
endobj
1812 0 obj
>
endobj
1813 0 obj
>
endobj
1814 0 obj
>
endobj
1815 0 obj
>
endobj
1816 0 obj
>
endobj
1817 0 obj
>
endobj
1818 0 obj
>
endobj
1819 0 obj
>
endobj
1820 0 obj
>
endobj
1821 0 obj
>
endobj
1822 0 obj
>
endobj
1823 0 obj
>
endobj
1824 0 obj
>
endobj
1825 0 obj
>
endobj
1826 0 obj
>
endobj
1827 0 obj
>
endobj
1828 0 obj
>
endobj
1829 0 obj
>
endobj
1830 0 obj
>
endobj
1831 0 obj
>
endobj
1832 0 obj
>
endobj
1833 0 obj
>
endobj
1834 0 obj
>
endobj
1835 0 obj
>
endobj
1836 0 obj
>
endobj
1837 0 obj
>
endobj
1838 0 obj
>
endobj
1839 0 obj
>
endobj
1840 0 obj
>
endobj
1841 0 obj
>
endobj
1842 0 obj
>
endobj
1843 0 obj
>
endobj
1844 0 obj
>
endobj
1845 0 obj
>
endobj
1846 0 obj
>
endobj
1847 0 obj
>
endobj
1848 0 obj
>
endobj
1849 0 obj
>
endobj
1850 0 obj
>
endobj
1851 0 obj
>
endobj
1852 0 obj
>
endobj
1853 0 obj
>
endobj
1854 0 obj
>
endobj
1855 0 obj
>
endobj
1856 0 obj
>
endobj
1857 0 obj
>
endobj
1858 0 obj
>
endobj
1859 0 obj
>
endobj
1860 0 obj
>
endobj
1861 0 obj
>
endobj
1862 0 obj
>
endobj
1863 0 obj
>
endobj
1864 0 obj
>
endobj
1865 0 obj
>
endobj
1866 0 obj
>
endobj
1867 0 obj
>
endobj
1868 0 obj
>
endobj
1869 0 obj
>
endobj
1870 0 obj
>
endobj
1871 0 obj
>
endobj
1872 0 obj
>
endobj
1873 0 obj
>
endobj
1874 0 obj
>
endobj
1875 0 obj
>
endobj
1876 0 obj
>
endobj
1877 0 obj
>
endobj
1878 0 obj
>
endobj
1879 0 obj
>
endobj
1880 0 obj
>
endobj
1881 0 obj
>
endobj
1882 0 obj
>
endobj
1883 0 obj
>
endobj
1884 0 obj
>
endobj
1885 0 obj
>
endobj
1886 0 obj
>
endobj
1887 0 obj
>
endobj
1888 0 obj
>
endobj
1889 0 obj
>
endobj
1890 0 obj
>
endobj
1891 0 obj
>
endobj
1892 0 obj
>
endobj
1893 0 obj
>
endobj
1894 0 obj
>
endobj
1895 0 obj
>
endobj
1896 0 obj
>
endobj
1897 0 obj
>
endobj
1898 0 obj
>
endobj
1899 0 obj
>
endobj
1900 0 obj
>
endobj
1901 0 obj
>
endobj
1902 0 obj
>
endobj
1903 0 obj
>
endobj
1904 0 obj
>
endobj
1905 0 obj
>
endobj
1906 0 obj
>
endobj
1907 0 obj
>
endobj
1908 0 obj
>
endobj
1909 0 obj
>
endobj
1910 0 obj
>
endobj
1911 0 obj
>
endobj
1912 0 obj
>
endobj
1913 0 obj
>
endobj
1914 0 obj
>
endobj
1915 0 obj
>
endobj
1916 0 obj
>
endobj
1917 0 obj
>
endobj
1918 0 obj
>
endobj
1919 0 obj
>
endobj
1920 0 obj
>
endobj
1921 0 obj
>
endobj
1922 0 obj
>
endobj
1923 0 obj
>
endobj
1924 0 obj
>
endobj
1925 0 obj
>
endobj
1926 0 obj
>
endobj
1927 0 obj
>
endobj
1928 0 obj
>
endobj
1929 0 obj
>
endobj
1930 0 obj
>
endobj
1931 0 obj
>
endobj
1932 0 obj
>
endobj
1933 0 obj
>
endobj
1934 0 obj
>
endobj
1935 0 obj
>
endobj
1936 0 obj
>
endobj
1937 0 obj
>
endobj
1938 0 obj
>
endobj
1939 0 obj
>
endobj
1940 0 obj
>
endobj
1941 0 obj
>
endobj
1942 0 obj
>
endobj
1943 0 obj
>
endobj
1944 0 obj
>
endobj
1945 0 obj
>
endobj
1946 0 obj
>
endobj
1947 0 obj
>
endobj
1948 0 obj
>
endobj
1949 0 obj
>
endobj
1950 0 obj
>
endobj
1951 0 obj
>
endobj
1952 0 obj
>
endobj
1953 0 obj
>
endobj
1954 0 obj
>
endobj
1955 0 obj
>
endobj
1956 0 obj
>
endobj
1957 0 obj
>
endobj
1958 0 obj
>
endobj
1959 0 obj
>
endobj
1960 0 obj
>
endobj
1961 0 obj
>
endobj
1962 0 obj
>
endobj
1963 0 obj
>
endobj
1964 0 obj
>
endobj
1965 0 obj
>
endobj
1966 0 obj
>
endobj
1967 0 obj
>
endobj
1968 0 obj
>
endobj
1969 0 obj
>
endobj
1970 0 obj
>
endobj
1971 0 obj
>
endobj
1972 0 obj
>
endobj
1973 0 obj
>
endobj
1974 0 obj
>
endobj
1975 0 obj
>
endobj
1976 0 obj
>
endobj
1977 0 obj
>
endobj
1978 0 obj
>
endobj
1979 0 obj
>
endobj
1980 0 obj
>
endobj
1981 0 obj
>
endobj
1982 0 obj
>
endobj
1983 0 obj
>
endobj
1984 0 obj
>
endobj
1985 0 obj
>
endobj
1986 0 obj
>
endobj
1987 0 obj
>
endobj
1988 0 obj
>
endobj
1989 0 obj
>
endobj
1990 0 obj
>
endobj
1991 0 obj
>
endobj
1992 0 obj
>
endobj
1993 0 obj
>
endobj
1994 0 obj
>
endobj
1995 0 obj
>
endobj
1996 0 obj
>
endobj
1997 0 obj
>
endobj
1998 0 obj
>
endobj
1999 0 obj
>
endobj
2000 0 obj
>
endobj
2001 0 obj
>
endobj
2002 0 obj
>
endobj
2003 0 obj
>
endobj
2004 0 obj
>
endobj
2005 0 obj
>
endobj
2006 0 obj
>
endobj
2007 0 obj
>
endobj
2008 0 obj
>
endobj
2009 0 obj
>
endobj
2010 0 obj
>
endobj
2011 0 obj
>
endobj
2012 0 obj
>
endobj
2013 0 obj
>
endobj
2014 0 obj
>
endobj
2015 0 obj
>
endobj
2016 0 obj
>
endobj
2017 0 obj
>
endobj
2018 0 obj
>
endobj
2019 0 obj
>
endobj
2020 0 obj
>
endobj
2021 0 obj
>
endobj
2022 0 obj
>
endobj
2023 0 obj
>
endobj
2024 0 obj
>
endobj
2025 0 obj
>
endobj
2026 0 obj
>
endobj
2027 0 obj
>
endobj
2028 0 obj
>
endobj
2029 0 obj
>
endobj
2030 0 obj
>
endobj
2031 0 obj
>
endobj
2032 0 obj
>
endobj
2033 0 obj
>
endobj
2034 0 obj
>
endobj
2035 0 obj
>
endobj
2036 0 obj
>
endobj
2037 0 obj
>
endobj
2038 0 obj
>
endobj
2039 0 obj
>
endobj
2040 0 obj
>
endobj
2041 0 obj
>
endobj
2042 0 obj
>
endobj
2043 0 obj
>
endobj
2044 0 obj
>
endobj
2045 0 obj
>
endobj
2046 0 obj
>
endobj
2047 0 obj
>
endobj
2048 0 obj
>
endobj
2049 0 obj
>
endobj
2050 0 obj
>
endobj
2051 0 obj
>
endobj
2052 0 obj
>
endobj
2053 0 obj
>
endobj
2054 0 obj
>
endobj
2055 0 obj
>
endobj
2056 0 obj
>
endobj
2057 0 obj
>
endobj
2058 0 obj
>
endobj
2059 0 obj
>
endobj
2060 0 obj
>
endobj
2061 0 obj
>
endobj
2062 0 obj
>
endobj
2063 0 obj
>
endobj
2064 0 obj
>
endobj
2065 0 obj
>
endobj
2066 0 obj
>
endobj
2067 0 obj
>
endobj
2068 0 obj
>
endobj
2069 0 obj
>
endobj
2070 0 obj
>
endobj
2071 0 obj
>
endobj
2072 0 obj
>
endobj
2073 0 obj
>
endobj
2074 0 obj
>
endobj
2075 0 obj
>
endobj
2076 0 obj
>
endobj
2077 0 obj
>
endobj
2078 0 obj
>
endobj
2079 0 obj
>
endobj
2080 0 obj
>
endobj
2081 0 obj
>
endobj
2082 0 obj
>
endobj
2083 0 obj
>
endobj
2084 0 obj
>
endobj
2085 0 obj
>
endobj
2086 0 obj
>
endobj
2087 0 obj
>
endobj
2088 0 obj
>
endobj
2089 0 obj
>
endobj
2090 0 obj
>
endobj
2091 0 obj
>
endobj
2092 0 obj
>
endobj
2093 0 obj
>
endobj
2094 0 obj
>
endobj
2095 0 obj
>
endobj
2096 0 obj
>
endobj
2097 0 obj
>
endobj
2098 0 obj
>
endobj
2099 0 obj
>
endobj
2100 0 obj
>
endobj
2101 0 obj
>
endobj
2102 0 obj
>
endobj
2103 0 obj
>
endobj
2104 0 obj
>
endobj
2105 0 obj
>
endobj
2106 0 obj
>
endobj
2107 0 obj
>
endobj
2108 0 obj
>
endobj
2109 0 obj
>
endobj
2110 0 obj
>
endobj
2111 0 obj
>
endobj
2112 0 obj
>
endobj
2113 0 obj
>
endobj
2114 0 obj
>
endobj
2115 0 obj
>
endobj
2116 0 obj
>
endobj
2117 0 obj
>
endobj
2118 0 obj
>
endobj
2119 0 obj
>
endobj
2120 0 obj
>
endobj
2121 0 obj
>
endobj
2122 0 obj
>
endobj
2123 0 obj
>
endobj
2124 0 obj
>
endobj
2125 0 obj
>
endobj
2126 0 obj
>
endobj
2127 0 obj
>
endobj
2128 0 obj
>
endobj
2129 0 obj
>
endobj
2130 0 obj
>
endobj
2131 0 obj
>
endobj
2132 0 obj
>
endobj
2133 0 obj
>
endobj
2134 0 obj
>
endobj
2135 0 obj
>
endobj
2136 0 obj
>
endobj
2137 0 obj
>
endobj
2138 0 obj
>
endobj
2139 0 obj
>
endobj
2140 0 obj
>
endobj
2141 0 obj
>
endobj
2142 0 obj
>
endobj
2143 0 obj
>
endobj
2144 0 obj
>
endobj
2145 0 obj
>
endobj
2146 0 obj
>
endobj
2147 0 obj
>
endobj
2148 0 obj
>
endobj
2149 0 obj
>
endobj
2150 0 obj
>
endobj
2151 0 obj
>
endobj
2152 0 obj
>
endobj
2153 0 obj
>
endobj
2154 0 obj
>
endobj
2155 0 obj
>
endobj
2156 0 obj
>
endobj
2157 0 obj
>
endobj
2158 0 obj
>
endobj
2159 0 obj
>
endobj
2160 0 obj
>
endobj
2161 0 obj
>
endobj
2162 0 obj
>
endobj
2163 0 obj
>
endobj
2164 0 obj
>
endobj
2165 0 obj
>
endobj
2166 0 obj
>
endobj
2167 0 obj
>
endobj
2168 0 obj
>
endobj
2169 0 obj
>
endobj
2170 0 obj
>
endobj
2171 0 obj
>
endobj
2172 0 obj
>
endobj
2173 0 obj
>
endobj
2174 0 obj
>
endobj
2175 0 obj
>
endobj
2176 0 obj
>
endobj
2177 0 obj
>
endobj
2178 0 obj
>
endobj
2179 0 obj
>
endobj
2180 0 obj
>
endobj
2181 0 obj
>
endobj
2182 0 obj
>
endobj
2183 0 obj
>
endobj
2184 0 obj
>
endobj
2185 0 obj
>
endobj
2186 0 obj
>
endobj
2187 0 obj
>
endobj
2188 0 obj
>
endobj
2189 0 obj
>
endobj
2190 0 obj
>
endobj
2191 0 obj
>
endobj
2192 0 obj
>
endobj
2193 0 obj
>
endobj
2194 0 obj
>
endobj
2195 0 obj
>
endobj
2196 0 obj
>
endobj
2197 0 obj
>
endobj
2198 0 obj
>
endobj
2199 0 obj
>
endobj
2200 0 obj
>
endobj
2201 0 obj
>
endobj
2202 0 obj
>
endobj
2203 0 obj
>
endobj
2204 0 obj
>
endobj
2205 0 obj
>
endobj
2206 0 obj
>
endobj
2207 0 obj
>
endobj
2208 0 obj
>
endobj
2209 0 obj
>
endobj
2210 0 obj
>
endobj
2211 0 obj
>
endobj
2212 0 obj
>
endobj
2213 0 obj
>
endobj
2214 0 obj
>
endobj
2215 0 obj
>
endobj
2216 0 obj
>
endobj
2217 0 obj
>
endobj
2218 0 obj
>
endobj
2219 0 obj
>
endobj
2220 0 obj
>
endobj
2221 0 obj
>
endobj
2222 0 obj
>
endobj
2223 0 obj
>
endobj
2224 0 obj
>
endobj
2225 0 obj
>
endobj
2226 0 obj
>
endobj
2227 0 obj
>
endobj
2228 0 obj
>
endobj
2229 0 obj
>
endobj
2230 0 obj
>
endobj
2231 0 obj
>
endobj
2232 0 obj
>
endobj
2233 0 obj
>
endobj
2234 0 obj
>
endobj
2235 0 obj
>
endobj
2236 0 obj
>
endobj
2237 0 obj
>
endobj
2238 0 obj
>
endobj
2239 0 obj
>
endobj
2240 0 obj
>
endobj
2241 0 obj
>
endobj
2242 0 obj
>
endobj
2243 0 obj
>
endobj
2244 0 obj
>
endobj
2245 0 obj
>
endobj
2246 0 obj
>
endobj
2247 0 obj
>
endobj
2248 0 obj
>
endobj
2249 0 obj
>
endobj
2250 0 obj
>
endobj
2251 0 obj
>
endobj
2252 0 obj
>
endobj
2253 0 obj
>
endobj
2254 0 obj
>
endobj
2255 0 obj
>
endobj
2256 0 obj
>
endobj
2257 0 obj
>
endobj
2258 0 obj
>
endobj
2259 0 obj
>
endobj
2260 0 obj
>
endobj
2261 0 obj
>
endobj
2262 0 obj
>
endobj
2263 0 obj
>
endobj
2264 0 obj
>
endobj
2265 0 obj
>
endobj
2266 0 obj
>
endobj
2267 0 obj
>
endobj
2268 0 obj
>
endobj
2269 0 obj
>
endobj
2270 0 obj
>
endobj
2271 0 obj
>
endobj
2272 0 obj
>
endobj
2273 0 obj
>
endobj
2274 0 obj
>
endobj
2275 0 obj
>
endobj
2276 0 obj
>
endobj
2277 0 obj
>
endobj
2278 0 obj
>
endobj
2279 0 obj
>
endobj
2280 0 obj
>
endobj
2281 0 obj
>
endobj
2282 0 obj
>
endobj
2283 0 obj
>
endobj
2284 0 obj
>
endobj
2285 0 obj
>
endobj
2286 0 obj
>
endobj
2287 0 obj
>
endobj
2288 0 obj
>
endobj
2289 0 obj
>
endobj
2290 0 obj
>
endobj
2291 0 obj
>
endobj
2292 0 obj
>
endobj
2293 0 obj
>
endobj
2294 0 obj
>
endobj
2295 0 obj
>
endobj
2296 0 obj
>
endobj
2297 0 obj
>
endobj
2298 0 obj
>
endobj
2299 0 obj
>
endobj
2300 0 obj
>
endobj
2301 0 obj
>
endobj
2302 0 obj
>
endobj
2303 0 obj
>
endobj
2304 0 obj
>
endobj
2305 0 obj
>
endobj
2306 0 obj
>
endobj
2307 0 obj
>
endobj
2308 0 obj
>
endobj
2309 0 obj
>
endobj
2310 0 obj
>
endobj
2311 0 obj
>
endobj
2312 0 obj
>
endobj
2313 0 obj
>
endobj
2314 0 obj
>
endobj
2315 0 obj
>
endobj
2316 0 obj
>
endobj
2317 0 obj
>
endobj
2318 0 obj
>
endobj
2319 0 obj
>
endobj
2320 0 obj
>
endobj
2321 0 obj
>
endobj
2322 0 obj
>
endobj
2323 0 obj
>
endobj
2324 0 obj
>
endobj
2325 0 obj
>
endobj
2326 0 obj
>
endobj
2327 0 obj
>
endobj
2328 0 obj
>
endobj
2329 0 obj
>
endobj
2330 0 obj
>
endobj
2331 0 obj
>
endobj
2332 0 obj
>
endobj
2333 0 obj
>
endobj
2334 0 obj
>
endobj
2335 0 obj
>
endobj
2336 0 obj
>
endobj
2337 0 obj
>
endobj
2338 0 obj
>
endobj
2339 0 obj
>
endobj
2340 0 obj
>
endobj
2341 0 obj
>
endobj
2342 0 obj
>
endobj
2343 0 obj
>
endobj
2344 0 obj
>
endobj
2345 0 obj
>
endobj
2346 0 obj
>
endobj
2347 0 obj
>
endobj
2348 0 obj
>
endobj
2349 0 obj
>
endobj
2350 0 obj
>
endobj
2351 0 obj
>
endobj
2352 0 obj
>
endobj
2353 0 obj
>
endobj
2354 0 obj
>
endobj
2355 0 obj
>
endobj
2356 0 obj
>
endobj
2357 0 obj
>
endobj
2358 0 obj
>
endobj
2359 0 obj
>
endobj
2360 0 obj
>
endobj
2361 0 obj
>
endobj
2362 0 obj
>
endobj
2363 0 obj
>
endobj
2364 0 obj
>
endobj
2365 0 obj
>
endobj
2366 0 obj
>
endobj
2367 0 obj
>
endobj
2368 0 obj
>
endobj
2369 0 obj
>
endobj
2370 0 obj
>
endobj
2371 0 obj
>
endobj
2372 0 obj
>
endobj
2373 0 obj
>
endobj
2374 0 obj
>
endobj
2375 0 obj
>
endobj
2376 0 obj
>
endobj
2377 0 obj
>
endobj
2378 0 obj
>
endobj
2379 0 obj
>
endobj
2380 0 obj
>
endobj
2381 0 obj
>
endobj
2382 0 obj
>
endobj
2383 0 obj
>
endobj
2384 0 obj
>
endobj
2385 0 obj
>
endobj
2386 0 obj
>
endobj
2387 0 obj
>
endobj
2388 0 obj
>
endobj
2389 0 obj
>
endobj
2390 0 obj
>
endobj
2391 0 obj
>
endobj
2392 0 obj
>
endobj
2393 0 obj
>
endobj
2394 0 obj
>
endobj
2395 0 obj
>
endobj
2396 0 obj
>
endobj
2397 0 obj
>
endobj
2398 0 obj
>
endobj
2399 0 obj
>
endobj
2400 0 obj
>
endobj
2401 0 obj
>
endobj
2402 0 obj
>
endobj
2403 0 obj
>
endobj
2404 0 obj
>
endobj
2405 0 obj
>
endobj
2406 0 obj
>
endobj
2407 0 obj
>
endobj
2408 0 obj
>
endobj
2409 0 obj
>
endobj
2410 0 obj
>
endobj
2411 0 obj
>
endobj
2412 0 obj
>
endobj
2413 0 obj
>
endobj
2414 0 obj
>
endobj
2415 0 obj
>
endobj
2416 0 obj
>
endobj
2417 0 obj
>
endobj
2418 0 obj
>
endobj
2419 0 obj
>
endobj
2420 0 obj
>
endobj
2421 0 obj
>
endobj
2422 0 obj
>
endobj
2423 0 obj
>
endobj
2424 0 obj
>
endobj
2425 0 obj
>
endobj
2426 0 obj
>
endobj
2427 0 obj
>
endobj
2428 0 obj
>
endobj
2429 0 obj
>
endobj
2430 0 obj
>
endobj
2431 0 obj
>
endobj
2432 0 obj
>
endobj
2433 0 obj
>
endobj
2434 0 obj
>
endobj
2435 0 obj
>
endobj
2436 0 obj
>
endobj
2437 0 obj
>
endobj
2438 0 obj
>
endobj
2439 0 obj
>
endobj
2440 0 obj
>
endobj
2441 0 obj
>
endobj
2442 0 obj
>
endobj
2443 0 obj
>
endobj
2444 0 obj
>
endobj
2445 0 obj
>
endobj
2446 0 obj
>
endobj
2447 0 obj
>
endobj
2448 0 obj
>
endobj
2449 0 obj
>
endobj
2450 0 obj
>
endobj
2451 0 obj
>
endobj
2452 0 obj
>
endobj
2453 0 obj
>
endobj
2454 0 obj
>
endobj
2455 0 obj
>
endobj
2456 0 obj
>
endobj
2457 0 obj
>
endobj
2458 0 obj
>
endobj
2459 0 obj
>
endobj
2460 0 obj
>
endobj
2461 0 obj
>
endobj
2462 0 obj
>
endobj
2463 0 obj
>
endobj
2464 0 obj
>
endobj
2465 0 obj
>
endobj
2466 0 obj
>
endobj
2467 0 obj
>
endobj
2468 0 obj
>
endobj
2469 0 obj
>
endobj
2470 0 obj
>
endobj
2471 0 obj
>
endobj
2472 0 obj
>
endobj
2473 0 obj
>
endobj
2474 0 obj
>
endobj
2475 0 obj
>
endobj
2476 0 obj
>
endobj
2477 0 obj
>
endobj
2478 0 obj
>
endobj
2479 0 obj
>
endobj
2480 0 obj
>
endobj
2481 0 obj
>
endobj
2482 0 obj
>
endobj
2483 0 obj
>
endobj
2484 0 obj
>
endobj
2485 0 obj
>
endobj
2486 0 obj
>
endobj
2487 0 obj
>
endobj
2488 0 obj
>
endobj
2489 0 obj
>
endobj
2490 0 obj
>
endobj
2491 0 obj
>
endobj
2492 0 obj
>
endobj
2493 0 obj
>
endobj
2494 0 obj
>
endobj
2495 0 obj
>
endobj
2496 0 obj
>
endobj
2497 0 obj
>
endobj
2498 0 obj
>
endobj
2499 0 obj
>
endobj
2500 0 obj
>
endobj
2501 0 obj
>
endobj
2502 0 obj
>
endobj
2503 0 obj
>
endobj
2504 0 obj
>
endobj
2505 0 obj
>
endobj
2506 0 obj
>
endobj
2507 0 obj
>
endobj
2508 0 obj
>
endobj
2509 0 obj
>
endobj
2510 0 obj
>
endobj
2511 0 obj
>
endobj
2512 0 obj
>
endobj
2513 0 obj
>
endobj
2514 0 obj
>
endobj
2515 0 obj
>
endobj
2516 0 obj
>
endobj
2517 0 obj
>
endobj
2518 0 obj
>
endobj
2519 0 obj
>
endobj
2520 0 obj
>
endobj
2521 0 obj
>
endobj
2522 0 obj
>
endobj
2523 0 obj
>
endobj
2524 0 obj
>
endobj
2525 0 obj
>
endobj
2526 0 obj
>
endobj
2527 0 obj
>
endobj
2528 0 obj
>
endobj
2529 0 obj
>
endobj
2530 0 obj
>
endobj
2531 0 obj
>
endobj
2532 0 obj
>
endobj
2533 0 obj
>
endobj
2534 0 obj
>
endobj
2535 0 obj
>
endobj
2536 0 obj
>
endobj
2537 0 obj
>
endobj
2538 0 obj
>
endobj
2539 0 obj
>
endobj
2540 0 obj
>
endobj
2541 0 obj
>
endobj
2542 0 obj
>
endobj
2543 0 obj
>
endobj
2544 0 obj
>
endobj
2545 0 obj
>
endobj
2546 0 obj
>
endobj
2547 0 obj
>
endobj
2548 0 obj
>
endobj
2549 0 obj
>
endobj
2550 0 obj
>
endobj
2551 0 obj
>
endobj
2552 0 obj
>
endobj
2553 0 obj
>
endobj
2554 0 obj
>
endobj
2555 0 obj
>
endobj
2556 0 obj
>
endobj
2557 0 obj
>
endobj
2558 0 obj
>
endobj
2559 0 obj
>
endobj
2560 0 obj
>
endobj
2561 0 obj
>
endobj
2562 0 obj
>
endobj
2563 0 obj
>
endobj
2564 0 obj
>
endobj
2565 0 obj
>
endobj
2566 0 obj
>
endobj
2567 0 obj
>
endobj
2568 0 obj
>
endobj
2569 0 obj
>
endobj
2570 0 obj
>
endobj
2571 0 obj
>
endobj
2572 0 obj
>
endobj
2573 0 obj
>
endobj
2574 0 obj
>
endobj
2575 0 obj
>
endobj
2576 0 obj
>
endobj
2577 0 obj
>
endobj
2578 0 obj
>
endobj
2579 0 obj
>
endobj
2580 0 obj
>
endobj
2581 0 obj
>
endobj
2582 0 obj
>
endobj
2583 0 obj
>
endobj
2584 0 obj
>
endobj
2585 0 obj
>
endobj
2586 0 obj
>
endobj
2587 0 obj
>
endobj
2588 0 obj
>
endobj
2589 0 obj
>
endobj
2590 0 obj
>
endobj
2591 0 obj
>
endobj
2592 0 obj
>
endobj
2593 0 obj
>
endobj
2594 0 obj
>
endobj
2595 0 obj
>
endobj
2596 0 obj
>
endobj
2597 0 obj
>
endobj
2598 0 obj
>
endobj
2599 0 obj
>
endobj
2600 0 obj
>
endobj
2601 0 obj
>
endobj
2602 0 obj
>
endobj
2603 0 obj
>
endobj
2604 0 obj
>
endobj
2605 0 obj
>
endobj
2606 0 obj
>
endobj
2607 0 obj
>
endobj
2608 0 obj
>
endobj
2609 0 obj
>
endobj
2610 0 obj
>
endobj
2611 0 obj
>
endobj
2612 0 obj
>
endobj
2613 0 obj
>
endobj
2614 0 obj
>
endobj
2615 0 obj
>
endobj
2616 0 obj
>
endobj
2617 0 obj
>
endobj
2618 0 obj
>
endobj
2619 0 obj
>
endobj
2620 0 obj
>
endobj
2621 0 obj
>
endobj
2622 0 obj
>
endobj
2623 0 obj
>
endobj
2624 0 obj
>
endobj
2625 0 obj
>
endobj
2626 0 obj
>
endobj
2627 0 obj
>
endobj
2628 0 obj
>
endobj
2629 0 obj
>
endobj
2630 0 obj
>
endobj
2631 0 obj
>
endobj
2632 0 obj
>
endobj
2633 0 obj
>
endobj
2634 0 obj
>
endobj
2635 0 obj
>
endobj
2636 0 obj
>
endobj
2637 0 obj
>
endobj
2638 0 obj
>
endobj
2639 0 obj
>
endobj
2640 0 obj
>
endobj
2641 0 obj
>
endobj
2642 0 obj
>
endobj
2643 0 obj
>
endobj
2644 0 obj
>
endobj
2645 0 obj
>
endobj
2646 0 obj
>
endobj
2647 0 obj
>
endobj
2648 0 obj
>
endobj
2649 0 obj
>
endobj
2650 0 obj
>
endobj
2651 0 obj
>
endobj
2652 0 obj
>
endobj
2653 0 obj
>
endobj
2654 0 obj
>
endobj
2655 0 obj
>
endobj
2656 0 obj
>
endobj
2657 0 obj
>
endobj
2658 0 obj
>
endobj
2659 0 obj
>
endobj
2660 0 obj
>
endobj
2661 0 obj
>
endobj
2662 0 obj
>
endobj
2663 0 obj
>
endobj
2664 0 obj
>
endobj
2665 0 obj
>
endobj
2666 0 obj
>
endobj
2667 0 obj
>
endobj
2668 0 obj
>
endobj
2669 0 obj
>
endobj
2670 0 obj
>
endobj
2671 0 obj
>
endobj
2672 0 obj
>
endobj
2673 0 obj
>
endobj
2674 0 obj
>
endobj
2675 0 obj
>
endobj
2676 0 obj
>
endobj
2677 0 obj
>
endobj
2678 0 obj
>
endobj
2679 0 obj
>
endobj
2680 0 obj
>
endobj
2681 0 obj
>
endobj
2682 0 obj
>
endobj
2683 0 obj
>
endobj
2684 0 obj
>
endobj
2685 0 obj
>
endobj
2686 0 obj
>
endobj
2687 0 obj
>
endobj
2688 0 obj
>
endobj
2689 0 obj
>
endobj
2690 0 obj
>
endobj
2691 0 obj
>
endobj
2692 0 obj
>
endobj
2693 0 obj
>
endobj
2694 0 obj
>
endobj
2695 0 obj
>
endobj
2696 0 obj
>
endobj
2697 0 obj
>
endobj
2698 0 obj
>
endobj
2699 0 obj
>
endobj
2700 0 obj
>
endobj
2701 0 obj
>
endobj
2702 0 obj
>
endobj
2703 0 obj
>
endobj
2704 0 obj
>
endobj
2705 0 obj
>
endobj
2706 0 obj
>
endobj
2707 0 obj
>
endobj
2708 0 obj
>
endobj
2709 0 obj
>
endobj
2710 0 obj
>
endobj
2711 0 obj
>
endobj
2712 0 obj
>
endobj
2713 0 obj
>
endobj
2714 0 obj
>
endobj
2715 0 obj
>
endobj
2716 0 obj
>
endobj
2717 0 obj
>
endobj
2718 0 obj
>
endobj
2719 0 obj
>
endobj
2720 0 obj
>
endobj
2721 0 obj
>
endobj
2722 0 obj
>
endobj
2723 0 obj
>
endobj
2724 0 obj
>
endobj
2725 0 obj
>
endobj
2726 0 obj
>
endobj
2727 0 obj
>
endobj
2728 0 obj
>
endobj
2729 0 obj
>
endobj
2730 0 obj
>
endobj
2731 0 obj
>
endobj
2732 0 obj
>
endobj
2733 0 obj
>
endobj
2734 0 obj
>
endobj
2735 0 obj
>
endobj
2736 0 obj
>
endobj
2737 0 obj
>
endobj
2738 0 obj
>
endobj
2739 0 obj
>
endobj
2740 0 obj
>
endobj
2741 0 obj
>
endobj
2742 0 obj
>
endobj
2743 0 obj
>
stream
HlWˮEܟ5ҙv_D@bbqJPD\${src3#r|W/=ZZKo~DX+#1wo//k^WޖgϞe~eq}]-J=fo|xߋ~e*h:^[m]}X{h\7ni^a1u9″B]Qm0:»N-u#tѯq+n
`vfǘܲKdwmcSǚ!k08lۺk@3,lΨn7?،tOX2?㖘 gɈB_A{wyIBFsWn;1[
Рекомендации по работе с веществами неизвестного происхождения
При обнаружении неизвестного вещества в заводской упаковке внимательно осмотрите тару на наличие трещин, проверьте целостность крышки, изучите этикетку.
Чаще всего при сохранности этикетки на ней указаны все опасные свойства данного вещества:
Токсичность: надпись «ЯД», череп и кости, желтая полоса.
Взрыво- Пожароопасность: Красная полоса, символ огня, надписи «ВЗРЫВООПАСНО», «ПОЖАРООПАСНО», «НЕ ТУШИТЬ ВОДОЙ».
Крупные надписи «КИСЛОТА», «ЩЕЛОЧЬ».
Если внутри стеклянного сосуда просматриваются крупные кристаллы по всему объему сосуда (не осадок) можно сделать вывод, что перед вами щелочной металл залитый масляным раствором (масло, бензин, керосин) для предотвращения взаимодействия с воздухом. Для данных металлов характерный следующие свойства:
— Бурно реагируют с водой с выделением тепла (брызги, воспламенение, искры).
— Окисляются (темнеют, покрываются «коркой») на воздухе.
— Очень едкие вызываю химические ожоги.
— Тушить, обезвреживать засыпая землей (лучше сухим песком).
К щелочным металлам относятся Натрий (Na), Калий (K), Кальций (Ca), Литий (Li), Барий (Ba). В скобках приведена латинская аббревиатура.
Если при открытии сосуда появляется характерный «белый дым», скорее всего в сосуде концентрированные кислоты (серная, соляная, азотная).
Основные свойства:
— Реагируют с водой с выделением тепла, возможно разбрызгивание воспламенение не происходит.
— Очень едкие, вызывают химические ожоги.
— Активно реагируют с металлами и оксидами металлов, вызывая коррозию (можно определить по выделению мельчайших пузырьков в местах соприкосновения с металлом или оксидами металлов). Данные пузырьки свидетельствую о выделении водорода (следует помнить, что водород взрывоопасен, поддерживает горение).
Аналогичные свойства у неконцентрированных кислот, но отсутствует испарение (нет «белого дыма»).
Химические формулы начинаются с водорода: Н2SO4 – серная кислота, HCl – соляная кислота, HNO3 – азотная кислота, h4PO4 – ортофосфорная кислота.
Щелочи, как и кислоты, представляют собой очень едкие химически опасные вещества:
— вызывают химические ожоги.
Менее опасны, чем кислоты, т.к. мало реагируют с металлами. Представляют собой соединения щелочных металлов
В химической формуле содержится группа ОН, например:
NaOH – гидрооксид натрия, KOH – гидрооксид калия, Ca(OH)2 – гидрооксид кальция, LiOH – гидрооксид лития.
Соли: в целом активность солей меньше, чем у кислот и щелочей. Но некоторые соли обладают особыми свойствами: токсичностью, взрывоопасностью (при ударе, при нагревании, при взаимодействии с водой).
Ввиду того, что номенклатура солей значительно больше, чем у кислот и щелочей (применимая на практике) охарактеризовать общие свойства солей не представляется возможным, поэтому при изъятии соли необходимо соблюдать осторожность.
Изъятие неизвестных веществ следует производить в средствах защиты:
— при изъятии твердых и порошкообразных химически опасных веществ в заводской упаковке — резиновые перчатки;
— при изъятии крупных партий жидких химически опасных веществ (крупные стеклянные бутыли по 20 литров, баллоны и т. д.) рекомендуется применять костюм Л-1, средства защиты глаз.
д.) рекомендуется применять костюм Л-1, средства защиты глаз.
При нарушении герметичности тары (вещество парит, распространяется пыль, порошок) – костюмы Л-1, средства индивидуальной защиты органов дыхания (при пылении респиратор, при испарении – ИДА).
!!! При подозрении на бактериологическое заражение. ОБЯЗАТЕЛЬНО: Средства индивидуальной защиты органов дыхания (противогаз, респиратор). Средства защиты кожи: Л-1, при распространении бактериологически опасных препаратов в атмосфере (капли жидкости, испарение) обязательно КИХ-4М.
Порядок изъятия химически опасных веществ:
1. Осмотреть неизвестное вещество и емкость для его хранения.
2. При наличии отличительных признаков, писанных выше, действовать согласно опасным свойствам вещества:
Кислоты не должны соприкасаться с водой, металлами, оксидами металлов. Переносить рекомендуется в заводской упаковке. При нарушении тары перелить в стеклянную тару (кроме плавиковой кислоты, она реагирует со стеклом), либо специальную пластиковую тару.
При нарушении тары перелить в стеклянную тару (кроме плавиковой кислоты, она реагирует со стеклом), либо специальную пластиковую тару.
Аналогично обращение со щелочами за исключением того, что для их переноски можно применять металлическую тару.
При изъятии щелочных металлов рекомендуется переносить их, засыпанными слоем сухого песка, желательно в герметичной таре.
При изъятии остальных опасных веществ рекомендуется переносить их в герметичной таре (загерметизировать ту упаковку, в которой они были обнаружены, например, при помощи целлофановой пленки).
3. Наиболее опасные вещества (при угрозе разрушения тары) рекомендуется перевозить в ящике с сухим песком.
Соляная кислота: влияние на экологию и здоровье человека. Справка
Получают соляную кислоту растворением в воде хлористого водорода, который синтезируют или непосредственно из водорода и хлора или получают действием серной кислоты на хлорид натрия.
Выпускаемая техническая соляная кислота имеет крепость не менее 31% HCl (синтетическая) и 27,5% HCl (из NaCI). Торговую кислоту называют концентрированной, если она содержит 24% и больше HCl, если содержание HCl меньше, то кислота называется разбавленной.
Соляную кислоту применяют для получения хлоридов различных металлов, органических полупродуктов и синтетических красителей, уксусной кислоты, активированного угля, различных клеев, гидролизного спирта, в гальванопластике. Ее применяют для травления металлов, для очистки различных сосудов, обсадных труб буровых скважин от карбонатов, окислов и др. осадков и загрязнений. В металлургии кислотой обрабатывают руды, в кожевенной промышленности – кожу перед дублением и крашением. Соляную кислоту применяют в текстильной, пищевой промышленности, в медицине и т. д.
Соляная кислота играет важную роль в процессах пищеварения, она является составной частью желудочного сока. Разведенную соляную кислоту назначают внутрь главным образом при заболеваниях, связанных с недостаточной кислотностью желудочного сока.
Транспортируют соляную кислоту в стеклянных бутылях или гуммированных (покрытых слоем резины) металлических сосудах, а также в полиэтиленовой посуде.
Соляная кислота очень опасна для здоровья человека. При попадании на кожу вызывает сильные ожоги. Особенно опасно попадание в глаза.
При попадании соляной кислоты на кожные покрытия ее необходимо немедленно смыть обильной струей воды.
Очень опасны туман и пары хлороводорода, образующиеся при взаимодействии с воздухом концентрированной кислоты. Они раздражают слизистые оболочки и дыхательные пути. Длительная работа в атмосфере HCl вызывает катары дыхательных путей, разрушение зубов, помутнение роговицы глаз, изъязвление слизистой оболочки носа, желудочно-кишечные расстройства.
Острое отравление сопровождается охриплостью голоса, удушьем, насморком, кашлем.
В случае утечки или разлива соляная кислота может нанести существенный ущерб окружающей среде. Во-первых, это приводит к выделению паров вещества в атмосферный воздух в количествах превышающих санитарно-гигиенические нормативы, что может повлечь отравление всего живого, а также появлению кислотных осадков, которые могут привести к изменению химических свойств почвы и воды.
Во-вторых, она может просочиться в грунтовые воды, в результате чего может произойти загрязнение внутренних вод.
Там, где вода в реках и озерах стала довольно кислой (рН менее 5) исчезает рыба. При нарушении трофических цепей сокращается число видов водных животных, водорослей и бактерий.
В городах кислотные осадки ускоряют процессы разрушения сооружений из мрамора и бетона, памятников и скульптур. При попадании на металлы соляная кислота вызывает их коррозию, а, реагируя с такими веществами, как хлорная известь, диоксид марганца, или перманганат калия, образует токсичный газообразный хлор.
В случае разлива соляную кислоту смывают с поверхностей большим количеством воды или щелочного раствора, который нейтрализует кислоту.
Материал подготовлен на основе информации открытых источников
6.2 Кислоты, их свойства и получение
6.2.
Кислоты, их свойства и получение
С точки зрения теории электролитической диссоциации кислота – химическое
соединение при диссоциации в воде которого в качестве катионов образуются
только ионы Н+. Представления о кислотах и основаниях, вытекающих из
теории электролитической диссоциации Аррениуса, применимы только для водных
растворов. Исследование процессов, протекающих в неводных средах, без участия
растворителя, потребовало существенных дополнений и привело появлению различных
теорий кислот и оснований.
Классификация и
номенклатура кислот
Различают бескислородные (H2S, HBr, HCl) и кислородсодержащие (H3PO4,
HNO3, HClO3) кислоты.
В свободном состоянии неустойчивы угольная (H2CO3) и
сернистая (H2SO3) кислоты. Различают также сильные (H2SO4,
HNO3, HCl, HBr, HI, HClO4 и др.) и слабые (H2S,
H2CO3, HCN, H2SO3, HClO и др.)
кислоты.
Число ионов водорода, образующихся при диссоциации формульной единицы
кислоты, определяет ее основность.
Названия кислородсодержащих кислот производятся от названия неметалла с
добавлением окончания -ная, -вая, если степень окисления неметалла является
максимальной. По мере понижения степени окисления суффиксы меняются следующим
образом: -оватая, -истая, -оватистая.
Примеры названий некоторых кислородсодержащих кислот приведены в табл.
Таблица Названия некоторых
кислородсодержащих кислот
| Формула кислоты | Название кислоты | Формула кислоты | Название кислоты |
| Хлорноватистая | |||
Названия бескислородных кислот состоят из названия
неметалла с добавлением соединительной гласной о и слова –водородная. Например:
HF – фтороводородная кислота,
HCl – хлороводородная кислота,
H2S – сероводородная кислота.
Получение
кислот
1. Большинство кислородсодержащих кислот получают при взаимодействии
кислотных оксидов с водой.
2. Для получения нерастворимых в воде кислот
используют косвенный метод (действием кислоты на соответствующую соль):
Na2SiO3 + H2SO4 → H2SiO3 ↑ + Na2SO4.
3. Некоторые бескислородные кислоты получают при непосредственном соединении
неметаллов с водородом:
или по реакции обмена между солью и кислотой:
NaCl + H2SO4(конц) → HCl + NaHSO4
Общие свойства кислот
Кислоты представляют собой жидкости (H2SO4, HNO3,
HCl и т.д.) или твердые вещества (H3PO4, H3BO3 и
др.).
Растворы сильных кислот могут разрушать ткани и кожу.
Растворы кислот изменяют цвет индикаторов, что используется для
их качественного обнаружения. В качестве индикаторов используют лакмус (в
нейтральной среде – фиолетовый, в кислой – красный, в щелочной – синий), метилоранж (в
нейтральной среде – оранжевый, в кислой – красный, в щелочной – желтый) и
другие.
Сила бескислородных кислот, например, в ряду HCl – HBr – HI, возрастает с
увеличением радиуса аниона, поскольку анион большего радиуса слабее удерживает
протон, облегчая тем самым диссоциацию кислоты. Таким образом, в главных
подгруппах периодической системы сверху вниз сила бескислородных кислот
возрастает с увеличением радиуса центрального атома.
Наоборот, в ряду HClO – HClO2 – HClO3 –
HClO4 с уменьшением радиуса катиона С1z+ и
увеличением его заряда сила кислородсодержащих возрастает.
Важнейшими химическими свойствами кислот являются:
взаимодействие с основными и амфотерными оксидами, основаниями и солями:
CaO + H2SO4 → CaSO4 + H2O,
ZnO + H2SO4 → ZnSO4 + H2O,
2 Fe(OН)3 + 3 H2SO4 → Fe2(SO4)3 + 6 H2O,
BaCl2 + H2SO4 → BaSO4 + 2HCl;
взаимодействие кислоты с
основанием – реакция нейтрализации;
взаимодействие с
металлами с образованием соли и выделением водорода:
Mg + 2 HCl → MgCl2 + H2,
Fe + H2SO4(разб) → FeSO4 + H2.
Водород из кислот не вытесняют металлы, стоящие в ряду стандартных
электродных потенциалов (в ряду напряжений) правее водорода. При взаимодействии
металлов с концентрированной серной кислотой и азотной кислотой водород как
правило не выделяется.
Свойства концентрированной серной кислоты
Концентрированная серная кислота в реакциях с металлами может
восстанавливаться до SO2, S или H2S. Состав продуктов
восстановления определяется активностью металла, концентрацией кислоты и
температурой реагирующей системы. При обычной температуре концентрированная H2SO4 не
реагирует с золотом и платиной, а некоторые металламы (Fe, Cr, Al) пассивируются в
концентрированной серной кислоте.
Малоактивные металлы (стоящие в ряду стандартных электродных потенциалов
правее водорода) восстанавливают концентрированную серную кислоту до SO2:
Cu + 2 H2SO4(конц) → CuSO4 + SO2 ↑+ 2 H2O.
Активные металлы (Ca, Mg, Zn и др.) восстанавливают концентрированную H2SO4 до
свободной серы или H2S:
3 Zn + 4 H2SO4(конц) → 3
ZnSO4 + S ↑ +
4H2O,
4 Ca + 5 H2SO4(конц) → 4 CaSO4 + H2S ↑ + 4H2O.
При взаимодействии
серной кислоты с неметаллами образуется SO2:
C + H2SO4(конц) → 2 SO2↑ + CO2↑ + 2H2O,
S + 2 H2SO4(конц) → 3 SO2↑ + 2H2O,
2 P + 5 H2SO4(конц) → 5 SO2 ↑ + 2 H3PO4 + 2H2O.
При взаимодействии концентрированной H2SO4 с
соединениями, содержащими катионы металлов, находящимися в низшей степени
окисления, происходит дальнейшее окисление этих металлов:
2 FeO + 4 H2SO4(конц) → Fe2(SO4)3 + SO2 ↑ + 4 H2O.
Свойства азотной кислоты
Азотная кислота окисляет большинство элементов до их высшей степени
окисления. Взаимодействие HNO3 различной концентрации с
металлами различной активности представлено в виде следующей схемы:
| Концентрированная | ||||
| С тяжелыми металлами | С щелочноземельными металлами, а также с Zn, Fe, Sn | Не действует на Fe, Cr, Al, Au, Pt | С щелочными и щелочноземельными металлами | С другими тяжелыми металлами |
Таким образом, при взаимодействии концентрированной HNO3 с
малоактивными металлами образуется NO2:
Ag + 2 HNO3(конц) → AgNO3 + NO2 ↑ + H2O.
При действии разбавленной HNO3 на малоактивные металлы
выделяется NO:
3 Cu + 8 HNO3(разб) → 3 Cu(NO3)2 + 2 NO ↑ + 4 H2O,
а в случае активных
металлов образуется NH4NO3:
4 Ca + 10 HNO3(разб) → 4 Ca(NO3)2 + NH4NO3 + 3 H2O.
При взаимодействии концентрированной азотной кислоты с неметаллами
образуется, как правило, NO:
3 C + 4 HNO3(разб) → 3 CO2 ↑ + 4 NO ↑ + 2H2O,
P + 5 HNO3(разб) + 2 H2O → 3H3PO4 + 5NO ↑.
При взаимодействии концентрированной HNO3 с соединениями,
содержащими катионы металлов, находящимися в низшей степени окисления,
происходит дальнейшее окисление этих металлов:
FeO + 4 HNO3(разб) → Fe(NO3)3 + NO2 ↑ + 2 H2O.
Следует отметить, что продуктами восстановления азотной кислоты с металлами
являются и азот, и даже водород, причем, как правило, образуется смесь веществ.
Чем активнее металл и чем меньше концентрация , тем глубже она
восстанавливается.
Fe*, Аl* с концентрированной азотной кислотой и холодной
концентрированной серной кислотой не реагируют, поэтому данные кислоты
можно перевозить в алюминиевых и стальных цистернах.
Например:
а) с азотной кислотой
10 HNO3(конц.) + 8Na = 8Na NO3 + N2O + 5H2O
4 H NO3(конц.) + Zn = Zn(NO3)2 + 2NO2 + 2H2O
4 H NO3(конц.) + Cu = Cu(NO3)2 + 2NO2 + 2H2O
8 HNO3(разб.) + 3Cu = 3Cu(NO3)2 + 2NO + 4H2O
36 H NO3(разб.) + 10Fe = 10Fe(NO3)3 + 3N2 + 18H2O
9 HNO3(разб.) + 8Na = 8Na NO3 + NH3 + 3H2O
б) с концентрированной
серной кислотой
Zn + 2H2SO4(конц.) = ZnSO4 + SO2 + 2H2O
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S +
4H2O
3Zn + 4H2SO4(конц.) = 3ZnSO4 + S + 4H2O
Сu + 2H2SO4(конц.) = Сu SO4 + SO2 + 2H2O
в) смесь, состоящая из
одной части концентрированной соляной кислоты и трёх частей концентрированной
азотной кислоты растворяет золото. Такая смесь называется
царской водкой.
Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
1.
Из приведённого перечня выберите кислоты, назовите их,
определите тип.
1) HNO2 2) Li2O 3) H2S 4) CuSO4 5) P2O5 6) Al(OH)3 7) HCl 8) H2SO4
1) Азотистая кислота – одноосновная,
кислородсодержащая
3) Сероводородная кислота – двухосновная,
бескислородная
7) Соляная кислота – одноосновная,
бескислородная
8) Серная кислота – двухосновная,
кислородсодержащая
________________________________________________________________
2.
С какими из перечисленных веществ может
реагировать а) HCl б) H2SO4(раствор)
1)Na2O 2)SO3 3)H2O 4) AgNO3 5)HNO3 6)Na2SO4 7)BaCl2 8)Mg 9)Cu 10) NaOH
HCl реагирует с веществами 1,4,8,10
H2SO4 реагирует с веществами 1,4,7,8,10
________________________________________________________________
3.
Имеются два сосуда,
содержащие 40 и 20 кг раствора кислоты различной концентрации. Если их слить
вместе, то получится раствор, содержащий 33% кислоты. Если же слить равные
массы этих растворов, то полученный раствор будет содержать 47% кислоты.
сколько килограммов кислоты содержится в первом растворе?
По известным данным составим пропорцию.
33% — х
кг х=60·33:100=19,8 (кг) — кислоты
содержится всего в двух растворах.
Возьмём по 20 кг каждого раствора, всего будет 40 кг и найдем
сколько там будет содержаться кислоты.
47% — х
кг х=47·40:100=18,8 (кг) — кислоты
содержится в растворах, если взять равные массы.
3). 19,8-18,8=1 (кг) — кислоты осталось в оставшихся двадцати
килограммах раствора. Это как раз первый раствор, содержание кислоты в котором
необходимо узнать.
Так как в двадцати килограммах содержится 1 кг кислоты, то в сорока
килограммах будет содержаться в два раза больше, то есть 2 кг кислоты.
________________________________________________________________
4.
Во что перейдёт сера? Допишите и уравняйте реакции:
(конц.)
(конц.)
(концентрированная азотная кислота очень сильный окислитель)
________________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО
РЕШЕНИЯ
1. С
какими из следующих металлов:
— реагирует разбавленная серная кислота?
Напишите уравнения реакций в молекулярном и ионном виде.
2. Напишите
уравнения реакций следующих превращений:
3.
Напишите молекулярные и ионные уравнения реакций
между:
а) хлороводородной кислотой и
гидроксидом магния;
б) азотной кислотой и гидроксидом калия;
в) азотной кислотой и гидроксидом цинка;
г) серной кислотой и гидроксидом меди (II).
4. С какими из
следующих веществ будет реагировать соляная кислота:
Напишите уравнения реакций в молекулярной и
ионной формах.
5. С какими из
следующих веществ будет реагировать сернистая кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
6. С какими из следующих веществ будет
реагировать соляная кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
7. С
какими из следующих веществ будет реагировать разбавленная серная кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
8. Сколько граммов
ортофосфорной кислоты получается при растворении 284 г Р2О5
в воде.
9. К 1 л 10%-ного
раствора Н2SO4 (p
= 1,066 г/ мл) добавили 50 г КОН. Какова среда полученного раствора: кислая,
щелочная, нейтральная.
10. На смесь меди и
оксида меди (II) массой 75 г подействовали избытком
концентрированной НNO3. При этом образовался газ объемом 28,88 л
(н.у.). Определите массовую долю оксида меди (II)
в исходной смеси.
1. | |
а) HCl, H3PO4, | б) H2SO4, H2SO3, HNO3 |
г) HNO2, HNO3, H2SO4 | |
2. | |
б) силикат калия | |
в) оксид кремния (IV) | г) сульфат меди (II) |
3. | |
а)ортофосфорную | |
4. | |
а) серная кислота и карбонат калия | б) нитрат серебра и ортофосфорная |
в) соляная кислота и железо | г) все ответы верны |
5. | |
в) ортофосфорная | |
6. | |
а) оксидом кальция | б) гидроксидом калия |
г) оксидом кремния (IV) | |
7. | |
б) все ответы верны | |
8. | |
9. | |
б) все ответы верны | |
10. | |
а) гидроксидом калия | б) нитратом натрия |
в) оксидом алюминия | г) оксидом углерода (IV) |
Есть металлы, которые реагируют с серной кислотой, но не с соляной (или наоборот)?
Хорошо, давайте наведем порядок.
Реакция кислоты с металлом обычно является окислительно-восстановительной реакцией. Окислителем являются протоны, образующиеся в процессе диссоциации кислоты (на секунду забудем об анионах). Свойство, определяющее, может ли металлический элемент окисляться протонами, является его стандартным восстановительным потенциалом. В общем, любой металл с отрицательным потенциалом восстановления будет реагировать с любой кислотой Бренстеда (той, которая производит протоны), независимо от того, является ли она слабой (например,g., уксусная) или сильная кислота (например, соляная). А если у металла есть положительный восстановительный потенциал, он не будет реагировать с кислотами. Следовательно, если не принимать во внимание другие факторы, нет примеров, показывающих, что разные кислоты по-разному реагируют с данным металлом, фактически все они должны вести себя одинаково.
Но что делает химию интересной, так это «другие факторы». Анионы, образующиеся в процессе диссоциации кислоты, также могут действовать как окислитель. Например, нитрат-ионы, образующиеся из азотной кислоты, окисляют медь, поэтому металл растворяется в азотной кислоте.Сульфат-ионы также являются окислителями, но намного слабее нитрат-ионов, поэтому медь не растворяется в разбавленной серной кислоте, но горячая и концентрированная серная кислота сделает свое дело. А соляная кислота в отсутствие некоторых других окислителей вообще не повредит медь. Еще один фактор, который следует учитывать, — это пассивация металла. Тонкий невидимый слой оксида или соли может защитить металл от воздействия кислоты. Алюминий, который является очень химически активным металлом, не растворяется в окисляющих кислотах (например,g., азотная), поскольку на его поверхности образуется защитный слой оксида алюминия. С другой стороны, неокисляющие кислоты легко справятся с этой задачей. Соли металлов, которые нерастворимы в воде, также могут создавать пассивирующий слой.
Что касается исходного вопроса, то есть несколько примеров для серной и соляной кислоты, где они будут вести себя по-разному из-за образования нерастворимых солей. Одним из примеров является таллий — он растворяется в серной кислоте, но не в соляной кислоте. Напротив, барий растворяется в соляной кислоте, но не в серной.
Соляная кислота — обзор
8.1.2.2 Коррозия в присутствии газообразных соединений хлора
Присутствие соляной кислоты или молекулярного хлора в газовой фазе значительно увеличивает скорость коррозии стали. Скорость, обнаруженная в установках для сжигания отходов, достигает 1000 нм / ч. Исследования [17] доказывают, что при отсутствии HCl образуется прочный прочный защитный слой. При концентрации 0,1% HCl на поверхности Fe 2 O 3 (гематит) образуются пузырьки, которые, тем не менее, не влияют на целостность защитной окалины.Однако концентрация HCl в дымовых газах 0,8% полностью нарушает целостность слоя гематита, а слой магнетита (Fe 3 O 4 ) становится неравномерным и пористым. Приблизительно 2% соляной кислоты в дымовых газах разрушают оба слоя. Когда рассматриваются окислительные условия, эти явления часто называют активным окислением, катализируемым присутствием хлора. Влияние летучих соединений хлора на высокотемпературную коррозию различных сплавов было предметом ряда исследований [6,11,12,14,19,23].Результаты исследований однозначно указывают на то, что летучие соединения хлора разрушают защитный оксидный слой и тем самым разрушают саму металлическую поверхность. Анализируемые механизмы основаны в основном на исследованиях HCl, Cl 2 и паров NaCl.
Газовая коррозия металлов может быть вызвана некоторыми соединениями, содержащими хлор, но чаще всего HCl и в меньшей степени Cl 2 . Первый преобладает в условиях котла, поскольку дымовой газ содержит водяной пар.Однако Cl 2 может образовываться в восстановительных условиях при термическом разложении HCl [6].
Если сталь подвергается воздействию окислительной атмосферы, образуются стабильные оксиды, слой которых постепенно уменьшает диффузию кислорода к металлической поверхности. Таким образом, окисление происходит по так называемому параболическому закону (постепенное уменьшение интенсивности во времени).
Тем не менее, хлор демонстрирует способность проникать через защитный слой оксидов. Он диффундирует через слой, проходит через щели или поры слоя окалины, пока не достигнет поверхности металла, и вступает с ней в реакцию с образованием хлоридов.На границе окалины и металла очень низкий кислородный потенциал. Это соответствует низкому парциальному давлению O 2 , поскольку кислород расходуется на образование оксидов. Такие условия способствуют термической стабильности хлоридов FeCl 2 и CrCl 2 (рис. 8.1). Летучая HCl и Cl 2 реагируют с металлами с образованием хлоридов в соответствии с реакцией (8.9). Кроме того, металлы могут напрямую реагировать с HCl в соответствии с реакцией (8.10). Хлориды металлов демонстрируют высокие парциальные давления своих паров на границе окалины и поверхности металла, поэтому их постоянная сублимация возможна по реакции (8.11)
(8,9) M (т) + Cl2 (г) → MCl2 (т)
(8,10) M (т) + 2HCl (г) → MCl2 (г) + h3 (г)
(8,11) MCl2 (s) → MCl2 (g)
, где M = Fe, Cr, Ni и (s), (g) обозначают твердую и газообразную фазы соответственно.
Образующиеся таким образом летучие хлориды металлов могут диффундировать от металлической поверхности к слою окалины. Концентрация кислорода, возрастающая по мере удаления от металлической поверхности, способствует снижению термодинамической стабильности хлоридов и их окислению в твердые оксиды.Тем не менее оксиды, выделяемые из газовых фаз, образуют очень рыхлый слой осаждения, который не защищает трубы от коррозии. В этом случае хлорная коррозия протекает по линейному правилу — линейное увеличение во времени.
(8,12) 3MCl2 (г) + 2O2 (г) → M3O4 (т) + 3Cl2 (г)
(8,13) 2MCl2 (г) + (3/2) O2 (г) → M2O3 (т) + 2Cl2 (g)
В результате реакций (8.12) и (8.13) хлор выделяется и диффундирует в дымовой газ или возвращается на металлическую поверхность и инициирует следующий цикл. Графическое изображение этого механизма показано на рис.8.2 [18]. Цикл постепенно перемещает материал с металлической поверхности в зону повышенной концентрации кислорода, а конечный расход хлоридов остается низким. Конечная реакция проходит в соответствии с:
Рисунок 8.2. Схема коррозии от летучих соединений хлора [18].
(8.14) 4M (s) + 3O2 (g) → 2M2O3 (s)
Было также обнаружено, что газообразные соединения хлора могут проникать по границам зерен стали, что называется межкристаллитной коррозией.
В восстановительной среде, где оксиды отсутствуют или нестабильны, хлориды металлов могут образовываться непосредственно на поверхности трубы в соответствии с формулой.(8.9). Скорость хлорной коррозии сильно (экспоненциально) зависит от температуры и теоретически [19] может возрасти примерно в 80 раз при повышении температуры с 300 до 450 ° C. В действительности такой сильной коррозии не наблюдается, поскольку хлоридная коррозия определяется не только кинетикой реакции, но и в большей степени диффузией газа через зазоры в отложениях и окалине. Поэтому свойства отложений могут иметь большее значение, чем градиенты температуры и парциального давления.Кроме того, скорость коррозии зависит от процесса испарения хлоридов металлов, который также является функцией температуры.
Вышеупомянутые процессы настолько сложны, что, несмотря на ряд исследований, нет единого подхода в их описании. Хлорная коррозия — это сложное взаимодействие реакций, которые регулируются кинетикой, диффузией и фазовым переходом, включая конденсацию, плавление, сублимацию и испарение. Согласно исх. Согласно [20] скорость коррозии определяется зависимостью между скоростью химической реакции и скоростью испарения образующихся хлоридов.При температуре дымовых газов ниже 500 ° C образуется защитный слой хлорида железа, скорость коррозии регулируется параболическим законом и со временем уменьшается. Для более высоких температур скорость коррозии сначала следует параболическому закону, а затем линейному правилу. Это происходит в результате повышения температуры, так как отложения хлоридов становятся более толстыми. Следовательно, достигается определенная толщина, при которой скорости осаждения и испарения находятся в равновесии, и осадок не растет. При температурах, превышающих 800 ° C, увеличения слоя хлоридов недостаточно, чтобы покрыть испарение, и скорость коррозии подчиняется линейному закону.
Усиление коррозии железа может быть вызвано образованием легкоплавкого хлорида железа FeCl 3 по реакции:
(8,15) FeCl2 + HCl + (1/4) O2 → FeCl3 + (1/2) h3O
В восстановительной атмосфере HCl может реагировать с CO и H 2 , поражая оксидный слой [9]:
(8.16) Fe2O3 + 2 HCl + CO → FeO + FeCl2 + h3O + CO2
(8.17) Fe3O4 + 2 HCl + CO → 2FeO + FeCl2 + h3O + CO2
Дополнительным источником разрушения, которое происходит при образовании твердых хлоридов, является механическое напряжение, связанное с увеличением объема FeCl 2 по сравнению с объемом железа.
HCl и Cl 2 из-за повреждения защитных слоев могут ускорить другие виды газовой коррозии, например коррозия, вызванная серой.
Типичная картина коррозии газообразными соединениями хлора выглядит следующим образом: темный многослойный осадок оксидов, слабо приставший к трубке. Его толщина составляет около 0,1-0,3 мм. При удалении открывается тонкий коричневатый слой, который непосредственно прилипает к поверхности трубки. В конкретном случае испарителя слой отложений обычно тонкий, однако он может быть толще, если коррозия такого рода происходит на трубках пароперегревателя.
На основании лабораторных исследований, представленных в работе. [21], можно сделать вывод, что быстрый рост оксидного слоя из-за воздействия хлора может также происходить, когда соединения хлора отсутствуют на металлической поверхности. Поэтому всегда следует учитывать воздействие хлора и хлоридов, если накипь на трубках отслоилась и отслоилась.
Реакции элементов 2 группы с кислотами
- Последнее обновление
- Сохранить как PDF
- Реакции с разбавленной соляной кислотой
- Реакции с разбавленной серной кислотой
- Бериллий и магний
- Кальций, стронций и барий
- Реакции с азотной кислотой
- Бериллий
- и атрибуция
Другие металлы группы 2
На этой странице обсуждаются реакции элементов 2-й группы (бериллий, магний, кальций, стронций и барий) с обычными кислотами.
Реакция с разбавленной соляной кислотой
Каждый металл реагирует с разбавленной соляной кислотой, образуя пузырьки газообразного водорода и бесцветный раствор хлорида металла:
\ [X + 2HCl \ стрелка вправо XCl_2 + H_2 \]
Эти реакции становятся более интенсивными в группе.
Реакция с разбавленной серной кислотой
Они более сложные из-за образования нерастворимых сульфатов.
Бериллий и магний
Эти металлы реагируют с разбавленной серной кислотой так же, как с разбавленной соляной кислотой; реакция между магнием и разбавленной серной кислотой знакома многим начинающим химикам.Образуется газообразный водород вместе с бесцветными растворами сульфата бериллия или магния. Например:
\ [Mg + H_2SO_4 \ стрелка вправо MgSO_4 + H_2 \]
Кальций, стронций и барий
Сульфат кальция малорастворим, а сульфаты стронция и бария практически нерастворимы. При воздействии серной кислоты на каждом из этих металлов образуется слой нерастворимого сульфата, полностью замедляя или останавливая реакцию. В случае кальция образуется некоторое количество водорода вместе с белым осадком сульфата кальция.
Реакции с азотной кислотой
Эти реакции более сложные. Когда металл реагирует с кислотой, металл обычно восстанавливает ионы водорода до газообразного водорода. При этом элементарный металл окисляется до катионов металлов.
Однако ионы нитрата легко восстанавливаются до окиси азота и двуокиси азота. Поэтому металлы, реагирующие с азотной кислотой, имеют тенденцию к образованию оксидов азота, а не газообразного водорода. Если кислота относительно разбавлена, в результате реакции образуется монооксид азота, хотя он немедленно вступает в реакцию с атмосферным кислородом с образованием диоксида азота.Если используется концентрированная азотная кислота, непосредственно образуется диоксид азота.
Бериллий
Различные источники расходятся во мнениях относительно того, реагирует ли бериллий с азотной кислотой. Бериллий образует прочный оксидный слой (похожий на слой алюминия), который замедляет реакцию до тех пор, пока он не будет удален.
В некоторых источниках говорится, что бериллий не реагирует с азотной кислотой. Однако легко доступны процедуры получения нитрата бериллия путем взаимодействия порошка бериллия с азотной кислотой.Один источник использует полуконцентрированную азотную кислоту, утверждая, что выделяющийся газ представляет собой монооксид азота. Это разумный вывод.
Реакционная способность бериллия, похоже, зависит от его источника и способа производства. Возможно, что небольшое количество примесей в металле может повлиять на его реакционную способность.
Прочие металлы 2 группы
Остальные металлы группы 2 производят газообразный водород из очень разбавленной азотной кислоты, но этот газ загрязнен оксидами азота.Также образуются бесцветные растворы нитратов металлов. Возьмем, к примеру, магний, если раствор очень разбавленный:
\ [Mg + 2HNO_3 \ rightarrow Mg (NO_3) _2 + H_2 \]
При умеренных концентрациях (даже с очень разбавленной кислотой в некоторой степени это происходит):
\ [3Mg + 8HNO_3 \ rightarrow 3Mg (NO_3) _2 + 2NO + 4H_2O \]
А с концентрированной кислотой:
\ [Mg + 4HNO_3 \ rightarrow Mg (NO_3) _2 + 2NO_2 + 2H_2O \]
Реакции элементов 2 группы с кислотами
Это посложнее.Когда большинство металлов вступают в реакцию с большинством кислот, то на самом деле они восстанавливают ионы водорода до газообразного водорода, добавляя электроны к ионам водорода. Металл, конечно, окисляется до положительных ионов металла, потому что он теряет электроны.
Но ионы нитрата также легко восстанавливаются до таких продуктов, как монооксид азота и диоксид азота.
Итак, металлы, реагируя с азотной кислотой, имеют тенденцию давать оксиды азота, а не водорода. Если кислота относительно разбавлена, вы, как правило, получаете монооксид азота, хотя он немедленно вступает в реакцию с кислородом воздуха с образованием коричневого диоксида азота.
Концентрированная азотная кислота дает диоксид азота.
Бериллий
Существует много разногласий между различными источниками относительно того, реагирует ли бериллий с азотной кислотой. Бериллий имеет прочный оксидный слой (похожий на более известный алюминий), который замедляет реакцию до тех пор, пока он не будет удален.
Некоторые источники говорят, что бериллий не реагирует с азотной кислотой. С другой стороны, легко найти практические детали получения нитрата бериллия путем взаимодействия порошка бериллия с азотной кислотой.Один источник использует полуконцентрированную азотную кислоту и сообщает, что выделяющийся газ представляет собой монооксид азота. Этого и следовало ожидать.
Похоже, что происходит то, что реагирует он или нет, зависит от источника бериллия (как он был произведен) — возможно, изменение небольших количеств примесей в металле, которые влияют на реакцию.
Это все настолько неопределенно, что трудно понять, как можно задать вопрос об этом на экзамене.
Прочие металлы 2 группы
Они будут производить водород из азотной кислоты, если кислота очень разбавлена, но даже в этом случае она будет загрязнена оксидами азота.Образуются бесцветные растворы нитратов металлов.
Возьмем для примера магний, если раствор очень разбавлен:
При умеренных концентрациях (и даже с очень разбавленной кислотой это в некоторой степени произойдет):
А с концентрированной кислотой:
Как соляная кислота реагирует с алюминием. Формулы и описание процесса
Алюминий — ковкий, легкий серебристо-белый металл.Это хороший электрический проводник. Он может реагировать как с кислотами, так и с основаниями. Объединение алюминия с кислотой приводит к типичной реакции однократного вытеснения с образованием соли алюминия и газообразного водорода. Это видно на простом примере — как соляная кислота реагирует с алюминием.
Со щелочами реакция протекает иначе: помимо выделения водорода в реакции образуется алюминат MeAlO₂ (где Me представляет собой катион металла из щелочи) и комплексное соединение с формулой Me [Al (OH) ₄] в решение.
Как алюминий реагирует с соляной кислотой
Алюминий реагирует с разбавленной соляной кислотой при комнатной температуре. Металл растворяется в соляной кислоте, давая хлорид алюминия и бесцветный газообразный водород. Эта реакция необратима, так как конечные продукты не вступают в реакцию друг с другом.
Реакция между металлическим алюминием и соляной кислотой известна как окислительно-восстановительная реакция. Алюминий действует как восстановитель, отдавая электроны:Al⁰ — 3e = Al³⁺
Катионы соляной кислоты захватывают эти электроны и восстанавливаются до молекулярного водорода:
2H⁺ + 2e = H₂
Полное уравнение ионной реакции:
2Al⁰ + 6H⁺ + 6Cl⁻ = 2Al³⁺ + 6Cl⁻ + 3H₂ ↑
Нетто-ионная форма:
2Al⁰ + 6H⁺ = 2Al³⁺ + 3H₂ ↑
В молекулярной форме реакция выглядит следующим образом:
2Al + 6HCl = 2AlCl₃ + 3H₂ ↑
Металлический алюминий — не единственное вещество, способное реагировать с соляной кислотой — этим свойством обладают многие соединения металлов.С солями происходит обменная реакция, когда ионы или реактивные группы обоих реагентов «меняются местами». Чтобы реакция с алюминием или его соединениями была необратимой, реагенты должны образовывать газ, осадок или плохо растворимое вещество. Необходимо точно рассчитать необходимое количество реагента.
Реакции гидроксидов и оксидов алюминия с соляной кислотой
Al (OH) ₃ представляет собой амфотерное основание, представляющее собой белый желеобразный осадок, плохо растворяющийся в воде.
Гидроксид алюминия вступает в реакцию нейтрализации соляной кислотой (для надежного протекания реакции гидроксид должен быть свежим осажденным):
Al (OH) ₃ + 3HCl = AlCl₃ + 3H₂O
Наблюдается растворение белого осадка гидроксида алюминия (хлорид алюминия AlCl₃ хорошо растворяется в воде). С оксидом алюминия реакция дает соль и воду в соответствии со следующим уравнением:
Al₂O₃ + 6HCl = 2AlCl₃ + 3H₂O
Реакции солей, гидридов и комплексов алюминия с соляной кислотой
Соляная кислота также реагирует со многими другими соединениями алюминия.
С карбидом алюминия
Al₄C₃ + 12HCl = 4AlCl₃ + 3CH₄ ↑
(карбид алюминия растворяется при обработке избытком соляной кислоты)
С ацетатом алюминия
(CH₃COO) ₃Al + 3HCl = AlCl₃ + 3CH₃COOH
С нитридом алюминия
AlN + 4HCl = AlCl₃ + NH₄Cl
(используется горячая концентрированная кислота; реакция идет медленно)
С сульфидом алюминия
Al₂S₃ + 6HCl = 2AlCl₃ + 3H₂S ↑
С фосфидом алюминия
AlP + 3HCl = AlCl₃ + PH₃ ↑
(Реакция предполагает обработку фосфида горячей концентрированной кислотой)
С фосфатом алюминия
AlPO₄ + 3HCl = AlCl₃ + H₃PO₄
С аланатом (тетрагидроалюминатом) лития
Li [AlH₄] + 4HCl = AlCl₃ + LiCl + 4H₂ ↑
(Реакция проводится при низкой температуре)
С алюминатом натрия
NaAlO₂ + 4HCl = NaCl + AlCl₃ + 2H₂O
С тетрагидроксоалюминатом натрия
Na [Al (OH) ₄] + 4HCl = AlCl₃ + NaCl + 4H₂O
Сульфаты и нитраты алюминия не реагируют с соляной кислотой, так как все соединения в смеси растворимы — не образуется осадка, не образуются малорастворимые вещества, не выделяется газ.
Щелкните здесь, чтобы узнать больше об алюминии и его свойствах.
Как смеси металлов реагируют с соляной кислотой
Если вы возьмете смесь нескольких металлов и обработаете их соляной кислотой, каждый металл будет реагировать отдельно. Например, если вы добавите HCl в смесь алюминиевой и железной стружки, реакция будет протекать следующим образом:
Fe + 2HCl = FeCl₂ + H₂ ↑
2Al + 6HCl = 2AlCl₃ + 3H₂ ↑
Поскольку разбавленная соляная кислота является слабым окислителем, железо восстанавливается только до степени окисления +2.
Продукты реакции алюминия с соляной кислотой и их применение
Почти все реакции соляной кислоты и алюминия (или его соединений) приводят к образованию хлорида алюминия (AlCl₃). Соль хорошо растворяется в органических растворителях (нитробензол, дихлорэтан, ацетон) и воде. В водных растворах можно наблюдать гидролиз AlCl₃, так как эта соль образована сильной кислотой HCl и слабым основанием Al (OH).
AlCl₃ используется в качестве катализатора в органическом синтезе. Например, его используют при изомеризации парафинов, инициировании реакций алкилирования, ацилировании и разложении масла на фракции. Гексагидрат хлорида алюминия AlCl₃ ・ 6H₂O используется для обработки древесины, очистки сточных вод и производства антиперспирантов.
Реакция алюминия с раствором соляной кислоты может использоваться как лабораторный метод получения водорода (но для этих целей чаще используется металлический цинк).
Ряд реакционной способности металлов — Реакции металлов — AQA — GCSE Chemistry (Single Science) Revision — AQA
Когда металлы вступают в реакцию с другими веществами, атомы металлов теряют электроны, образуя положительные ионы.
Ряд реактивности металлов представляет собой диаграмму, показывающую металлы в порядке уменьшения реакционной способности. В общем, чем более реакционноспособен металл:
- , чем интенсивнее его реакции
- , тем легче он теряет электроны в реакциях с образованием положительных ионов (катионов)
В таблице приведены некоторые реакции металлов в ряду реакционной способности .Для сравнения показаны водород и углерод.
Реакции металлов с водой
Когда металл реагирует с водой, образуются гидроксид металла и водород. Например, натрий быстро реагирует с холодной водой:
Натрий + вода → гидроксид натрия + водород
2Na (s) + 2H 2 O (л) → 2NaOH (водн.) + H 2 (г)
Как правило, чем более активен металл, тем быстрее протекает реакция.
- Вопрос
Опишите и объясните наблюдения, когда небольшой кусочек лития помещается на поверхность большой емкости с водой.В воду добавлено несколько капель универсального индикатора.
- Показать ответ
При реакции лития с водой образуется газообразный водород. Цвет универсального индикатора меняется с зеленого на пурпурный по мере образования щелочного раствора гидроксида лития.
Реакции металлов с разбавленными кислотами
Когда металл реагирует с разбавленной кислотой, образуются соль и водород. Например, магний быстро реагирует с разбавленной соляной кислотой:
Магний + соляная кислота → хлорид магния + водород
Mg (s) + 2HCl (водный) → MgCl 2 (водный) + H 2 (g)
Чем более активен металл, тем быстрее реакция.Металл ниже водорода в ряду реактивности не будет реагировать с разбавленными кислотами.
- Вопрос
Платина располагается ниже золота в ряду реактивности. Предскажите его реакцию с разбавленными кислотами и объясните свой ответ.
- Показать ответ
Платина не реагирует с разбавленными кислотами. Металлы ниже водорода в ряду реактивности не реагируют с разбавленными кислотами, а золото и платина находятся ниже водорода.
Водород всегда образуется, когда металл реагирует с водой или разбавленной кислотой.
Реакции металлов с кислотами с образованием солей | Эксперимент
Эксперимент сначала проводится в меньшем масштабе с использованием пробирок (урок 1 ниже), без попытки восстановить образовавшиеся соли. Это устанавливает, что образование водорода является характерным свойством реакции металлов и кислот. Затем это можно сделать в большем масштабе (урок 2 ниже), а образовавшиеся соли можно извлечь путем кристаллизации.
Урок 1 представляет собой серию экспериментов с пробирками, в которых каждая рабочая группа устанавливает общий признак того, что водород выделяется, когда металлы реагируют с кислотой — если металл вообще реагирует.Это должно занять около 40 минут, и большинство классов должно уметь выполнять эту версию. Каждой рабочей группе требуется небольшой набор металлов и кислот для тестирования.
Диапазон протестированных металлов и кислот может быть расширен на демонстрации учителю в заключительной части этого урока.
Урок 2, в котором образовавшаяся соль восстанавливается путем кристаллизации, занимает больше времени, и класс должен быть достаточно надежным в поведении и навыках манипулирования, чтобы справиться с опасностями, связанными с нагреванием кислотных растворов в мензурках на треногах.
Время, необходимое для реакции, зависит от размера частиц используемого металла. Использование мелких гранул помогает сократить затрачиваемое время.
Оборудование
Аппарат
Урок 1
- Защита глаз
- Пробирки, 100 мм x 16 мм или аналогичные, x8
- Штатив для пробирок
- Пробки или пробки для свободного размещения пробирок, 2 шт.
- Горелка Бунзена
- Шина
Урок 2
- Колба коническая, 100 см 3
- Стакан, 100 см 3
- Измерительный цилиндр, 100 см 3
- Стеклянный стержень для перемешивания
- Шпатель
- Фильтровальная воронка диаметром примерно 65 мм
- Фильтровальная бумага
- Горелка Бунзена
- Штатив
- Треугольник Пипекле или керамическая сетка (см. Примечание 1)
- Термостойкий мат
- Испарительная ванна, мин. 50 см 3 емкость
- Чаша для кристаллизации (см. Примечание 2)
Примечания к аппарату
- Керамическую сетку можно использовать вместо треугольников для пипетки для поддержки испарительной ванны, но в этом случае испарение займет больше времени.
- Стадии испарения и кристаллизации могут быть неполными за время, отведенное на Урок 2. В этом случае чашки для кристаллизации необходимо отложить, чтобы кристаллизация проходила медленно. Однако нельзя допускать полного высыхания посуды, так как это портит качество кристаллов. При периодических проверках должно быть возможно решить, когда слить излишки раствора из каждой чашки, чтобы студенты могли проверить на следующем уроке хорошие кристаллы.
Химия
Урок 1
- Разбавленная соляная кислота, 1 M, 25 см 3
- Разбавленная серная кислота, 0,5 M (РАЗДРАЖАЮЩИЙ), 25 см 3
- Мелкие гранулы, крупная опилка или кусочки фольги из этих металлов в небольших емкостях с этикетками: медь, железо, магний, цинк
Урок 2
- Маленькие гранулы цинка, примерно 5 г в маркированном контейнере
- Разбавленная серная кислота, 0.5 M (РАЗДРАЖАЮЩИЙ), 50 см 3
Примечания по технике безопасности, охране труда и технике
- Прочтите наше стандартное руководство по охране труда и технике безопасности.
- Всегда используйте защитные очки.
- Выбор металлов может варьироваться в зависимости от того, какие металлы доступны в виде мелких гранул (до 5 мм), крупных опилок или фольги. Важно то, что в каждой группе есть по крайней мере два металла, которые легко реагируют, а один — нет.
- Медь, Cu (s) — см. CLEAPSS Hazcard HC026.
- Железные опилки, Fe (s) — см. CLEAPSS Hazcard HC055a.
- Магниевая лента, мг (ов) — см. CLEAPSS Hazcard HC059a. Магниевые стружки ОЧЕНЬ ВОСПЛАМЕНЯЮТСЯ. Следует контролировать распределение кусочков магниевой ленты, чтобы учащиеся не брали несколько кусочков и не экспериментировали с их воспламенением.
- Гранулы цинка, Zn (s) — см. CLEAPSS Hazcard HC107. В то время как другие комбинации металла / кислоты реагируют таким же образом, восстановление соли путем кристаллизации (в Уроке 2) может быть не таким успешным, как при использовании цинка и серной кислоты.
- Разбавленная соляная кислота, HCl (водн.) — см. CLEAPSS Hazcard HC047a и CLEAPSS Recipe Book RB043.
- Разбавленная серная кислота, H 2 SO 4 (водный), (РАЗДРАЖАЮЩИЙ при используемой концентрации) — см. CLEAPSS Hazcard HC098a и книгу рецептов CLEAPSS RB098.
Процедура
Урок 1
- Поместите шесть пробирок в штатив для пробирок.
- Добавьте разбавленную соляную кислоту на глубину 2–3 см в первые три пробирки и на глубину 2–3 см разбавленной серной кислоты в остальные три пробирки.
- Добавьте по маленькому кусочку другого металла в каждую из пробирок с соляной кислотой. Запишите, какой металл вы добавляете в каждую трубку.
- Добавьте небольшой кусок того же металла в каждую из пробирок с серной кислотой. Запишите, какой металл вы добавляете в каждую трубку.
- Ваш учитель покажет вам, как проверять газ, образующийся в этих реакциях.
- Выберите один из металлов, который быстро реагирует с кислотами, и в чистой пробирке добавьте кусочек этого металла на глубину 2–3 см от одной из кислот.На этот раз неплотно вставьте пробку в верхнюю часть пробирки, чтобы выделяемый газ медленно выходил. Зажгите деревянную ленту, снимите пробку и сразу же поднесите пламя к горловине трубки. Если ничего не происходит, возможно, вам придется попробовать еще раз.
Урок 2
Показать в полноэкранном режиме
- Отмерьте 50 см 3 разбавленной серной кислоты с помощью мерного цилиндра и налейте ее в стакан. Осторожно нагрейте эту кислоту на слабом, не дымном пламени Бунзена.Выключите горелку Бунзена до того, как раствор закипит. Осторожно снимите стакан с кислотой со штатива в соответствии с инструкциями учителя и поставьте его на термостойкий коврик. Будьте очень осторожны, чтобы не ударить по штативу, когда стакан находится на нем.
- К этой горячей кислоте добавьте примерно половину предоставленных кусочков цинка. Избегайте вдыхания кислых паров, которые могут подняться из стакана в результате сильного пузырения.
- Если весь цинк вступает в реакцию, добавьте еще две части и перемешайте стеклянной палочкой.Добавьте еще цинка, пока не перестанут образовываться пузырьки. Кислота израсходована.
- Отфильтруйте теплый раствор в коническую колбу, чтобы удалить излишки цинка. Перелейте фильтрат в испарительную ванну.
- Поместите испарительную ванну на треугольник или марлю на штатив и осторожно прокипятите раствор на слабом пламени Бунзена. Будьте очень осторожны, чтобы не ударить по штативу, поддерживающему чашу. Когда объем уменьшится примерно наполовину, окуните в раствор стеклянную палочку и подержите ее, пока она не остынет.Если на стеклянном стержне образуются маленькие кристаллы, прекратите нагревание, в противном случае продолжайте до достижения этой точки. Не продолжайте нагревать сверх точки, когда кристаллы начинают появляться на верхнем крае раствора.
- Вылейте оставшийся горячий раствор в форму для кристаллизации в соответствии с инструкциями учителя. Промаркируйте блюдо и оставьте до следующего урока, чтобы оно кристаллизовалось. Затем кристаллы можно исследовать с помощью ручного объектива или микроскопа.
Учебные заметки
Используйте раздаточный материал для учащихся, доступный с этим ресурсом, и попросите учащихся ответить на каждый вопрос, наблюдая за реакцией.
Безопасность особенно важна для младших школьников. Помните о проблемах, связанных с нагреванием стаканов или испарением посуды на штативе, а также с снятием таких горячих контейнеров со штатива после нагрева. Студенты не должны сидеть на лабораторных стульях при выполнении этих операций.
Использование щипцов подходящего размера — хороший способ подъема горячих контейнеров, но в некоторых школах их может не быть. Если есть какие-либо сомнения в безопасности этого шага, учитель должен сначала поднять каждый стакан на термостойкий коврик, используя толстую ткань или надев подходящие термозащитные перчатки, прежде чем ученики добавят кусочки цинка.То же самое относится к перемещению испарительной ванны перед переливанием ее содержимого в кристаллизатор.
Процедура безопасного тестирования выделившегося газообразного водорода в реакциях пробирки должна быть продемонстрирована в подходящий момент в уроке 1. Неплотно вставленная пробка позволяет накопить достаточно газа в медленной реакции, чтобы провести успешный тест. Тем не менее многим студентам сложно пройти успешный «всплывающий» тест на водород, поэтому вам, возможно, также придется провести дополнительные демонстрации.
Эта пара экспериментов является важным этапом для младших школьников в понимании того, что такое кислота. Им нужно понимать, как делать обобщения на основе достаточного количества примеров, и видеть пределы этого обобщения в металлах, которые не реагируют. Возможно, на заключительных этапах урока 1 это обсуждение будет продолжено путем дополнительных демонстраций других металлов и кислот. В частности, разбавленная азотная кислота (<0,5 М) действительно производит водород с умеренно химически активными металлами, такими как магний и цинк, хотя реакции отличаются при более высоких концентрациях и с другими металлами.К концу урока учащиеся должны легко сделать вывод:
Металл + кислота → соль + водород
Этот эксперимент также является хорошей возможностью для студентов научиться составлять подходящие таблицы для записи экспериментальных наблюдений.
В уроке 2 выбор цинка и серной кислоты в качестве примера для получения кристаллов соли обусловлен необходимостью иметь соль, которая легко кристаллизируется. К сожалению, хлориды магния и цинка нелегко кристаллизовать, в то время как сульфат магния настолько растворим, что для достаточного испарения требуется больше времени.Соединения железа (II) могут страдать от окисления при испарении раствора, в результате чего получается продукт с видимыми загрязнениями.
Существует вероятность образования опасных паров, если классам разрешено чрезмерное испарение солевых растворов либо из-за испарения любого избытка серной кислоты, либо из-за разложения соли. Также существует опасность выплескивания горячего материала из контейнера. Если кристаллы начинают появляться, например, на верхнем крае раствора, горелку Бунзена следует немедленно выключить и дать раствору остыть.Обратитесь к разделу 13.2.6 лабораторного справочника CLEAPSS для обсуждения.
Если ученики старшего возраста проводят эти эксперименты, их можно попросить написать символьные уравнения:
Mg (тв) + 2HCl (водн.) → MgCl 2 (водн.) + H 2 (г)
и
Mg (тв) + H 2 SO 4 (водн.) → MgSO 4 (водн.) + H 2 (г)
Для реакций этих кислот с железом или цинком студенты просто заменяют Mg на Fe или Zn в этих уравнениях.
Вопросы для студентов
Загрузите эти вопросы в виде рабочего листа внизу этой статьи.
- Какие металлы реагируют с соляной кислотой? Как узнать, что происходит реакция? Нарисуйте в блокноте таблицу, чтобы записать все эти наблюдения.
- Какие металлы реагируют с серной кислотой? Как узнать, что происходит реакция? Расширьте таблицу наблюдений в записной книжке, включив их.


