Содержание
Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) (задание 12 КИМ ЕГЭ)
Автор — Афанасьева Маргарите Николаевна, заместитель директора по учебно-воспитательной работе, учитель химии и биологии МБОУ «Средняя общеобразовательная школа с углубленным изучением отдельных предметов № 7 имени А. С. Пушкина» города Курска
Цели:
- образовательные: на основе изученных в курсе органической химии 10 класса понятий изомерии, структурной формулы, классификации и номенклатуры органических соединений, закрепить знания обучающихся по изученным темам, отработать навыки решения тестовых заданий различных типов;
- воспитательные: продолжить формирование научной картины мира, умение находить решения в различных ситуациях, обосновывая собственную точку зрения;
- развивающие: развивать у обучающихся способность анализировать, систематизировать, делать выводы по теме.
Тип урока: комбинированный
Оборудование: ноутбук, проектор, раздаточный материал кейса.
Ход урока
1. Оргмомент
2. Вступительное слово учителя
Древний Египет. Самые почитаемые люди – жрецы. В Древнем Египте их искусству обучали только самых подготовленных, прошедших процедуру серьезных испытаний: огонь, вода, угроза смерти… и шанс еще раз тщательно подумать, с какой стороны будет закрыта дверь в храм. Преодолев эту суровую систему, Пифагор основал собственную школу, и испытания при поступлении в нее были очень серьезными.
Древний Вавилон. В школах, где готовились писцы, проводились серьезные испытания, так как профессиональный писец должен был очень много знать и уметь и даже играть на музыкальных инструментах.
Нередко, результаты, достигнутые при испытаниях, были предметом гордости того или иного народа, а иногда служили даже для извлечения доходов. Индийский царь Девсарам, чтобы испытать мудрость иранцев, прислал им шахматы. Девсарам думал, что иранцы не сумеют разгадать смысл этой игры, и потому, по условию, отошлют в Индию подать. Однако один из визирей понял правила игры и, в свою очередь, изобрел игру, называемую сейчас нарды, которую он отослал в Индию, и там выяснилось, что разгадать правила игры в нарды индийцы не сумели.
Индийский царь Девсарам, чтобы испытать мудрость иранцев, прислал им шахматы. Девсарам думал, что иранцы не сумеют разгадать смысл этой игры, и потому, по условию, отошлют в Индию подать. Однако один из визирей понял правила игры и, в свою очередь, изобрел игру, называемую сейчас нарды, которую он отослал в Индию, и там выяснилось, что разгадать правила игры в нарды индийцы не сумели.
В 1884 году выходит первая книга с материалами тестирования, которая содержит задания и ответы к ним с оценкой по пятибалльной шкале. Книга была сборником заданий по математике, истории, грамматике, навигации, примерных текстов для сочинений.
А спустя 120 лет тестовые испытания пришли в Россию для всех выпускников сначала 11, а затем и 9-х классов.
Но прежде чем мы перейдем к теме занятия несколько вопросов:
- Поднимите руки те, кто из вас считает, что знания по химии пригодятся для продолжения обучения в ВУЗе?
- Поднимите руки те, кто из вас считает, что знания по химии пригодятся в дальнейшем в повседневной жизни?
- Поднимите руки те, кто считает, что знания по химии в дальнейшей жизни не пригодятся?
(Результаты опроса фиксируются, так как будут использованы в конце урока при подведении итогов).
Сегодня в рамках занятия элективного учебного предмета мы повторим вопросы классификации и номенклатуры органических веществ.
Итак, тема занятия: «Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)» (задание 12 КИМ ЕГЭ)
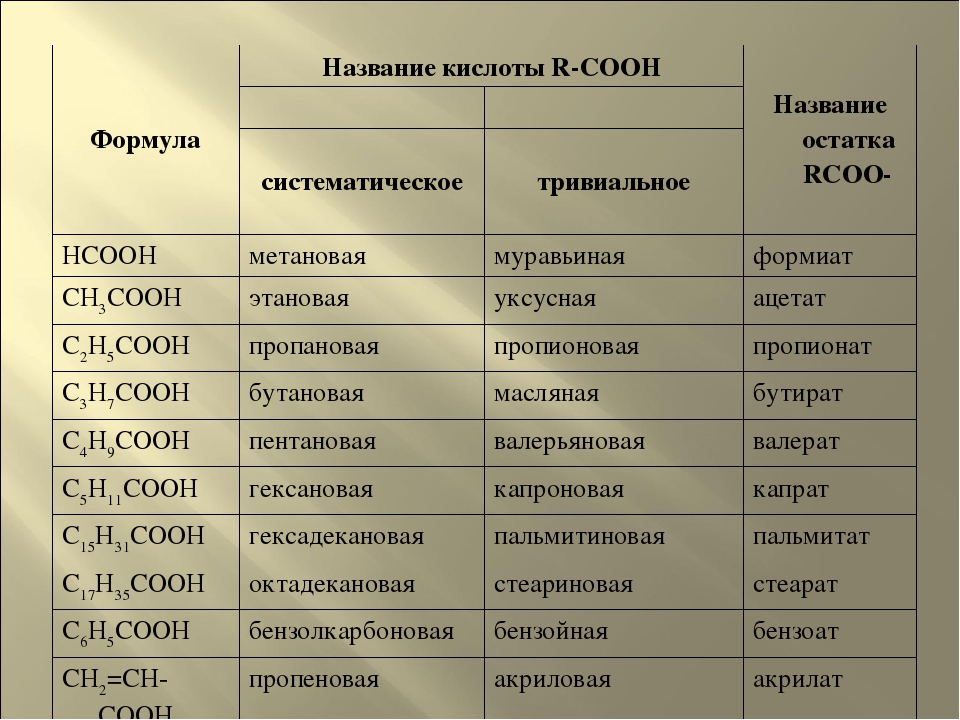
Система названий веществ – интереснейший предмет для исследования, так как на протяжении веков в истории химии появилось огромное количество названий, данных первооткрывателями веществам. Поэтому наряду с международной, тривиальные названия в органической химии используются и по сей день довольно часто.
Вот два примера:
|
| |
|
|
|
|
| |
Поэтому при подготовке к ЕГЭ вам необходимо знать два названия вещества: международной номенклатуры и тривиальные.
3. Устный опрос
А) Ацетилен — представитель класса ______________, имеет формулу _______;
Б) Дивинил – это ______________ (класс), потому что название по международной номенклатуре __________________;
В) Глицерин – это не аминокислота, а ________________ (класс), так как название вещества — _______________;
4. Переход к отработке навыков решения тестовых заданий
(Разбор задания 12 КИМ ЕГЭ совместно с учителем.)
12. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
5. Самостоятельная работа обучающихся с тестовыми заданиями (форма работы – решение кейса)
Кейс
Анна Ивановна – выпускница химического факультета Московского государственного университета. Однако в силу обстоятельств, она много лет не работала по специальности.
Подруга Анны Ивановны, с которой они вместе учились, работает в Центре тестирования. Она и предложила Анне Ивановне попробовать устроиться к ним на работу.
Для успешного прохождения собеседования Анне Ивановне было предложено составить одно из заданий КИМов по химии.
В ее распоряжении был необходимый информационный материал и через 15 минут Анна Ивановна с заданием справилась.
Однако на работу ее не приняли.
Что же не так было с тестом, составленным Анной Ивановной?
Задание:
- Проанализируйте тест, составленный Анной Ивановной.
- Найдите ошибки и исправьте их.
- Из имеющегося информационного материала предложите свой вариант вопроса № 12 КИМов ЕГЭ.
1. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.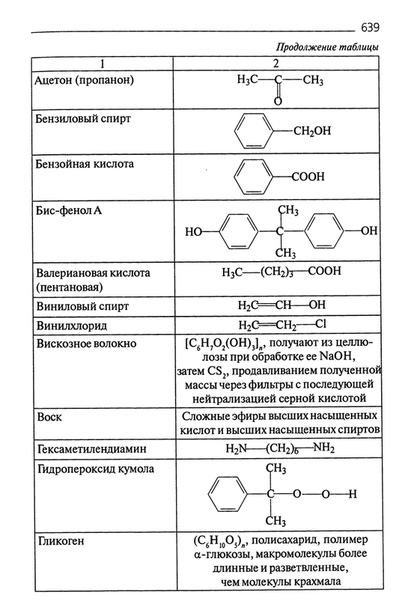
Ответ:
2. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
3. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
4. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.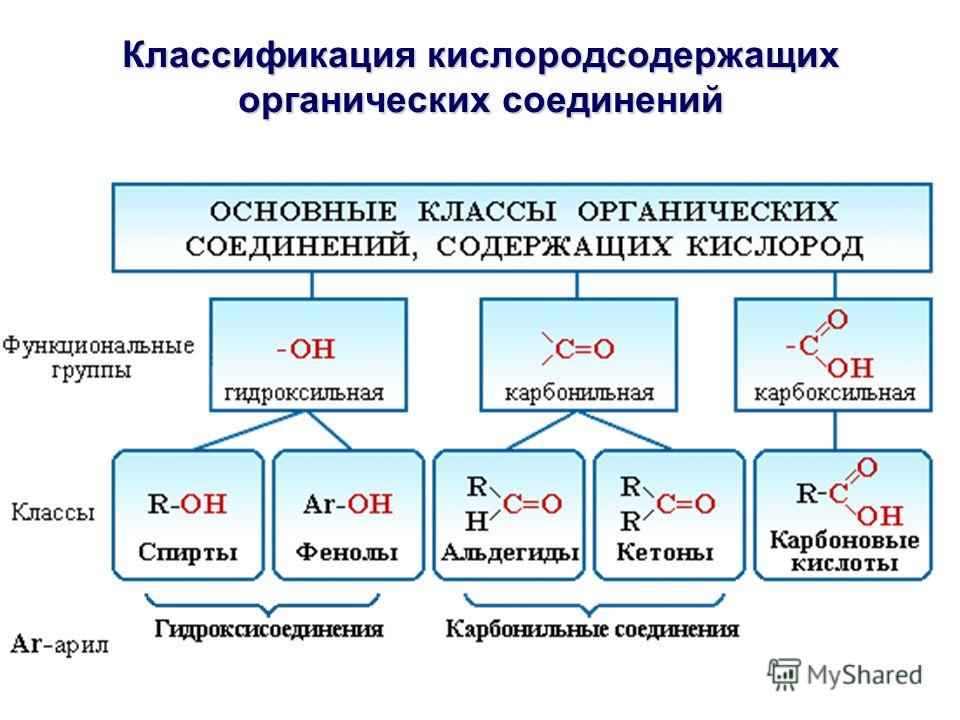
Ответ:
Вещества: Метилциклопропан; аланин; 3 – метилгептанол-1; 3 – метилгексин — 1; 3 – метилоктаналь; 2 – метилпентин — 2;3,3 – диметилгептадиен – 1,4; 2,2,5,5 — тетраметилоктан
Работа с тестом занимает у обучающихся от 15 до 20 минут. Затем подводятся итоги работы, тесты собираются учителем и проходит устное обсуждение.
Проверка кейса
1. (Задание составлено правильно)
Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.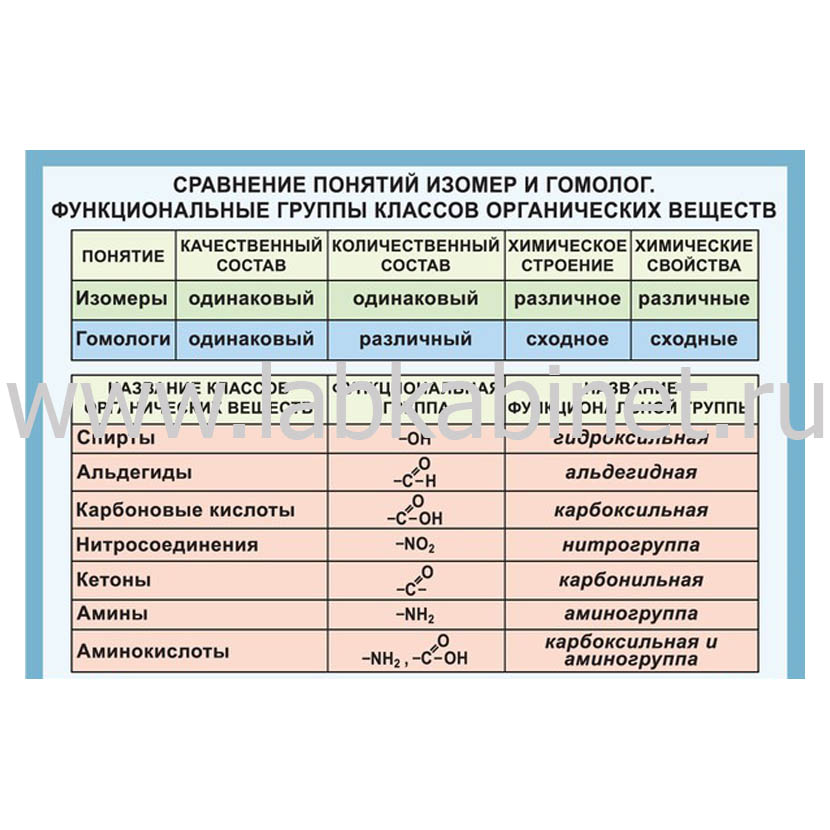
Ответ:
2. (Первая формула (А) составлена неправильно – возможное правильное вещество – 2,3 – диметил, 4 – этилоктен – 1). Кроме того, это — алкен (в ответах данного класса веществ – нет)
Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: (с учетом исправленных ошибок)
3. (Первая формула (А) составлена неправильно – возможное правильное вещество – 3 – метил, 4 – этилгептен – 1). Вторая формула (Б) неправильно – названа – правильное название – 3 – метилпентан). Это алкан. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
4. Установите соответствие между названием вещества и классом/группой, к которому (-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
|
|
|
|
|
|
|
Запишите в таблицу выбранные цифры под соответствующими буквами.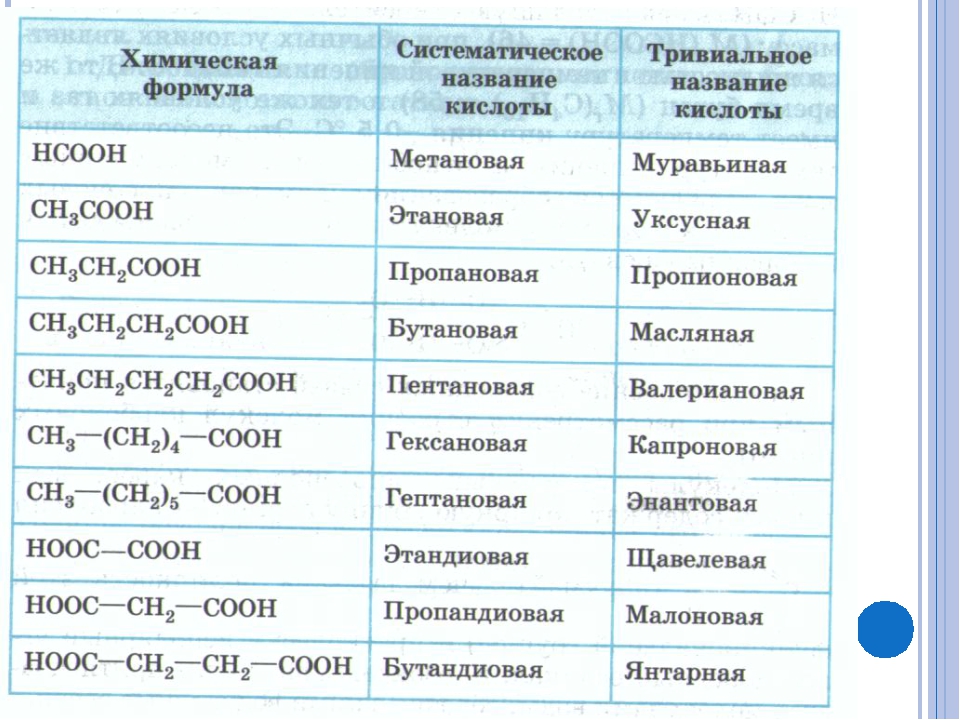
Ответ:
Вещества: Метилциклопропан; аланин; 3 – метилгептанол-1; 3 – метилгексин — 1; 3 – метилоктаналь; 2 – метилпентин — 2;3,3 – диметилгептадиен – 1,4; 2,2,5,5 — тетраметилоктан
6. Веселые картинки….
Размести в таблице картинки, вспомнив тривиальные названия кислот.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Картинки:
Проверка:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7.
 Рефлексия, подведение итогов занятия
Рефлексия, подведение итогов занятия
В начале урока мы провели опрос, который повторяем снова. (Детям предлагается ответить на вопросы начала урока о том, насколько им пригодятся знания по химии. Результаты двух опросов – в начале и в конце урока — сравниваются и анализируются учителем).
8. Подведение итогов урока
Рождаясь, человек получает по наследству от родителей способности к определенной деятельности, которые он развивает всю жизнь. Насколько хорошо у него это получается, показывают жизненные испытания, которые человек преодолевает в течение всей жизни. Одно из таких испытаний – Единый государственный экзамен. Надеюсь, что все у всех получится.
9. Домашнее задание
Составить 5 заданий вопроса 12 спецификации ЕГЭ 2017 года.
Химическая технология органических веществ, ГБПОУ «26 КАДР», Москва
Поступай в Колледж Дизайна, Архитектуры и Реинжиниринга №26 –
построй будущее своими руками!
Пройди обучение по специальности «Химическая технология органических веществ» в Колледже Дизайна, Архитектуры и Реинжиниринга №26, и ты узнаешь секреты соединения углерода с другими элементами, научишься создавать различные продукты органического синтеза посредством химических манипуляций. Присоединяйся к миру веществ, созданных природой и человеком — стань частью научного сообщества!
Присоединяйся к миру веществ, созданных природой и человеком — стань частью научного сообщества!
Отделение: «Ресурсосберегающие и химические технологии»
Основа обучения: бюджет, платно
Очная форма обучения: на базе 9 класса со сроком обучения 3 года 10 месяцев
Документ об образовании:
По окончании обучения выпускникам выдается диплом государственного образца с присвоением квалификации «Техник-технолог».
Дополнительно осваивается рабочая профессия Оператор технологических установок.
Как поступить?
Зачисление на бюджетное отделение Колледжа Архитектуры, Дизайна и Реинжиниринга №26 проходит на основе конкурса аттестатов. Не прошел отбор? Не беда. Ждем тебя на платном отделении!
Обратись к специалисту приемной комиссии — получи ответы на все вопросы!
Контакты приемной комиссии: Тел.: +7 (499) 653-70-77
Обучение проходит по адресу: м. Авиамоторная, шоссе Энтузиастов, д. 19, стр. 2
Авиамоторная, шоссе Энтузиастов, д. 19, стр. 2
Отправь заявку на обучение на сайте www.priem.26kadr.ru или заполни форму ниже.
Преимущества программы обучения:
- профессия входит в Топ-50 самых востребованных новых и перспективных профессий, требующих среднего профессионального образования (по версии Министерства труда и социальной защиты РФ)
- с целью повышения конкурентоспособности выпускников на рынке труда, к разработке учебных и методических материалов образовательных программ привлекаются специалисты ведущих компаний: ГНЦ РФ ГНИИХТЭОС, ЗАО НПО «Пим-Инвест» и ПАО «НК «Роснефть» — Московский завод »Нефтепродукт»
- возможность манипулирования дипломом на рынке труда в трех направлениях: работа в цеху на технологических установках производства органических веществ, в лабораториях технологического контроля качества продукции или проведения органического синтеза
- студенты принимают участие в лучших образовательных и научных мероприятиях отрасли, являются призерами Всероссийской Олимпиады профессионального мастерства, регионального чемпионата WSR в компетенции «Лабораторный химический анализ» и «Водные технологии»
- педагогический коллектив отделения входит в состав совета по профессиональным квалификациям химического и биотехнологического комплекса Национального совета при Президенте Российской Федерации по профессиональным квалификациям
О программе
Программа направленна на формирование теоретических и практических знаний в области разработки, проектирования, наладки, эксплуатации и совершенствования процессов переработки химического сырья, нефти, газа и промежуточных продуктов органического синтеза с целью производства мономеров и вспомогательных веществ для получения полимеров и полимерных материалов, топлив, масел специальных жидкостей, поверхностно-активных веществ и моющих средств, продуктов органического синтеза в рамках дисциплин и профессиональных модулей:
- Экологические основы природопользования
- Общая и неорганическая химия
- Инженерная графика
- Электротехника и электроника
- Органическая химия
- Аналитическая химия
- Физическая и коллоидная химия
- Теоретические основы химической технологии
- Процессы и аппараты
- Информационные технологии в профессиональной деятельности
- Основы автоматизации технологических процессов
- Основы технического обслуживания промышленного оборудования
- Управление технологическими процессами производства органических веществ
- Обеспечение качества продукции
- Управление персоналом структурного подразделения
В результате освоения программы ты научишься:
- Обслуживанию и эксплуатации технологического оборудования (подготовке оборудования к безопасному пуску, выводу на технологический режим и остановке, контролю работы основного и вспомогательного оборудования, технологических линий, коммуникаций и средств автоматизации)
- Ведению технологических процессов производства органических веществ (подготовке исходного сырья и материалов, поддержание заданных параметров технологического процесса с помощью контрольно-измерительных приборов и результатов аналитического контроля, расчету технико-экономических показателей технологического процесса)
- Контролю ресурсов и обеспечению качества продукции (контролировать и вести учет расхода сырья, материалов, энергоресурсов, полупродуктов, готовой продукции и отходов, контролировать качество сырья, полуфабрикатов (полупродуктов) и готовой продукции, выявлять и устранять причины технологического брака, принимать участие в разработке мероприятий по снижению расхода сырья, энергоресурсов и материалов).

- и многому другому!
Знакомься с техническим процессами, оборудованием и инструментарием, экспериментируй с веществами и проводи опыты в лабораториях и мастерских колледжа.
Лаборатории: неорганической и органической химии, процессов и аппаратов, аналитической химии, физической и коллоидной химии, технологии органических веществ и органического синтеза, автоматизации технологических процессов.
Практика
Уже во время обучения тебя ждет огромный объем практической работы под руководством мастеров своего дела в таких компаниях партнерах колледжа как ГНЦ РФ ГНИИХТЭОС, ЗАО НПО «Пим-Инвест», ПАО «НК «Роснефть» — Московский завод »Нефтепродукт», Институт химической физики им. Н.Н. Семенова Российской академии наук, Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
Посещай вместе с нами лучшие образовательные и научные мероприятия отрасли, прояви себя в научно-практической конференции «Будущее нефтехимии в профессионализме молодых» и профильных олимпиадах.
Профессиональные перспективы
Пройди обучение по специализации «Химическая технология органических веществ» в Колледже Архитектуры, Дизайна и Реинжиниринга № 26, и ты получишь качественное образование, содействие в трудоустройстве, профессию и соответствующую квалификацию уже в 18 лет. Приобретай опыт и становись незаменимым профессионалом на рынке труда. Твои знания будут широко востребованы в химических и нефтехимических отраслях.
Уровень подготовки наших выпускников позволяет решать любые проблемы, связанные с работой предприятий в нефтеперерабатывающей и химической отраслях. Наши партнеры — это крупнейшие компании Российской Федерации, предоставляющие высокооплачиваемую работу выпускникам нашего колледжа. Мы сотрудничаем c ОАО «Газпромнефть МНПЗ», ОАО «НК «Роснефть».
Также рекомендуем следующие специальности и профессии в колледже:
18.02.13 Технология производства полимерных композитов с присвоением квалификации техник-технолог
18. 01.02 Лаборант-эколог с присвоением квалификации «Лаборант химического анализа»
01.02 Лаборант-эколог с присвоением квалификации «Лаборант химического анализа»
Льготы и социальная ответственность
Социальный пакет для студентов колледжа:
-
Льготный проезд в городском пассажирском транспорте
-
Бесплатное посещение театров, зоопарка, музеев, выставочных залов, парков культуры и отдыха, находящихся в ведении Правительства Москвы
-
Бесплатное горячее питание (для студентов бюджетной основы обучения)
-
Бесплатные учебники
-
Бесплатное посещение кружков, спортивных секций и творческих объединений колледжа
-
Академическая стипендия
Социальный пакет для детей-сирот:
-
Полное государственное обеспечение в период обучения в колледже
-
Социальная стипендия, увеличенная на 50% от размера академической стипендии;
-
академическая стипендия;
-
ежегодное пособие на приобретение учебной литературы и письменных принадлежностей в размере трехмесячной академической стипендии;
-
бесплатное получение первого, второго начального профессионального образования и среднего специального образования в колледже
-
бесплатный проезд в городском пассажирском транспорте и железнодорожном пригородном транспорте;
-
единовременное денежное пособие;
-
выплата средств на выпуск при трудоустройстве;
-
выплата средств на выпуск при поступлении на дальнейшее обучение ;
-
текущее обеспечение питанием, одеждой, обувью, мягким инвентарем, предметами хозяйственного обихода, личной гигиены, медицинскими препаратами, средствами на культурно-массовую работу и личные нужды;
Социальный пакет для студентов из малообеспеченных семей:
-
Льготный проезд в городском пассажирском транспорте
-
Бесплатное посещение театров, зоопарка, музеев, выставочных залов, парков культуры и отдыха, находящихся в ведении Правительства Москвы
-
Бесплатное горячее питание
-
Бесплатные учебники
-
Бесплатное посещение кружков, спортивных секций и творческих объединений колледжа
-
Социальная стипендия, увеличенная на 50% от размера академической стипендии
-
Академическая стипендия
Социальный пакет для студентов, имеющих инвалидность:
-
Бесплатный проезд в городском пассажирском транспорте
-
Бесплатное посещение театров, зоопарка, музеев, выставочных залов, парков культуры и отдыха, находящихся в ведении Правительства Москвы
-
Бесплатное горячее питание
-
Бесплатные учебники
-
Бесплатное посещение кружков, спортивных секций и творческих объединений колледжа
-
Социальная стипендия, увеличенная на 50% от размера академической стипендии
-
Академическая стипендия
Сайт преподавателя биологии и химии Дмитрия Андреевича Соловкова
Обновлены задания 3, 6, 11, 27 и 28 по биологии — добавлены новые номера из ЕГЭ-2020.
Рубрика: Абитуриенту
Обновил задания 1, 2, 20 и 21 в первой части — добавил около 30 новых номеров.
Рубрика: Абитуриенту
За последний месяц обновлены все задания второй части экзамена (№№30-35) — добавлены задания образца 2020 года. Согласно проекту ЕГЭ-2021, изменений во второй части по химии не планируется.
Рубрика: Абитуриенту
Обновлено задание 33 — добавлено около 15 новых цепочек.
Рубрика: Без рубрики
|
В задания 34 добавлен новый раздел — задачи на атомистику и молярные соотношения. Также обновлены задачи по электролизу с учетом новых задач ЕГЭ-2020.
Рубрика: Абитуриенту
|
Обновлены задания 32 и 35 — добавлены задачи 2020 года
Рубрика: Абитуриенту
|
Обновлены задания 30 и 31 — добавлены номера образца 2020 года. Посмотреть их можно здесь.
Посмотреть их можно здесь.
Рубрика: Абитуриенту
Задания 19 и 20 первой части обновлены в соответствии со спецификатором ЕГЭ-2021 года. В задание 24 добавлено около 10 номеров.
Рубрика: Абитуриенту
Выложены последние 2 презентации по цитологии — репликация ДНК и биосинтез белка. Таким образом, полностью закончен целый раздел общей биологии. Всем рекомендую для подготовки к ЕГЭ.
Рубрика: Абитуриенту
|
Добавлены очередные презентации по цитологии: по диссимиляции и автотрофному питанию
Рубрика: Абитуриенту
Классификация органических веществ для ЕГЭ 2021 / Блог / Справочник :: Бингоскул
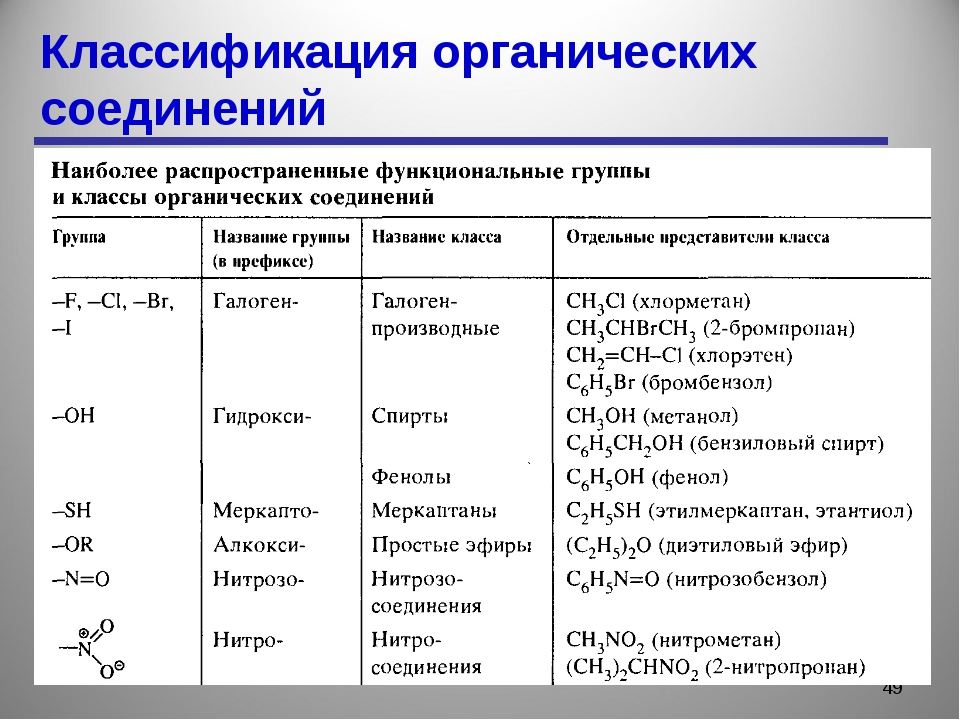
Классификация органических веществ
- Циклические — содержат замкнутые цепи углеродных атомов.

- карбоциклические — содержат только атомы углерода: алициклические (не содержат бензольных колец) и ароматические (содержат одно или несколько бензольных колец).
- гетероциклические — содержат атомы углерода, кислорода, азота, серы.
- Ациклические (алифатические) — содержат незамкнутые цепи углеродных атомов.
- предельные (насыщенные)
- непредельные (ненасыщенные)
Класс органических веществ
| Алканы | СnH2n+2 |
| Алкены | СnH2n |
| Алкины | СnH2n-2 |
| Алкадиены | СnH2n-2 |
| Гомологи бензола | СnH2n-6 |
| Предельные одноатомные спирты | СnH2n+2О |
| Многоатомные спирты | СnH2n+2-x(OH)x |
| Предельные альдегиды | СnH2n О |
| Кетоны | СnH2n О |
| Фенолы | СnH2n-6О |
| Предельные карбоновые кислоты | СnH2n+1СООН |
| Сложные эфиры | СnH2n О2; СnH2n+1 — С-О-СmН2m+1 |
| Амины | СnH2n+3N; СnH2n+1NH2 |
| Аминокислоты (предельные одноосновные) | СnH2n+1NО2 |
Характерные особенности органических веществ:
- атомы углерода в молекулах органических соединений способны соединяться друг с другом;
- атомы углерода в молекулах органических соединений образуют цепи и кольца, что является одной из причин многообразия органических соединений;
- связи между атомами в молекулах органических соединений ковалентные. В своем большинстве органические вещества являются неэлектролитами, т.е. не диссоциируют на ионы в растворах, а также сравнительно медленно взаимодействуют друг с другом.
- для органических соединений характерно явление изомерии, в связи с чем имеется множество соединений углерода, которые обладают одинаковым качественным и количественным составом, одинаковой молекулярной массой, но совершенно различными физическими и даже химическими свойствами;
- многие органические соединения являются непосредственными носителями, участниками или продуктами процессов, которые протекают в живых организмах, – ферменты, гормоны, витамины.
Химические реакции органических веществ подразделяются
По числу и составу исходных и образовавшихся веществ:
- реакции соединения — реакции, при которых из двух или нескольких веществ образуется одно новое вещество:
- реакции разложения — реакции, в результате которых из одного вещества образуется несколько новых веществ:
- реакции замещения — реакции, в результате которых атомы простого вещества замещают в молекулах других веществ:
- реакции обмена — реакции, в результате которых два вещества обмениваются атомами или группировками атомов, образуя два новых вещества
По тепловому эффекту:
- Экзотермические – протекают с выделением энергии + Q
- Эндотермические – протекают с поглощением энергии — Q
По агрегатному состоянию реагирующих веществ:
- Гетерогенные – исходные вещества и продукты реакции находятся в разных агрегатных состояниях
- Гомогенные – исходные вещества и продукты реакции находятся в одном агрегатном состоянии
По наличию катализатора:
- Каталитические
- Некаталитические
По направлению:
- Необратимые – протекают в данных условиях только в одном направлении
- Обратимые – протекают в данных условиях одновременно в двух противоположных направлениях
По изменению степени окисления атомов элементов:
- Окислительно-восстановительные – реакции, идущие с изменением степени окисления
- Неокислительно-восстановительные – реакции, идущие без изменения степени окисления
Решай с ответами:
СПИСОК ВЕЩЕСТВ, ОТНОСЯЩИХСЯ К ЛЕТУЧИМ ОРГАНИЧЕСКИМ СОЕДИНЕНИЯМ (ЛОС) ПОСТАНОВЛЕНИЕ Госкомстата РФ от 29.09.2000 N 90 (ред. от 01.09.2003) «ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИЙ ПО ЗАПОЛНЕНИЮ ФОРМ ФЕДЕРАЛЬНОГО ГОСУДАРСТВЕННОГО СТАТИСТИЧЕСКОГО НАБЛЮДЕНИЯ ЗА ОКРУЖАЮЩЕЙ СРЕДОЙ И ГЕОЛОГОРАЗВЕДОЧНЫМИ РАБОТАМИ»
не действует
Редакция от 01.09.2003
Подробная информация
| Наименование документ | ПОСТАНОВЛЕНИЕ Госкомстата РФ от 29.09.2000 N 90 (ред. от 01.09.2003) «ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИЙ ПО ЗАПОЛНЕНИЮ ФОРМ ФЕДЕРАЛЬНОГО ГОСУДАРСТВЕННОГО СТАТИСТИЧЕСКОГО НАБЛЮДЕНИЯ ЗА ОКРУЖАЮЩЕЙ СРЕДОЙ И ГЕОЛОГОРАЗВЕДОЧНЫМИ РАБОТАМИ» |
| Вид документа | постановление, инструкция, перечень |
| Принявший орган | госкомстат рф |
| Номер документа | 90 |
| Дата принятия | 01.01.1970 |
| Дата редакции | 01.09.2003 |
| Дата регистрации в Минюсте | 01.01.1970 |
| Статус | не действует |
| Публикация |
|
| Навигатор | Примечания |
СПИСОК ВЕЩЕСТВ, ОТНОСЯЩИХСЯ К ЛЕТУЧИМ ОРГАНИЧЕСКИМ СОЕДИНЕНИЯМ (ЛОС)
Предельные углеводороды
1 Бутан 2 Гексан 3 Пентан 4 Циклогексан
Непредельные углеводороды
5 Амилены (смесь изомеров) 6 Бутилен 7 Пропилен 8 Этилен 9 1,3-бутадиен (дивинил) 10 Гептен
Ароматические углеводороды
11 Бензол 12 Изопропилбензол (кумол) 13 Ксилол 14 альфа-метилстирол 15 Растворитель мебельный (АМР-3) (контроль по толуолу) 16 Стирол 17 Толуол 18 Этилбензол 19 1,3,5-Триметилбензол (мезитилен) 20 2,6-Диметилфенол (2,6-ксиленол)
Ароматические полициклические углеводороды
21 Нафталин
Галогенопроизводные углеводороды
22 1-Бромгексан (гексил бромистый) 23 1-Бромгептан (гептил бромистый) 24 1-Бромдекан (децил бромистый) 25 1-Бром-3-метилбутан (изоамил бромистый) 26 1-Бром-2-метилпропан (изобутил бромистый) 27 1-Бромпентан (амил бромистый) 28 1-Бромпропан (пропил бромистый) 29 2-Бромпропан (изопропил бромистый) 30 Бромбензол 31 Бутил хлористый 32 1-Бромбутан (бутил бромистый) 33 Гексафторбензол 34 Дихлорэтан 35 Дихлордифторметан (фреон 12) 36 Дихлорфторметан (фреон 21) 37 Дифторхлорметан (фреон 22) 38 Дибромбензол 39 1,2-Дихлорпропан 40 1,3-Дихлорпропилен 41 Метилен хлористый 42 Тетрахлорэтилен (перхлорэтилен) 43 Тетрафторэтилен 44 Тетрахлорпропен 45 Трихлорметан (хлороформ) 46 Трихлорфторметан (фреон 11) 47 Трихлорэтилен 48 Трибромметан (бромоформ) 49 1,2,3-трихлорпропан 50 Углерод четыреххлористый 51 Хлорбензол 52 Хлоропрен 53 Эпихлоргидрин 54 Трихлорбензол 55 Аллил хлористый 56 Бензолсульфохлорид
Спирты и фенолы
57 бета-нафтол 58 Спирт амиловый 59 Спирт бутиловый 60 Спирт изобутиловый 61 Спирт изооктиловый 62 Спирт изопропиловый 63 Спирт метиловый 64 Спирт пропиловый 65 Спирт этиловый 66 Трикрезол (смесь изомеров: орто-, мета-, пара-) 67 Фенол 68 Циклогексанол 69 Этиленхлоргидран
Простые эфиры
70 Метилаль (диметоксиметан) 71 Динил (смесь 25% дифенила и 75% дифенилоксида) 72 Диметиловый эфир терефталевой кислоты 73 Моноизобутиловый эфир этиленгликоля (бутилцеллозольв) 74 Моноизопропиловый эфир этиленгликоля (пропилцеллозольв) 75 Диэтиловый эфир
Сложные эфиры (кроме эфиров фосфорной кислоты)
76 н-Амилацетат 77 Бутилацетат 78 Винилацетат 79 Метилакрилат 80 Метилацетат 81 Метилметакрилат 82 Этилацетат 83 Бутилакрилат (бутиловый эфир акриловой кислоты)
Альдегиды
84 Акролеин 85 Альдегид масляный 86 Ацетальдегид 87 Метальдегид (ацетальдегид тетрамер) 88 Формальдегид 89 Альдегид каприловый 90 Альдегид каприновый 91 Альдегид капроновый 92 Альдегид пелларгоновый
Кетоны
93 Ацетон 94 Ацетофенон 95 Дикетен 96 Растворитель древесноспиртовой марки А (ацетоноэфирный)
(контроль по ацетону) 97 Растворитель древесноспиртовой марки Э (эфирноацетоновый)
(контроль по ацетону) 98 Циклогексанон 99 Метилизобутилкетон 100 Метилэтилкетон
Органические кислоты
101 Ангидрид малеиновый (пары, аэрозоль) 102 Ангидрид уксусный 103 Ангидрид фталевый 104 Диметилформамид 105 Капролактам (пары, аэрозоль) 106 Кислота валериановая 107 Кислота капроновая 108 Кислота масляная 109 Кислота пропионовая 110 Кислота уксусная 111 Кислота терефталевая 112 Кислота муравьиная 113 Кислота перфторвалериановая
Органические окиси и перекиси
114 Гидроперекись изопропилбензола (гидроперекись кумола) 115 4,4-Диметилдиоксан-1,3 116 Этилена окись 117 Пропилена окись
Серосодержащие соединения
118 Альдегид метилмеркаптопропионовый 119 Тетраметилтиурамдисульфид (ТМТД, тиурам Д) 120 Диметилсульфид 121 2-Меркаптоэтанол (монотиоэтиленгликоль) 122 Метилмеркаптан 123 Этиленсульфид
Амины
124 5/6 Амино(2-парааминофенил) бензимидазол 125 Амины алифатические С15 — С20 126 2-Амино-1,3,5-триметилбензол (мезидин) 127 Анилин 128 Гексаметилендиамин 129 Гексаметиленимин 130 Диметиламин 131 Диметиланилин 132 3,4-Дихлоранилин 133 Диэтиламин 134 бета-Диэтиламиноэтилмеркаптан 135 Монометиланилин 136 Моноэтиламин 137 Триметиламин 138 Триэтиламин 139 м-Хлоранилин 140 п-Хлоранилин 141 Этиленимин 142 Циклогексиламин 143 4-Бутиланилин 144 Монометиламин 145 Ксилидин
Нитросоединения
146 Нитробензол 147 м-Нитробромбензол 148 м-Нитрохлорбензол 149 о-Нитрохлорбензол 150 п-Нитрохлорбензол
Прочие азотосодержащие
151 Акрилонитрил 152 Толуилендиизоцианат 153 N, N1 — Диметилацетамид 154 Дифенилметандинзодианат
Хиноны
155 альфа-Нафтахинон
Гетероциклические соединения
156 Пиридин 157 Тетрагидрофуран 158 Тиофен (тиофуран) 159 Фурфурол
Технические смеси
160 Бензин (нефтяной, малосернистый в пересчете на углерод) 161 Бензин сланцевый (в пересчете на углерод) 162 Уайт — спирит 163 Сольвент 164 Скипидар
УТВЕРЖДЕНА
Постановлением
Госкомстата России
от 29 сентября 2000 г. N 90
Химическая технология неорганических, органических веществ, природных энергоносителей и лекарственных препаратов
Описание программы:
18.03.01
Химическая технология
Инженерное дело, технологии и технические науки
Химико-технологический институт
Бакалавриат
2014-2019
Программа бакалавриата «Химическая технология неорганических, органических веществ, природных энергоносителей и лекарственных препаратов» направлена на подготовку специалистов широкого профиля в области химической технологии. Обучение ведется по нескольким траекториям:
В рамках траектории «Химическая технология органических веществ» готовят специалистов в области основного и тонкого органического синтеза, производства химико-фармацевтических препаратов и полимеров, создания новых материалов с уникальными свойствами для микроэлектроники, лазерной техники, цветного копирования, органических полупроводников и жидких кристаллов.
Программа траектории « Химическая технология синтетических биологически активных веществ, химико-фармацевтических препаратов и косметических средств» предполагает овладение студентами комплексом существующих методов синтеза, проведения физико-химических исследований, анализа строения органических соединений и материалов на их основе.
Бакалавры-неорганики (траектория «Химическая технология неорганических веществ») являются специалистами в области неорганического синтеза: производство чистых реактивов, кислот, минеральных удобрений, солей, переработка отходов металлургических предприятий (отходящие газы, пыли, сточные воды),
Обучение на траектории «Технология электрохимических производств» позволяет студентам приобрести навыки в области теории и практики электрохимических технологий: производство чистых металлов электролизом, нанесение защитно-декоративных и функциональных покрытий методом гальванотехники, получение изделий методом гальванопластики, производство химических источников тока и топливных элементов, защита от коррозии металлов.
В рамках траектории «Физико-химические технологии материалов электронной техники и энергетики» готовят специалистов в области технологии выращивания оптико-волокнистых материалов – средств связи XXI века, производства приборов для лазерной эндоскопической и терапевтической медицины, создание сенсорных элементов тепловидения, технология синтеза «электронного носа» для экологического контроля, нанесение покрытий химическим методом, в том числе при производстве печатных плат.
В ходе обучения на траектории «Химическая технология природных энергоносителей и углеродных материалов» студенты приобретают навыки в области переработки углехимического сырья, нефти и газа, что позволяет им в дальнейшем работать на нефтеперерабатывающих, газоперерабатывающих и коксохимический предприятиях, в системе сбыта нефтепродуктов.
Профессиональная деятельность выпускников траектории «Инструментальные методы анализа природных и технических объектов» будет связана с аналитическим контролем и мониторингом технологических процессов, материалов, объектов окружающей среды, диагностическими исследованиями в медицине и биологии; в фирмах-производителях фармацевтической продукции, центрах и лабораториях по контролю качества лекарственных средств.
После окончания университета выпускники направления «Химическая технология» могут работать в различных сферах: на предприятиях химической, фармацевтической и косметической промышленности, в области приборо- и машиностроения, электрометаллургии (получение чистых металлов электролизом), на предприятиях, выпускающих химические источники тока, ювелирные изделия (гальванотехника и гальванопластика), в службах электрохимической защиты предприятий по добыче и транспорту нефти и газа, на нефтеперерабатывающих, газоперерабатывающих и коксохимических предприятиях, в коррозионно-исследовательских и аналитических лабораториях.
↕ Общая информация о кафедре — Кафедра органической химии
Общая информация Заведующий кафедрой — доктор химических наук, профессор Воскресенский Леонид Геннадьевич Педагогический состав кафедры: Варламов А.В. профессор-консультант д.х.н., Борисова Т.Н. доцент к.х.н., Зубков Ф.И. доцент к.х.н., Борисов Р.С. доцент к.х.н., Зайцев В.П. доцент к.х.н., Никитина Е.В. доцент к.х.н., Сорокина Е.А. доцент к.х.н., Голанцов Н.Е. доцент к.х.н., Куликова Л.Н. ст.преп. к.х.н., Листратова А.В. ст. преп. к.х.н., Титов А.А. ст. преп. к.х.н., Феста А.А. ст. преп. к.х.н., Стороженко О.А. ассист. к.х.н.
Направления, специальности и специализации, по которым кафедра обеспечивает обучение студентов: Химия (04.03.01, 04.04.01), Лечебное дело (31.05.01), Фармация (33.05.02), Агрономия (35.03.04), Ветеринария (36.05.01), Экология и природопользование (05.03.06), Энерго- и ресурсосберегающие процессы в химической технологии (18.03.02), Ветеринарно-санитарная экспертиза (36.03.01), Стандартизация и метрология (27.03.01). Магистратура кафедры готовит специалистов в области синтеза азотсодержащих гетероциклических соединений, которые владеют соответствующей экспериментальной техникой, теоретическими и практическими знаниями в области теоретической органической химии, стереохимии тонкого органического синтеза и физико-химическими методами исследования органических веществ. Основные дисциплины: • Органическая химия, включая практикум, для специальностей химия, фармация, экология, лечебное дело, агрономия, ветеринария, ветеринарно-санитарная экспертиза, стандартизация и метрология, энерго- и ресурсосберегающие процессы в химической технологии. • Химическая технология. • Высокомолекулярные соединения. • Химические основы биологических процессов. • Основы ЯМР. • Основы масс-спектрометрии. Дисциплины специализации: • Актуальные проблемы современной химии. • Методы органической химии. • Теоретическая органическая химия. • Химия гетероциклических соединений. • ЯМР органических соединений. • Молекулярный спектральный анализ. • Химия природных соединений. • Основы стереохимии. • Химия лекарственных веществ. Спецкурсы: • Основы биотехнологии. • Основы масс-спектрометрии. • Поиск информации в химических базах данных. Кафедра является выпускающей. Контингент студентов в 2018 году: • Количество студентов, специализирующихся по кафедре — 22 • Число бакалавров и магистров, выпущенных в текущем году — 21 • Количество аспирантов, стажеров на кафедре — 16 • Число аспирантов, защитивших диссертации в уч.году — 2 Аспирантура кафедры с 1962 года по настоящее время подготовила 119 кандидатов химических наук (из них 44 иностранцы) и 5 докторов химических наук. Наука. Научная работа кафедры. Основное направление научной работы кафедры связано с разработкой методов синтеза азотсодержащих гетероциклических соединений, изучением их стереохимии и реакционной способности. Кафедре принадлежит приоритет в разработке каталитических методов синтеза и изучении реакционной способности азафлуоренов, азаантраценов, аза- и диазафлуорантенов, дигидросилаазаантраценов, пирролопиридинов и пирролоазоцинов. В настоящее время научные исследования проводятся кафедрой по двум фундаментальным научным направлениям – изучение тандемных превращений конденсированных тетрагидропиридинов под действием активированных алкинов и синтез конденсированных и замещенных азотсодержащих соединений на основе фурилзамщенных гомоаллиламинов. Реакции тандемных превращений тетрагидропиридинов впервые открыта на кафедре органической химии. Она позволяет получать уникальные по своей структуре восьми и девятичленные циклы – азоцины и азопины. На основе этих гетероциклов могут быть созданы препараты для лечения болезни Альцгеймера. На основе фурилзамещенных гомоаллиламинов разработаны препаративные методики синтеза ранее неизвестных изоиндолотетрагидрохинолинов и азепинов, а также карбоновых кислот этого ряда. Сотрудники кафедры опубликовали более 750 научных статей и получено более 60 авторских свидетельств. Научная работа кафедры поддержана 3 грантами РФФИ и 2 грантами Министерства науки и образования. Руководители грантов РФФИ: 1. Борисова Т. Н., к.х.н., доцент 2. Воскресенский Л.Г., д.х.н., профессор 3. Зубков Ф.И., к.х.н., доцент Руководитель грантов Министерства науки и образования: “Университеты России” и “Поддержка научного потенциала высшей школы” – Варламов А.В., д.х.н., профессор. На кафедре работает научный студенческий кружок, где студенты 2-5 курсов постигают основы тонкого органического синтеза. Члены научного студенческого кружка и магистры кафедры опубликовали в 2006-2007 г 4 статьи в центральной печати и сделали 8 докладов на различных конференциях. Участие в научных конференциях: • 20й Международный конгресс по химии гетероциклов, Палермо, Италия, 2016 г. • ХVI Молодежная конференция “Проблемы теоретической и экспериментальной химии” ,Екатеринбург, апрель 2017 г. • Международная конференция по химии гетероциклических соединений, посвященной 90-летию со дня рождения профессора А.Н.Коста, Москва. Опубликованные монографии, учебники и учебные пособия: o Бельский И.Ф., Дорофенко Г.Н., Простаков Н.С., Шестюк В.П., Чумаков Ю.И.Гетероциклы в органическом синтезе, Киев, Техника, 1970, 381 с. o Пожарский А.Ф., Солдатенков А.Т.Молекулы-перстни, Москва, Химия, 1993 г., 256 с. o Солдатенков А.Т., Колядина Н.М., Шендрик И.В.Основы органической химии лекарственных веществ, М., Химия, 2001 г., 188 с. o Заикин В.Г., Варламов А.В. Микая А.И., Простаков Н.С. Основы масс-спектрометрии органических соединений, Москва, Наука, 2001 г., 286 с. Список учебно-методических публикаций действующих преподавателей кафедры: o Н.С.Простаков Начала органической химии, ч. 1-3. o Н.С.Простаков, Т.Н.Борисова Основы биотехнологии. o Сборник лабораторных работ по общей химической технологии. o А.В.Варламов, С.А.Солдатова, Т.Н.Борисова, А.И.Чернышев. Методические указания к выполнению лабораторных работ по биоорганической химии. o Методические рекомендации к проведению экспериментальных исследований по спецкурсу «Химия гетероциклических соединений». o Методические рекомендации к изучению спецкурса «Химия природных соединений», ч. 1 и 2 o А.В. Варламов, Е.А. Сорокина, Л.Г. Воскресенский, Ф.И. Зубков. Методическое руководство к выполнению лабораторных работ по органической химии. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Л.Г. Воскресенский, Е.В. Никитина. Основы органической химии. Учебное пособие. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Е.В. Никитина. Вопросы и задачи по органической химии. Учебное пособие. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Е.В. Никитина. Основное содержание лабораторного практикума по курсу «Органический синтез». Учебное пособие. Учёба Преподаватели кафедры читают лекционные курсы по органической, биоорганической химии для студентов трех факультетов – медицинского (лечебное дело, фармация), аграрного (агрономия, ветеринария) и экологического. Также ведется преподавание биоорганической химии на английском языке для студентов медицинского факультета (лечебное дело). Лекционная форма учебной работы составляет примерно 550 часов. Ежегодно на кафедре проходят обучение до 1200 студентов. Плановая учебная нагрузка кафедры варьируется на уровне 9-10 тысяч часов. Одним из важнейших аспектов учебной работы по органической химии – это лабораторные и практические занятия. В этой части заняты как преподаватели, так и весь обслуживающий персонал и аспиранты кафедры. За организацию учебного процесса и методическую работу конкретного лекционного потока отвечает руководитель потока. Содержание химического курса с учетом профильной направленности находит отражение в материалах, составляющих «Учебно-методический комплекс курса». Такими материалами обеспечен каждый из читаемых кафедрой курсов. На сегодня их 72. В состав методического комплекса входят: учебная программа курса; календарные планы лекций и лабораторного практикума; список рекомендуемой учебной литературы; рекомендации реализации бально-рейтинговой системы учета и контроля знаний; варианты контрольных работ. Внедрение бально-рейтинговой системы способствовало тому, что за последние 10 лет педагогического эксперимента на кафедре были разработаны единые критерии требований, предъявляемых к выполнению лабораторных и практических работ. Большое внимание уделяется индивидуальной работе со студентами. Организуются еженедельные консультации для каждой из групп. Преподаватели кафедры стремятся найти правильный подход к каждому, вовлечь студентов в активную работу, организовать дополнительные занятия с отстающими студентами. Методические пособия и лабораторные практикумы разрабатывают опытные преподаватели — руководители лекционных потоков. Преподаватели кафедры подготовили и опубликовали следующие издания: o Солдатенков А.Т., Колядина Н.М., Шендрик И.В.Основы органической химии лекарственных веществ. o Заикин В.Г., Варламов А.В. Микая А.И., Простаков Н.С. Основы масс-спектрометрии органических соединений. o Н.С.Простаков Начала органической химии, ч. 1-3. o Н.С.Простаков, Т.Н. Борисова Основы биотехнологии. o Сборник лабораторных работ по химической технологии. o А.В.Варламов, Е.А. Сорокина, Е.В. Никитина Методические указания к выполнению лабораторных работ по биоорганической химии. o Методические рекомендации к проведению экспериментальных исследований по спецкурсу «Химия гетероциклических соединений». o Методические рекомендации к изучению спецкурса «Химия природных соединений», ч. 1 и 2 o А.В. Варламов, Е.А. Сорокина, Л.Г. Воскресенский, Ф.И. Зубков. Методическое руководство к выполнению лабораторных работ по органической химии. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Л.Г. Воскресенский, Е.В. Никитина. Основы органической химии. Учебное пособие. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Е.В. Никитина. Вопросы и задачи по органической химии. Учебное пособие. Т.Н. Борисова, А.В. Варламов, Е.А. Сорокина, Е.В. Никитина. Основное содержание лабораторного практикума по курсу «Органический синтез». Учебное пособие.
3.7: Названия формул органических соединений
Цели обучения
- Объясните следующие законы Закона об идеальном газе:
Углеводороды
Примерно одна треть соединений, производимых промышленным способом, представляет собой органические соединения. Все живые организмы состоят из органических соединений, как и большинство продуктов питания, лекарств, волокон одежды и пластика. Обнаружение органических соединений полезно во многих областях. В одном недавно разработанном приложении ученые изобрели новый метод, названный «материальная деградомика», для отслеживания деградации старых книг и исторических документов.С возрастом бумага издает знакомый «запах старой книги» из-за выделения органических соединений в газообразной форме. Состав газа зависит от исходного типа используемой бумаги, переплета книги и применяемого носителя. Анализируя эти органические газы и изолировав отдельные компоненты, специалисты по охране окружающей среды могут лучше определить состояние объекта и тех книг и документов, которые больше всего нуждаются в немедленной защите.
Простейшим классом органических соединений являются углеводороды, которые полностью состоят из углерода и водорода.Нефть и природный газ представляют собой сложные природные смеси множества различных углеводородов, которые служат сырьем для химической промышленности. К четырем основным классам углеводородов относятся следующие: алканы, которые содержат только одинарные углерод-водородные и углерод-углеродные одинарные связи; алкены, содержащие по крайней мере одну двойную углерод-углеродную связь; алкины, содержащие по крайней мере одну тройную углерод-углеродную связь; и ароматические углеводороды, которые обычно содержат кольца из шести атомов углерода, которые могут быть образованы чередующимися одинарными и двойными связями.Алканы также называют насыщенными углеводородами , тогда как углеводороды, содержащие кратные связи (алкены, алкины и ароматические соединения), являются ненасыщенными .
Алканы
Простейшим алканом является метан (CH 4 ), бесцветный газ без запаха, который является основным компонентом природного газа. В более крупных алканах, атомы углерода которых соединены в неразветвленную цепь ( алканов с прямой цепью ), каждый атом углерода связан максимум с двумя другими атомами углерода.Структуры двух простых алканов показаны на рисунке \ (\ PageIndex {1} \), а названия и сжатые структурные формулы для первых 10 алканов с прямой цепью приведены в таблице \ (\ PageIndex {1} \). Названия всех алканов заканчиваются на — ane , и их температуры кипения увеличиваются с увеличением числа атомов углерода.
Рисунок \ (\ PageIndex {1} \): Алканы с прямой цепью с двумя и тремя атомами углерода
| Имя | Количество атомов углерода | Молекулярная формула | Концентрированная структурная формула | Температура кипения (° C) | использует |
|---|---|---|---|---|---|
| метан | 1 | CH 4 | CH 4 | −162 | газовая составляющая |
| этан | 2 | С 2 В 6 | СН 3 СН 3 | −89 | газовая составляющая |
| пропан | 3 | С 3 В 8 | Канал 3 Канал 2 Канал 3 | −42 | газ баллонный |
| бутан | 4 | С 4 В 10 | Канал 3 Канал 2 Канал 2 Канал 3 или Канал 3 (Канал 2 ) 2 Канал 3 | 0 | зажигалки газовые баллонные |
| пентан | 5 | С 5 В 12 | Канал 3 (Канал 2 ) 3 Канал 3 | 36 | растворитель, бензин |
| гексан | 6 | С 6 В 14 | Канал 3 (Канал 2 ) 4 Канал 3 | 69 | растворитель, бензин |
| гептан | 7 | С 7 В 16 | Канал 3 (Канал 2 ) 5 Канал 3 | 98 | растворитель, бензин |
| октановое число | 8 | С 8 В 18 | Канал 3 (Канал 2 ) 6 Канал 3 | 126 | бензин |
| нонан | 9 | С 9 В 20 | Канал 3 (Канал 2 ) 7 Канал 3 | 151 | бензин |
| декан | 10 | С 10 В 22 | Канал 3 (Канал 2 ) 8 Канал 3 | 174 | керосин |
Алканы с четырьмя или более атомами углерода могут иметь более одного расположения атомов.Атомы углерода могут образовывать одну неразветвленную цепь, или первичная цепь атомов углерода может иметь одну или несколько более коротких цепей, образующих разветвления. Например, бутан (C 4 H 10 ) имеет две возможные структуры. Нормальный бутан (обычно называемый n -бутаном) представляет собой CH 3 CH 2 CH 2 CH 3 , в котором атомы углерода образуют единую неразветвленную цепь. Напротив, конденсированная структурная формула для изобутана : (CH 3 ) 2 CHCH 3 , в которой первичная цепь из трех атомов углерода имеет одноуглеродное разветвление у центрального атома углерода.Трехмерные изображения обеих структур следующие:
В систематических названиях разветвленных углеводородов используется наименьшее возможное число, чтобы указать положение разветвления вдоль самой длинной прямой углеродной цепи в структуре. Таким образом, систематическое название изобутана — 2-метилпропан, что указывает на то, что метильная группа (ветвь, состоящая из –CH 3 ) присоединена ко второму атому углерода молекулы пропана. Точно так же в разделе 2.6 «Промышленно важные химические вещества» говорится, что один из основных компонентов бензина обычно называется изооктаном; его структура выглядит следующим образом:
Соединение имеет цепочку из пяти атомов углерода, поэтому оно является производным пентана.Есть две ветви метильной группы у одного атома углерода и одна метильная группа у другого. Использование наименьших возможных чисел для разветвлений дает 2,2,4-триметилпентан для систематического названия этого соединения.
Алкенес
Самыми простыми алкенами являются этилен , C 2 H 4 или CH 2 = CH 2 и пропилен , C 3 H 6 или CH 3 CH = CH 2 (часть (a) на рисунке \ (\ PageIndex {2} \)).Имена алкенов, которые имеют более трех атомов углерода, используют те же основы, что и названия алканов (Таблица \ (\ PageIndex {1} \) «Первые 10 алканов с прямой цепью»), но вместо этого заканчиваются на — ene из — анэ .
Как и в случае алканов, для алкенов с четырьмя или более атомами углерода возможно более одной структуры. Например, алкен с четырьмя атомами углерода имеет три возможных структуры. Один из них — CH 2 = CHCH 2 CH 3 (1-бутен), который имеет двойную связь между первым и вторым атомами углерода в цепи.Две другие структуры имеют двойную связь между вторым и третьим атомами углерода и представляют собой формы CH 3 CH = CHCH 3 (2-бутен). Все четыре атома углерода в 2-бутене лежат в одной плоскости, поэтому есть две возможные структуры (часть (а) на рисунке \ (\ PageIndex {2} \)). Если две метильные группы находятся на одной стороне двойной связи, соединение представляет собой цис -2-бутен (от латинского цис , что означает «на одной стороне»). Если две метильные группы находятся на противоположных сторонах двойной связи, соединение представляет собой транс, -2-бутен (от латинского транс , что означает «поперек»).Это совершенно разные молекулы: цис -2-бутен плавится при -138,9 ° C, тогда как транс -2-бутен плавится при -105,5 ° C.
Рисунок \ (\ PageIndex {2} \): некоторые простые (а) алкены, (б) алкины и (в) циклические углеводороды. Положения атомов углерода в цепи обозначены C 1 или C 2 .
Точно так же, как число указывает положения разветвлений в алкане, число в названии алкена указывает положение первого атома углерода двойной связи.Название основано на наименьшем возможном номере, начинающемся от до конца углеродной цепи, поэтому CH 3 CH 2 CH = CH 2 называется 1-бутеном, а не 3-бутеном. Обратите внимание, что CH 2 = CHCH 2 CH 3 и CH 3 CH 2 CH = CH 2 представляют собой разные способы записи одной и той же молекулы (1-бутена) в двух разных ориентациях.
Название соединения не не зависит от его ориентации. Как показано для 1-бутена, как конденсированные структурные формулы, так и молекулярные модели показывают разные ориентации одной и той же молекулы. Важно уметь распознавать одну и ту же структуру независимо от ее ориентации.
Примечание
Положения групп или множественных связей всегда указываются наименьшим возможным числом.
Алкины
Простейшим алкином является ацетилен , C 2 H 2 или HC≡CH (часть (b) на рисунке \ (\ PageIndex {2} \)).Поскольку смесь ацетилена и кислорода горит пламенем, которое достаточно горячее (> 3000 ° C) для резки металлов, таких как закаленная сталь, ацетилен широко используется в резаках и сварочных горелках. Названия других алкинов аналогичны названиям соответствующих алканов, но заканчиваются на — yne . Например, HC≡CCH 3 представляет собой пропин , а CH 3 C≡CCH 3 представляет собой 2-бутин , потому что кратная связь начинается со второго атома углерода.
Примечание
Число связей между атомами углерода в углеводороде указывается в суффиксе:
- alk ane : только одинарные углерод-углеродные связи
- alk ene : по крайней мере, одна углерод-углеродная двойная связь
- alk yne : как минимум одна тройная связь углерод-углерод
Циклические углеводороды
В циклическом углеводороде концы углеводородной цепи соединены с образованием кольца из ковалентно связанных атомов углерода.Циклические углеводороды называются добавлением префикса цикло — к названию алкана, алкена или алкина. Простейшие циклические алканы — это циклопропан, (C 3 H 6 ), горючий газ, который также является сильнодействующим анестетиком, и циклобутан (C 4 H 8 ) (часть (c) на рисунке \ (\ PageIndex {2} \)). Самый распространенный способ нарисовать структуры циклических алканов — это нарисовать многоугольник с тем же числом вершин, что и количество атомов углерода в кольце; каждая вершина представляет собой блок CH 2 .Структуры циклоалканов, содержащих от трех до шести атомов углерода, схематически показаны на рисунке \ (\ PageIndex {3} \).
Рисунок \ (\ PageIndex {3} \): простые циклоалканы
Ароматические углеводороды
Алканы, алкены, алкины и циклические углеводороды обычно называют алифатическими углеводородами. Название происходит от греческого aleiphar , что означает «масло», потому что первые образцы были извлечены из животных жиров. Напротив, первые образцы ароматических углеводородов , также называемые аренами , были получены путем дистилляции и разложения сильно ароматизированных (таким образом, ароматических ) смол тропических деревьев.
Простейшим ароматическим углеводородом является бензол (C 6 H 6 ), который впервые был получен из угольного дистиллята. Слово ароматический теперь относится к бензолу и аналогичным по структуре соединениям. Как показано в части (а) на рисунке \ (\ PageIndex {4} \), можно изобразить структуру бензола двумя разными, но эквивалентными способами, в зависимости от того, какие атомы углерода связаны двойными или одинарными связями. Толуол аналогичен бензолу, за исключением того, что один атом водорода заменен группой –CH 3 ; он имеет формулу C 7 H 8 (часть (b) на рисунке \ (\ PageIndex {4} \)).Химическое поведение ароматических соединений отличается от поведения алифатических соединений. Бензол и толуол содержатся в бензине, и бензол является исходным материалом для получения таких разнообразных веществ, как аспирин и нейлон.
Рисунок \ (\ PageIndex {4} \) : Два ароматических углеводорода: (а) бензол и (б) толуол
На рисунке \ (\ PageIndex {5} \) показаны две молекулярные структуры, возможные для углеводородов с шестью атомами углерода.Как показано, соединения с одинаковой молекулярной формулой могут иметь очень разные структуры.
Рисунок \ (\ PageIndex {5} \): два углеводорода с молекулярной формулой C 6 H 12
Пример \ (\ PageIndex {1} \)
Напишите сжатую структурную формулу для каждого углеводорода.
- н-гептан
- 2-пентен
- 2-бутин
- циклооктен
Дано : название углеводорода
Запрошено : сокращенная структурная формула
Стратегия :
- Используйте префикс, чтобы определить количество атомов углерода в молекуле и то, является ли она циклической.По суффиксу определите, присутствуют ли множественные связи.
- Определите положение любых кратных связей по числу (ам) в имени, а затем запишите сжатую структурную формулу.
Решение :
а. A Приставка hept- говорит нам, что этот углеводород имеет семь атомов углерода, а n- указывает, что атомы углерода образуют прямую цепь. Суффикс -ан указывает на то, что это алкан без двойных или тройных связей углерод-углерод. B Сводная структурная формула: CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3 , что также может быть записано как \ (CH_3 (CH_2) _5CH_3 \).
г. A Префикс pent- говорит нам, что этот углеводород имеет пять атомов углерода, а суффикс -ene указывает на то, что это алкен с двойной углерод-углеродной связью. B Число 2- говорит нам, что двойная связь начинается со второго атома углерода в цепи из пяти атомов углерода.Конденсированная структурная формула соединения, следовательно, CH 3 CH = CHCH 2 CH 3 .
г. A Приставка but- говорит нам, что соединение имеет цепочку из четырех атомов углерода, а суффикс -yne указывает на то, что оно имеет тройную связь углерод-углерод. B Число 2- говорит нам, что тройная связь начинается со второго атома углерода цепи из четырех атомов углерода. Таким образом, сжатая структурная формула соединения: CH 3 C≡CCH 3 .
г. Префикс цикло- говорит нам, что этот углеводород имеет кольцевую структуру, а окт- указывает, что он содержит восемь атомов углерода, которые мы можем нарисовать как
.
Суффикс -ene говорит нам, что соединение содержит двойную связь углерод-углерод, но где в кольце мы разместим двойную связь? B Поскольку все восемь атомов углерода идентичны, это не имеет значения. Мы можем изобразить структуру циклооктена как
Упражнение \ (\ PageIndex {1} \)
Напишите сжатую структурную формулу для каждого углеводорода.
- н-октан
- 2-гексен
- 1-гептин
- циклопентан
Ответ :
- Канал 3 (Канал 2 ) 6 Канал 3
- CH 3 CH = CHCH 2 CH 2 CH 3
- HC≡C (канал 2 ) 4 канал 3
Общее название группы атомов, производных от алкана, — это алкильная группа .Название алкильной группы происходит от названия алкана с добавлением суффикса — ил . Таким образом, фрагмент –CH 3 представляет собой группу метил , фрагмент –CH 2 CH 3 представляет собой группу этил и т. Д., Где тире обозначает одинарную связь с каким-либо другим атомом или группой. . Точно так же группы атомов, полученных из ароматических углеводородов, представляют собой арильные группы , которые иногда имеют неожиданные названия. Например, фрагмент –C 6 H 5 является производным бензола, но его называют фенильной группой .В общих формулах и структурах алкильные и арильные группы часто обозначают аббревиатурой R
.
Строения алкильных и арильных групп. Метильная группа является примером алкильной группы, а фенильная группа является примером арильной группы .
Спирты
Замена одного или нескольких атомов водорода в углеводороде группой –ОН дает спирт, обозначенный как ROH. Самый простой спирт (CH 3 OH) называется либо метанол (его систематическое название), либо метиловый спирт (его обычное название).Метанол является антифризом в жидкостях для мытья стекол автомобилей, а также используется в качестве эффективного топлива для гоночных автомобилей, особенно в Индианаполисе 500. Этанол (или этиловый спирт, CH 3 CH 2 OH) известен как алкоголь в ферментированных или дистиллированных напитках, таких как пиво, вино и виски; он также используется в качестве присадки к бензину (Раздел 2.6 «Промышленно важные химикаты»). Самый простой спирт, полученный из ароматического углеводорода, — это C 6 H 5 OH, фенол (сокращенный от фенил спирт), сильнодействующее дезинфицирующее средство, используемое в некоторых лекарствах от боли в горле и жидкостях для полоскания рта.
Этанол, который легко получить в процессе ферментации, успешно используется в качестве альтернативного топлива в течение нескольких десятилетий. Хотя это «зеленое» топливо, полученное из растений, это несовершенная замена ископаемым видам топлива, поскольку оно менее эффективно, чем бензин. Более того, поскольку этанол поглощает воду из атмосферы, он может вызвать коррозию уплотнений двигателя. Таким образом, разрабатываются другие типы процессов, в которых используются бактерии для создания более сложных спиртов, таких как октанол, которые более энергоэффективны и имеют меньшую тенденцию к поглощению воды.Поскольку ученые пытаются уменьшить зависимость человечества от ископаемого топлива, разработка так называемого биотоплива является особенно активной областью исследований.
Сводка
Самыми простыми органическими соединениями являются углеводородов , которые содержат только углерода и водорода. Алканы содержат только одинарные связи углерод-водород и углерод-углерод, алкены содержат по крайней мере одну двойную связь углерод-углерод, а алкины содержат одну или несколько тройных связей углерод-углерод.Углеводороды также могут быть циклическими, , с концами цепи, соединенными с образованием кольца. В совокупности алканы, алкены и алкины называются алифатическими углеводородами . Ароматические углеводороды , или арены , являются другим важным классом углеводородов, которые содержат кольца из атомов углерода, связанных со структурой бензола (C 6 H 6 ). Производное алкана или арена, из которого удален один атом водорода, называется алкильной группой или арильной группой соответственно. Спирты — еще один распространенный класс органических соединений, которые содержат группу –OH, ковалентно связанную либо с алкильной группой, либо с арильной группой (часто сокращенно R ).
Органическое соединение | Использование органических соединений |
Метан | Черный цвет, при изготовлении автомобильных шин и печатных красок, при производстве света и энергии, при производстве метилового спирта, формальдегида, хлороформа и т. Д. |
Бутан | В жидком состоянии используется как сжиженный нефтяной газ. |
Этилен | Для созревания и консервирования плодов, при приготовлении горчичного газа, в виде анестезии, в оксиэтиленовом пламени |
Ацетилен | При производстве света оксиэтиленового пламени, в форме наркоза нарселин, при производстве неопрена (искусственного каучука), при искусственном созревании и т. Д. |
Полиэтилен | Используется для создания электрического сопротивления в проводах и кабелях, в создании слоя в крышке бутылки при производстве не трескающихся бутылок, труб, ведер и т. Д. |
Полистирол | Используется для производства крышек от бутылок с кислотой, изготовления корпусов аккумуляторных ячеек и т. Д. |
Этилбром | Для местной анестезии. |
Хлороформ | При хирургической операции в качестве анестезии, в виде растворителя каучука, жира, лака и т. Д., В качестве инсектицида и т. Д. |
Метиловый спирт | При производстве метилового спирта, искусственных красителей, полироли и полироли, смешивания с бензином и использования в качестве топлива для двигателей и т. Д. |
Формамент | При изготовлении лекарств от горла При изготовлении жевательных таблеток. |
Этиловый спирт | Используется для изготовления вина и других алкогольных напитков, настойки, полировки и полироли в виде растворителей, в метиловом спирте, в искусственных красителях в парфюмерии и аромате фруктов, в прозрачном мыле, в спиртовых лампах и печах в виде автомобильного топлива при очистке ран, в виде инсектицидов и т. д. |
Глицерин | Применяется для изготовления нитроглицерина, для чистки деталей часов, в чернилах штампа, в кремах для обуви и косметике, в прозрачном мыле, в обезболивающих лекарствах от любых переломов органов тела, в конфетах, вине. и консерванты фруктов и т. д. |
Формальдегид | При изготовлении инсектицидов, при фиксации желатиновой пленки на фотопластинках, при изготовлении водонепроницаемой ткани путем смешивания ее с внешней белой частью яйца и т. Д. |
Ацетальдегид | При изготовлении цветных лекарств, при производстве лекарств на основе метацетальдегида, используемых для сна, при производстве пластмасс. |
Ацетон | При производстве барнира, кордита, клодиевой целлюлозы, искусственного шелка, синтетического каучука, сульфона, хлортона, хлороформа, йодоформа и т. Д.в качестве лекарств и т. д. |
Муравьиная кислота | При производстве инсектицидов, в качестве консерванта фруктовых соков, в торговле кожей, резиной и т. Д. |
Уксусная кислота | В качестве лабораторного реагента в виде уксуса, при приготовлении соусов, желе и т. Д. |
Ацетилхлорид | При производстве ацетамида, уксусного ангидрида и т. Д. |
Уксусный ангидрид | В цветной промышленности, при производстве лекарств, таких как аспирин, при производстве искусственного или синтетического шелка из целлюлозы и т. Д. |
Ацетамид | Для смягчения кожи, ткани и замораживания целлюлозы и бумаги. |
Этилацетат | При изготовлении лекарств, парфюмерии и т. Д. |
Мочевина | В виде удобрений, при производстве формальдегида и карбамида, лекарств и т. Д. |
Щавелевая кислота | При окраске и печати на тканях, при окрашивании чернил и каменноугольной смолы, при отбеливании кожи, при очистке пятна чернил ее 10% -ным раствором и т. Д. |
Глюкоза | При изготовлении различных вин, конфет и консервантов фруктовых соков, лекарств, таких как глюконат и т. Д. |
Бензол | В виде растворителя, при химической чистке, при смешивании с бензином и в качестве топлива для двигателей и т. Д. |
Толуол | В химической чистке, в виде растворителей, при производстве лекарств, взрывчатых веществах и т. Д. |
Хлорбензол | При производстве анилина, фенола и т. Д. |
Нитробензол | При производстве мыла в виде мирбанового масла, в производстве полиролей и т. Д. |
Анилин | В торговле красками, в производстве лекарств и т. Д. |
Фенол | При производстве карболового мыла в форме инсектицидов, бакелита, предестина, аспирина, целолаля и т. Д. |
Бензальдегид | В цветной промышленности, производстве парфюмерии и т. Д. |
Бензойная кислота | При изготовлении лекарств, в качестве консерванта фруктовых соков и т. Д. |
Бензолсульфоновая кислота | В производстве сахарина, в производстве растворенных веществ, в производстве сульфатных лекарств и т. Д. |
Эфир | В качестве обезболивающего, растворителя, охлаждающей жидкости, при производстве спирта и т.д … |
Четыреххлористый углерод | В виде огнетушителя. |
Уротропин | В лечении урологических заболеваний. |
Гаммексен | В форме гермицида / инсектицида |
Органический 101: разрешенные и запрещенные вещества
Автор: Майлз МакЭвой, директор Национальной программы по органическим продуктам, в
Еда и питание
Исследования и наука
27 октября 2020 г.
Основное правило органического сельского хозяйства — разрешить использование натуральных веществ и запретить синтетические.Однако для такого домашнего скота, как эти здоровые коровы, вакцины играют важную роль в здоровье животных, особенно с учетом того, что терапия антибиотиками запрещена. (Фото любезно предоставлено Pleasantview Farm, сертифицированной органической молочной фермой в Огайо)
Это вторая часть серии Organic 101, в которой исследуются различные аспекты органических нормативов Министерства сельского хозяйства США.
Органические стандарты разработаны, чтобы разрешить использование натуральных веществ в органическом сельском хозяйстве, в то же время запрещая использование синтетических веществ. В Национальном списке разрешенных и запрещенных веществ — одном из компонентов органических стандартов — перечислены исключения из этого основного правила.
Национальный совет по органическим стандартам (NOSB) создан в соответствии с законом, чтобы давать рекомендации Национальной органической программе (NOP) о том, какие вещества следует разрешить или запретить. В состав совета входят преданные обществу добровольцы, назначаемые министром сельского хозяйства, и в его состав входят органические производители, обработчики, розничные торговцы, экологи, ученые, аккредитованные Министерством сельского хозяйства США сертифицирующие агенты и защитники прав потребителей.
Члены NOSB должны использовать определенные критерии при голосовании, включая потребность в веществе и его влияние на здоровье человека и окружающую среду.В определенных случаях NOSB также голосует за то, чтобы разрешить использование неорганических версий вещества, если оно недоступно в органической форме в масштабах, достаточных для поддержки органического сельского хозяйства.
Некоторые синтетические вещества перечислены как исключения из основного правила и разрешены для использования в органическом сельском хозяйстве. Например, феромоны давно используются как эффективный, нетоксичный способ «запутать» насекомых, которые в противном случае могут заразить органические культуры, особенно фрукты. Точно так же вакцины для животных являются важным средством профилактики многих инфекционных заболеваний, особенно потому, что антибиотикотерапия запрещена в органическом животноводстве.
Национальный список также разрешает использование некоторых вспомогательных средств обработки, таких как пищевая сода. Это вещество осветляет (или придает форму) тесто для органических блинов, выпечки и других продуктов.
И наоборот, некоторые вещества, такие как стрихнин и мышьяк, являются примерами природных токсичных веществ, запрещенных в органическом производстве.
Процесс добавления или удаления разрешенных веществ — это открытый процесс, позволяющий вносить непосредственный вклад со стороны органического сообщества. Обычно процесс состоит из следующих шагов:
- Физическое лицо или организация подают официальное ходатайство о добавлении, удалении или изменении списка определенного вещества.
- NOSB рассматривает петицию. Сторонний технический отчет часто используется для сбора научной информации о веществе и выявления любых негативных воздействий на здоровье человека или окружающую среду.
- Подкомитет NOSB публикует предложенную рекомендацию по этому веществу с запросом на публичные комментарии перед публичным собранием, которое обычно проводится два раза в год.
- Во время собрания NOSB обсуждает общественные комментарии, связанные с петицией, а затем голосует на открытом форуме.Все собрания NOSB бесплатны и открыты для публики.
- NOP рассматривает рекомендацию NOSB. NOP может отклонить рекомендацию NOSB о добавлении вещества в Национальный список, но не может добавить вещество, которое не было рекомендовано NOSB.
- Если NOP соглашается с рекомендацией NOSB, он инициирует нормотворчество для внесения поправок в Национальный список для этого вещества.
Подкомитет
В ходе этого процесса NOSB посвящает бесчисленное количество часов обсуждению диапазона точек зрения по каждому исследуемому веществу.Процесс общественного обсуждения играет важную роль в обеспечении тщательного рассмотрения всех точек зрения.
Поскольку этот консультативный совет граждан представляет все ключевые секторы органического сообщества, рекомендации NOSB дают NOP бесценную информацию о том, какие вещества следует разрешить или запретить в органическом сельском хозяйстве. NOP приглашает общественность участвовать в этом процессе, поскольку мы формируем будущее органического сельского хозяйства.
Категория / Тема:
Еда и питание
Исследования и наука
Написать ответ
Комментарии
Типы органических соединений в химии и биологии
Органические соединения называются «органическими», потому что они связаны с живыми организмами.Эти молекулы составляют основу жизни и очень подробно изучаются в химических дисциплинах органической химии и биохимии.
Существует четыре основных типа или класса органических соединений, обнаруженных во всем живом: углеводы, липиды, белки и нуклеиновые кислоты. Кроме того, существуют другие органические соединения, которые могут быть обнаружены в некоторых организмах или вырабатываются ими. Все органические соединения содержат углерод, обычно связанный с водородом (также могут присутствовать другие элементы).Давайте подробнее рассмотрим ключевые типы органических соединений и рассмотрим примеры этих важных молекул.
Углеводы — органические соединения
Масанянка / Getty Images
Углеводы — это органические соединения, состоящие из элементов углерода, водорода и кислорода. Отношение атомов водорода к атомам кислорода в молекулах углеводов составляет 2: 1. Организмы используют углеводы в качестве источников энергии, структурных единиц и для других целей. Углеводы — это самый большой класс органических соединений, содержащихся в организмах.
Углеводы классифицируются по количеству содержащихся в них субъединиц. Простые углеводы называются сахарами. Сахар, состоящий из одной единицы, является моносахаридом. Если две единицы соединяются вместе, образуется дисахарид. Более сложные структуры образуются, когда эти более мелкие единицы соединяются друг с другом с образованием полимеров. Примеры этих более крупных углеводных соединений включают крахмал и хитин.
Примеры углеводов:
- Глюкоза
- Фруктоза
- Сахароза (столовый сахар)
- Хитин
- Целлюлоза
- Глюкоза
Липиды — органические соединения
дулезидар / Getty Images
Липиды состоят из атомов углерода, водорода и кислорода.Липиды имеют более высокое отношение водорода к кислороду, чем углеводы. Три основные группы липидов — это триглицериды (жиры, масла, воски), стероиды и фосфолипиды. Триглицериды состоят из трех жирных кислот, соединенных с молекулой глицерина. Каждый стероид имеет основу из четырех углеродных колец, соединенных друг с другом. Фосфолипиды напоминают триглицериды, за исключением того, что вместо одной из цепей жирных кислот есть фосфатная группа.
Липиды используются для хранения энергии, построения структур и в качестве сигнальных молекул, помогающих клеткам общаться друг с другом.
Примеры липидов:
- Холестерин
- Парафин
- Оливковое масло
- Маргарин
- Кортизол
- Эстроген
- Фосфолипидный бислой, образующий клеточную мембрану
Белки — органические соединения
Максимилиан Сток Лтд. / Getty Images
Белки состоят из цепочек аминокислот, называемых пептидами. Белок может быть получен из одной полипептидной цепи или может иметь более сложную структуру, в которой полипептидные субъединицы упаковываются вместе, образуя единицу.Белки состоят из атомов водорода, кислорода, углерода и азота. Некоторые белки содержат другие атомы, такие как сера, фосфор, железо, медь или магний.
Белки выполняют в клетках множество функций. Они используются для создания структуры, катализатора биохимических реакций, иммунного ответа, упаковки и транспортировки материалов, а также для воспроизведения генетического материала.
Примеры белков:
- Ферменты
- Коллаген
- Кератин
- Альбумин
- Гемоглобин
- Миоглобин
- Фибрин
Нуклеиновые кислоты — органические соединения
Stocktrek Images / Getty Images
Нуклеиновая кислота — это тип биологического полимера, состоящего из цепочек нуклеотидных мономеров.Нуклеотиды, в свою очередь, состоят из азотистого основания, молекулы сахара и фосфатной группы. Клетки используют нуклеиновые кислоты для кодирования генетической информации организма.
Примеры нуклеиновых кислот:
- ДНК (дезоксирибонуклеиновая кислота)
- РНК (рибонуклеиновая кислота)
Другие виды органических соединений
Ирина Имаго / Getty Images
В дополнение к четырем основным видам органических молекул, обнаруженных в организмах, существует множество других органических соединений.К ним относятся растворители, лекарства, витамины, красители, искусственные ароматизаторы, токсины и молекулы, используемые в качестве предшественников биохимических соединений. Вот некоторые примеры:
- Ацетальдегид
- Ацетаминофен
- Ацетон
- Ацетилен
- Бензальдегид
- Биотин
- Бромфеноловый синий
- Кофеин
- Тетрахлорметан
- Фуллерен
- Гептан
- Метанол
- Горчичный газ
- Ванилин
наименований и формул органических соединений, начинающихся с A
Это список органических соединений и их формул, названия которых начинаются с буквы А.
Абиетан — C 20 H 36
Абиетиновая кислота — C 20 H 30 O 2
Аценафтен — C 12 H 10
Аценафтохинон — C 12 H 6 O 2
Аценафтилен — C 12 H 8
Ацепромазин — C 19 H 22 N 2 OS
Ацеталь (1,1-диэтоксиэтан) — C 6 H 14 O 2
Ацетальдегид — C 2 H 4 O
Тример ацетальдегида аммиака — C 6 H 15 N 3
Ацетамид — C 2 H 5 NO
Ацетаминофен — C 8 H 9 NO 2
Ацетаминофен (модель с шариком и клюшкой) — C 8 H 9 NO 2
Ацетаминосалол — C 15 H 13 NO 4
Ацетамиприд — C 10 H 11 ClN 4
Ацетанилид — C 90 021 6 H 5 NH (COCH 3 )
Уксусная кислота — CH 3 COOH
Ацетогуанамин — C 4 H 7 N 5
Ацетон — CH 3 COCH 3 или (CH 3 ) 2 CO
Ацетон (модель, заполняющая пространство) — CH 3 COCH 3 или (CH 3 ) 2 CO
Ацетонитрил — C 2 H 3 N
Ацетофенон — C 8 H 8 O
Ацетилхлорид — C 2 H 3 ClO
Ацетилхолин — (CH 3 ) 3 N + CH 2 CH 2 OCOCH 3 .
Ацетилен — C 2 H 2
N-Ацетилглутамат — C 7 H 11 NO 5
Ацетилсалициловая кислота — C 9 H 8 O 4 (также известный как аспирин)
Кислый фуксин — C 20 H 17 N 3 Na 2 O 9 S 3
Акридин — C 13 H 9 N
Акридиновый оранжевый — C 17 H 19 N 3
Акролеин — C 3 H 4 O
Акриламид — C 3 H 5 NO
Акриловая кислота — C 3 H 4 O 2
Акрилонитрил — C 3 H 3 N
Акрилоилхлорид — C 3 H 3 ClO
Ацикловир — C 8 H 11 N 5 O 3
Адамантан — C 10 H 16
Аденозин — C 10 H 13 N 5 O 4
Адипамид — C 6 H 12 N 2 O 2
Адипиновая кислота — C 6 H 10 O 4
Адипонитрил — C 6 H 8 N 2
Адипоил дихлорид — C 6 H 8 Cl 2 O 2
Адонитол — C 5 H 12 O 5
Адренохром — C 9 H 9 NO 3
Адреналин (адреналин) — C 9 H 13 NO 3
Афлатоксин
AIBN (2-2′-азобисизобутиронитрил)
Аланин — C 3 H 7 NO 2
D-аланин — C 3 H 7 NO 2
L-аланин — C 3 H 7 NO 2
Альбумины
синий альциан — C 56 H 58 Cl 14 CuN 16 S 4
Альдостерон — C 21 H 28 O 5
Альдрин — C 12 H 8 Cl 6
Аликват 336 — C 25 H 54 ClN
Ализарин — C 14 H 8 O 4
Аллантоиновая кислота — C 4 H 8 N 4 O 4
Аллантоин — C 4 H 6 N 4 O 3
Allegra — C 32 H 39 NO 4
Аллетрин
Аллилпропилдисульфид — C 6 H 12 S 2
Аллиламин — C 3 H 7 N
Аллилхлорид — C 3 H 5 Cl
Общая структура амида
Амидный черный 10b — C 22 H 14 N 6 Na 2 O 9 S 2
п-Аминобензойная кислота (ПАБК) — C 7 H 7 NO 2
Аминоэтилпиперазин — C 6 H 15 N 3
5-амино-2-гидроксибензойная кислота — C 7 H 90 021 7 NO 3
Аминофиллин — C 16 H 24 N 10 O 4
5-аминосалициловая кислота — C 7 H 7 NO 3
Аминотиазол — C 3 H 4 N 2 S
Амиодарон — C 25 H 29 I 2 NO 3
Amiton — C 10 H 24 NO 3 PS
Amobarbital — C 11 H 18 N 2 O 3
Амоксициллин — C 16 H 19 N 3 O 5 S.3H 2 O
Амфетамин — C 9 H 13 N
Амилнитрат — C 5 H 11 NO 3
Амилнитрит — C 5 H 11 NO 2
Анандамид — C 22 H 37 NO 2
Анетол — C 10 H 12 O
Ангелиновая кислота — C 5 H 8 O 2
Анилазин — C 9 H 5 Cl 3 N 4
Анилин — C 6 H 5 -NH 2 / C 6 H 7 N
Гидрохлорид анилина — C 6 H 8 ClN
Анисальдегид — C 8 H 8 O 2
Анизол — C 6 H 5 OCH 2
Анизоилхлорид — C 8 H 7 ClO 2
Антантрен — C 22 H 12
антрацен — (C 6 H 4 CH) 2 90 022
Антрамин — C 14 H 11 N
Антраниловая кислота — C 7H7 NO 2
Антрахинон — C 14 H 8 O 2
Антрон — C 14 H 10 O
Антипирин — C 11 H 12 N 2 O
Апротинин — C 284 H 432 N 84 O 79 S 7
Арабиноза — C 5 O 10 H 5
Аргинин — C 6 H 14 N 4 O 2
D-аргинин — C 6 H 14 N 4 O 2
L-аргинин — C 6 H 14 N 4 O 2
Aroclor (полихлорированные дифенилы) — C 12 H 10-x Cl x , где x> 1
Arsole — C 4 H 5 As
Аскорбиновая кислота (витамин C) — C 6 H 8 O 6
Аспараги ne — C 4 H 8 N 2 O 3
D-аспарагин — C 4 H 8 N 2 O 3
L-аспарагин — C 4 H 8 N 2 O 3
Аспарагусная кислота — C 4 H 6 O 2 S 2
Аспартам — C 14 H 18 N 2 O 5
Аспарагиновая кислота — C 4 H 7 NO 4
D-аспарагиновая кислота — C 4 H 7 NO 4
L-аспарагиновая кислота — C 4 H 7 NO 4
Аспидофрактинин — C 19 H 24 N 2
Асфидофитидин — C 17 H 22 ClN 3
Аспидоспермидин — C 19 H 26 N 2
Astra синий C 47 H 52 CuN 14 O 6 S 3
Атразин — C 8 9 0022 H 14 ClN 5
Аурамин O — C 8 H 14 ClN 5
Ауреин — C 18 H 25 NO 5
Аурин — C 19 H 14 O 3
Авобензон — C 20 H 22 O 3
Азадирахтин — C 35 H 44 O 16
Азатиоприн — C 9 H 7 N 7 O 2 S
Азелаиновая кислота — C 9 H 16 O 4
Азепан — C 6 H 13 N
Азинфос-метил — C 10 H 12 N 3 O 3 PS 2
Азиридин — C 2 H 5 N
Азитромицин — C 38 H 72 N 2 O 12
2-2′-азобисизобутиронитрил (AIBN)
Азобензол — C 12 H 9 N 3 O 4
Азобензол — C 1 2 H 10 N 2
Азулен — C 10 H 8
Azure A — C 14 H 14 ClN 3 S
2.5 органических соединений, необходимых для функционирования человека — анатомия и физиология
Цели обучения
К концу этого раздела вы сможете:
- Определение органических молекул, необходимых для функционирования человека
- Объясните химию, лежащую в основе сродства углерода к ковалентным связям в органических соединениях
- Приведите примеры углеводов и определите основные функции углеводов в организме
- Обсудить липиды, важные для функционирования человека
- Опишите структуру белков и обсудите их важность для функционирования человека
- Определить строительные блоки нуклеиновых кислот и роль ДНК, РНК и АТФ в функционировании человека
Органические соединения обычно состоят из групп атомов углерода, ковалентно связанных с водородом, обычно с кислородом, а также часто с другими элементами.Созданные живыми существами, они встречаются по всему миру, в почвах и морях, в промышленных продуктах и в каждой клетке человеческого тела. Четыре типа, наиболее важные для структуры и функций человека, — это углеводы, липиды, белки и нуклеотиды. Прежде чем исследовать эти соединения, вам нужно сначала понять химию углерода.
Химия углерода
То, что делает органические соединения повсеместными, — это химический состав их углеродного ядра. Вспомните, что атомы углерода имеют четыре электрона в валентной оболочке и что правило октетов диктует, что атомы имеют тенденцию реагировать таким образом, чтобы заполнить свою валентную оболочку восемью электронами.Атомы углерода не завершают свою валентную оболочку, отдавая или принимая четыре электрона. Вместо этого они легко обмениваются электронами через ковалентные связи.
Обычно атомы углерода делятся с другими атомами углерода, часто образуя длинную углеродную цепочку, называемую углеродным скелетом. Однако, когда они делятся, они не делят все свои электроны исключительно друг с другом. Скорее, атомы углерода имеют тенденцию делить электроны с множеством других элементов, одним из которых всегда является водород. Углеродные и водородные группы называются углеводородами.Если вы изучите фигуры органических соединений в оставшейся части этой главы, вы увидите несколько с цепочками углеводородов в одной области соединения.
Для заполнения четырех «вакансий» углерода возможно множество комбинаций. Углерод может делить электроны с кислородом, азотом или другими атомами в определенной области органического соединения. Более того, атомы, с которыми связаны атомы углерода, также могут быть частью функциональной группы. Функциональная группа представляет собой группу атомов, связанных прочными ковалентными связями, которые, как правило, действуют в химических реакциях как единое целое.Вы можете думать о функциональных группах как о сплоченных «кликах», члены которых вряд ли разделятся. Для физиологии человека важны пять функциональных групп: гидроксильная, карбоксильная, амино, метильная и фосфатная группы (таблица 2.1).
| Функциональная группа | Структурный Формула | Важность |
| Гидроксил | —O — H | Гидроксильные группы полярны. Они являются компонентами всех четырех типов органических соединений, обсуждаемых в этой главе.Они участвуют в реакциях дегидратационного синтеза и гидролиза. |
| Карбоксил | О-С-ОН | Карбоксильные группы находятся в жирных кислотах, аминокислотах и многих других кислотах. |
| Амино | —N — H 2 | Аминогруппы находятся в аминокислотах, строительных блоках белков. |
| метил | —C — H 3 | Метильные группы находятся в аминокислотах. |
| Фосфат | —P — O 4 2– | Фосфатные группы обнаружены в фосфолипидах и нуклеотидах. |
Сродство углерода к ковалентным связям означает, что многие отдельные и относительно стабильные органические молекулы легко образуют более крупные и сложные молекулы. Любая большая молекула обозначается как макромолекула (макро- = «большой»), и все органические соединения в этом разделе соответствуют этому описанию.Однако некоторые макромолекулы состоят из нескольких «копий» единичных единиц, называемых мономером (моно- = «один»; -мер = «часть»). Подобно бусам в длинном ожерелье, эти мономеры связываются ковалентными связями с образованием длинных полимеров (поли- = «много»). Среди органических соединений много примеров мономеров и полимеров.
Мономеры образуют полимеры путем дегидратационного синтеза (см. Рисунок 2.4.1). Как было отмечено ранее, в результате этой реакции выделяется молекула воды. Каждый мономер вносит свой вклад; один отдает атом водорода, а другой отдает гидроксильную группу.Полимеры разделяются на мономеры путем гидролиза (-lysis = «разрыв»). Связи между их мономерами разрываются из-за пожертвования молекулы воды, которая вносит атом водорода в один мономер и гидроксильную группу в другой.
Углеводы
Термин углевод означает «гидратированный углерод». Напомним, что корень гидро- указывает на воду. Углевод представляет собой молекулу, состоящую из углерода, водорода и кислорода; в большинстве углеводов водород и кислород находятся в тех же относительных пропорциях два к одному, что и в воде.Фактически, химическая формула «общей» молекулы углевода: (CH 2 O) n .
Углеводы называются сахаридами, что означает «сахара». В организме важны три формы: моносахариды, дисахариды и полисахариды. Моносахариды — это мономеры углеводов. Дисахариды (ди- = «два») состоят из двух мономеров. Полисахариды представляют собой полимеры и могут состоять из сотен и тысяч мономеров.
Моносахариды
Моносахарид представляет собой мономер углеводов. Для организма важны пять моносахаридов. Три из них представляют собой гексозные сахара, названные так потому, что каждый из них содержит шесть атомов углерода. Это глюкоза, фруктоза и галактоза, показанные на рис. 2.5.1 a . Остальные моносахариды — это два пентозных сахара, каждый из которых содержит пять атомов углерода. Это рибоза и дезоксирибоза, показанные на рисунке 2.5.1 б .
Рисунок 2.5.1 Пять важных моносахаридов
Дисахариды
Дисахарид представляет собой пару моносахаридов. Дисахариды образуются путем дегидратационного синтеза, и связывающая их связь называется гликозидной связью (глико- = «сахар»). Три дисахарида (показаны на рисунке 2.5.2) важны для человека. Это сахароза, обычно называемая столовым сахаром, лактозой или молочным сахаром, и мальтоза или солодовый сахар.Как вы можете понять по их обычным названиям, вы потребляете их в своем рационе, однако ваше тело не может использовать их напрямую. Вместо этого в пищеварительном тракте они расщепляются на составляющие их моносахариды посредством гидролиза.
Рисунок 2.5.2 — Три важных дисахарида: Все три важных дисахарида образуются путем дегидратационного синтеза.
Внешний веб-сайт
Посмотрите это видео, чтобы понаблюдать за образованием дисахарида. Что происходит, когда вода встречает гликозидную связь?
Полисахариды
Полисахариды могут содержать от нескольких до тысячи и более моносахаридов.Для организма важны три (рис. 2.5.3):
- Крахмалы — это полимеры глюкозы. Они образуются в виде длинных цепочек, называемых амилозой, или разветвленных цепей, называемых амилопектином, которые хранятся в растительной пище и относительно легко перевариваются.
- Гликоген также представляет собой полимер глюкозы, но он хранится в тканях животных, особенно в мышцах и печени. Он не считается диетическим углеводом, потому что после убоя в тканях животных остается очень мало гликогена, однако человеческий организм сохраняет избыток глюкозы в виде гликогена, опять же, в мышцах и печени.
- Целлюлоза, полисахарид, который является основным компонентом клеточной стенки зеленых растений, является компонентом растительной пищи, называемым «клетчаткой». У людей целлюлоза / клетчатка не усваиваются, однако пищевые волокна имеют много преимуществ для здоровья. Это помогает вам чувствовать себя сытым, поэтому вы меньше едите, способствует здоровому пищеварительному тракту, а диета с высоким содержанием клетчатки, как считается, снижает риск сердечных заболеваний и, возможно, некоторых форм рака.
Рисунок 2.5.3 — Три важных полисахарида: Три важных полисахарида — это крахмалы, гликоген и клетчатка.
Функции углеводов
Организм получает углеводы из растительной пищи. Зерновые, фрукты, бобовые и другие овощи обеспечивают большую часть углеводов в рационе человека, хотя лактоза содержится в молочных продуктах.
Хотя большинство клеток организма могут расщеплять другие органические соединения в качестве топлива, все клетки организма могут использовать глюкозу. Более того, нервные клетки (нейроны) головного и спинного мозга и периферической нервной системы, а также эритроциты могут использовать глюкозу только в качестве топлива.При расщеплении глюкозы для получения энергии образуются молекулы аденозинтрифосфата, более известного как АТФ. Аденозинтрифосфат (АТФ) состоит из сахара-рибозы, основания аденина и трех фосфатных групп. АТФ высвобождает свободную энергию, когда его фосфатные связи разрываются, и, таким образом, поставляет готовую энергию клетке. В присутствии кислорода (O2) вырабатывается больше АТФ, чем в путях, не использующих кислород. Общая реакция преобразования энергии глюкозы в энергию, запасенную в АТФ, может быть записана:
C 6 H 12 O 6 + 6 O 2 → 6 CO 2 + 6 H 2 O + ATP
Углеводы не только являются важным источником топлива, но и присутствуют в структуре клеток в очень малых количествах.Например, некоторые молекулы углеводов связываются с белками с образованием гликопротеинов, а другие соединяются с липидами с образованием гликолипидов, оба из которых находятся в мембране, которая окружает содержимое клеток организма.
Липиды
A липид — одно из очень разнообразных соединений, состоящих в основном из углеводородов. Немногочисленные атомы кислорода, которые они содержат, часто находятся на периферии молекулы. Их неполярные углеводороды делают все липиды гидрофобными.В воде липиды не образуют настоящий раствор, но они могут образовывать эмульсию, что является термином для смеси растворов, которые плохо смешиваются.
Триглицериды
Триглицерид — одна из наиболее распространенных групп пищевых липидов, наиболее часто встречающаяся в тканях организма. Это соединение, которое обычно называют жиром, образуется в результате синтеза двух типов молекул (рис. 2.5.4):
- Глицериновая основа в основе триглицеридов, состоящая из трех атомов углерода.
- Три жирные кислоты, длинные цепи углеводородов с карбоксильной группой и метильной группой на противоположных концах, отходящие от каждого из атомов углерода глицерина.
Рисунок 2.5.4 — Триглицериды: Триглицериды состоят из глицерина, присоединенного к трем жирным кислотам посредством синтеза дегидратации. Обратите внимание, что глицерин отдает атом водорода, а каждая карбоксильная группа жирных кислот отдает гидроксильную группу.
Триглицериды образуются посредством синтеза дегидратации. Глицерин отдает атомы водорода из своих гидроксильных групп по каждой связи, а карбоксильная группа на каждой цепи жирной кислоты отдает гидроксильную группу.Таким образом высвобождаются три молекулы воды.
Цепи жирных кислот, которые не имеют двойных углеродных связей по длине и, следовательно, содержат максимальное количество атомов водорода, называются насыщенными жирными кислотами. Эти прямые жесткие цепи плотно соединяются друг с другом и при комнатной температуре являются твердыми или полутвердыми (рис. 2.5.5 a ). Например, масло и сало, а также жир, который содержится в стейке или в вашем собственном теле. Напротив, жирные кислоты с одной двойной углеродной связью изогнуты по этой связи (Рисунок 2.5.5 b ). Следовательно, эти мононенасыщенные жирные кислоты не могут плотно упаковываться вместе и являются жидкими при комнатной температуре. Полиненасыщенные жирные кислоты содержат две или более двойных углеродных связи и также являются жидкими при комнатной температуре. Растительные масла, такие как оливковое масло, обычно содержат как моно-, так и полиненасыщенные жирные кислоты.
Рисунок 2.5.5 — Формы жирных кислот: Уровень насыщения жирной кислоты влияет на ее форму. (а) Цепи насыщенных жирных кислот прямые. (b) Цепи ненасыщенных жирных кислот перекручены.
В то время как диета с высоким содержанием насыщенных жирных кислот увеличивает риск сердечных заболеваний, считается, что диета с высоким содержанием ненасыщенных жирных кислот снижает риск. Это особенно верно в отношении ненасыщенных жирных кислот омега-3, содержащихся в холодноводной рыбе, такой как лосось. Эти жирные кислоты имеют свою первую двойную углеродную связь у третьего углеводорода от метильной группы (называемого омега-концом молекулы).
Наконец, транс жирные кислоты, содержащиеся в некоторых обработанных пищевых продуктах, в том числе в некоторых маргаринах в палочках и бочках, считаются даже более вредными для сердца и кровеносных сосудов, чем насыщенные жирные кислоты. Trans жиры создаются из ненасыщенных жирных кислот (таких как кукурузное масло) при химической обработке для получения частично гидрогенизированных жиров.
Как группа, триглицериды являются основным источником топлива для организма. Когда вы спите или отдыхаете, большая часть энергии, используемой для поддержания вашей жизни, поступает из триглицеридов, хранящихся в ваших жировых (жировых) тканях. Триглицериды также способствуют длительной и медленной физической активности, такой как садоводство или походы, и дают небольшой процент энергии для энергичной физической активности.Пищевой жир также способствует усвоению и транспортировке неполярных жирорастворимых витаминов A, D, E и K. Кроме того, накопленный телесный жир защищает и смягчает кости и внутренние органы тела, а также действует как изоляция для сохранения тепла тела.
Жирные кислоты также являются компонентами гликолипидов, которые представляют собой соединения сахара и жира, обнаруженные в клеточной мембране. Липопротеины — это соединения, в которых гидрофобные триглицериды упакованы в белковые оболочки для транспортировки в жидкостях организма.
Фосфолипиды
Как следует из названия, фосфолипид представляет собой связь между глицериновым компонентом липида и молекулой фосфора.Фактически, фосфолипиды похожи по структуре на триглицериды. Однако вместо трех жирных кислот фосфолипид образуется из диглицерида, глицерина с двумя цепями жирных кислот (рис. 2.5.6). Третий сайт связывания на глицерине захватывается фосфатной группой, которая, в свою очередь, присоединяется к полярной «головной» области молекулы. Напомним, что триглицериды неполярны и гидрофобны. Это все еще справедливо для жирнокислотной части фосфолипидного соединения. Однако головка фосфолипида содержит заряды на фосфатных группах, а также на атоме азота.Эти заряды делают головку фосфолипида гидрофильной. Поэтому говорят, что фосфолипиды имеют гидрофобные хвосты, содержащие нейтральные жирные кислоты, гидрофильные головки, заряженные фосфатные группы и атом азота.
Рисунок 2.5.6 — Другие важные липиды: (a) Фосфолипиды состоят из двух жирных кислот, глицерина и фосфатной группы. (б) Стерины представляют собой липиды кольцевой формы. Здесь показан холестерин. (c) Простагландины получают из ненасыщенных жирных кислот. Простагландин E2 (PGE2) включает гидроксильные и карбоксильные группы.
Стероиды
Стероидное соединение (называемое стеролом) имеет в качестве своей основы набор из четырех углеводородных колец, связанных с множеством других атомов и молекул (см. Рис. 2.5.6 b ). Хотя и растения, и животные синтезируют стерины, наиболее важный вклад в структуру и функции человека вносит холестерин, который синтезируется печенью человека и животных и также присутствует в большинстве продуктов животного происхождения. Как и другие липиды, углеводороды холестерина делают его гидрофобным, однако он имеет полярную гидроксильную головку, которая является гидрофильной.Холестерин — важный компонент желчных кислот и соединений, которые помогают эмульгировать диетические жиры. Фактически, корень этого слова — холе — относится к желчи. Холестерин также является строительным материалом для многих гормонов, сигнальных молекул, которые организм высвобождает для регулирования процессов на удаленных участках. Наконец, как и фосфолипиды, молекулы холестерина находятся в клеточной мембране, где их гидрофобные и гидрофильные участки помогают регулировать поток веществ в клетку и из нее.
Простагландины
Подобно гормону, простагландин является одной из группы сигнальных молекул, но простагландины являются производными ненасыщенных жирных кислот (см. Рисунок 2.5.6 c ). Одна из причин того, что жирные кислоты омега-3, содержащиеся в рыбе, полезны, заключается в том, что они стимулируют выработку определенных простагландинов, которые помогают регулировать аспекты артериального давления и воспаления и тем самым снижают риск сердечных заболеваний. Простагландины также повышают чувствительность нервов к боли. Один класс обезболивающих, называемых нестероидными противовоспалительными препаратами (НПВП), снижает действие простагландинов.
Белки
Вы можете ассоциировать белки с мышечной тканью, но на самом деле белки являются важнейшими компонентами всех тканей и органов.Белок представляет собой органическую молекулу, состоящую из аминокислот, связанных пептидными связями. Белки включают кератин в эпидермисе кожи, который защищает подлежащие ткани, и коллаген, находящийся в дерме кожи, в костях и мозговых оболочках, покрывающих головной и спинной мозг. Белки также являются компонентами многих функциональных химических веществ организма, включая пищеварительные ферменты в пищеварительном тракте, антитела, нейротрансмиттеры, которые нейроны используют для связи с другими клетками, и гормоны на основе пептидов, которые регулируют определенные функции организма (например, гормон роста ).В то время как углеводы и липиды состоят из углеводородов и кислорода, все белки также содержат азот (N), а многие из них содержат серу (S), помимо углерода, водорода и кислорода.
Микроструктура белков
Белки — это полимеры, состоящие из азотсодержащих мономеров, называемых аминокислотами. Аминокислота представляет собой молекулу, состоящую из аминогруппы и карбоксильной группы вместе с вариабельной боковой цепью. Всего 20 различных аминокислот вносят вклад почти во все тысячи различных белков, важных в структуре и функциях человека.Белки организма содержат уникальную комбинацию от нескольких десятков до нескольких сотен из этих 20 аминокислотных мономеров. Все 20 этих аминокислот имеют схожую структуру (рис. 2.5.7). Все они состоят из центрального атома углерода, с которым связаны:
- атом водорода
- щелочная (основная) аминогруппа Nh3 (см. Таблицу 2.1)
- кислая карбоксильная группа COOH (см. Таблицу 2.1)
- группа переменных
Рисунок 2.5.7 Структура аминокислоты
Обратите внимание, что все аминокислоты содержат как кислоту (карбоксильная группа), так и основание (аминогруппа) (амин = «азотсодержащий»).По этой причине они создают отличные буферы, помогая организму регулировать кислотно-щелочной баланс. Что отличает 20 аминокислот друг от друга, так это их вариабельная группа, которая называется боковой цепью или R-группой. Эта группа может различаться по размеру и может быть полярной или неполярной, что придает каждой аминокислоте свои уникальные характеристики. Например, боковые цепи двух аминокислот — цистеина и метионина — содержат серу. Сера не участвует в водородных связях, в отличие от всех других аминокислот.Это изменение влияет на способ сборки белков, содержащих цистеин и метионин.
Аминокислоты соединяются посредством синтеза дегидратации с образованием белковых полимеров (рис. 2.5.8). Уникальная связь, удерживающая аминокислоты вместе, называется пептидной связью. Пептидная связь представляет собой ковалентную связь между двумя аминокислотами, которая образуется путем дегидратационного синтеза. Пептид, по сути, представляет собой очень короткую цепочку аминокислот. Нити, содержащие менее примерно 100 аминокислот, обычно называют полипептидами, а не белками.
Рисунок 2.5.8 — Структура аминокислоты: Различные аминокислоты соединяются вместе, образуя пептиды, полипептиды или белки посредством синтеза дегидратации. Связи между аминокислотами представляют собой пептидные связи.
Организм способен синтезировать большинство аминокислот из компонентов других молекул, однако девять не могут быть синтезированы и должны потребляться с пищей. Они известны как незаменимые аминокислоты.
Считается, что
свободных аминокислот, доступных для построения белков, находятся в пуле аминокислот внутри клеток.Структуры внутри клетки используют эти аминокислоты при сборке белков. Однако, если конкретная незаменимая аминокислота недоступна в достаточном количестве в аминокислотном пуле, синтез белков, содержащих ее, может замедлиться или даже прекратиться.
Форма белков
Подобно тому, как вилкой нельзя есть суп и ложку нельзя использовать для разделки мяса, форма белка важна для его функции. Форма белка в основном определяется последовательностью аминокислот, из которых он состоит (рис. 2.5.9 a ). Последовательность называется первичной структурой белка.
Рисунок 2.5.9 — Форма белков: (a) Первичная структура — это последовательность аминокислот, составляющих полипептидную цепь. (b) Вторичная структура, которая может принимать форму альфа-спирали или бета-складчатого листа, поддерживается водородными связями между аминокислотами в различных областях исходной полипептидной цепи. (c) Третичная структура возникает в результате дальнейшего складывания и связывания вторичной структуры.(d) Четвертичная структура возникает в результате взаимодействий между двумя или более третичными субъединицами. Показанный здесь пример — гемоглобин, белок красных кровяных телец, который транспортирует кислород к тканям тела.
Хотя некоторые полипептиды существуют в виде линейных цепей, большинство из них скручены или свернуты в более сложные вторичные структуры, которые образуются, когда происходит связывание между аминокислотами с разными свойствами в разных областях полипептида. Наиболее распространенная вторичная структура — это спираль, называемая альфа-спиралью.Если вы возьмете веревку и просто скрутите ее в спираль, она не сможет удерживать форму. Точно так же цепочка аминокислот не могла бы поддерживать стабильную спиральную форму без помощи водородных связей, которые создают мосты между различными участками одной и той же цепи (см. Рис. 2.5.9 b ). Реже полипептидная цепь может образовывать бета-складчатый лист, в котором водородные связи образуют мостики между различными областями одного полипептида, который сам на себя свернут, или между двумя или более соседними полипептидными цепями.
Вторичная структура белков затем складывается в компактную трехмерную форму, называемую третичной структурой белка (см. Рис. 2.5.9 c ). В этой конфигурации аминокислоты, которые были очень далекими в первичной цепи, могут быть доставлены довольно близко через водородные связи или, в белках, содержащих цистеин, через дисульфидные связи. Дисульфидная связь представляет собой ковалентную связь между атомами серы в полипептиде. Часто два или более отдельных полипептида связываются с образованием еще более крупного белка с четвертичной структурой (см. Рисунок 2.5.9 д ). Полипептидные субъединицы, образующие четвертичную структуру, могут быть одинаковыми или разными. Например, гемоглобин, белок, содержащийся в красных кровяных тельцах, состоит из четырех третичных полипептидов, два из которых называются альфа-цепями, а два — бета-цепями.
Когда они подвергаются воздействию высоких температур, кислот, оснований и некоторых других веществ, белки денатурируют. Денатурация — это изменение структуры молекулы с помощью физических или химических средств.Денатурированные белки теряют свою функциональную форму и больше не могут выполнять свою работу. Обычным примером денатурации белка является свертывание молока при добавлении кислого лимонного сока.
Трудно переоценить вклад формы белка в его функцию. Например, длинная и тонкая форма белковых нитей, из которых состоит мышечная ткань, важна для их способности сокращаться (укорачиваться) и расслабляться (удлиняться). В качестве другого примера, кости содержат длинные нити белка, называемого коллагеном, который действует как каркас, на котором откладываются костные минералы.Эти удлиненные белки, называемые волокнистыми белками, прочны, долговечны и обычно гидрофобны.
Напротив, глобулярные белки представляют собой глобулы или сферы, которые, как правило, обладают высокой реакционной способностью и гидрофильны. Белки гемоглобина, упакованные в эритроциты, являются примером (см. Рис. 2.59 d ), однако глобулярные белки широко распространены по всему телу, играя критическую роль в большинстве функций организма. Ферменты, ранее введенные в качестве белковых катализаторов, являются примерами этого.В следующем разделе более подробно рассматривается действие ферментов.
Белки действуют как ферменты
Если вы пытались напечатать бумагу и каждый раз, когда вы нажимали клавишу на своем портативном компьютере, вам приходилось ждать шесть или семь минут с задержкой, вы, вероятно, получили бы новый портативный компьютер. Точно так же без ферментов, катализирующих химические реакции, человеческое тело было бы нефункциональным. Он функционирует только потому, что функционируют ферменты.
Ферментативные реакции — химические реакции, катализируемые ферментами, — начинаются, когда субстрат связывается с ферментом.Субстрат является реагентом в ферментативной реакции. Это происходит на участках фермента, известных как активные центры (рис. 2.5.10). Любой фермент катализирует только один тип химической реакции. Эта характеристика, называемая специфичностью, обусловлена тем фактом, что подложка с определенной формой и электрическим зарядом может связываться только с активным центром, соответствующим этой подложке.
Рисунок 2.5.10 — Этапы ферментативной реакции: (a) Субстраты приближаются к активным центрам фермента.(б) Субстраты связываются с активными центрами, образуя комплекс фермент-субстрат. (c) Изменения внутри комплекса фермент-субстрат облегчают взаимодействие субстратов. (d) Продукты высвобождаются, и фермент возвращается в свою первоначальную форму, готовую к другой ферментативной реакции.
Связывание субстрата дает фермент-субстратный комплекс. Вероятно, что ферменты ускоряют химические реакции отчасти потому, что комплекс фермент-субстрат претерпевает набор временных и обратимых изменений, которые заставляют субстраты ориентироваться друг к другу в оптимальном положении, чтобы облегчить их взаимодействие.Это способствует увеличению скорости реакции. Затем фермент высвобождает продукт (продукты) и принимает первоначальную форму. Затем фермент может снова участвовать в процессе, пока остается субстрат.
Другие функции белков
В рекламе протеиновых батончиков, порошков и коктейлей говорится, что белок важен для построения, восстановления и поддержания мышечной ткани, но правда в том, что белки вносят свой вклад во все ткани тела, от кожи до клеток мозга.Кроме того, определенные белки действуют как гормоны и химические посредники, которые помогают регулировать функции организма. Например, гормон роста важен, среди прочего, для роста скелета.
Как было отмечено ранее, основные и кислотные компоненты позволяют белкам действовать в качестве буферов при поддержании кислотно-щелочного баланса, но они также помогают регулировать баланс жидкости и электролитов. Белки притягивают жидкость, и здоровая концентрация белков в крови, клетках и промежутках между клетками помогает обеспечить баланс жидкости в этих различных «отсеках».«Более того, белки клеточной мембраны помогают транспортировать электролиты в клетку и из клетки, поддерживая здоровый баланс этих ионов. Как и липиды, белки могут связываться с углеводами. Таким образом, они могут производить гликопротеины или протеогликаны, которые выполняют множество функций в организме.
Организм может использовать белки для получения энергии, когда потребление углеводов и жиров недостаточное, а запасы гликогена и жировой ткани истощаются. Однако, поскольку нет места для хранения белка, кроме функциональных тканей, использование белка для получения энергии вызывает разрушение тканей и приводит к истощению организма.
Нуклеотиды
Четвертым типом органических соединений, важных для структуры и функций человека, являются нуклеотиды (рис. 2.5.11). Нуклеотид является одним из класса органических соединений, состоящих из трех субъединиц:
- одна или несколько фосфатных групп
- пентозный сахар: дезоксирибоза или рибоза
- азотсодержащее основание: аденин, цитозин, гуанин, тимин или урацил
Нуклеотиды могут быть собраны в нуклеиновые кислоты (ДНК или РНК) или энергетическое соединение аденозинтрифосфат.
Рисунок 2.5.11 — Нуклеотиды: (a) Строительными блоками всех нуклеотидов являются одна или несколько фосфатных групп, пентозный сахар и азотсодержащее основание. (б) Азотсодержащие основания нуклеотидов. (c) Два пентозных сахара ДНК и РНК.
Нуклеиновые кислоты
Нуклеиновые кислоты различаются по типу пентозного сахара. Дезоксирибонуклеиновая кислота (ДНК) — это нуклеотид, хранящий генетическую информацию. ДНК содержит дезоксирибозу (так называемую, потому что она имеет на один атом кислорода меньше, чем рибоза) плюс одну фосфатную группу и одно азотсодержащее основание.«Выбор» основания для ДНК — аденин, цитозин, гуанин и тимин. Рибонуклеиновая кислота (РНК) — это рибозосодержащий нуклеотид, который помогает проявить генетический код в виде белка. РНК содержит рибозу, одну фосфатную группу и одно азотсодержащее основание, но «выбор» основания для РНК — это аденин, цитозин, гуанин и урацил.
Азотсодержащие основания аденин и гуанин классифицируются как пурины. Пурин представляет собой азотсодержащую молекулу с двойной кольцевой структурой, которая вмещает несколько атомов азота.Основания цитозин, тимин (только в ДНК) и урацил (только в РНК) представляют собой пирамидины. Пирамидин представляет собой азотсодержащее основание с одинарной кольцевой структурой
Связи, образованные дегидратационным синтезом между пентозным сахаром одного мономера нуклеиновой кислоты и фосфатной группой другого мономера, образуют «каркас», из которого выступают азотсодержащие основания компонентов. В ДНК два таких скелета прикрепляются к выступающим основаниям посредством водородных связей. Они скручиваются, образуя форму, известную как двойная спираль (Рисунок 2.5.12). Последовательность азотсодержащих оснований в цепи ДНК формирует гены, которые действуют как молекулярный код, инструктирующий клетки по сборке аминокислот в белки. Человеческая ДНК имеет почти 22000 генов, запертых в 46 хромосомах внутри ядра каждой клетки (за исключением красных кровяных телец, которые теряют свои ядра в процессе развития). Эти гены несут в себе генетический код для построения тела и уникальны для каждого человека, кроме однояйцевых близнецов.
Рисунок 2.5.12 — ДНК: В двойной спирали ДНК две цепи соединяются посредством водородных связей между основаниями составляющих нуклеотидов.
Напротив, РНК состоит из одной цепи сахарно-фосфатного остова, усеянной основаниями. Информационная РНК (мРНК) создается во время синтеза белка для передачи генетических инструкций от ДНК к заводам-производителям белка клетки в цитоплазме и рибосомах.
Аденозинтрифосфат
Нуклеотид-аденозинтрифосфат (АТФ) состоит из рибозного сахара, аденинового основания и трех фосфатных групп (рис.13). АТФ классифицируется как высокоэнергетическое соединение, потому что две ковалентные связи, связывающие его три фосфата, хранят значительное количество потенциальной энергии. В организме энергия, высвобождаемая из этих высокоэнергетических связей, помогает подпитывать деятельность организма, от сокращения мышц до транспортировки веществ в клетки и из клеток и до анаболических химических реакций.
Рисунок 2.5.13 Структура аденозинтрифосфата (АТФ)
Когда фосфатная группа отщепляется от АТФ, продуктами являются аденозиндифосфат (АДФ) и неорганический фосфат (P i ).Эту реакцию гидролиза можно записать:
ATP + H 2 O → ADP + P i + энергия
Удаление второго фосфата оставляет аденозинмонофосфат (АМФ) и две фосфатные группы. Опять же, эти реакции также высвобождают энергию, которая была сохранена в фосфатно-фосфатных связях. Они также обратимы, например, когда АДФ подвергается фосфорилированию. Фосфорилирование — это добавление фосфатной группы к органическому соединению, в данном случае с образованием АТФ.В таких случаях тот же уровень энергии, который был высвобожден во время гидролиза, необходимо реинвестировать в синтез энергии при дегидратации.
Клетки также могут передавать фосфатную группу от АТФ к другому органическому соединению. Например, когда глюкоза впервые попадает в клетку, фосфатная группа переносится из АТФ, образуя фосфат глюкозы (C 6 H 12 O 6 -P) и АДФ. Когда глюкоза фосфорилируется таким образом, она может храниться в виде гликогена или метаболизироваться для получения немедленной энергии.
Обзор главы
Органические соединения, необходимые для функционирования человека, включают углеводы, липиды, белки и нуклеотиды. Эти соединения считаются органическими, потому что они содержат как углерод, так и водород. Атомы углерода в органических соединениях легко делятся электронами с водородом и другими атомами, обычно кислородом, а иногда и азотом. Атомы углерода также могут связываться с одной или несколькими функциональными группами, такими как карбоксилы, гидроксилы, амины или фосфаты. Мономеры представляют собой отдельные звенья органических соединений.Они связываются путем дегидратационного синтеза с образованием полимеров, которые, в свою очередь, могут разрушаться при гидролизе.
Углеводные соединения обеспечивают организм жизненно важным топливом. Их структурные формы включают моносахариды, такие как глюкоза, дисахариды, такие как лактоза, и полисахариды, включая крахмалы (полимеры глюкозы), гликоген (форма хранения глюкозы) и клетчатка. Все клетки организма могут использовать глюкозу в качестве топлива. Он превращается через реакцию окисления-восстановления в АТФ.
Липиды — это гидрофобные соединения, которые обеспечивают организм топливом и являются важными компонентами многих биологических соединений.Триглицериды являются наиболее распространенным липидом в организме и состоят из глицериновой основы, присоединенной к трем цепям жирных кислот. Фосфолипиды — это соединения, состоящие из диглицерида с фосфатной группой, присоединенной к голове молекулы. В результате получается молекула с полярными и неполярными областями. Стероиды — это липиды, образованные из четырех углеводородных колец. Самое главное — холестерин. Простагландины — это сигнальные молекулы, полученные из ненасыщенных жирных кислот.
Белки являются важнейшими компонентами всех тканей организма.Они состоят из мономеров, называемых аминокислотами, которые содержат азот, соединенный пептидными связями. Форма белка имеет решающее значение для его функции. Большинство белков тела глобулярны. Примером могут служить ферменты, катализирующие химические реакции.
Нуклеотиды — это соединения с тремя строительными блоками: одна или несколько фосфатных групп, пентозный сахар и азотсодержащее основание. ДНК и РНК — это нуклеиновые кислоты, которые участвуют в синтезе белка. АТФ — это основная молекула организма, передающая энергию.Удаление или добавление фосфатов высвобождает или тратит энергию.
Вопросы по интерактивной ссылке
Посмотрите это видео, чтобы понаблюдать за образованием дисахарида. Что происходит, когда вода встречает гликозидную связь?
Вода гидролизует или разрывает гликозидную связь, образуя два моносахарида.
Контрольные вопросы
Вопросы о критическом мышлении
Если дисахарид мальтоза образован из двух моносахаридов глюкозы, которые представляют собой гексозные сахара, сколько атомов углерода, водорода и кислорода содержит мальтоза и почему?
Мальтоза содержит 12 атомов углерода, но только 22 атома водорода и 11 атомов кислорода, поскольку молекула воды удаляется во время ее образования посредством дегидратационного синтеза.
Почему пищевые жиры перевариваются и всасываются, почему они не могут попадать непосредственно в кровоток?
Все липиды гидрофобны и не могут растворяться в водянистой среде крови. Они упакованы в липопротеины, внешняя белковая оболочка которых позволяет им переносить жиры в кровоток.
органических химикатов | Глоссарий | Marquard & Bahls
Химические вещества — это все химические соединения, производимые химическими процессами в лаборатории или промышленным способом.Это могут быть чистые вещества или смеси веществ. Химические вещества делятся на органических и неорганических химикатов . Органическая химия охватывает практически все углеродсодержащие соединения, в то время как неорганическая химия (неорганические вещества) относится к другим элементам периодической таблицы и их соединениям. Нефтехимия — важный раздел органической химии.
Термин «органическая химия» был введен в 1806 году шведским химиком Йенсом Якобом Берцелиусом и в начале 19 века ограничивался соединениями, которые могут быть образованы живыми организмами.Однако предположение о том, что органические соединения не могут быть произведены синтетическим путем, было окончательно опровергнуто Фридрихом Велером в 1828 году. Велеру удалось синтезировать мочевину (производство мочевины из неорганических веществ).
Только в середине 19 века ученые осознали, что содержание углерода является определяющей характеристикой органического соединения, и границы двух дисциплин — органической и неорганической химии — теперь становятся все более размытыми. Тем не менее, различие по-прежнему полезно, потому что механизмы реакции и структуры материалов часто различаются в неорганической и органической химии.
Органическая химия охватывает около 19 миллионов известных углеродных соединений, что значительно превышает количество известных неорганических соединений (около 500 000). Это связано с особой способностью углерода образовывать разветвленные цепи и кольцевые структуры с другими атомами углерода. Обозначение органических соединений определяется правилами Международного союза теоретической и прикладной химии (IUPAC) и изложено в его «Синей книге». (Неорганические соединения занесены в «Красную книгу».)
Органические химические вещества очень разнообразны.Они варьируются от газообразного метана (природный газ, см. Также газы), простейшего углеводородного соединения, до макромолекулярных пластиков. Они подразделяются на группы материалов, например их функциональными группами или углеродными цепями / скелетами. Функциональные группы включают, например:
- Углеводороды
- Кислород и гидроксисоединения (спирты, альдегиды, карбоновые кислоты, кетоны)
- Соединения азота (амины, амиды, нитросоединения, нитрилы)
- Соединения серы (алкантиолаты, сульфаты)
- Соединения фосфора (фосфаты, фосфины)
- Металлоорганические соединения (ферроцен)
При классификации по углеродной цепи / скелету химические вещества можно далее дифференцировать на алифатические углеводороды (напр.грамм. алканы, алкены), ароматические углеводороды (ароматические соединения), гетероциклы и биохимические соединения (аминокислоты, белки и т. д.).
В зависимости от свойств веществ или химикатов они должны быть соответствующим образом классифицированы, маркированы и упакованы. Аналогичным образом, при их хранении необходимо учитывать химическую совместимость, то есть то, как различные химические вещества будут реагировать друг с другом; см. подробные комментарии в разделе «Химические вещества».
Органическая химия радикально изменила жизнь людей за последние 150 лет.Почти все товары, которые используются ежедневно, содержат органические химические вещества. В настоящее время большинство органических химикатов производится из сырой нефти, при этом сырая нефть и природный газ также используются в качестве сырья при производстве нефтехимических продуктов. В повседневной жизни нас окружают всевозможные продукты на нефтяной основе, которые мы часто принимаем как должное, в том числе мыло, пластмассы, краски, автомобили, оправы для очков, одноразовые подгузники и т. Д. Примерно 5% масла и ежегодно потребляемый газ необходим для производства нефтехимической продукции.