Содержание
7.9 Виды веществ и их агрегатное состояние
С точки зрения физики различные системы,
состоящие из огромного количества
частиц, образуют макроскопические
тела (или макротела).Макротела могут
перемещаться относительно друг друга
по законам динамики. С другой стороны
– макротела обладают свойствами,
обусловленными их микроскопическим
строением, хаотическим движением
микрочастиц.
Свойства макрочастиц характеризуются:
плотностью вещества, давлением,
температурой, химической структурой,
радиоактивностью.
Плотность вещества –
это количество вещества, приходящееся
в среднем на единицу объема тела, т.е.
= m/v, [кг/м3], где m –
масса, кг; v – объем, м3
Плотности известных в настоящее время
веществ находятся в очень широком
диапазоне – от 1017кг/м3(плотности атомных ядер) до
10 –26 кг/м3(плотности газов
межгалактического пространства). Вместе
Вместе
с тем, плотности жидкостей и твердых
тел независимо от степени сжатия лежат
в достаточно узком диапазоне. Это
объясняется плотной “упаковкой” частиц
жидкостей и твердых тел в отличие от
газов. Самый ковкий металл – золото (из
1 г – проволока 2,4 км), самый тугоплавкий
– вольфрам (3420оС), самый твердый
– хром, самый тепло-и электропроводный
– серебро.
Давление – это
сила, действующая со стороны газа или
жидкости на единицу поверхности: т.е.
где F – сила, H ; S – площадь поверхности,
м2
Силы, действующие внутри твердых тел,
характеризуются механическим
напряжением (?). Давление и механическое
напряжение в системе СИ измеряется в
Паскалях (1Па = 1Н/м2)
Температура – это
степень нагретости тела.
Она характеризует интенсивность
теплового движения частиц тела.
Чем больше скорость движения частиц
тела, тем больше скорость движения тела,
тем выше его температура. Абсолютная
температура пропорциональна средней
кинетической энергии поступательного
движения частиц, т. е.
е.
3/2kТ = mv2/2 ,
где v – скорость движения частиц:
k = 1,38 10-23Дж/К – постоянная Больцмана.
При изменении температуры изменяются
некоторые физические свойства тел:
объём, электрическое сопротивление,
интенсивность излучения, вязкость и
др. Например, при температуре жидкого
гелия многие металлы и сплавы становятся
сверхпроводниками, т.е. у них исчезает
электрическое сопротивление. Изменяются
и другие физические характеристики:
свинец становится твердым, как сталь,
а резина – хрупкой как стекло.
За единицу измерения температуры принят
градус. Наряду со стоградусной
шкалой (шкала Цельсия) применяется также
шкалаабсолютных температур,ноль
которой лежит на 273о(округленно)
ниже температуры точки плавления льда.
Величина абсолютной температуры Т = t
+273, где t – температура в оС.
Понятие химической структуры было
рассмотрено в п.6.8, а радиоактивность —
в п.6.5.
С позиций физики, вещество — это вид
материи, обладающий массой покоя. Физика
Физика
различает: аморфное вещество—
твердое вещество, не обладающее
упорядоченным строением;
кристаллическое вещество— твердое
вещество, имеющее периодическое
расположение составляющих его частиц;
оптически активное вещество—
вещество способное вызывать поворот
плоскости поляризации проходящего
через него света;
поверхностно-активное вещество—
вещество, способное адсорбироваться
на поверхности раздела фаз и понижать
их поверхностную энергию;
радиоактивное вещество — вещество,
в котором осуществляется радиоактивный
распад, т.е. когда вещество самопроизвольно
испускает частицы.
Таким образом, физика рассматривает
неорганические вещества в четырех
агрегатных состояниях: газообразном,
жидком, твердом и плазменном.
Химия рассматривает вещество через
понятия химического элемента и соединения.
Взаимосвязь, закономерности и свойства
элементов отражает периодическая
система химических элементов Д.И.
Менделеева.
Биология имеет дело с живыми веществами,
т.е. с совокупностью тел живых организмов,
населяющих землю.
При изучении живых организмов биология
рассматривает биогенные, биокостные,
межклеточные, физиологически активные
вещества.
Биогены (от греч. биос-жизнь,
генос-рождающийся) — вещества, в том
числе химические элементы, абсолютно
необходимые для существования живых
организмов и обязательно входящие в их
состав.
Биокостные вещества— вещества,
создающиеся одновременно живыми
организмами и костными процессами и
являющиеся по формулировке акад. В.И.
Вернадского «закономерной структурой
из живого и костного вещества».
Вещество биокостное особенно характерно
для почвы; фактически все поверхностные
слои Земли (осадочные породы) — результат
преобразования вещества биокостного.
Межклеточное вещество— бесструктурная
аморфная масса, состоящая из тончайших
нитевидных структур (фибрилл), особенно
хорошо развитое в соединительных тканях
и определяющее их структуру.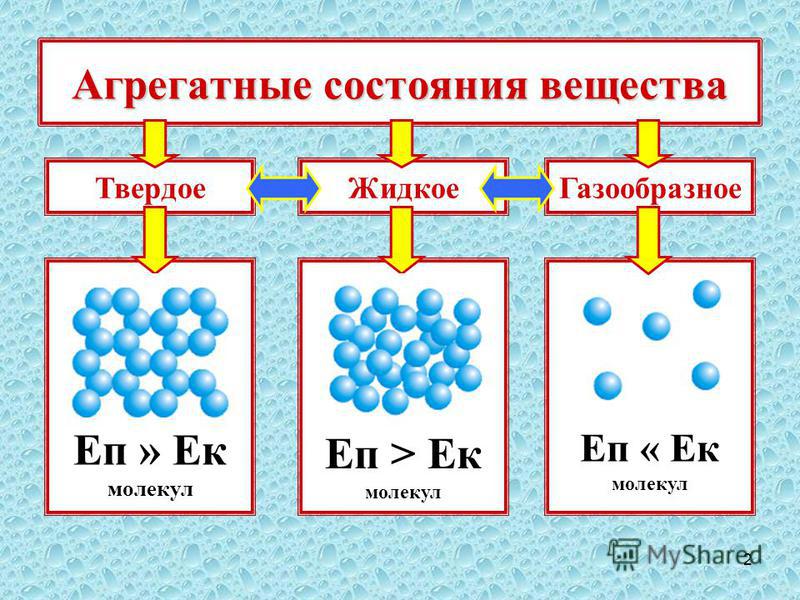
Вещество физиологически активное —
любое вещество, вырабатываемое организмом
и получаемое извне и оказывающее либо
стимулирующее, либо подавляющее
воздействие на происходящие в организме
процессы (биогены, гормоны, ингибиторы,
ферменты и др.)
Например, если бы железо, подобно золоту
и серебру не ржавело, т.е. не окислялось,
то мы бы не существовали, и ни одно
растение на Земле не зеленело. Та же
«ржавчина» снабжает железом нашу
кровь и придает ей красный цвет. Самый
«живой» металл — кальций. В организме
взрослого человека его около 1,5 кГ.
Зубная эмаль — это соединение фосфора.
Щитовидная железа содержит поразительно
много йода и вырабатывает йодосодержащие
гормоны. Много йода содержит лук, яйца,
молоко, морская рыба, морская капуста.
Итак, все окружающее пространство
заполнено физическими телами,
которые образованы различными
веществами. Вещества могут находиться
в твердом, жидком, газообразном и
плазменном состоянии в зависимости от
температуры и давления. Вещества
Вещества
образуются из химических элементов.
Аварийно химические опасные вещества
Аварийно химические опасные вещества (аммиак, хлор). Их воздействие на организм человека. Предельно допустимые и поражающие концентрации
Растет ассортимент применяемых в промышленности, сельском хозяйстве и быту химических веществ. Некоторые из них токсичны и вредны. При проливе или выбросе в окружающую среду способны вызвать массовые поражения людей, животных, приводят к заражению воздуха, почвы, воды, растений. Их называют аварийно химические опасные вещества(АХОВ). Определенные виды АХОВ находятся в больших количествах на предприятиях, их производящих или использующих в производстве. В случае аварии может произойти поражение людей не только непосредственно на объекте, но и за его пределами, в ближайших населенных пунктах.
Крупными запасами опасных веществ располагают предприятия химической, целлюлозно-бумажной, оборонной, нефтеперерабатывающей и нефтехимической промышленности, черной и цветной металлургии, промышленности минудобрений.
Значительные их количества сосредоточены на объектах пищевой, мясо-молочной промышленности, холодильниках, торговых базах, различных АО, в жилищно-коммунальном хозяйстве.
Наиболее распространенными из них являются хлор, аммиак, сероводород, двуокись серы (сернистый газ), нитрил акриловой кислоты, синильная кислота, фосген, метилмеркаптан, бензол, бромистый водород, фтор, фтористый водород.
Хлор
При нормальных условиях газ желто-зеленого цвета с резким раздражающим специфическим запахом. При обычном давлении затвердевает при -101 °С и сжижается при -34° С. Тяжелее воздуха примерно в 2,5 раза. Вследствие этого стелется по земле, скапливается в низинах, подвалах, колодцах, тоннелях.
Ежегодное потребление хлора в мире достигает 40 млн. т.
Используется он в производстве хлорорганических соединений (винил хлорида, хлоропренового каучука, дихлорэтана, хлорбензола и др.). В большинстве случаев применяется для отбеливания тканей и бумажной массы, обеззараживания питьевой воды, как дезинфицирующее средство и в различных других отраслях промышленности.
Хранят и перевозят его в стальных баллонах и железнодорожных цистернах под давлением. При выходе в атмосферу дымит, заражает водоемы.
В первую мировую войну применялся в качестве отравляющего вещества удушающего действия. Поражает легкие, раздражает слизистые и кожу.
Первые признаки отравления — резкая загрудинная боль, резь в глазах, слезоотделение, сухой кашель, рвота, нарушение координации, одышка. Соприкосновение с парами хлора вызывает ожоги слизистой оболочки дыхательных путей, глаз, кожи.
Воздействие в течение 30 — 60 мин при концентрации 100 — 200 мг/м3 опасно для жизни.
Если все-таки произошло поражение хлором, пострадавшего немедленно выносят на свежий воздух, тепло укрывают и дают дышать парами спирта или воды.
При интенсивной утечке хлора используют распыленный раствор кальцинированной соды или воду, чтобы осадить газ. Место разлива заливают аммиачной водой, известковым молоком, раствором кальцинированной соды или каустика с концентрацией 60 —80% и более (примерный расход — 2л раствора на 1 кг хлора).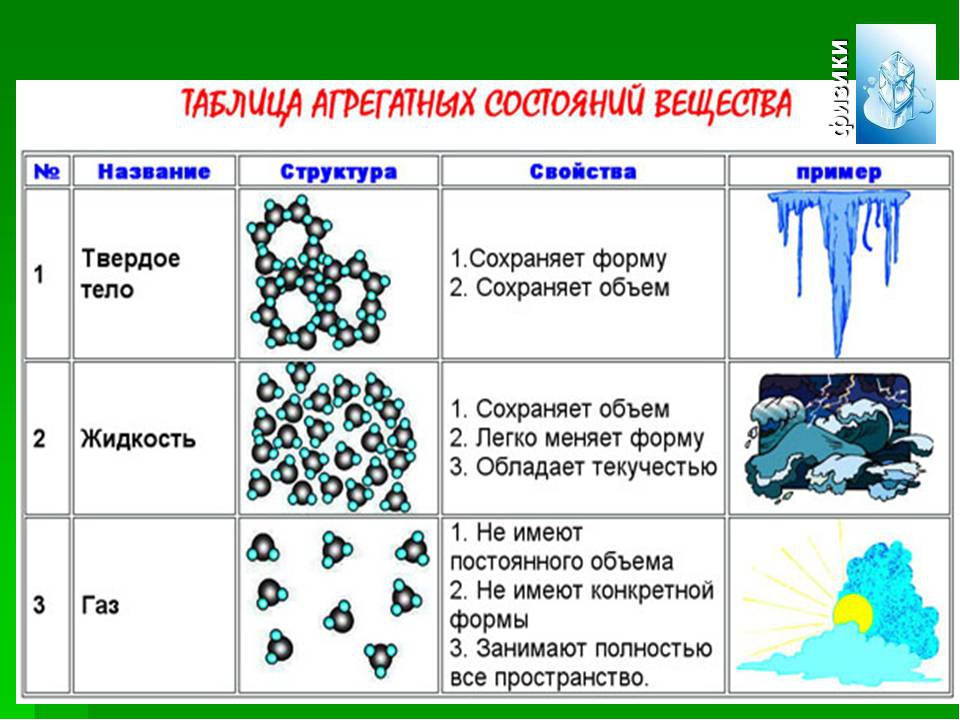
Аммиак
При нормальных условиях бесцветный газ с характерным резким запахом («нашатырного спирта»), почти в два раза легче воздуха. При выходе в атмосферу дымит. При обычном давлении затвердевает при температуре -78°С и сжижается при -34°С. С воздухом образует взрывоопасные смеси в пределах 15 — 28 объемных процентов.
Растворимость его в воде больше, чем у всех других газов: один объем воды поглощает при 20°С около 700 объемов аммиака, 10%-й раствор аммиака поступает в продажу под названием «нашатырный спирт». Он находит применение в медицине и в домашнем хозяйстве (при стирке белья, выведении пятен и т.д.). 18-20%-й раствор называется аммиачной водой и используется как удобрение.
Жидкий аммиак — хороший растворитель большинства органических и неорганических соединений.
Мировое производство аммиака ежегодно составляет около 90 млн.т. Его используют при получении азотной кислоты, азотосодержащих солей, соды, мочевины, синильной кислоты, удобрений, диазотипных светокопировальных материалов. Жидкий аммиак широко применяется в качестве рабочего вещества (хладагента) в холодильных машинах и установках.
Жидкий аммиак широко применяется в качестве рабочего вещества (хладагента) в холодильных машинах и установках.
Перевозится в сжиженном состоянии под давлением. Предельно допустимые концентрации (ПДК) в воздухе населенных мест: среднесуточная и максимально разовая — 0,2 мг/м3, в рабочем помещении промышленного предприятия — 20 мг/м3. Если же его содержание в воздухе достигает 500 мг/м3, он опасен для вдыхания (возможен смертельный исход).
Вызывает поражение дыхательных путей. Признаки: насморк, кашель, затрудненное дыхание, удушье, учащается сердцебиение, нарастает частота пульса. Пары сильно раздражают слизистые оболочки и кожные покровы, вызывают жжение, покраснение и зуд кожи, резь в глазах, слезотечение. При соприкосновении жидкого аммиака и его растворов с кожей возникает обморожение, жжение, возможен ожог с пузырями, изъязвления.
Если поражение аммиаком все же произошло, следует немедленно вынести пострадавшего на свежий воздух. Транспортировать надо в лежачем положении. Необходимо обеспечить тепло и покой, дать увлажненный кислород. При отеке легких искусственное дыхание делать нельзя.
Транспортировать надо в лежачем положении. Необходимо обеспечить тепло и покой, дать увлажненный кислород. При отеке легких искусственное дыхание делать нельзя.
В случае аварии необходимо опасную зону изолировать, удалить людей и не допускать никого без средств защиты органов дыхания и кожи. Около зоны следует находиться с наветренной стороны. Место разлива нейтрализуют слабым раствором кислоты, промывают большим количеством воды. Если произошла утечка газообразного аммиака, то с помощью поливомоечных машин, авторазливочных станций, пожарных машин распыляют воду, чтобы поглотить пары.
Зоны заражения АХОВ
В большинстве случаев при аварии и разрушении емкости давление над жидкими веществами падает до атмосферного, АХОВ вскипает и выделяется в атмосферу в виде газа, пара или аэрозоля. Облако газа (пара, аэрозоля) АХОВ, образовавшееся в момент разрушения емкости в пределах первых 3 минут, называется первичным облаком зараженного воздуха. Оно распространяется на большие расстояния.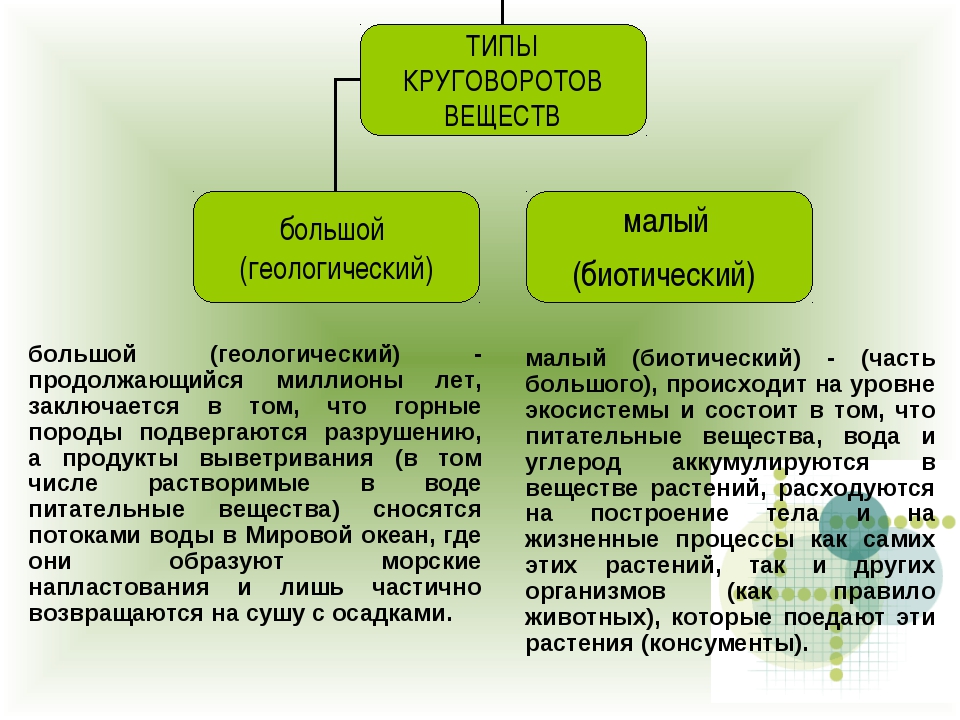 Оставшаяся часть жидкости (особенно с температурой кипения выше 20°С) растекается по поверхности и также постепенно испаряется. Пары (газы) поступают в атмосферу, образуя вторичное облако зараженного воздуха, которое распространяется на меньшее расстояние.
Оставшаяся часть жидкости (особенно с температурой кипения выше 20°С) растекается по поверхности и также постепенно испаряется. Пары (газы) поступают в атмосферу, образуя вторичное облако зараженного воздуха, которое распространяется на меньшее расстояние.
Таким образом, зона заражения АХОВ — это территория, зараженная ядовитыми веществами в опасных для жизни людей пределах (концентрациях).
Глубина зоны распространения зараженного воздуха зависит от концентрации АХОВ и скорости ветра. Например, при ветре 1 м/с за один час облако от места аварии удалится на 5 — 7 км, при 2 м/с — на 10 — 14, а при З м/с — на 16 — 21 км. Значительное увеличение скорости ветра (6-7 м/с и более) способствует его быстрому рассеиванию. Повышение температуры почвы и воздуха ускоряет испарение АХОВ, а следовательно, увеличивает концентрацию его над зараженной территорией. На глубину распространения АХОВ и величину его концентрации в значительной степени влияют вертикальные перемещения воздуха, как мы говорим, погодные условия.
Форма (вид) зоны заражения АХОВ в значительной мере зависит от скорости ветра. Так, например, при скорости менее 0,5 м/с она принимается за окружность, при скорости от 0,6 до 1 м/с — за полуокружность, при скорости от 1,1 м/с до 2 м/ с — за сектор с углом в 90°, при скорости более 2м/с — за сектор с углом в 45°.
Надо иметь в виду, что здания и сооружения городской застройки нагреваются солнечными лучами быстрее, чем расположенные в сельской местности. Поэтому в городе наблюдается интенсивное движение воздуха, связанное обычно с его притоком от периферии к центру по магистральным улицам. Это способствует проникновению АХОВ во дворы, тупики, подвальные помещения и создает повышенную опасность поражения населения. В целом можно считать, что стойкость АХОВ в городе выше, чем на открытой местности.
Вот почему все население, проживающее вблизи химически опасного объекта, должно знать, какие АХОВ используются на этом предприятии, какие ПДК установлены для рабочей зоны производственных помещений и для населенных пунктов, какие меры безопасности требуют неукоснительного соблюдения, какие средства и способы защиты надо использовать в различных аварийных ситуациях.
Защита от АХОВ
Защитой от АХОВ служат фильтрующие промышленные и гражданские противогазы, промышленные респираторы, изолирующие противогазы, убежища ГО.
Промышленные противогазы надежно предохраняют органы дыхания, глаза и лицо от поражения. Однако их используют только там, где в воздухе содержится не менее 18% кислорода, а суммарная объемная доля паро- и газообразных вредных примесей не превышает 0,5%.
Недопустимо применять промышленные противогазы для защиты от низкокипящих, плохо сорбирующихся органических веществ (метан, ацетилен, этилен и др.)
Если состав газов и паров неизвестен или их концентрация выше максимально допустимой, применяется только изолирующие противогазы ИП-4 и ИП-5.
Коробки промышленных противогазов строго специализированы по назначению (по составу поглотителей) и отличаются окраской и маркировкой. Некоторые из них изготавливаются с аэрозольными фильтрами, другие без них. Белая вертикальная полоса на коробке означает, что она оснащена фильтром.
Белая вертикальная полоса на коробке означает, что она оснащена фильтром.
Рассмотрим несколько примеров по основным АХОВ. Для защиты от хлора можно использовать промышленные противогазы марок А (коробка коричневого цвета), БКФ (защитного), В (желтого), Г (половина черная, половина желтая), а также гражданские противогазы ГП-5, ГП-7 и детские.
А если их нет? Тогда ватно-марлевую повязку, смоченную водой, а лучше 2%-м раствором питьевой соды.
От аммиака защищает противогаз с другой коробкой, марки КД (серого цвета) и промышленные респираторы РПГ-67КД, РУ-60МКД.
У них две сменных коробки (слева и справа). Они имеют ту же маркировку, что и противогазы. Надо помнить, что гражданские противогазы от аммиака не защищают. В крайнем случае надо воспользоваться ватно-марлевой повязкой, смоченной водой или 5%-м раствором лимонной кислоты.
Для защиты от АХОВ в очаге аварии используются в основном средства индивидуальной защиты кожи (СИЗК) изолирующего типа, общевойсковой защитный комплект ОЗК.
Для населения рекомендуются подручные средства защиты кожи в комплекте с противогазами. Это могут быть обычные непромокаемые накидки и плащи, а также пальто из плотного толстого материала, ватные куртки. Для ног — резиновые сапоги, боты, калоши. Для рук — все виды резиновых и кожаных перчаток и рукавицы.
В случае аварии с выбросом АХОВ убежища обеспечивают надежную защиту. Во-первых, если неизвестен вид вещества или его концентрация слишком велика, можно перейти на полную изоляцию (третий режим), можно также какое-то время находиться в помещении с постоянным объемом воздуха. Во-вторых, фильтропоглотители защитных сооружений препятствуют проникновению хлора, фосгена, сероводорода и многих других ядовитых веществ, обеспечивая безопасное пребывание людей.
В крайнем случае при распространении газов, которые тяжелее воздуха и стелются по земле, как хлор и сероводород, можно спасаться на верхних этажах зданий, плотно закрыв все щели в дверях, окнах, задраив вентиляционные отверстия.
Выходить из зоны заражения нужно в одну из сторон, перпендикулярную направлению ветра, ориентируясь на показания флюгера, развевание флага или любого другого куска материи, наклон деревьев на открытой местности.
Первая помощь пораженным АХОВ
Она складывается из двух частей. Первая — обязательная для всех случаев поражения, вторая — специфическая, зависящая от характера воздействия вредных веществ на организм человека.
Итак, общие требования. Надо как можно скорее прекратить воздействия АХОВ. Для этого необходимо надеть на пострадавшего противогаз и вынести его на свежий воздух, обеспечить полный покой и создать тепло. Расстегнуть ворот, ослабить поясной ремень. При возможности снять верхнюю одежду, которая может быть заражена парами хлора, сероводорода, фосгена или другого вещества.
Специфические. Например, при поражении хлором, чтобы смягчить раздражение дыхательных путей, следует дать вдыхать аэрозоль 0,5%-го раствора питьевой соды. Полезно также вдыхать кислород. Кожу и слизистые промывать 2%-м содовым раствором не менее 15 мин. Из-за удушающего действия хлора пострадавшему передвигаться самостоятельно нельзя. Транспортируют его только в лежачем положении. Если человек перестал дышать, надо немедленно сделать искусственное дыхание методом «изо рта в рот».
Полезно также вдыхать кислород. Кожу и слизистые промывать 2%-м содовым раствором не менее 15 мин. Из-за удушающего действия хлора пострадавшему передвигаться самостоятельно нельзя. Транспортируют его только в лежачем положении. Если человек перестал дышать, надо немедленно сделать искусственное дыхание методом «изо рта в рот».
При поражении аммиаком пострадавшему следует дышать теплыми водяными парами 10%-го раствора ментола в хлороформе, дать теплое молоко с боржоми или содой. При удушье необходим кислород, при спазме голосовой щели — тепло на область шеи, теплые водяные ингаляции. Если произошел отек легких, искусственное дыхание делать нельзя. Слизистые и глаза промывать не менее 15 мин водой или 2%-м раствором борной кислоты. В глаза закапать 2-3 капли 30%-го раствора альбуцида, в нос — теплое оливковое, персиковое или вазелиновое масло. При поражении кожи обливают чистой водой, накладывают примочки из 5%-го раствора уксусной, лимонной или соляной кислоты.
Виды и действие наркотиков и статистика смертности от них. Справка
Опиаты – наркотики, обладающие седативным, «затормаживающим» действием. К этой группе относятся природные и синтетические морфиноподобные соединения. Все природные наркотические средства опийной группы получают из мака. Вызывают состояние эйфории, спокойствия, умиротворения. Включаясь в обменные процессы, приводят к быстрому возникновению сильнейшей психической и физической зависимости. Крайне разрушительно действуют на организм. Наркотические зависимости, вызываемые опиатами, очень трудно поддаются лечению. К опиатам относятся: героин, маковая соломка, ацетилированный опий, опий-сырец, метадон.
Признаки употребления – непродолжительное состояние эйфории, необычная сонливость в самое разное время; медленная, «растянутая» речь; часто «отстает» от темы и направления разговора; добродушное, покладистое, предупредительное поведение вплоть до полного подчинения; стремление к уединению в тишине, в темноте, несмотря на время суток; бледность кожных покровов; очень узкий зрачок, не реагирующий на изменения освещения; замедление сердцебиения, дыхания, снижение болевой чувствительности; понижение аппетита, жажды, рефлексов и сексуального влечения.
Последствия употребления опиатов – огромный риск заражения ВИЧ-инфекцией и гепатитами из-за использования общих шприцев; поражение печени из-за низкого качества наркотиков: в них остается уксусный ангидрид, который используется при приготовлении; сильное снижение иммунитета и, как следствие, подверженность инфекционным заболеваниям; заболевания вен, разрушение зубов из-за нарушения кальциевого обмена; импотенция; снижение уровня интеллекта. Очень велика опасность передозировки с тяжелыми последствиями, вплоть до смерти.
Препараты конопли. Конопля произрастает в регионах с умеренно теплым климатом. Чем южнее выращено растение, тем больший наркотический эффект вызывает изготовленный из него наркотик. Действующие вещества – каннабиноиды. Воздействие – изменение сознания. В помещении надолго остается характерный запах жженной травы. Сохраняет этот запах и одежда. Самые распространенные препараты конопли: марихуана, гашиш и др.
Признаки употребления препаратов конопли – эйфория, чувство беззаботности; несдержанность, повышенная разговорчивость; состояние сильного голода и жажды, покраснение глаз; при небольшой дозе – расслабленность, обостренное восприятие цвета, звуков, повышенная чувствительность к свету из-за сильно расширенных зрачков; при большой дозе – заторможенность, вялость, сбивчивая речь у одних, агрессивность, с немотивированными действиями у других; безудержная веселость, нарушение координации движений, восприятия размеров предметов и их пространственных отношений, галлюцинации, беспочвенные страхи и паника.
Последствия употребления – неразбериха в мыслях, разочарованность, депрессия и ощущение изолированности; нарушение координации движения, памяти и умственных способностей; замедленное половое развитие и созревание; при приеме большой дозы наркотика могут возникнуть галлюцинации и паранойя; формирование психической зависимости, когда курение не приносит удовлетворения, но становится необходимым; провокация одновременного употребления алкоголя и перехода к более тяжелым наркотикам; бронхит, рак легких.
Амфетамины – наркотики, обладающие психостимулирующим, «возбуждающим» действием. К этой группе относятся синтетические вещества, содержащие соединения амфетамина. В большинстве случаев вводятся внутривенно. Эти наркотики получают из лекарственных препаратов, содержащих эфедрин. В природе эфедрин содержится в растении «эфедра». Действие наркотика продолжается 2-12 часов. Формируется психическая и физическая зависимость. Продолжительное употребление требует постоянного увеличения дозы наркотика. Обостряются вспыльчивость, злобность, агрессивность. Со временем появляется необоснованная тревожность и подозрительность. Возможны попытки суицида. Амфетаминовая наркомания имеет характер «запойной» или «сессионной» – периоды употребления наркотика сменяются «холодными» периодами, продолжительность которых со временем сокращается. Самые распространенные виды амфетаминов: эфедрон, первитин, эфедрин и др.
Признаки употребления – ощущение безмятежности и эйфории; учащение сердечного ритма и повышение кровяного давления; расширение зрачков глаз; излишняя двигательная активность, сильное сексуальное раскрепощение; болтливость, деятельность носит непродуктивный и однообразный характер; отсутствует чувство голода; нарушение режима сна и бодрствования.
Последствия употребления амфетаминов – головокружение, головные боли, ухудшение зрения и сильное потоотделение; инфаркты, инсульты; нервное истощение; сильные изменения психики и необратимые изменения головного мозга; поражения сердечно-сосудистой системы и всех внутренних органов; поражения печени из-за низкого качества наркотиков – в них остается йод, марганцовка и красный фосфор, которые используются при приготовлении наркотика; риск заражения ВИЧ-инфекцией и гепатитами из-за использования общих шприцев; сильное снижение иммунитета, опасность передозировки с тяжелыми последствиями, вплоть до смерти.
Кокаин – психостимулятор растительного происхождения, получаемый из листьев растения коки. Привыкание развивается незаметно, но стойко. Кокаин вымораживает область от глаз до груди – тело становится нечувствительным. Различается на кокаин и крек.
Признаки употребления – вызывает короткое, но интенсивное ощущение эйфории и повышение работоспособности; стимулирует центральную нервную систему; учащенный пульс, дыхание, повышение кровяного давления, потливость; расширение зрачков, отсутствие аппетита; излишняя активность, возбужденность, чувство тревоги, бессонница.
Последствия употребления – аритмия, кровотечения и другие повреждения носовой полости; разрушение слизистой и утрата обоняния, вкуса; глухота; параноидальные психозы, галлюцинации, агрессивность; смерть в результате нарушения сердечной деятельности (инфаркт миокарда) или остановки дыхания.
Галлюциногены – неоднородная по происхождению и химическому составу группа психоделических препаратов, изменяющих сознание – ощущения, мысли, эмоции и восприятие. К ним относятся: ЛСД, псилоцин, псилоцибин и др.
Признаки опьянения – повышенная частота пульса, повышенное давление, расширение зрачков, дрожание рук, сухость кожи. Наркотическое опьянение сопровождается изменением восприятия внешнего мира –те, кто принимает галлюциногены, говорят, что они «видят звуки» и «слышат цвета»; галлюцинации, сильное ощущение счастья, перевозбуждение; нарушения ощущения своего тела, координации движений; утрата самоконтроля.
Последствия употребления – необратимые изменения в структуре головного мозга, психические нарушения различной степени тяжести, вплоть до полного распада личности. Даже однократный прием ЛСД может привести к изменению генетического кода и необратимо повредить головной мозг. Психические нарушения неотличимы от заболевания шизофренией. Наркотик накапливается в клетках мозга. Оставаясь там длительное время, он может и спустя несколько месяцев вызывать те же ощущения, что и непосредственно после приема. Действие наркотика продолжается 2-12 часов. Формируется психическая и физическая зависимость. Продолжительное употребление требует постоянного увеличения дозы наркотика. Обостряются вспыльчивость, злобность, агрессивность. Со временем появляется необоснованная тревожность и подозрительность. Возможны попытки суицида.
Экстази – общее название для группы синтетических наркотиков-стимуляторов амфетаминной группы, часто с галлюциногенным эффектом. Белые, коричневые, розовые и желтые таблетки или разноцветные, часто с рисунками, капсулы содержат около 150 мг препарата. «Экстази» – дорогой наркотик, и обычно его потребители переходят на систематический прием героина или амфетаминов.
Признаки опьянения – наркотическое действие продолжается от 3 до 6 часов. Возбуждается центральная нервная система, повышается тонус организма, увеличивается выносливость, физическая сила. Под действием «экстази» принявший может выдержать экстремальные эмоциональные и физические нагрузки, не спать, не чувствовать усталости. За искусственный «разгон» организма приходится расплачиваться: после прекращения действия наркотика наблюдается состояние апатии, подавленности, сильной усталости, сонливости. Это состояние может продолжаться несколько дней, так как организму требуется восстановить израсходованные силы.
Последствия употребления – психическая зависимость; депрессия, вплоть до самоубийства; физическое и нервное истощение; страдает нервная система, сердце, печень, дистрофия внутренних органов; изменение генетического кода. Возможны смертельные исходы от обезвоживания, перегрева организма, острой почечной недостаточности.
Снотворные – группа седативных (успокаивающих) и снотворных веществ, встречающихся в виде официальных препаратов, обычно таблеток («колеса») или капсул. Существует много разновидностей, наиболее опасны – производные барбатуратовой кислоты, но и другие, более или менее свободно продающиеся в аптеках, могут вызвать психическую и физическую зависимость. Снотворные обычно принимаются внутрь, но иногда их вводят внутривенно. Вызывают сильную зависимость как на физическом, так и на психологическом уровнях. Особенно опасны при использовании вместе с алкоголем.
Признаки опьянения – замешательство, невнятная речь, неуклюжесть, нарушение координации, дезориентация схожие с алкогольным опьянением; агрессивность, грубость, раздражительность, депрессия.
Последствия употребления – стойкая бессонница; повреждение головного мозга, клинически сходное с эпилепсией; психозы с галлюцинациями, бредом преследования; дистрофия сердечной мышцы; истощение печени; смерть от передозировки и от быстрого отказа от больших доз.
Ингалянты – летучие вещества наркотического действия. Содержатся в препаратах бытовой химии: красителях, растворителях, клее, бензине, лаке для волос, средствах от насекомых. Сами по себе они к наркотикам не относятся. Опьяняющее действие возможно, если количество вещества, поступившее в организм, очень велико.
Признаки опьянения – возникновение галлюцинаций; вызывающее, неадекватное поведение; нарушение координации движений.
Последствия употребления – чихание, кашель, насморк, носовые кровотечения, тошнота, нарушение сердечного ритма и боли в области грудной клетки, потеря координации, равновесия; острая интоксикация психоактивными веществами, вплоть до смертельного исхода; токсическое поражение печени через 8‑10 месяцев; необратимое поражение головного мозга; частые и тяжелые пневмонии; изменение характера, отставание в умственном и психическом развитии.
Курительные смеси (или курительные миксы) состоят из трав и экстрактов. Травы, входящие в состав любой курительной смеси, являются энтеогенами и известны человечеству с давних пор.
Исследования специалистов показывают, что употребление курительных смесей с одурманивающим эффектом вызывает психические расстройства. Накурившись, человек теряет способность сосредоточиться, нарушается способность восприятия мира. Человек, выкурив такую сигарету, вдруг начинает беспричинно хохотать, не может общаться с теми, кто рядом. Такие изменения поведения могут длиться долго. По словам главного государственного санитарного врача РФ Геннадия Онищенко, действие курительных смесей способно изменить личность не на время, а навсегда, превратить нормального человека в наркозависимого больного, привести к тяжелой инвалидности.
Статистика потребления
В России, по данным на февраль 2010 года, официально зарегистрировано около 550 тысяч потребителей наркотиков. По экспертным оценкам, эта цифра достигает примерно 2,5 миллиона или составляет почти два процента населения. Ежегодно почти 75 тысяч человек впервые пробуют наркотики, а 30 тысяч – погибают вследствие их потребления. Специализированными наркологическими учреждениями зарегистрировано почти 138 тысяч детей и подростков, страдающих наркологическими расстройствами. Почти 90 процентов наркозависимых потребляют опиаты афганского происхождения.
Согласно докладу экспертов Управления ООН по наркотикам и предупреждению преступности, опубликованному в октябре 2009 года, Россия занимает первое место в мире по потреблению героина, на ее долю приходится 21% всего производимого в мире героина и 5% всех опиумосодержащих наркотиков.
Материал подготовлен на основе информации РИА Новости и открытых источников
КЛАССИФИКАЦИЯ ОПАСНЫХ ХИМИЧЕСКИХ ВЕЩЕСТВ — На букву К — Термины МЧС России
распределение веществ по отдельно избранному признаку, например, по степени их опасности, токсичности, физико-химическим свойствам и т.д. По степени опасности химические вещества подразделяют на: чрезвычайно опасные вещества (I класс), у которых средняя смертельная доза при введении в желудок — менее 15 мг/кг, средняя смертельная концент-рация в воздухе — менее 500 мг/куб. м, коэффициент вероятности ингаляционного отравления (отношение насыщающей концентрации паров вещества в воздухе при 20 °С к средней смертельной концентрации вещества для мышей при 2-часовой экспозиции и 2-недельном сроке наблюдения) — более 300, предельно допустимая концентрация в воздухе рабочей зоны — менее 0,1 мг/куб. м; высоко опасные вещества (II класс), у которых средняя смертельная доза при введении в желудок — от 15 до 150 мг/кг, средняя смертельная концентрация в воздухе — от 500 до 5 000 мг/куб. м, коэффициент вероятности ингаляционного отравления — от 300 до 30, предельно допустимая концентрация в воздухе рабочей зоны — от 0,1 до мг/куб. м; умеренно опасные вещества (III класс), у которых средняя смертельная доза при введении в желудок — от 151 до 5 000 мг/кг, средняя смертельная концентрация в воздухе — от 5 001 до 50 000 мг/куб. м, коэффициент вероятности ингаляционного отравления — от 29 до 3, предельно допустимая концентрация в воздухе рабочей зоны — от 1,1 до 10,0 мг/куб. м; мало опасные вещества (IV класс), у которых средняя смертельная доза при введении в желудок — более 5 000 мг/кг, средняя смертельная концентрация в воздухе — более 50 000 мг/куб. м, коэффициент вероятности ингаляционного отравления — менее 3, предельно допустимая концентрация в воздухе рабочей зоны — более 10,0 мг/куб. м. По характеру действия на организм химические вещества подразделяют на раздражающие, общеядовитые, нейротропные и цитотоксические — см. также Опасное химическое вещество.
Ростехнадзор разъясняет: Вопросы идентификации видов опасных веществ на ОПО
Вопрос от 27.05.2020:
Что понимается под формулировкой «Транспортирование воспламеняющихся, окисляющих, горючих, взрывчатых, токсичных, высокотоксичных веществ и веществ, представляющих опасность для окружающей среды, на объектах»? Каким нормативным актом регламентировано данное понятие? Относятся ли к таким веществам бензин, дизельное топливо, керосин?
Ответ: На данный вопрос ответ дан Управлением общепромышленного надзора Ростехнадзора.
К функциям и полномочиям органов Ростехнадзора относятся полномочия и функции, связанные с промышленной безопасностью опасных производственных объектов на основе законодательных и нормативных требований.
Идентификация видов работ Положением о лицензировании эксплуатации взрывопожароопасных и химически опасных производственных объектов I, II и III классов опасности, утвержденного постановлением Правительства Российской Федерации от 10.06.2013 № 492, не предусмотрена. Понятие «транспортирование» относится к общепринятым.
При этом учитывается, что согласно ГОСТ 25866-83 «Эксплуатация техники. Термины и определения» к транспортированию относится перемещение изделия в заданном состоянии с применением, при необходимости, транспортных и грузоподъемных средств, начинающееся с погрузки и кончающееся разгрузкой на месте назначения.
Учитывается также, что согласно Примечанию 1 к Положению о лицензировании эксплуатации взрывопожароопасных и химически опасных производственных объектов I, II и III классов опасности, утвержденному постановлением Правительства Российской Федерации от 10.06.2013 № 492, воспламеняющиеся, окисляющие, горючие, взрывчатые, токсичные, высокотоксичные вещества и вещества, представляющие опасность для окружающей среды, определены отсылочно к приложению 1 Федерального закона от 21.07.1997 № 116-ФЗ «О промышленной безопасности опасных производственных объектов».
При этом, соответственно, рассматриваются установленные законодательно критерии отнесения рабочих продуктов к вышеуказанным видам веществ, включая воспламеняющиеся, окисляющие, горючие, взрывчатые, токсичные, высокотоксичные вещества и вещества, представляющие опасность для окружающей среды, с учетом установленных проектной документацией, нормативной документацией, документацией изготовителей и поставщиков, параметров и характеристик, включая меры безопасности.
Как следует из п. 6 и п. 14 Требований к регистрации объектов в государственном реестре опасных производственных объектов и ведению государственного реестра опасных производственных объектов (далее – Требования), утвержденных приказом Ростехнадзора от 25.11.2016 № 495, зарегистрированным в Минюсте России в 22.02.2017 № 45760, отнесение объектов к опасным производственным объектам осуществляется эксплуатирующей организацией на основании проведения их идентификации в соответствии с данными Требованиями.
При идентификации веществ (в том числе состоящих из нескольких компонентов), в целях отнесения их к опасным, могут использоваться данные паспортов безопасности химических веществ и карточек перевозимых опасных грузов, результаты исследований и испытаний, а также другие информационные источники, официально принятые, изданные, и находящиеся в открытом доступе.
В указанных целях учитывается, что одно и то же вещество (включая их растворы различных концентраций) может, в зависимости от физико-химических свойств, идентифицироваться и учитываться как одновременно относящееся к нескольким видам опасных веществ (к примеру, бензины, дизельное топливо, керосины).
Вопрос от 16.05.2017г.:
В Ростехнадзор поступило обращение с вопросом о том, необходимо ли учитывать обводненность нефти при расчете количества вещества для идентификации класса опасности опасного производственного объекта?
Ответ: Ответ на данный вопрос подготовлен специалистами Управления по надзору за объектами нефтегазового комплекса.
Согласно положениям п. 1 приложения 1 и п. 1 приложения 2 Федерального закона от 21 июля 1997 г. № 116-ФЗ «О промышленной безопасности опасных производственных объектов» при идентификации опасных производственных объектов не учитывается содержание массовой доли воды, концентрации хлористых солей и механических примесей.
Вопрос от 13.11.2015г.:
Прошу разъяснить, необходимо ли при определении массы Горючих жидкостей, используемых в технологическом процессе или транспортируемых по магистральному трубопроводу для идентификации опасных производственных объектов согласно Федеральному закону от 21 июля 1997 г. N 116-ФЗ «О промышленной безопасности опасных производственных объектов», учитывать массу воды, находящейся в обводненной нефти (т.е. учитывать массу всей смеси), либо необходимо учитывать только массу нефти без учета воды (т.к. вода не является горючим веществом и в физико-химическом процессе горения принимать участия не может).
Ответ Ростехнадзора: Управление но надзору за объектами нефтегазового комплекса рассмотрело обращение, поступившее по электронным средствам связи в Общественную приемную Ростехнадзора, и разъясняет.
Нефть, поставляемая на нефтеперерабатывающие предприятия и экспортируемая за рубеж по магистральным трубопроводам, является товарной нефтью – продукция нефтегазодобывающего предприятия, прошедшая весь цикл подготовки и удовлетворяющая требованиям ГОСТ Р 51858-2002 по одной из трех групп ее качества. По степени подготовки нефти к транспортировке нормируются следующие показатели: содержание воды, содержание механических примесей, давление насыщенных паров, содержание хлористых солей и содержание хлорорганических соединений.
При определении массы горючих жидкостей, используемых в технологическом процессе при транспортировании по магистральным трубопроводам, в целях идентификации опасных производственных объектов нормативными правовыми актами не установлено требование учета массы нефти без учета воды.
|
Затрагивает вопросы экономического развития регионов |
False |
|
Обязательные требования (КНД) |
True |
|
Обязательные требования (Регуляторная гильотина) |
False |
|
Электронный адрес для отправки своих предложений |
[email protected] |
|
Степень регулирующего воздействия |
Средняя |
|
Дата начала публичного обсуждения |
3 декабря 2019 г. |
|
Дата окончания публичного обсуждения |
23 декабря 2019 г. |
|
Ответственный за разработку |
Марюха Ольга Юрьевна |
|
Почтовый адрес для отправки своих предложений |
127994, г. Москва, ул. Ильинка, д. 21 |
|
Контактный телефон ответственного лица |
+7(495) 926-99-01 доб. 1541 |
|
Дата начала независимой антикоррупционной экспертизы |
3 декабря 2019 г. |
|
Дата окончания независимой антикоррупционной экспертизы |
17 декабря 2019 г. |
|
Адрес электронной почты для получения заключений по результатам проведения антикоррупционной экспертизы |
[email protected] |
|
Почтовый адрес для получения заключений по результатам проведения антикоррупционной экспертизы |
127994, ГСП-4, г. Москва, ул. Ильинка, 21 |
Опасные и легковоспламеняющиеся вещества » Предметы запрещенные для пересылки » Посылка » Бизнес » Omniva
Взрывоопасные и взрывчатые вещества
Определение:
Любые химические соединения, смеси или средства, которые могут вызвать взрыв или использование которых сопровождается риском моментального разогревания и выделения газа. Все взрывчатые вещества запрещены.
Пример:
нитроглицерин, пистоны, ракеты для салюта, зажигательные смеси, взрывчатка, осветительные ракеты, амуниция и т.д.
Газы (сжатые, сжиженные или растворенные под давлением)
Определение:
Стабильные газы, которые не сжижаются под воздействием температуры окружающей среды, растворенные в растворителе под давлением. Запрещены:
- сжатые и воспламеняющиеся газы: водород, этан, метан, пропан, бутан, зажигалки, газовые цилиндры для примусов, паяльные лампы и т.д.
- токсичные сжатые газы: хлор, фтор и др.
- невоспламеняющиеся сжатые газы: диоксид углерода, азот, неон, огнетушительные аппараты, в которых есть такие газы, и т.п.
- аэрозоли
ВОСПЛАМЕНЯЮЩИЕСЯ ЖИДКОСТИ
Определение:
Жидкости, смеси жидкостей или жидкости, в которых есть твердые частицы в виде раствора или суспензии, создающие горючие пары. Запрещены все жидкости, температура возгорания которых в закрытом сосуде ниже 55ºC.
Пример:
ацетон, бензол, чистящие средства, бензин, горючее для зажигалок, растворители для красок и чистящие средства, керосин, растворители и т.п.
ЛЕГКОВОСПЛАМЕНЯЮЩИЕСЯ ТВЕРДЫЕ ВЕЩЕСТВА
Определение:
Твердые материалы. причиной возгорания которых может быть трения, поглощения влаги, спонтанной химической реакции или тепло, удерживаемого в процессе обработки, или которые легко воспламеняется и горят.
Пример:
спички, карбид кальция, целлюлоза, вещества, содержащие нитрат, металлический магний, пленка на базе нитроцеллюлозы, фосфор, калий, натрий, гидрид натрия, порошок цинка, гидрид циркония и т.п.
ОКСИДИРУЮЩИЕ ВЕЩЕСТВА И ОРГАНИЧЕСКИЕ ПЕРОКСИДЫ
Определение:
Эти вещества являются самовоспламеняемыми, хоть и не всегда, но они могут вызвать или способствовать воспламенению других веществ. Кроме этого, они могут взорваться, вызвать опасную реакцию, взаимодействовать с другими веществами и создавать угрозу для здоровья.
Пример:
броматы, хлораты, компоненты средств для ремонта изделий из стекловолокна, перхлораты, перманганаты, пероксиды и т.п.
ТОКСИЧНЫЕ ВЕЩЕСТВА И ВЕЩЕСТВА, СПОСОБСТВУЮЩИЕ РАСПРОСТРАНЕНИЮ ИНФЕКЦИЙ, ДРУГИЕ МЕДИЦИНСКИЕ ВЕЩЕСТВА
Определение:
Вещества, которые после их заглатывания, вдыхания или соприкосновения с кожей могут вызвать смерть или повреждения. Вещества, содержащие микроорганизмы или их токсины, которые определенно или, возможно, могут способствовать распространению заболеваний.
Пример:
мышьяк, бериллий, цианид, фтор, водород, селенит, ртуть, ртутные соли, иприт, диоксид азота, патогенный материал, крысиный яд, сыворотка, вакцины и т.п.
РАДИОАКТИВНЫЙ МАТЕРИАЛ
Определение:
Все материалы, специфическая активность которых выше 74 килобеккерелей на килограмм (0,002 микрокюри на грамм). Все радиоактивные материалы запрещены.
Пример:
распадающиеся вещества (уран 235 и т.п.), радиоактивные отходы, урановая руда или ториевая руда и т.п.
ЕДКИЕ ВЕЩЕСТВА
Определение:
Вещества, которые могут причинить серьезный вред, поскольку они оказывают химическое воздействие на живые ткани, товары или транспортное средство.
Пример:
хлорид алюминия, гидроксид натрия, едкая чистящая жидкость, средство для снятия/предотвращения ржавчины, едкое средство для снятия краски, электробатарейки, соляная кислота, азотная кислота, серная кислота и т.п.
ДРУГИЕ ОПАСНЫЕ ВЕЩЕСТВА
Определение:
Вещества, создающие угрозу, которую невозможно классифицировать в соответствии с вышеуказанными категориями.
Пример:
асбест, сухой лед, магнетизированный материал с силой магнитного поля 0,159 А или выше на расстоянии 2,1 м от упаковки и т.п.
Что такое вещество? — Определение, типы и примеры — Science Class [2021 Video]Типы веществПродолжая нашу технологическую схему, мы видим, что чистые вещества можно разделить на две подкатегории: элементы и соединения. Элементы представляют собой простейшую форму материи, что означает, что они не могут быть разделены на более мелкие компоненты физически или химически. Все элементы перечислены в таблице Менделеева, а человечеству известно как минимум 118 из них! Примеры элементов включают углерод (C), водород (H), кислород (O) и натрий (Na), и это лишь некоторые из них. Соединения , с другой стороны, состоят из двух или более различных элементов, удерживаемых вместе химическими связями и функционирующих как единое целое.Хотя соединения также являются чистыми веществами, они отличаются от элементов, потому что соединения могут быть разбиты на более простые компоненты (элементы, составляющие соединение). Некоторыми примерами соединений являются диоксид углерода (CO2), ржавчина (Fe2O3) и поваренная соль (NaCl). Примеры веществДавайте обсудим несколько примеров чистых веществ. Образец кремния состоит только из одного типа атомов: атомов кремния. Следовательно, кремний — чистое вещество. Поскольку эти атомы кремния находятся в своей простейшей форме и не могут быть расщеплены дальше, вещество, кремний, также является элементом.Помните, что простой способ выяснить, является ли что-то элементом, — это найти его в таблице Менделеева. Все, что изображено в таблице Менделеева, является элементом и, следовательно, чистым веществом! Кремний находится под номером 14 в периодической таблице и имеет символ Si. Сахар имеет химическую формулу C12h32O11. Это говорит нам о том, что он состоит из 12 атомов углерода, 22 атомов водорода и 11 атомов кислорода, связанных вместе и функционирующих как единое целое, что означает, что сахар представляет собой соединение (и может быть далее разбит на отдельные элементы: углерод, водород и кислород. ).Таким образом, сахар — это чистое вещество. Простой способ выяснить, является ли что-то составным, — это выяснить, есть ли у него химическая формула. Все, что может быть представлено химической формулой, является химическим соединением и, следовательно, чистым веществом! Вода — это чистое вещество, в зависимости от его разновидности. Например, дистиллированная вода и морская вода имеют разные свойства. Морская вода содержит молекулы h3O, а также молекулы соли и, вероятно, многие другие ионы и атомы. Таким образом, морская вода считается смесью.Однако дистиллированная вода содержит только молекулы h3O и, следовательно, является чистым веществом. Поскольку молекулы h3O в дистиллированной воде состоят из 2 атомов водорода и 1 атома кислорода, связанных вместе и функционирующих как единое целое, чистое вещество вода классифицируется как соединение и может быть химически разложено на отдельные элементы — водород и кислород. Краткое содержание урокаВещество — это просто чистая форма вещества . Другими словами, вещество — это материя, содержащая только один тип атома или молекулы.Чистые вещества можно разделить на две подкатегории: элементы и соединения. Элементы представляют собой простейшую форму материи, что означает, что они не могут быть разделены на более мелкие компоненты физически или химически. Соединения , с другой стороны, состоят из двух или более различных элементов, удерживаемых вместе химическими связями и действующих как единое целое. Два типа чистых веществ
Результаты обученияКогда вы закончите, вы должны уметь:
Назовите два типа чистых веществПонимание чистых веществ очень важно в химии.Например, алмазы — это один из видов чистого вещества, потому что они состоят только из атомов углерода. С другой стороны, янтарь не является чистым, потому что он содержит растительные смолы с различными соединениями. В реальном мире за пределами лаборатории трудно выделить чистые материалы. Даже алмазы содержат примеси, такие как азот или бор, когда они добываются в природе. TL; DR (слишком долго; не читал)Два основных типа чистых веществ — это соединения и элементы. Они состоят из частиц или соединений одного типа. Два основных типа чистых веществЭлементы и соединения — это два типа чистых веществ. Примеры общих элементов включают углерод, азот и водород. Они состоят из одного типа атомов и не могут распасться на что-то другое. Например, каждое чистое углеродное вещество содержит одни и те же частицы. Такие соединения, как вода, соль и сахар, также являются чистыми веществами. Несмотря на то, что они представляют собой комбинацию различных элементов, эти вещества по-прежнему соответствуют критериям, поскольку они имеют постоянный состав и содержат только один тип соединения.У них также есть фиксированное количество элементов. Например, чашка дистиллированной стерильной воды является чистым веществом, потому что единственное соединение в ней — H 2 O. Типы материи, которые являются чистыми веществамиВещество, имеющее постоянный и постоянный состав, квалифицируется как чистое вещество. субстанция. Одним из примеров является обычная поваренная соль, потому что в ней есть только один тип соединения, а именно NaCl. Неважно, смотрите ли вы на щепотку соли или на чашку соли, поскольку внутри находятся только соединения NaCl.Вы не найдете других соединений в чистой поваренной соли. Точно так же сахар — это чистый материал, который содержит только соединения C 12 H 22 O 11 . Проблемы с выделением чистых веществОбычно трудно выделить чистые вещества за пределами лаборатории. Например, элемент натрия (Na) бурно реагирует с водой и не существует сам по себе в природе, но его легко найти в таком соединении, как соль (NaCl) или гидроксид натрия (NaOH). Элемент калий (K) обладает высокой реакционной способностью, что затрудняет его выделение. Примеси — еще одна проблема, которая затрудняет поиск чистого вещества. Золото (Au) часто содержит другие элементы, такие как серебро или медь, которые требуют очистки или плавления металла для их удаления. Алмаз — еще один пример чистого вещества, которое имеет проблемы с примесями, влияющими на его стоимость. Азот может сделать бриллиант желтым, и этот недостаток может значительно снизить цену. 3.5: Чистые вещества и смесиУчебная цель
Чистые веществаКогда мы говорим о чистом веществе , мы говорим о чем-то, что содержит только один вид материи.Это может быть один-единственный элемент или одно-единственное соединение, но каждый образец этого вещества, который вы исследуете, должен содержать в точности одно и то же с фиксированным, определенным набором свойств.
* Примечание: чистый газообразный кислород состоит из молекул, но по-прежнему считается элементом, а не соединением, поскольку молекулы состоят из элементов одного типа.Соединения состоят из одного или нескольких элементов. СмесиЕсли мы берем два или более чистых вещества и смешиваем их вместе, мы называем это смесью . Смеси всегда можно снова разделить на составляющие чистые вещества, потому что связывание между атомами составляющих веществ не происходит в смеси. В то время как соединение может иметь свойства, сильно отличающиеся от свойств составляющих его элементов, в смесях вещества сохраняют свои индивидуальные свойства.Например, натрий — мягкий блестящий металл, а хлор — едкий зеленый газ. Эти два элемента могут объединяться с образованием соединения, хлорида натрия (поваренная соль), которое представляет собой белое кристаллическое твердое вещество, имеющее , ни свойств натрия или хлора. Если, однако, вы смешали поваренную соль с молотым перцем, вы все равно могли бы видеть отдельные зерна каждого из них, и, если бы вы были терпеливы, вы могли бы взять пинцет и осторожно разделить их обратно на чистую соль и чистый перец. . Гетерогенная смесьГетерогенная смесь представляет собой смесь, состав которой неоднороден по всей смеси. Овощной суп — это неоднородная смесь. Любая данная ложка супа будет содержать различное количество различных овощей и других компонентов супа. Гомогенная смесь / РастворГомогенная смесь представляет собой комбинацию двух или более веществ, которые настолько тщательно перемешаны, что смесь ведет себя как единое вещество.Еще одно слово для обозначения однородной смеси — раствор. Таким образом, комбинация соли и стальной ваты представляет собой неоднородную смесь, поскольку легко увидеть, какие частицы вещества представляют собой кристаллы соли, а какие — стальную вату. С другой стороны, если вы возьмете кристаллы соли и растворите их в воде, очень трудно определить наличие более одного вещества, просто взглянув, даже если вы используете мощный микроскоп. Соль, растворенная в воде, представляет собой гомогенную смесь или раствор (Рисунок \ (\ PageIndex {3} \)). Рисунок \ (\ PageIndex {3} \): Типы смесей © Thinkstock Слева комбинация двух веществ представляет собой гетерогенную смесь, поскольку частицы двух компонентов выглядят по-разному. Справа кристаллы соли растворились в воде настолько тонко, что вы не можете сказать, присутствует ли соль. Гомогенная смесь выглядит как единое вещество. Пример \ (\ PageIndex {3} \) Определять следующие комбинации как гетерогенные смеси или гомогенные смеси.
Рисунок \ (\ PageIndex {4} \): Смесь железной стружки и порошка серы ( Asoult, смесь Fe-S 03, CC BY 4.0) Раствор
Упражнение \ (\ PageIndex {3} \) Являются ли следующие комбинации гомогенными смесями или гетерогенными смесями?
Ответы
Классификация материаловРисунок \ (\ PageIndex {1} \): Взаимосвязь между типами веществ и методами, используемыми для разделения смесей Обычная поваренная соль называется хлоридом натрия.Его считают веществом , потому что оно имеет однородный и определенный состав. Все образцы хлорида натрия химически идентичны. Вода также является чистым веществом. Соль легко растворяется в воде, но соленую воду нельзя классифицировать как вещество, поскольку ее состав может варьироваться. Вы можете растворить небольшое или большое количество соли в определенном количестве воды. Смесь представляет собой физическую смесь двух или более компонентов, каждый из которых сохраняет свою идентичность и свойства в смеси .Меняется только форма соли, когда она растворяется в воде. Он сохраняет свой состав и свойства. Фаза Фаза — это любая часть образца, имеющая однородный состав и свойства. По определению, чистое вещество или гомогенная смесь состоит из одной фазы. Гетерогенная смесь состоит из двух или более фаз. Когда масло и вода смешиваются, они не смешиваются равномерно, а образуют два отдельных слоя. Каждый из слоев называется фазой. Пример \ (\ PageIndex {1} \) Обозначьте каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
Дано : химическое вещество Спрошенный : его классификация Стратегия:
Раствор:
Упражнение \ (\ PageIndex {1} \) Обозначьте каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
Пример \ (\ PageIndex {2} \) Как химик классифицирует каждый образец материи?
РЕШЕНИЕ
Упражнение \ (\ PageIndex {2} \) Как химик классифицирует каждый образец материи?
РезюмеВещество можно разделить на две большие категории: чистые вещества и смеси. Чистое вещество — это форма вещества, имеющая постоянный состав и постоянные свойства во всем образце. Смеси представляют собой физические комбинации двух или более элементов и / или соединений. Смеси можно разделить на однородные и гетерогенные. Элементы и соединения являются примерами чистых веществ. Соединения — это вещества, состоящие из более чем одного типа атомов.Элементы — это простейшие вещества, состоящие только из одного типа атомов. Основные выводы
Чистые вещества и смеси — химия для детейЧто такое материя?Материя может быть определена как любое вещество, обладающее инерцией, занимающее пространство и обладающее массой. Как классифицируется материя?Ученые мира классифицируют материю как твердую, жидкую или газообразную, но есть еще один интересный способ ее классификации. Материю также можно отнести к чистым веществам и смесям. Что такое чистое вещество?Чистая субстанция — это материя, которая существует в своей самой основной или самой чистой форме и не может быть подвергнута дальнейшему разложению.Примеры чистых веществ включают воду, газы, такие как углекислый газ, кислород и металлы, такие как платина, золото и серебро. Каждое чистое вещество обладает собственным набором уникальных химических и физических свойств, которые помогают нам идентифицировать его. Примеры чистых веществ Вода имеет температуру замерзания и плавления 0 ° C и точку кипения 100 ° C. Он бесцветный, безвкусный и без запаха. Виды чистых веществ Чистые вещества можно разделить на две категории — элементы и соединения. Что такое смесь?Смесь — это комбинация двух или более чистых веществ, каждое из которых сохраняет свою индивидуальность при смешивании. Смеси присутствуют практически повсюду на Земле. Посмотрите на скалы, океан, реки или даже на атмосферу. Все они смеси! Другими словами, все, что вы можете смешать, является смесью. Даже продукты, которые вы едите. Почему это называется смесью?Это означает, что основная химическая структура компонентов смеси не изменяется при смешивании. Примеры смесейХотя вода — чистое вещество, если вы поместите песок в стакан с водой, он превратится в смесь. Каждый из компонентов смеси можно отделить друг от друга. Вы всегда можете отделить песок от воды, отфильтровав ее. Если вы возьмете смесь соли и воды, ее можно разделить, выпарив воду, чтобы в емкость попала соль. Воздух тоже представляет собой смесь разных газов, таких как углекислый газ, кислород, азот, водяной пар и т. Д.Кровь представляет собой смесь, состоящую из разных типов клеток крови и плазмы. Виды смесей
Как отличить чистые вещества от смесей?
Примеры чистых веществЧистые вещества имеют однородный химический состав. Примеры включают воду (жидкость), алмаз (твердое тело) и кислород (газ). В химии чистое вещество — это материал с постоянным составом. Другими словами, он однороден независимо от того, когда вы его пробуете. Чистое вещество целиком состоит из одного типа атома или соединения. Он предсказуемо участвует в химической реакции. Примеры чистых веществЛучшими примерами чистых веществ являются чистые элементы, молекулы и соединения:
Серая зонаНекоторые люди считают любую однородную смесь или сплав примером чистого вещества.Это обычное определение, но оно не даст вам оценки на уроке химии. Эти примеры чистых веществ не состоят из одного типа атома или соединения, но имеют однородную структуру. Этот тип чистого вещества не должен содержать загрязняющих веществ или примесей:
Примеры нечистых веществНекоторые образцы являются яркими примерами нечистых веществ:
Как определить чистое веществоЕдинственный способ точно узнать, является ли образец чистым веществом, — это провести химический анализ.Однако есть и другие подсказки, которые помогут вам определиться:
Примечания к типам веществТипы веществ: Вещества подразделяются на два типа. Они, Чистое вещество: Вещество, состоящее из частиц одного вида. Смеси: Вещество, содержащее две или более различных частиц, называется смесями. Чистые вещества: типы Элемент: Чистое вещество, которое состоит только из одного вида атомов и не может быть разделено на два или более простых вещества физическими или химическими средствами, называется элементом. Характеристики элементов:
Элементы классифицируются как металлы, неметаллы и металлоиды. Металлы: Металлы — это элементы, которые легко теряют электрон с образованием положительного иона или катиона. Пример: золото, серебро, медь, железо, калий и т. Д. Свойства металлов:
Исключения:
Неметаллы: Неметаллы — это те элементы, которые легко получают электрон (ы) с образованием отрицательного иона или аниона. Свойства неметаллов:
Металлоиды: Элементы, которые имеют промежуточные свойства между металлами и неметаллами, называются металлоидами .
Соединение: Чистое вещество, состоящее из двух или более элементов, которые химически объединены в фиксированной пропорции, называется соединением. Свойства соединения:
Смеси: Вещество, состоящее из двух или более веществ, которые могут быть элементами, соединениями или тем и другим, физически смешанными вместе в любой пропорции, но не химически соединенными. Свойства смеси:
Смесь: Классификация: Смеси подразделяются на однородные и гетерогенные. Гомогенная смесь: Смесь, в которой различные компоненты смешаны равномерно, называется гомогенной смесью. Гетерогенная смесь: Неоднородная смесь называется гетерогенной смесью. Различия между смесью и компаундом:
|
