Содержание
Углеводы (моносахариды, дисахариды, полисахариды).
Углеводы — органические соединения, чаще всего природного происхождения, состоящие только из углерода, водорода и кислорода.
Углеводы играют огромную роль в жизнедеятельности всех живых организмов.
Свое название данный класс органических соединений получил за то, что первые изученные человеком углеводы имели общую формулу вида Cx(H2O)y . Т.е. их условно посчитали соединениями углерода и воды. Однако позднее оказалось, что состав некоторых углеводов отклоняется от этой формулы. Например, такой углевод как дезоксирибоза имеет формулу С5Н10О4. В то же время существуют некоторые соединения, формально соответствующие формуле Cx(H2O)y, однако к углеводам не относящиеся, как, например, формальдегид (СН2О) и уксусная кислота (С2Н4О2).
Тем не менее, термин «углеводы» исторически закрепился за данным классом соединений, в связи с чем повсеместно используется и в наше время.
Классификация углеводов
В зависимости от способности углеводов расщепляться при гидролизе на другие углеводы с меньшей молекулярной массой их делят на простые (моносахариды) и сложные (дисахариды, олигосахариды, полисахариды).
Как легко догадаться, из простых углеводов, т.е. моносахаридов, нельзя гидролизом получить углеводы с еще меньшей молекулярной массой.
При гидролизе одной молекулы дисахарида образуются две молекулы моносахарида, а при полном гидролизе одной молекулы любого полисахарида получается множество молекул моносахаридов.
Химические свойства моносахаридов на примере глюкозы и фруктозы
Самыми распространенными моносахаридами являются глюкоза и фруктоза, имеющие следующие структурные формулы:
Как можно заметить, и в молекуле глюкозы, и в молекуле фруктозы присутствует по 5 гидроксильных групп, в связи с чем их можно считать многоатомными спиртами.
В составе молекулы глюкозы имеется альдегидная группа, т.е. фактически глюкоза является многоатомным альдегидоспиртом.
В случае фруктозы можно обнаружить в ее молекуле кетонную группу, т.е. фруктоза является многоатомным кетоспиртом.
Химические свойства глюкозы и фруктозы как карбонильных соединений
Все моносахариды могут реагировать в присутствии катализаторов с водородом. При этом карбонильная группа восстанавливается до спиртовой гидроксильной. Так, в частности, гидрированием глюкозы в промышленности получают искусственный подсластитель – гексаатомный спирт сорбит:
Молекула глюкозы содержит в своем составе альдегидную группу, в связи с чем логично предположить, что ее водные растворы дают качественные реакции на альдегиды. И действительно, при нагревании водного раствора глюкозы со свежеосажденным гидроксидом меди (II) так же, как и в случае любого другого альдегида, наблюдается выпадение из раствора кирпично-красного осадка оксида меди (I). При этом альдегидная группа глюкозы окисляется до карбоксильной – образуется глюконовая кислота:
Также глюкоза вступает и в реакцию «серебряного зеркала» при действии на нее аммиачного раствора оксида серебра. Однако, в отличие от предыдущей реакции вместо глюконовой кислоты образуется ее соль – глюконат аммония, т.к. в растворе присутствует растворенный аммиак:
Однако, в отличие от предыдущей реакции вместо глюконовой кислоты образуется ее соль – глюконат аммония, т.к. в растворе присутствует растворенный аммиак:
Фруктоза и другие моносахариды, являющиеся многоатомными кетоспиртами, в качественные реакции на альдегиды не вступают.
Химические свойства глюкозы и фруктозы как многоатомных спиртов
Поскольку моносахариды, в том числе глюкоза и фруктоза, имеют в составе молекул несколько гидроксильных групп. Все они дают качественную реакцию на многоатомные спирты. В частности, в водных растворах моносахаридов растворяется свежеосажденный гидроксид меди (II). При этом вместо голубого осадка Cu(OH)2 образуется темно-синий раствор комплексных соединений меди.
Реакции брожения глюкозы
Спиртовое брожение
При действии на глюкозу некоторых ферментов глюкоза способна превращаться в этиловый спирт и углекислый газ:
Молочнокислое брожение
Помимо спиртового типа брожения существует также и немало других. Например, молочнокислое брожение, которое протекает при скисании молока, квашении капусты и огурцов:
Например, молочнокислое брожение, которое протекает при скисании молока, квашении капусты и огурцов:
Особенности существования моносахаридов в водных растворах
Моносахариды существуют в водном растворе в трех формах – двух циклических (альфа- и бета-) и одной нециклической (обычной). Так, например, в растворе глюкозы существует следующее равновесие:
Как можно видеть, в циклических формах отсутствует альдегидная группа, в связи с тем что она участвует в образовании цикла. На ее основе образуется новая гидроксильная группа, которую называют ацетальным гидроксилом. Аналогичные переходы между циклическими и нециклической формами наблюдаются и для всех других моносахаридов.
Дисахариды. Химические свойства.
Общее описание дисахаридов
Дисахаридами называют углеводы, молекулы которых состоят из двух остатков моносахаридов, связанных между собой за счет конденсации двух полуацетальных гидроксилов либо же одного спиртового гидроксила и одного полуацетального. Связи, образующиеся таким образом между остатками моносахаридов, называют гликозидными. Формулу большинства дисахаридов можно записать как C12H22O11.
Связи, образующиеся таким образом между остатками моносахаридов, называют гликозидными. Формулу большинства дисахаридов можно записать как C12H22O11.
Наиболее часто встречающимся дисахаридом является всем знакомый сахар, химиками называемый сахарозой. Молекула данного углевода образована циклическими остатками одной молекулы глюкозы и одной молекулы фруктозы. Связь между остатками дисахаридов в данном случае реализуется за счет отщепления воды от двух полуацетальных гидроксилов:
Поскольку связь между остатками моносахаридов образована при конденсации двух ацетальных гидроксилов, для молекулы сахара невозможно раскрытие ни одного из циклов, т.е. невозможен переход в карбонильную форму. В связи с этим сахароза не способна давать качественные реакции на альдегиды.
Подобного рода дисахариды, которые не дают качественные реакции на альдегиды, называют невосстанавливающими сахарами.
Тем не менее, существуют дисахариды, которые дают качественные реакции на альдегидную группу. Такая ситуация возможна, когда в молекуле дисахарида остался полуацетальный гидроксил из альдегидной группы одной из исходных молекул моносахаридов.
Такая ситуация возможна, когда в молекуле дисахарида остался полуацетальный гидроксил из альдегидной группы одной из исходных молекул моносахаридов.
В частности, в реакцию с аммиачным раствором оксида серебра, а также гидроксидом меди (II) подобно альдегидам вступает мальтоза. Связано это с тем, что в её водных растворах существует следующее равновесие:
Как можно видеть, в водных растворах мальтоза существует в виде двух форм – с двумя циклами в молекуле и одним циклом в молекуле и альдегидной группой. По этой причине мальтоза, в отличие от сахарозы, дает качественную реакцию на альдегиды.
Гидролиз дисахаридов
Все дисахариды способны вступать в реакцию гидролиза, катализируемую кислотами, а также различными ферментами. В ходе такой реакции из одной молекулы исходного дисахарида образуется две молекулы моносахарида, которые могут быть как одинаковыми, так и различными в зависимости от состава исходного моносахарида.
Так, например, гидролиз сахарозы приводит к образованию глюкозы и фруктозы в равных количествах:
А при гидролизе мальтозы образуется только глюкоза:
Дисахариды как многоатомные спирты
Дисахариды, являясь многоатомными спиртами, дают соответствующую качественную реакцию с гидроксидом меди (II), т.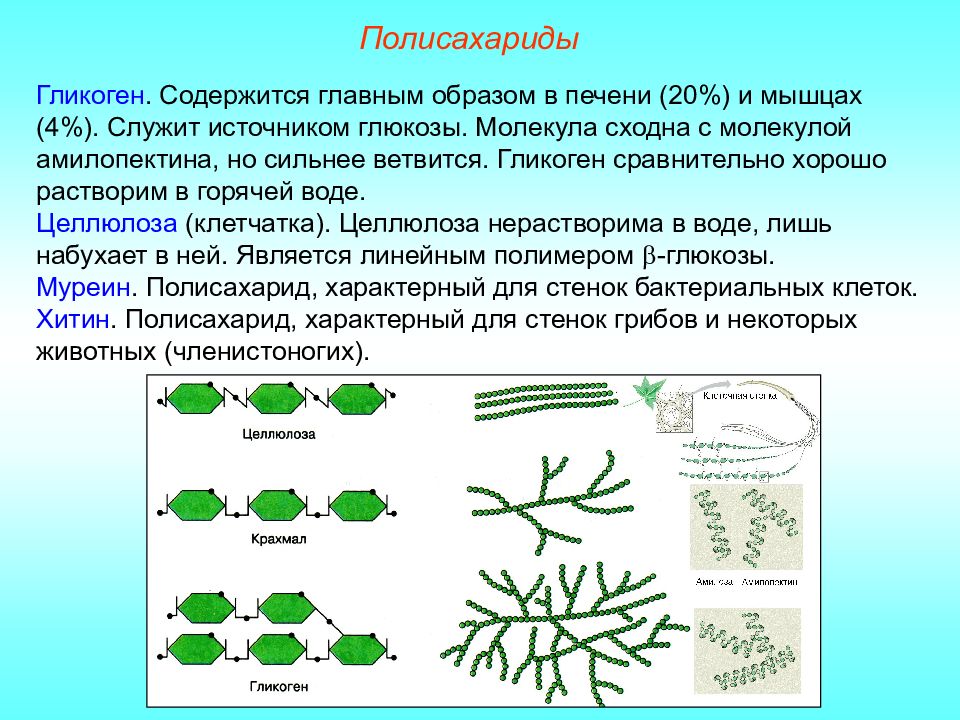 е. при добавлении их водного раствора ко свежеосажденному гидроксиду меди (II) нерастворимый в воде голубой осадок Cu(OH)2 растворяется с образованием темно-синего раствора.
е. при добавлении их водного раствора ко свежеосажденному гидроксиду меди (II) нерастворимый в воде голубой осадок Cu(OH)2 растворяется с образованием темно-синего раствора.
Полисахариды. Крахмал и целлюлоза
Полисахариды — сложные углеводы, молекулы которых состоят из большого числа остатков моносахаридов, связанных между собой гликозидными связями.
Есть и другое определение полисахаридов:
Полисахаридами называют сложные углеводы, молекулы которых образуют при полном гидролизе большое число молекул моносахаридов.
В общем случае формула полисахаридов может быть записана как (C6H10O5)n.
Крахмал – вещество, представляющее собой белый аморфный порошок, не растворимый в холодной воде и частично растворимый в горячей с образованием коллоидного раствора, называемого в быту крахмальным клейстером.
Крахмал образуется из углекислого газа и воды в процессе фотосинтеза в зеленых частях растений под действием энергии солнечного света. В наибольших количествах крахмал содержится в картофельных клубнях, пшеничных, рисовых и кукурузных зернах. По этой причине указанные источники крахмала и являются сырьем для его получения в промышленности.
В наибольших количествах крахмал содержится в картофельных клубнях, пшеничных, рисовых и кукурузных зернах. По этой причине указанные источники крахмала и являются сырьем для его получения в промышленности.
Целлюлоза – вещество, в чистом состоянии представляющее собой белый порошок, не растворимый ни в холодной, ни в горячей воде. В отличие от крахмала целлюлоза не образует клейстер. Практически из чистой целлюлозы состоит фильтровальная бумага, хлопковая вата, тополиный пух. И крахмал, и целлюлоза являются продуктами растительного происхождения. Однако, роли, которые они играют в жизни растений, различны. Целлюлоза является в основном строительным материалом, в частности, главным образом ей образованы оболочки растительных клеток. Крахмал же несет в основном запасающую, энергетическую функцию.
Химические свойства крахмала и целлюлозы
Горение
Все полисахариды, в том числе крахмал и целлюлоза, при полном сгорании в кислороде образуют углекислый газ и воду:
Образование глюкозы
При полном гидролизе как крахмала, так и целлюлозы образуется один и тот же моносахарид – глюкоза:
Качественная реакция на крахмал
При действии йода на что-либо, в чем содержится крахмал, появляется синее окрашивание.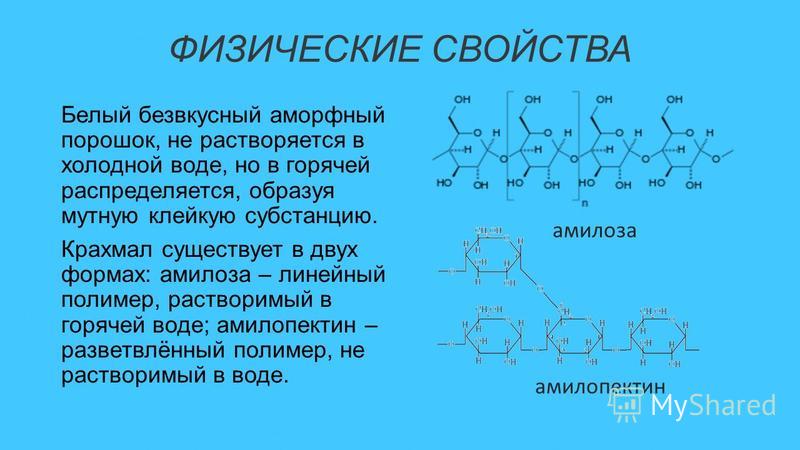 При нагревании синяя окраска исчезает, при охлаждении появляется вновь.
При нагревании синяя окраска исчезает, при охлаждении появляется вновь.
При сухой перегонке целлюлозы, в частности древесины, происходит ее частичное разложение с образованием таких низкомолекулярных продуктов как метиловый спирт, уксусная кислота, ацетон и т.д.
Поскольку и в молекулах крахмала, и в молекулах целлюлозы имеются спиртовые гидроксильные группы, данные соединения способны вступать в реакции этерификации как с органическими, так и с неорганическими кислотами:
Урок 10. углеводы. глюкоза. олигоса- хариды. сахароза — Химия — 10 класс
Химия, 10 класс
Урок № 10. Углеводы. Глюкоза. Олигосахариды. Сахароза
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению углеводов, особенностям их строения. Рассмотрено влияние функциональных групп на свойства углеводов. Даётся характеристика химических свойств глюкозы и сахарозы. Объяснена биологическая роль углеводов и области их применения.
Глоссарий
Алкилирование – реакция образования простых эфиров в результате замещения атома водорода углеводородным радикалом в гидроксогруппе.
Ацилирование – реакция образования сложных эфиров в результате взаимодействия спиртов, в том числе многоатомных, с кислотами или кислотными ангидридами.
Брожение маслянокислое – превращение глюкозы под действием маслянокислых бактерий в масляную кислоту. Сопровождается выделением углекислого газа и водорода.
Брожение молочнокислое – превращение глюкозы под действием молочнокислых бактерий в молочную кислоту.
Брожение спиртовое – разложение глюкозы под действием дрожжей с образованием этилового спирта и углекислого газа.
Глюкоза – моносахарид состава С6Н12О6, состоящий из 6 атомов углерода, 5 гидроксильных групп и альдегидной группы. Может существовать как в виде линейной, так и циклической молекул. Вступает в реакции окисления, восстановления, ацилирования, алкилирования, подвергается молочнокислому, спиртовому, маслянокислому брожению.
Крахмал – полисахарид, состоящий из остатков α-глюкозы.
Лактоза, или молочный сахар – дисахарид С12Н22О11, состоящий из остатков глюкозы и галактозы, подвергается гидролизу, может окисляться до сахариновых кислот.
Моносахариды – углеводы, не подвергающиеся гидролизу, состоят из 3–10 атомов углерода, могут образовывать циклические молекулы с одним циклом (глюкоза, фруктоза, рибоза).
Невосстанавливающие углеводы – углеводы, не содержащие альдегидной группы и не способные к реакциям восстановления (фруктоза, сахароза, крахмал).
Олигосахариды – углеводы, образующие при гидролизе от 2 до 10 молекул моносахаридов (сахароза, лактоза).
Полисахариды – углеводы, образующие при гидролизе от нескольких десятков до сотен тысяч молекул моносахаридов (целлюлоза, крахмал).
Рибоза— моносахарид, относится к пентозам. Линейная молекула содержит альдегидную группу. Образует пятичленный цикл. Входит в состав РНК.
Входит в состав РНК.
Сахароза – дисахарид, состоящий из остатков α-глюкозы и β-фруктозы. Относится к невосстанавливающим углеводам, так как не содержит альдегидную группу и не может восстанавливать гидроксид меди (II) до одновалентного оксида меди и серебро из аммиачного раствора гидроксида серебра. Является многоатомным спиртом. Подвергается гидролизу.
Углеводы – кислородсодержащие органические соединения, содержащие карбонильную и несколько гидроксильных групп.
Фруктоза – моносахарид состава С6Н12О6, относится к кетозам. Может существовать как в виде линейной молекулы, так и образовывать пятичленный цикл.
Целлюлоза – полисахарид, состоящий из остатков β-глюкозы.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Понятие об углеводах, их классификация
Углеводами называются кислородсодержащие органические соединения, содержащие карбонильную и несколько гидроксильных групп и обычно отвечающие общей формуле Сп(Н2О)т. К углеводам относятся глюкоза, фруктоза, рибоза, сахароза, лактоза, крахмал, целлюлоза и другие. Углеводы могут существовать как в виде линейных, так и циклических молекул. Углеводы, молекулы которых могут образовывать только один цикл, называют моносахаридами (глюкоза, фруктоза, рибоза). Если молекула углевода при гидролизе распадается на несколько (от двух до десяти моносахаридов), они называются олигосахаридами (сахароза, лактоза). Углеводы, образующие при гидролизе десятки, сотни и более моносахаридов, называются полисахаридами (крахмал, целлюлоза).
Углеводы, молекулы которых могут образовывать только один цикл, называют моносахаридами (глюкоза, фруктоза, рибоза). Если молекула углевода при гидролизе распадается на несколько (от двух до десяти моносахаридов), они называются олигосахаридами (сахароза, лактоза). Углеводы, образующие при гидролизе десятки, сотни и более моносахаридов, называются полисахаридами (крахмал, целлюлоза).
Моносахариды
В молекуле моносахарида может быть от двух до десяти атомов углерода. Все моносахариды имеют окончание -оза. В названии сначала указывается количество атомов углерода, а затем прибавляется окончание: триоза, тетроза, пентоза, гексоза.
Для живых организмов наиболее важны пентоза и гексоза. Моносахариды с альдегидной группой называют альдозами (например, глюкоза), а содержащие кетогруппу – кетозами (например, фруктоза). Нумерация атомов углерода в альдозах начинается с атома альдегидной группы, а в кетозах – с крайнего атома, наиболее близкого к карбонильной группе.
Глюкоза
Самым распространённым моносахаридом в природе является глюкоза. Она содержится в сладких ягодах и фруктах. Мёд также содержит много глюкозы.
Она содержится в сладких ягодах и фруктах. Мёд также содержит много глюкозы.
Глюкоза относится к группе гексоз, так как содержит шесть атомов углерода. Молекулы глюкозы могут быть как линейными (D-глюкоза, альдоза), так и циклическими (α и β-глюкоза). Линейная молекула глюкозы содержит на конце альдегидную группу. Общей формулой С6Н12О6 можно обозначить как глюкозу, так и фруктозу.
Фруктоза относится к кетозам и образуется пятичленный цикл. Она является изомером глюкозы. Фруктоза, также, как и глюкоза, может существовать в виде линейных и циклических молекул, в зависимости от положения заместителей у второго атома углерода различают α- и β-фруктозу.
Глюкоза – бесцветное кристаллическое вещество. Она хорошо растворяется в воде, имеет сладкий вкус. Факт наличия в молекуле глюкозы альдегидной группы доказывает реакция «серебряного зеркала». С фруктозой эта реакция не идёт. Один моль глюкозы реагирует с пятью молями уксусной кислоты с образованием сложного эфира, что доказывает наличие в молекуле глюкозы пяти гидроксильных групп.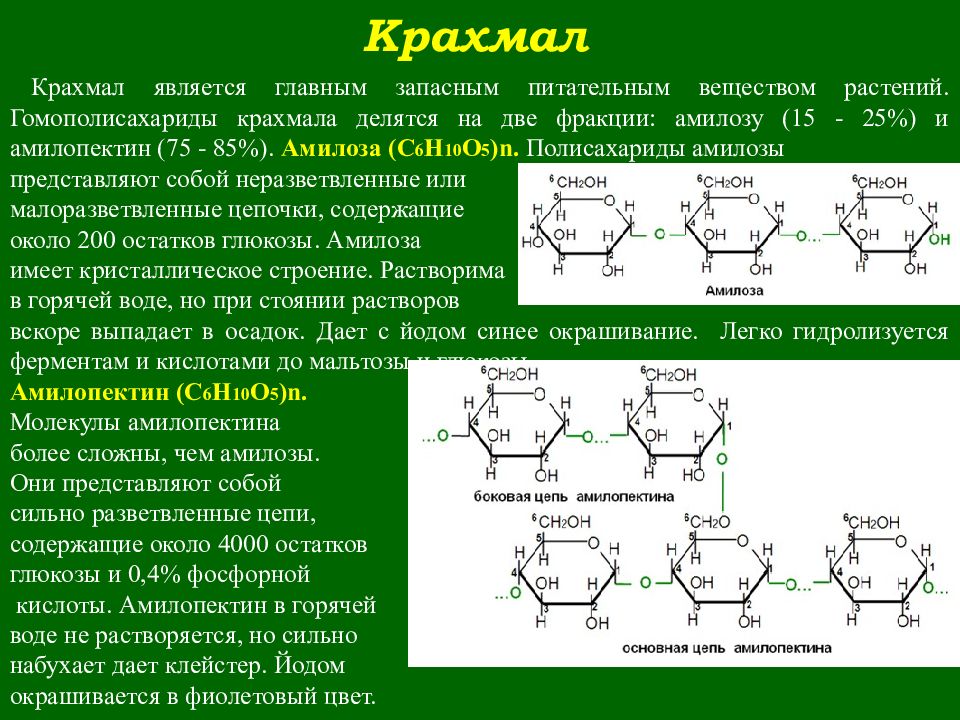 Такая реакция называется ацилированием. Если к раствору глюкозы на холоде добавить растворы сульфата меди и щелочи, то вместо осадка образуется ярко-синее окрашивание. Эта реакция доказывает, что глюкоза – многоатомный спирт. Благодаря наличию в молекуле глюкозы альдегидной группы, она может не только вступать в реакцию «серебряного зеркала», но и восстанавливать гидроксид меди (II) до одновалентного оксида. Водород в присутствии никелевого катализатора восстанавливает глюкозу до сорбита – шестиатомного спирта. В реакциях с низшими спиртами в кислой среде или с йодистым метилом в щелочной среде гидроксильные группы участвуют в образовании простых эфиров – происходит реакция алкилирования.
Такая реакция называется ацилированием. Если к раствору глюкозы на холоде добавить растворы сульфата меди и щелочи, то вместо осадка образуется ярко-синее окрашивание. Эта реакция доказывает, что глюкоза – многоатомный спирт. Благодаря наличию в молекуле глюкозы альдегидной группы, она может не только вступать в реакцию «серебряного зеркала», но и восстанавливать гидроксид меди (II) до одновалентного оксида. Водород в присутствии никелевого катализатора восстанавливает глюкозу до сорбита – шестиатомного спирта. В реакциях с низшими спиртами в кислой среде или с йодистым метилом в щелочной среде гидроксильные группы участвуют в образовании простых эфиров – происходит реакция алкилирования.
Глюкоза, в зависимости от условий, вступает в реакции брожения с образованием различных продуктов. Под действием молочнокислых бактерий глюкоза превращается в молочную кислоту – этот процесс получил название «молочнокислое брожение». Он используется при изготовлении кисломолочных продуктов. В присутствии дрожжей глюкоза подвергается спиртовому брожению.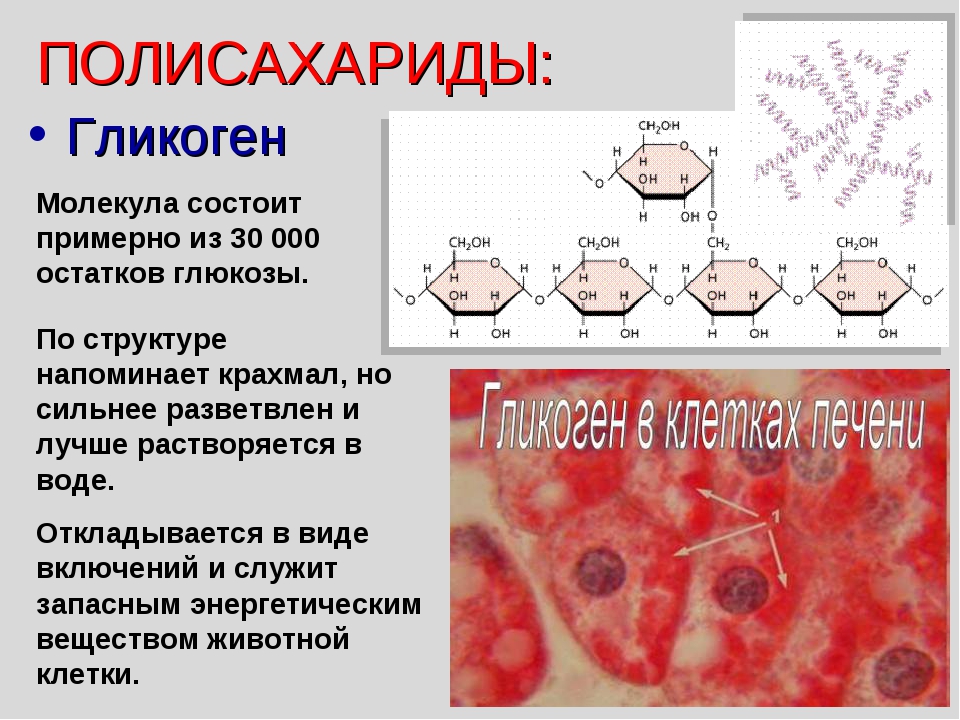 Этот вид брожения используется при изготовлении алкогольных напитков, а также дрожжевого теста. В этом процессе, кроме спирта, образуется углекислый газ, который делает тесто пышным. Брожение глюкозы, в результате которого образуется масляная кислота, происходит под действием особых маслянокислых бактерий. Этот вид брожения применяют в производстве масляной кислоты, эфиры которой широко используют в парфюмерии. Но если маслянокислые бактерии попадут в пищевые продукты, они могут вызвать их гниение.
Этот вид брожения используется при изготовлении алкогольных напитков, а также дрожжевого теста. В этом процессе, кроме спирта, образуется углекислый газ, который делает тесто пышным. Брожение глюкозы, в результате которого образуется масляная кислота, происходит под действием особых маслянокислых бактерий. Этот вид брожения применяют в производстве масляной кислоты, эфиры которой широко используют в парфюмерии. Но если маслянокислые бактерии попадут в пищевые продукты, они могут вызвать их гниение.
Одним из продуктов фотосинтеза, который идет с участием зеленых растений, является глюкоза. Для человека и животных глюкоза является основным источником энергии для осуществления обменных процессов. В организмах животных глюкоза накапливается в виде гликогена (полисахарида, образованного остатками глюкозы). В растениях глюкоза превращается в крахмал (полисахарид, состоящий из остатков α-глюкозы). Клеточные оболочки высших растений построены из целлюлозы (полисахарид, состоящий из остатков β-глюкозы).
В крови человека находится около 0,1% глюкозы. Этой концентрации достаточно для снабжения организма энергией. Но при заболевании, называемом «сахарный диабет», глюкоза не расщепляется, её концентрация в крови может достигать 12%, что приводит к серьёзным нарушениям в работе всего организма.
В лабораторных условиях глюкозу можно получить из формальдегида в присутствии гидроксида кальция. Впервые этот синтез осуществил Александр Михайлович Бутлеров в 1861 году. В промышленности глюкозу получают гидролизом крахмала под действием серной кислоты.
Сахароза
Самым распространенным дисахаридом является сахароза. В природе она в большом количестве находится в свёкле и в сахарном тростнике. Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы.
Сахароза – бесцветное кристаллическое вещество, хорошо растворимое в воде, в два раза слаще глюкозы. Температура плавления равна 160 оС. В результате реакции сахарозы с гидроксидом меди появляется ярко-синее окрашивание, что характерно для многоатомных спиртов, но при нагревании раствора красный осадок не образуется, что указывает на отсутствие альдегидной группы. В присутствии минеральных кислот при нагревании сахароза подвергается гидролизу, распадаясь на α-глюкозу и β-фруктозу. Если к суспензии известкового молока прилить раствор сахарозы, то осадок растворяется. Образуется растворимый в воде сахарат кальция. Эта реакция лежит в основе получения сахарозы из сахарной свеклы и сахарного тростника. Если через раствор сахарата кальция пропустить углекислый газ, то образуется осадок карбоната кальция и раствор сахарозы.
В присутствии минеральных кислот при нагревании сахароза подвергается гидролизу, распадаясь на α-глюкозу и β-фруктозу. Если к суспензии известкового молока прилить раствор сахарозы, то осадок растворяется. Образуется растворимый в воде сахарат кальция. Эта реакция лежит в основе получения сахарозы из сахарной свеклы и сахарного тростника. Если через раствор сахарата кальция пропустить углекислый газ, то образуется осадок карбоната кальция и раствор сахарозы.
Сахарозу применяют в пищевой промышленности для изготовления кондитерских изделий, консервирования (джемы, варенья, компоты).
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Расчет количества реагента, необходимого для реакции с глюкозой
Условие задачи: Для получения ацетоуксусного эфира глюкозы на 1 моль глюкозы необходимо 5 моль уксусной кислоты. Сколько граммов 35%-ного раствора уксусной кислоты требуется, чтобы полностью прореагировать с 10 г глюкозы, если выход продукта реакции равен 75%?
Ответ запишите в виде целого числа.
Шаг первый: найдём молярные массы глюкозы и уксусной кислоты.
М(С6Н12О6) = 6·12 + 12·1 + 6·16 = 180 (г/моль).
М(СН3СООН) = 2·12 + 1·16 + 4·1 = 60 (г/моль).
Шаг второй: Найдём массу уксусной кислоты, которая вступает в реакцию с 10 г глюкозы. Для этого составим пропорцию:
180 г глюкозы реагирует с 5·60 г уксусной кислоты;
10 г глюкозы реагирует с х1 г уксусной кислоты.
(г).
Шаг третий: Найдём массу уксусной кислоты с учетом выхода продукта реакции. Для этого составим пропорцию:
16,7 г уксусной кислоты прореагирует с 75% глюкозы;
х2 г уксусной кислоты прореагирует со 100% глюкозы.
(г).
Шаг четвёртый: Найдём массу 35%-ного раствора уксусной кислоты, в котором содержится 22,2 г кислоты. Для этого составим пропорцию:
В 100 г раствора содержится 35 г кислоты;
в х3 г раствора содержится 22,2 г кислоты.
(г)
Ответ: 63
2. Расчёт количества энергии, полученной организмом при расщеплении глюкозы.
Условие задачи: В процессе расщепления 1 моль глюкозы в организме человека выделяется 200 кДж энергии. В сутки старшекласснику необходимо 12500 кДж энергии. Какой процент от суточной потребности в энергии восполнит ученик, съевший 200 г винограда, если содержание глюкозы в винограде составляет 30%? Ответ запишите с точностью до десятых долей.
Шаг первый: Найдём молярную массу глюкозы:
М(С6Н12О6) = 6·12 + 12·1 + 6·16 = 180 (г/моль).
Шаг второй: Найдём массу глюкозы, которая содержится в 200 г винограда.
Для этого массу винограда умножим на 30% и разделим на 100%:
г.
Шаг третий: Найдём количество моль глюкозы, которое содержится в 60 г этого углевода.
Для этого массу глюкозы разделим на её молярную массу:
(моль).
Шаг четвёртый: Найдём количество энергии, которая выделится при расщеплении 0,33 моль глюкозы.
Для этого составим пропорцию:
При расщеплении 1 моль глюкозы выделяется 200 кДж энергии;
при расщеплении 0,33 моль глюкозы выделяется х1 кДж энергии.
(кДж).
Шаг пятый: Найдём, какой процент от суточной потребности составляет это количество энергии.
Для этого составим пропорцию:
12500 кДж составляет 100% суточной потребности;
66 кДж составляет х2% суточной потребности.
(%).
Ответ: 0,5.
Все о пектине: виды, состав, как работать с ним
Пектины
31.05.2019
Пектин – это один из тех продуктов, которые наиболее часто используют кондитеры по всему миру. Это удивительный продукт, который применяют как крупные производства, так и обычные домохозяйки. Ведь именно он позволяет готовить великолепные джемы, соки, пастилы, и даже соки и майонез, а также для стабилизации пенной структуры, корпусов сбивных конфет и много чего еще. И, в то же время, это тот продукт, к которому до сих пор есть много вопросов – чем отличаются различные виды пектинов, как правильно использовать с различными продуктами и т.д.
В этой статье постараемся ответить на большинство вопросов.
ЧТО ТАКОЕ ПЕКТИН
Пектин является гелеобразователем, стабилизатором, загустителем, влагоудерживающим агентом, осветлителем, и средством для капсулирования, зарегистрирован в качестве пищевой добавки E440. Как и некоторые другие вещества (кукурузный крахмал, желатин), пектин в небольших количествах – сгущает смеси, а в больших количествах – желирует.
Пектин – это полисахарид, который входит в состав практически каждого растительного продукта. Пектин также присутствует во всех фруктах и ягодах, но они отличаются по количеству содержащегося в них пектина. Из фруктов и ягод, содержащих много пектина (яблоко, слива, клюква, смородина), можно приготовить джем или желе, не добавляя дополнительного пектина. К тому же, уровень содержания пектина сильно зависит от степени зрелости и спелости плодов.
Пектин любим еще и потому, что образовывает достаточно прочную текстуру, не влияя в то же время на вкус, запах и цвет готового продукта.
КЛАССИИКАЦИЯ ПЕКТИНА
Сразу хотим сказать — не существует единой мировой утвержденной классификации пектинов. Каждый производитель создает свой уникальный продукт! Читайте состав и назначение.
В целом можно выделить несколько групп пектинов в зависимости от их свойств.
На данный момент существуют различные классификации пектинов.
По форме пектин может встречаться:
• в порошке. Вводится в смеси вместе с сахаром при температуре 50 градусов.
• в жидком виде (экстракт, жидкий пектин). Он предварительно разводится в горячей воде.
Оба вида нельзя заменить друг другом!
По химическим свойствам.
В процессе производства пектин проходит процесс этерификации (взаимодействует со спиртом и кислотой), что и придает ему различные свойства, о которых читайте ниже. В особых случаях пектин обрабатывают еще и аммиаком для получения амидированного пектина.
При производстве была обнаружена закономерность – чем выше степень этерификации пектина, тем быстрее он желирует и при более высокой температуре. Поэтому стали производить множество видов пектина с разной степенью этерификации.
Таким образом выделятся следующие группы пектинов:
• низкоэтерифицированный (LM – low methoxyl) (степень этерификации ниже 50%) способен желировать вне зависимости от кислотности ягод или сахара, но в присутствии ионов кальция. Это как раз, например, пектин FX58 – тот, который работает с молочными продуктами. Также такие пектины работают со смесями с низким содержанием сухих веществ (с пониженным содержанием сахара, например).
• высокоэтерифицированный (HM – high methoxyl) (степень этерификации выше 50%)- это самый популярный пектин. Он способен желировать при высокой кислотности, при низком уровне pH смеси, при высоком содержании сахара или других сухих веществ. При этом, чем выше степень этерификации, тем больше растворимых сухих веществ и выше уровень рН необходимы для образования устойчивого каркаса студня.
Он быстрее растворяется в воде, быстрее желирует смеси.
Высокоэтерифицированные пектины используют в основном в кондитерской промышленности для производства зефира , пастилы и мармелада. Т.е. это самые обычные виды пектина, которые мы с вами используем каждый день (желтый пектин, яблочный).
• амидированный пектин (LMA) – это низкоэтерифицированный пектин, обработанный аммиаком в процессе производства. Это особый тип пектина, в молекуле которого часть эфирных групп была преобразована в амидные.
Амидированные пектины желируют при меньшем количестве кальция, в смесях с нейтральным уровнем pH, и они менее подвержены осаждению при высоких концентрациях кальция. Его часто используют для производства фруктовых начинок для йогуртов, термостабильных начинок. На упаковке вы можете встретить обозначение (i) или (ii) относящееся к пектину. Это означает:
(i) – пектин
(ii) – пектин амидированный.
Иногда в пектин добавляют буферные соли, после чего он может желировать без присутствия кислот. Тогда, в зависимости от результата, выделяют два вида желе:
• термостабильное (смесь желируется после повторного нагрева)
• нетермостабильное (разрушается при температуре выше 90-100°С при повторном нагреве)
Также пектин различают по времени садки (время, в течение которого из добавки образуется гель):
• пектин быстрой садки (температура желирования 75-85°С; степень этерификации выше 70-76%; время желирования 10-15 мин)
• средней садки (степень этерификации 70-72 % и средние температуры желирования; время желирования – 15-20 минут)
• пектин медленной садки (температура желирования 45-60°С; степень этерификации 56-68%; время 20-25 мин)
Скорость желирования (садки) регулируют с помощью соединений, замедляющих студнеобразование и называемых ретардаторами (они есть в составе пектина).
Чем выше степень этерификации, тем быстрее происходит желирование, и тем более высокая температура нужна.
Каждый производитель “играет” составами пектинов, программируя предсказуемый и точный результат. Отсюда и получается, что у каждого производителя – свои составы, свой ассортимент.
ОСНОВНЫЕ ВИДЫ ПЕКТИНА
Пектин яблочный или цитрусовый – это базовый, обычный пектин. В составе – только пектин (максимум может быть указана декстроза, глюкоза или сахароза, которые помогают стандартизировать пектин). Производится из кожуры яблок или цитрусовых. Используется для любых целей, чаще для мармелада, конфитюров.
Обычный пектин – имеет степень этерификации – 60-66% (высокоэтерифицированный), что означает более быстрое желирование и потребность в высоких температурах для желирования. Работает в кислой среде (рН в диапазоне 2,8-3,4). Т.е. чтобы получить устойчивый студень, этому виду пектина нужно большое количество сахара в составе, наличие кислоты и высокая температура.
Кстати, уровень pH алкогольных напитков тоже низкий (2,5-3.5), что позволяет делать алкогольные мармелады также на обычном пектине.
Но обратите внимание, что производители могут под таким названием продавать и амидированный пектин, т.е. обработанный аммиаком. И у него уже немного другие свойства – более низкий уровень этерификации (а значит и замедленная скорость желирования), более высокий уровень pH (а значит могут работать практически с любыми фруктами и ягодами), и возможность работать со смесями с более низким содержанием сахара. Это, например, яблочный пектин “Айдиго”. Также есть подобный пектин и у французов – это Pectin 325NH95 в ассортименте Louis Francois.
Внимательно читайте упаковку! Если указано, что пектин для джемов – значит он точно не подойдет для мармелада, т.к. не будет давать плотной консистенции.
Гели из яблочного пектина имеют более высокую прочность по сравнению с цитрусовым, т.е. получение продукта с одинаковой прочностью на излом требует меньшего расхода яблочного пектина.
Слева – гель с яблочным пектином. Справа – с цитрусовым.
Пектин (желтый) – чаще производится из кожуры яблок или цитрусовых. Что это за продукт – зависит от производителя! Обязательно читайте состав и назначение продукта. Чаще всего в Европе под “желтым” понимают обычный яблочный или цитрусовый пектин. В нашей стране такое определение только путает…
Например, желтый пектин PatisFrance – это состав, больше похожий на пектин наппаж (пектин + E337 + E452 + декстроза). Желтый пектин Sosa – это чистый яблочный пектин, годится для мармелада. А желтый пектин Louis Francois похож на PatisFrance (59-65% уровень этерификации) – тоже смесь из пектина и буферных солей E337 и E452, и работает при содержании сахара 76% и уровне pH смеси – 3,2-3,5.
В составе вы можете увидеть различные буферные соли, которые и будут давать продукту те или иные свойства.
Пектин NH – это термообратимый пектин с низким уровнем этерификации (28-40%). Чаще всего его используют в смесях с меньшим количеством сахара, и также для начинок муссовых тортов, т.к. он отлично переносит заморозку и не отпускает воду при оттаивании (т.е. начинка не потечет).
Этот пектин не требует присутствия большого содержания сахара и большого содержания кислоты в смеси. Но вновь их процентное содержание напрямую зависит от состава и пропорций ингредиентов в пектине NH, которые подобрал производитель. Настоятельно рекомендую вновь – внимательно читать состав и рекомендации.
Если в составе есть лактат натрия (sodium lactate, Е325), то такой пектин будет работать только с фруктами и ягодами, содержащими кислоты, т.е. с низким уровнем pH (см. таблицу по уровню pH). Эта добавка – эмульгатор, влагоудерживающий агент, регулирует кислотность. В таком составе расход будет примерно 20 г на 1 кг мармелада.
Пектин наппаж (pectine nappage) – низкоэтерифицированный пектин, термообратимый. Работает в смесях с содержанием сахара 60-70% и с кислотными фруктами и ягодами. Обычно используется для приготовления нейтрального геля, глазурей. Для активации нужна лимонная кислота.
У многих производителей пектин NH и пектин наппаж – это одно и тоже. Вы даже можете встретить название – пектин NH nappage. Просто знайте, что он будет хорош именно для глазурей.
Важное отличие наппажа от NH – более прозрачный гель (это важно при приготовлении нейтральной глазури, например, или глазури для покрытия свежих ягод на десертах).
Пектин NH plus – cреднеэтерифицированный пектин (степень этерификации – 30%). Рекомендуемая дозировка 1,2-2,5 %.
Новый продукт на российском рынке и довольно редкий – на западном. Опыты показывают, что смеси с этим пектином застывают быстрее, чем с пектином NH. Он не дает плотной мармеладной консистенции, но хорошо загущает, оставляя текстуру тянущейся.
Предполагается его использование также для начинок, глазурей.
Пектин FX – пектин с низкой степенью этерификации, работает только с кальцийсодержащими продуктами. С ним готовим молочные и сливочные начинки, мармелад, конфитюр. В этом случае уровень кислотности не играет значения. Примером такого пектина является пектин X58 от испанского производителя Sosa.
Пектин acid free (безкислотный) – аналог обычного пектина, которому для работы не важен уровень кислотности смеси. В составе содержит сульфат кальция (calcium sulfate) – очень гигроскопичный стабилизатор, эмульгатор, фактически это гипс, который в силу своих свойств (застывания после охлаждения) и помогает смеси схватываться после охлаждения и оставаться стабильной.
Удобен тем, что работает с любыми фруктами и ягодами, которые не содержат кислоту – бананы, яблоки, кокосы, финики, арбуз, апельсины, а также с ореховыми пастами. На таком пектине делают мармелад из фисташковой пасты, например.
Пектин slow set (медленной садки) – аналог обычного пектина, которому нужно больше времени для студнеобразования. Подходит для случаев, когда вы разливаете начинки или мармеладки в маленькие формочки и вам нужно время на эту разливку (не более 3-4 минут). Ведь любой другой пектин схватывается почти моментально и не дает возможности разлить мармелад по формочках.
Цитрусовые волокна – производятся из внутренних белых оболочек цитрусовых, из перегородок. Свойства схожи с пектином, годится для конфитюров
СОСТАВ ПЕКТИНА
Пектины – это не всегда просто пектины, а вообще разные продукты, состав которых напрямую зависит от производителя.
Самые распространенные виды пектина – это яблочный и цитрусовый, в составе которых присутствует только сам пектин и иногда декстроза или сахароза в незначительных количествах.
Также многие производители чистый пектин смешивают с различными добавками (буферные соли), которые придают пектину необходимые свойства. Выбирая буферные соли и их дозировку, производитель имеет возможность индивидуально адаптировать продукт к имеющейся технологии. Какой процент добавок в составах пектина – сказать невозможно, т.к. это индивидуально разработанные формулы, свои у каждого производителя. И да, это их коммерческая тайна.
В качестве добавок к пектину могут применяться пирофосфаты (Е450), полифосфаты (Е452), фосфат кальция (Е341), лактат натрия (Е325), сульфат кальция (Е516).
Чем выше концентрация буферной соли, тем ниже температура желирования и тем больше время желирования.
КАК РАССЧИТАТЬ КОЛИЧЕСТВО ПЕКТИНА
Когда вы собираетесь что-то приготовить с пектином (вне зависимости – есть у вас конкретный рецепт или нет, и там иногда бывают ошибки и опечатки), вам нужно понимать важные моменты:
• плотность – что именно вы хотите получить: жидковатый соус (кули), устойчивую и мягкую начинку для торта, плотный мармелад, густой конфитюр
• исходное содержание пектина в ягодах или фруктах, которые вы собираетесь использовать. Потому что количество пектина будет разным
• какой тип пектина у вас есть (желтый, NH, FX).
Для образования студня необходимо присутствие 3 компонентов – сахар, пектин и кислота либо кальций. Их количество и соотношение напрямую зависит от вида пектина. Оптимальным ученые считают сочетание 60 : 1 : 1 (60 частей сахара, 1 часть пектина, 1 часть кислоты – лимонной, винной, молочной и пр.) – это сочетание для обычного пектина высокоэтерифицированного (HM).
Обратите внимание, что вид сахара – также влияет на плотность получаемого продукта. Поэтому не стоит самостоятельно урезать количество сахара или заменять другим видом сахара.
Самый прочный гель образует пектин совместно с обычным сахаром (сахароза). А самый непрочный – с фруктозой.
Присутствие глюкозы в рецептах мармелада возможно (около 30%), но не обязательно. Глюкоза в мармеладах предотвращает процессы кристаллизации сахарозы, а также удлиняет срок годности.
Создать единую таблицу с универсальными пропорциями пектина, к сожалению, не возможно… Поскольку пропорции сильно зависят от вида и формулы самого пектина, вида ягод или фруктов, которые вы используете.
Но что касается мармеладов, подобная таблица уже существует. Здесь даны расчеты, исходя из использования яблочного пектина.
КАК ДОБАВЛЯТЬ ПЕКТИН В СМЕСЬ
Есть 3 различных способа, как добавляют пектин в смесь, которую нужно зажелировать:
- Сухой пектин смешать с сахаром
Самый распространенный способ, когда пектин смешивают с сахаром и “дождиком” всыпают в горячее (50-60 С) ягодное пюре, тщательно перемешивая венчиком.
При более низкой температуре – пектин начнет схватываться, будут комки, размешать смесь и получить хорошую текстуру не получится.
С научной точки зрения считается, что пектин растворится лучше, если основную часть сахара добавить после того, как добавлен и растворен пектин.
А если добавить щепотку соли в смесь, то можем увеличить вязкость.
- Пектин предварительно растворить в кипятке
Порошок пектина добавляют в кипящую воду, тщательно пробивая блендером. Соотношение – 5-8% пектина
Затем эту воду тонкой струйкой выливают в горячее ягодное пюре, перемешивая венчиком.
Этот метод используется, если смесь может “вместить” в себя дополнительную жидкость. Больше подходит для крупных производств.
- Пектин предварительно растворить в сахарном сиропе
Пектин добавляется к готовому сахарному сиропу, тщательно перемешивается до полного растворения. И уже потом – добавляется ягодное пюре.
Нужно ли добавлять лимонную кислоту к пектину?
Лимонная кислота играет роль катализатора желирования, а также – регулятора уровня pH. Поэтому ее обязательно нужно добавлять к смесям с низким уровнем pH. Это, например, лимон, вишня, апельсины, черника, клюква.
Количество добавляемой кислоты зависит от:
• типа используемого пектина
• дозировки пектина
• содержания растворимых сухих веществ (сахара)
• дозировки и вида используемых буферных солей
Увеличивая количество добавляемой кислоты и не меняя другие параметры рецептуры, можно повысить температуру и уменьшить время желирования по причине большей склонности молекулярных цепочек пектина к сближению. Однако в этом случае повышается вероятность преждевременного желирования. Именно поэтому лимонную кислоту добавляют в самом конце.
Для инициирования желирования в продукт вводят водный раствор пищевой кислоты, т.е. предварительно растворяют в равном количестве воды.
Добавление кислоты вызывает необратимый процесс желирования. Поэтому приготовленный продукт необходимо быстро отлить в формы и оставить в покое до завершения желирования. Значительное снижение температуры или увеличение времени отлива после добавления кислоты могут вызвать преждевременное желирование. Это приведёт к снижению качества конечного продукта.
Статья написана на основании глубокого анализа маркетолога-кондитера Сидоровой Жанны (SuperBaker.ru @zanna.superbaker)
Пектины в нашем ассортименте
Всё о крахмал: история, польза, свойства, калорийность и многое другое
«Молочные реки, кисельные берега», «накрахмаленные рубашки», «…за 7 верст киселя хлебать» – в повседневной жизни мы часто сталкиваемся с таким продуктом, как крахмал. Знаем, что без него кисель не сваришь или соус получится не такой густой, как хотелось бы, понимаем, что много его в картофеле. А какой он – полезный или все-таки вредный, только картофельный или бывают и другие разновидности, в каких продуктах содержится и в какие блюда добавляется – сегодня мы попробуем разобраться во всех этих тонкостях вместе с REDMOND Club.
Если не углубляться в биологию и рассматривать крахмал с «пищевой» точки зрения, то это основной полисахарид в нашем повседневном меню. Белый, безвкусный и аморфный крахмальный порошок практически не растворяется в холодной воде: его структура разрушается при нагревании жидкости, он набухает и образует клейкую массу.
Слово «крахмал» происходит от немецкого kraftmehl и означает «крепкая мука».
О ПОЛЬЗЕ И ВРЕДЕ
Крахмал используется для загущения разнообразных продуктов и блюд, заправок и соусов. И, в отличие от других сахаров, потребление крахмала не вызывает резкого увеличения концентрации сахара в крови и не напрягает поджелудочную железу. Чтобы обеспечить организм суточной нормой крахмала – а это 330-450 грамм – достаточно употреблять в пищу следующие продукты: хлеб, макароны, кукурузу и хлопья кукурузные, мучные изделия, горох, картофель, пшено, рис, гречка, овес, пшеница, ячмень – словом, все крупы (разумеется, в меру). В природном виде крахмал обычно не несет вреда организму и даже ему полезен.
Крахмал издавна применялся для защиты кожи от солнечных ожогов.
Кстати, о плюсах крахмала: это вещество помогает выводить излишки воды из организма, позволяет ему эффективнее бороться с воспалительными процессами и поддерживать иммунитет, улучшает обмен веществ и пищеварительные процессы, снижает риск появления язвенных заболеваний. Продукты питания, содержащие крахмал, дают нам до 80% суточной нормы углеводов и быстро восполняют затраченную интенсивными нагрузками энергию.
А вот если крахмалом и продуктами, его содержащими, злоупотреблять, произойдет перенасыщение энергией и превращение ее жировые ткани. Модифицированная версия – крахмальный порошок – может серьезно навредить здоровью, если добавлять его в пищу в больших количествах. Это повышает уровень инулина и приводит к изменениям гормонального фона организма, ухудшению зрения, проблемам с сердечно-сосудистой системой, может вызвать расстройства желудка и проблемы с поджелудочной железой, не говоря уж о лишнем весе. Тем не менее, применение такого крахмала допустимо при производстве детского питания.
Не нужно пугаться названия «модифицированный крахмал» – это вещество никакого отношения к генетически модифицированным продуктам не имеет, а всего лишь представляет собой обычный крахмал с необходимыми для определенных целей добавками.
ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ
Крахмал можно изготовить и в домашних условиях, но это достаточно трудоемкий процесс, поэтому проще приобрести готовый расфасованный продукт в магазине. Вы не ошибетесь, выбрав в магазине крахмал HAAS и другие незаменимые в кулинарии смеси этого бренда.
На фабриках картофельный крахмал производится поэтапно. Сначала картофель (с содержанием крахмала не менее 13-15%) тщательно промывают на картофелемойке, затем он отправляется на измельчение. Здесь он проходит две стадии: сперва его дважды измельчают на скоростных картофелетерках, причем свежий картофель измельчается гораздо лучше, чем вялый. Измельчив таким образом клубни, получают смесь из крахмала, клеток, клеточных оболочек и картофельного сока (иначе говоря, «кашицу»).
Чтобы повысить качество крахмала, предотвратить развитие микроорганизмов и придать продукту белизну, в кашицу добавляют диоксид серы или сернистую кислоту. Кроме того, для безупречного вида продукта сок отделяют от кашицы сразу же после измельчения. Потом с помощью гидроциклонов от кашицы отделяют крахмальный песок, который после данного этапа превращается в суспензию (сырой картофельный крахмал). Такой крахмал, конечно, может являться и конечным продуктом, однако он быстро портится, поэтому чаще всего его консервируют.
Если же целью производства является порошкообразный крахмал, то наступает следующий этап обработки – сушка. С помощью пневматических сушилок крахмальная суспензия потоками горячего воздуха превращается в сухое вещество, которое фасуется в разнообразную упаковку. Сухой крахмал бывает уже четырех сортов: «Экстра», высший, первый и второй. Учитывается даже такой показатель, как количество крапин на 1 дм², видное невооруженным глазом. Средний срок хранения сухого крахмала составляет примерно 2 года.
РАЗНОВИДНОСТИ КРАХМАЛА
Картофельный крахмал
Самый популярный в северных широтах вид крахмала производят из картофеля. Здесь он используется при приготовлении фруктовых и ягодных киселей, для добавления густоты некоторым супам, соусам и подливам, в производстве колбасных изделий, стабилизации кондитерских кремов и начинок для пирогов. Картофельный крахмал важен и для изготовления клеящих веществ, в текстильной и бумажной промышленности, да и в быту ему часто находится применение.
100 граммов картофельного крахмала в среднем содержат:
- Белки – 0,1 г
- Жиры – 0 г
- Углеводы – 80 г
- Калорийность – 327 кКал
Кроме того, этот продукт содержит большое количество калия.
Кукурузный крахмал
Его получают из кукурузы примерно таким же способом, как и картофельный, и часто используют для приготовления пудингов, для придания мягкости и нежности хлебобулочным и кондитерским изделиям, для отливки мягких сладостей и корпусов для шоколадных конфет, а также при производстве консервов.
Пшеничный крахмал
Такой вид крахмала чаще всего используют в хлебобулочной и кондитерской промышленности, для производства лукума, рахат-лукума и других желейных изделий.
Сорговый крахмал
Очень похож по свойствам на кукурузный и применяется в тех же целях.
Рисовый крахмал
Такой крахмал образует клейстерные массы низкой вязкости, но при этом устойчивые к длительному хранению. Чаще всего используется для приготовления белых соусов (лучше переносят заморозку и оттаивание) и пудингов. Такой крахмал лучше всего подходит для изготовления парфюмерной продукции, идеален он и для текстильной и бумажной промышленности.
Тапиоковый крахмал
Его производят из клубней маниока съедобного (кассавы) – тропического корнеплодного растения. По свойствам он очень напоминает картофельный крахмал и используется в тех же целях с разницей в географии применения.
20.10: Полисахариды — Chemistry LibreTexts
- Последнее обновление
- Сохранить как PDF
- Участники
Как следует из названия, полисахариды — это вещества, образованные в результате конденсации очень большого количества моносахаридных единиц.Например, целлюлоза представляет собой полимер β-глюкозы, содержащий более 3000 единиц глюкозы в цепи. Крахмал в значительной степени представляет собой полимер α-глюкозы.
Эти два вещества являются классическим примером того, как незначительное различие в мономере может привести к значительным различиям в макроскопических свойствах полимера. Хлопок и бумага хорошего качества — это почти чистая целлюлоза, и они дают нам хорошее представление о ее свойствах. Целлюлоза образует прочные, но гибкие волокна и не растворяется в воде.Напротив, крахмал вообще не имеет механической прочности, а некоторые формы растворимы в воде. Часть молекулярной структуры целлюлозы и крахмала показана на Рисунке \ (\ PageIndex {1} \).
Рисунок \ (\ PageIndex {1} \) Структуры (а) целлюлозы и (б) амилозы (крахмала). Связи C-O, связывающие единицы глюкозы, показаны цветом, а водородные связи показаны одиночными черными линиями. Атомы водорода опущены для упрощения структуры. Обратите внимание, как единицы β-глюкозы в целлюлозе образуют линейную цепь, потому что стрелки C — O по обе стороны от единицы глюкозы параллельны.В амилозе, где α-глюкоза является мономером, цепь вынуждена изгибаться. Обратите внимание также на многочисленные водородные связи между двумя показанными цепями целлюлозы и водородные связи, соединяющие последовательные витки спиральной цепи амилозы. Когда йод контактирует с крахмалом, молекулы I 2 могут умещаться вдоль спирали каждой молекулы амилозы. Образующийся комплекс крахмал-йод отвечает за темно-синий цвет, наблюдаемый при контакте йода с крахмалом. группы в составе. Как следствие, водородная связь с молекулами растворителя остается только на поверхности волокна.Это объясняет, почему целлюлоза не растворяется в воде. Рисунок \ (\ PageIndex {1} \). Поскольку амилоза представляет собой полимер α-глюкозы, связи C-O на каждом конце мономера больше не параллельны, и это не позволяет им образовывать прямую цепь. Вместо этого создается спиральная структура, подобная изображенной на рисунке. Эта спираль до некоторой степени стабилизируется за счет возникновения водородных связей между каждым кольцом глюкозы и кольцами непосредственно над ним и под ним в спирали. Каждая спираль содержит от 100 до 1000 колец глюкозы.Другая форма крахмала, амилопектин, также представляет собой полимер α-глюкозы, но содержит много разветвленных цепей. Поскольку эти ветви расположены в молекуле случайным образом, амилопектин не имеет общей регулярной структуры.
Целлюлоза и крахмал различаются не только общей структурой и макроскопическими свойствами. С биохимической точки зрения они ведут себя настолько по-разному, что трудно поверить, что они оба являются полимерами одного и того же моносахарида. Ферменты, способные гидролизовать крахмал, не соприкасаются с целлюлозой, и наоборот.С точки зрения растений это также хорошо, поскольку целлюлоза составляет структурный материал, а крахмал служит хранилищем энергии. Если бы между ними не было резкого биохимического различия, потребность растения в немного большей энергии могла бы привести к разрушению клеточных стенок или других необходимых структурных компонентов.
Бактерии, простейшие, термиты, некоторые тараканы и жвачные млекопитающие (крупный рогатый скот, овцы и т. Д.) Способны переваривать целлюлозу. Сами жвачные млекопитающие, термиты и тараканы не производят целлюлазу, фермент, расщепляющий целлюлозу, а, скорее, поддерживают симбиотические отношения с бактериями в кишечнике, которые действительно расщепляют целлюлозу для пищеварения.Большинство организмов, включая человека, не способны переваривать целлюлозу ни за счет собственных ферментов, ни за счет симбиотических отношений с организмом, который может. Если бы наши пищеварительные ферменты могли гидролизовать целлюлозу, людям было бы доступно гораздо больше пищи. В буквальном смысле мы сможем есть опилки! В лаборатории можно гидролизовать целлюлозу с помощью сильной кислоты или целлюлазы, фермента, используемого бактериями. Однако пока такие процессы производят более дорогую (и менее вкусную!) Еду, чем у нас уже есть.
II. Определения диетической клетчатки | Рекомендации по употреблению пищевых продуктов: предлагаемое определение диетической клетчатки
Стр.8
В 1987 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) приняло метод AOAC 985.29 для нормативных целей, чтобы идентифицировать пищевые волокна как смесь некрахмальных полисахаридов, лигнина и некоторых резистентных крахмалов (USFDA, 1987) (
Таблица 1). Родственные методы, которые выделяли те же компоненты, что и метод AOAC 985.29, были разработаны независимо (методы AOAC 991.42, 991,43, 992,16, 993,19, 993,21 и 994,13; видеть
Таблица 2) и принят AOAC в последующие годы. Эти методы также одобрены FDA. Определение Троуэлла 1976 г. послужило основанием для принятия FDA методов AOAC по выделению пищевых волокон. Эти методы исключают из определения все олигосахариды (от 3 до 9 степеней полимеризации) и включают все полисахариды, лигнин и некоторые из резистентных крахмалов, устойчивых к ферментам (протеазе, амилазе и амилоглюкозидазе), используемым в методах AOAC.Однако FDA не имело и до сих пор не имеет письменного определения пищевых волокон для целей маркировки пищевых продуктов и заявлений о пользе для здоровья.
Как и в США, в Японии нет официального определения пищевых волокон. Стандартный метод измерения пищевых волокон в Японии основан на методе 985.29 AOAC и хроматографическом методе выделения мальтодекстринов с низким молекулярным весом (Gordon and Ohkuma, в печати) (
Таблица 1). Пищевые волокна также могут быть одобрены в Японии в качестве эффективных ингредиентов в продуктах питания для особого оздоровительного применения; к ним относятся неперевариваемый мальтодекстрин, гидролизованная гуаровая камедь, хитозан, полидекстроза, псиллиум, пшеничные отруби и деполимеризованный альгинат натрия (DeVries, 2001).Для многих азиатских стран таблицы потребления пищевых волокон основаны на методах 985.29 и 991.43 AOAC, хотя определение, используемое Китаем с 1995 года, не определяет конкретный метод (Jian-xian, 1995) (
Таблица 1).
Группа экспертов по диетическим волокнам Управления биологических исследований (LSRO) предложила определение диетической клетчатки в 1987 году, аналогичное тому, которое было определено Министерством здравоохранения и социального обеспечения Канады в 1985 году. Это определение включало некрахмальные полисахариды и лигнин и исключало вещества, связанные с клетчаткой. обнаружены в клеточной стенке растений, такие как фитаты, кутины, сапонины, лектины, белки, воски, кремний и другие неорганические компоненты (LSRO, 1987).Другие вещества, которые не считаются диетической клетчаткой в соответствии с определением LSRO, включают неперевариваемые соединения, образующиеся во время приготовления или обработки (например, резистентный крахмал, продукты реакции Майяра), олигосахариды и углеводные полимеры с степенью полимеризации менее 50-60, которые не восстанавливаются в анализ пищевых волокон, соединений нерастительного происхождения (например, хитина, хитозана) и синтетических углеводных полимеров.
В 1988 г. Министерство здравоохранения Канады опубликовало руководящие принципы для новых источников клетчатки и пищевых продуктов, содержащих их, которые могут быть обозначены как источники клетчатки в дополнение к тем, которые включены в их определение 1985 г. (Health Canada, 1988) (
Таблица 1).Основанием для этих рекомендаций было то, что существуют проблемы безопасности, уникальные для новых источников клетчатки, и, если продукт был представлен как содержащий клетчатку, он должен иметь положительные физиологические эффекты, связанные с пищевыми волокнами, которые
Биохимия | Химия для неосновных
- Определите углевод.
- Определите моносахарид.
- Приведите структуры для важных моносахаридов.
Что у вас на уме?
Мозг — чудесный орган.И он тоже голодный. Основное топливо для мозга — это углевод глюкоза. В среднем мозг взрослого человека составляет около 2% веса нашего тела, но использует 25% глюкозы в организме. Более того, определенные области мозга используют глюкозу с разной скоростью. Если вы усиленно концентрируетесь (например, проходите тест), определенным частям мозга требуется много дополнительной глюкозы, в то время как другие части мозга используют только свое нормальное количество. Что-то думать о.
Моносахариды
Некоторые продукты с высоким содержанием углеводов включают хлеб, макароны и картофель.Поскольку углеводы легко усваиваются, спортсмены часто полагаются на продукты, богатые углеводами, чтобы обеспечить высокий уровень работоспособности.
Рисунок 26.1
Продукты питания, являющиеся источниками углеводов.
Термин углевод происходит из-за того, что большинство из них содержат углерод, водород и кислород в соотношении 1: 2: 1, что дает эмпирическую формулу CH 2 O. Это несколько вводит в заблуждение, потому что на самом деле молекулы не являются гидраты углерода вообще. Углеводы — это мономеры и полимеры альдегидов и кетонов, к которым присоединено несколько гидроксильных групп.
Углеводы — самый распространенный источник энергии, который содержится в большинстве продуктов питания. Простейшие углеводы, также называемые простыми сахарами, содержатся во фруктах. Моносахарид представляет собой углевод, состоящий из одной сахарной единицы. Обычными примерами простых сахаров или моносахаридов являются глюкоза и фруктоза. Оба эти моносахарида называются гексозами, поскольку они имеют шесть атомов углерода.Глюкоза богата многими растительными источниками и входит в состав сладких веществ, таких как кукурузный или виноградный сахар. Фруктоза содержится во многих фруктах, а также в меде. Эти сахара являются структурными изомерами друг друга, с той разницей, что глюкоза содержит функциональную группу альдегида, тогда как фруктоза содержит функциональную группу кетона.
Рисунок 26.2
Глюкоза и фруктоза — моносахариды или простые сахара.
Глюкоза и фруктоза хорошо растворимы в воде.В водном растворе преобладающие формы не имеют линейной структуры, показанной выше. Скорее, они принимают циклическую структуру (см. рисунок ниже). Глюкоза — это шестичленное кольцо, а фруктоза — пятичленное кольцо. Оба кольца содержат атом кислорода.
Рисунок 26,3
Циклическая форма сахаров является предпочтительной формой в водном растворе.
Другой важной группой моносахаридов являются пентозы, содержащие пять атомов углерода в цепи.Рибоза и дезоксирибоза — две пентозы, входящие в структуру ДНК и РНК.
Рисунок 26,4
Рибоза и дезоксирибоза
Сводка
- Определен моносахарид.
- Приведены структуры обычных моносахаридов.
Практика
Вопросы
Прочтите материал по ссылке ниже и ответьте на следующие вопросы.
- Какова общая формула моносахарида?
- К какому типу моносахаридов относится глюкоза?
- Какой тип моносахарида представляет собой фруктоза?
Обзор
Вопросы
- Какие функциональные группы относятся к глюкозе?
- Какие функциональные группы входят в состав фруктозы?
- Какая форма предпочтительна в водном растворе?
- углеводы: Мономеры и полимеры альдегидов и кетонов, к которым присоединено несколько гидроксильных групп.
- моносахарид: Углевод, состоящий из одной сахарной единицы.
- Определите дисахарид.
- Приведите примеры распространенных дисахаридов.
Есть молоко?
Молоко — один из основных продуктов питания, необходимых для полноценного питания, особенно для растущих детей. Он содержит витамины и минералы, необходимые для здорового развития. К сожалению, молоко и другие молочные продукты также содержат лактозу — углевод, который может вызвать у некоторых людей серьезные заболевания.Непереносимость лактозы — это состояние, при котором лактоза, содержащаяся в молоке, не может хорошо перевариваться в тонком кишечнике. Затем непереваренная лактоза попадает в толстую кишку, где бактерии атакуют ее, образуя большое количество газа. Симптомы непереносимости лактозы включают вздутие живота, судороги, тошноту и рвоту. Часто человек перерастает эту проблему. Людям с признаками непереносимости лактозы рекомендуется избегать продуктов, содержащих лактозу. Поскольку молочные продукты могут содержать множество жизненно важных питательных веществ, можно принимать таблетки, которые обеспечивают необходимые пищеварительные материалы в тонком кишечнике.Также доступно молоко без лактозы.
Дисахариды
Простые сахара составляют основу более сложных углеводов. Циклические формы двух сахаров могут быть связаны друг с другом посредством реакции конденсации. На рисунке ниже показано, как молекула глюкозы и молекула фруктозы объединяются, образуя молекулу сахарозы. Атом водорода одной молекулы и гидроксильная группа другой молекулы удаляются в виде воды, в результате чего образуется ковалентная связь, связывающая два сахара вместе в этой точке.
Рисунок 26,5
Глюкоза и фруктоза объединяются с образованием дисахарида сахарозы в реакции конденсации.
Сахароза, широко известная как столовый сахар, является примером дисахарида. Дисахарид представляет собой углевод, образованный соединением двух моносахаридов. Другие распространенные дисахариды включают лактозу и мальтозу. Лактоза, компонент молока, образуется из глюкозы и галактозы, а мальтоза — из двух молекул глюкозы.
Во время пищеварения эти дисахариды гидролизуются в тонком кишечнике с образованием составляющих моносахаридов, которые затем абсорбируются через стенку кишечника и попадают в кровоток для транспортировки к клеткам.
Рисунок 26,6
Лактоза
Рисунок 26.7
Мальтоза
Сводка
- Дисахарид определен.
- Приведены примеры распространенных дисахаридов.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http://www.wisegeek.com/what-are-disaccharides.htm
- Какой тип реакции приводит к образованию дисахаридов?
- Какая молекула удаляется при этом?
- Какой пример сахарозы?
Обзор
Вопросы
- Какой мост между двумя моносахаридами в дисахариде?
- Из чего состоит сахароза?
- Из чего состоит лактоза?
- Из чего состоит мальтоза?
- дисахарид: Углевод, образованный соединением двух моносахаридов.
- Определите полисахарид.
- Перечислите общие полисахариды и способы их использования.
Мы еще на месте?
По мере того, как становится теплее, бегуны выходят. Не только случайные бегуны, но и действительно серьезные, которым действительно нравится пробегать все 26,2 мили марафона. Перед этими гонками (и многими более короткими) вы много слышите о углеводной загрузке. Эта практика предполагает употребление в пищу большого количества крахмала за несколько дней до забега.Крахмал превращается в глюкозу, которая обычно используется для получения биохимической энергии. Избыточная глюкоза хранится в виде гликогена в печени и мышечной ткани для использования при необходимости. Если доступно много гликогена, у мышц будет больше биохимической энергии, которую они могут использовать в долгосрочной перспективе. Остальные из нас будут просто сидеть в ресторане на тротуаре, есть наши спагетти и наслаждаться тем, как другие люди усердно работают.
Полисахариды
Многие простые сахара могут объединяться в результате повторяющихся реакций конденсации, пока не образуется очень большая молекула.Полисахарид представляет собой сложный углеводный полимер, образованный связью многих мономеров моносахаридов. Одним из наиболее известных полисахаридов является крахмал, основная форма хранения энергии в растениях. Крахмал — один из основных продуктов питания большинства людей. Такие продукты, как кукуруза, картофель, рис и пшеница, имеют высокое содержание крахмала. Крахмал состоит из мономеров глюкозы и имеет как прямую, так и разветвленную формы. Амилоза представляет собой форму с прямой цепью и состоит из сотен связанных молекул глюкозы.Разветвленная форма крахмала называется амилопектином. В тонком кишечнике крахмал гидролизуется с образованием глюкозы. Затем глюкозу можно преобразовать в биохимическую энергию или сохранить для дальнейшего использования.
Рисунок 26,8
Амилоза и амилопектин — два наиболее распространенных компонента природного крахмала. Оба состоят из множества мономеров глюкозы, соединенных в полимер. Крахмал служит хранилищем энергии в растениях.
Гликоген — это еще более разветвленный полисахарид мономеров глюкозы, который выполняет функцию хранения энергии у животных.Гликоген производится и хранится в основном в клетках печени и мышц.
Рисунок 26.9
Гликоген — это разветвленный полимер глюкозы, который служит хранилищем энергии у животных.
Целлюлоза — еще один полимер глюкозы, состоящий из сотен и более чем десяти тысяч мономеров. Это структурный компонент клеточных стенок зеленых растений и самая распространенная органическая молекула на Земле. Примерно 33% всего растительного вещества составляет целлюлоза.Структура связей в целлюлозе отличается от структуры крахмала, и целлюлоза не переваривается, за исключением нескольких микроорганизмов, которые живут в пищеварительном тракте крупного рогатого скота и термитов. На рисунке ниже показана тройная нить целлюлозы. Нет разветвлений, и волокна имеют очень жесткую стержнеобразную структуру с многочисленными водородными связями между волокнами, повышающими их прочность. Целлюлоза является основным компонентом бумаги, картона и текстиля из хлопка, льна и других растительных волокон.
Рисунок 26.10
Целлюлоза состоит из очень длинных нитей мономеров глюкозы, связанных водородными связями друг с другом. Целлюлоза в значительной степени неперевариваема и входит в состав клеточных стенок растений.
Сводка
- Полисахарид определен.
- Перечислены общие примеры полисахаридов.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http: // www.nytimes.com/2008/11/14/science/14visuals.html
- Действительно ли термиты переваривают древесину, которую они едят?
- Какую роль играет амеба в питании термитов?
- Почему важно понимать этот процесс?
Обзор
Вопросы
- Из какого мономера входят все упомянутые полисахариды?
- Какая форма хранения энергии у растений?
- Какая форма хранения энергии у животных?
- полисахарид: Сложный углеводный полимер, образованный связью многих моносахаридных мономеров.
- Определите аминокислоту.
- Изобразите общую структуру аминокислоты.
- Перечислите двадцать распространенных аминокислот.
Действительно ли помогут добавки?
Легкая атлетика в наши дни очень конкурентоспособна на всех уровнях, от школьного спорта до профи. Все ищут то преимущество, которое сделает их быстрее, сильнее и физически лучше. Один из подходов, используемых многими спортсменами, — это использование аминокислотных добавок.Теория состоит в том, что увеличение количества аминокислот в рационе приводит к увеличению протеина для мышц. Однако единственная реальная выгода — это люди, которые производят и продают таблетки. Исследования не показали никакого преимущества, полученного самими спортсменами. Намного лучше будет просто придерживаться здоровой диеты.
Аминокислоты
Аминокислота представляет собой соединение, которое содержит как аминогруппу (-NH 2 ), так и карбоксильную группу (-COOH) в одной и той же молекуле.Хотя можно вообразить любое количество аминокислот, биохимики обычно оставляют термин для группы из 20 аминокислот, которые образуются и используются живыми организмами. Рисунок ниже показывает общую структуру аминокислоты.
Рисунок 26.11
Аминокислота — это органическая молекула, которая содержит аминогруппу, карбоксильную группу и боковую цепь (R), которые связаны с центральным атомом углерода.
Амино- и карбоксильные группы аминокислоты ковалентно связаны с центральным атомом углерода.Этот атом углерода также связан с атомом водорода и группой R. Именно эта группа R изменяется от одной аминокислоты к другой и называется боковой цепью аминокислоты.
Природа боковых цепей объясняет разнообразие физических и химических свойств различных аминокислот. Некоторые боковые цепи состоят из неполярных алифатических или ароматических углеводородов. Другие боковые цепи полярны, а некоторые являются кислотными или основными.
Рисунок 26.12
Пять из двадцати биологически релевантных аминокислот, каждая из которых имеет отличительную боковую цепь (R).Боковая цепь аланина неполярна, а треонин полярен. Триптофан — одна из нескольких аминокислот, боковая цепь которой ароматическая. Аспарагиновая кислота имеет кислотную боковую цепь, а лизин — основную боковую цепь.
В приведенной ниже таблице перечислены названия 20 встречающихся в природе аминокислот вместе с трехбуквенным сокращением, которое используется для описания последовательностей связанных аминокислот.
Аминокислота | Аббревиатура | Аминокислота | Аббревиатура |
Аланин | Ала | лейцин | лей |
Аргинин | Арг | Лизин | Lys |
Аспарагин | Asn | метионин | Встреча |
Аспарагиновая кислота | Асп | фенилаланин | Phe |
Цистеин | Cys | Proline | Pro |
Глютамин | Gln | Серин | Ser |
Глутаминовая кислота | Glu | Треонин | Thr |
Глицин | Gly | Триптофан | Trp |
Гистидин | Его | Тирозин | Тир |
Изолейцин | Иль | Валин | Вал |
В другом, более позднем наборе сокращений используется только одна буква.Лейцин обозначается L, серин — S, тирозин — Y. Преимущество этой системы проявляется в перечислении аминокислотной последовательности белка, который может содержать более 100 аминокислот в своей цепи.
Сводка
- Аминокислота определена.
- Показана общая аминокислотная структура.
- Перечислены общие аминокислоты.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http: // гиперфизика.phy-astr.gsu.edu/hbase/organic/essam.html
- Что такое незаменимые аминокислоты?
- Что такое заменимые аминокислоты?
- Что произойдет, если вам не хватает аминокислоты?
Обзор
Вопросы
- Что такое аминокислота?
- Какое трехбуквенное сокращение для гистидина?
- В чем преимущество однобуквенной системы сокращения?
- аминокислота: Соединение, которое содержит как аминогруппу (-NH 2 ), так и карбоксильную группу (-COOH), связанную с центральным атомом углерода в одной и той же молекуле.
- Определите пептид.
- Опишите образование пептидной связи.
Ваши клетки умнее вас?
Пептидные клетки в нашем организме имеют сложный механизм производства белков. Людям приходится использовать другие методы, чтобы синтезировать те же белки в лаборатории. Химия пептидного синтеза сложна. Обе активные группы аминокислоты могут реагировать, и аминокислотная последовательность должна быть конкретной, чтобы белок функционировал.Роберт Меррифилд разработал первый синтетический подход к производству белков в лаборатории, ручной подход, который был долгим и утомительным (и в 1984 году он получил Нобелевскую премию по химии за свою работу). Однако сегодня автоматизированные системы могут производить пептид за очень короткий период времени.
Пептиды
Пептид представляет собой комбинацию аминокислот, в которой аминогруппа одной аминокислоты подверглась реакции с карбоксильной группой другой аминокислоты.Реакция представляет собой реакцию конденсации с образованием амидной группы (CO-N), показанной ниже.
Рисунок 26.13
Аминокислоты объединяются в молекулу, называемую дипептидом. Связь C-N называется пептидной связью. Порядок аминокислот условно показан со свободной аминогруппой слева и свободной карбоксильной группой справа.
Пептидная связь — это амидная связь, которая возникает между азотом аминогруппы одной аминокислоты и углеродом карбоксила другой аминокислоты.Полученная молекула называется дипептидом. Обратите внимание, что конкретные боковые цепи каждой аминокислоты не имеют значения, поскольку группы R не участвуют в пептидной связи.
Дипептид имеет свободную аминогруппу на одном конце молекулы и свободную карбоксильную группу на другом конце. Каждый из них способен удлинить цепь за счет образования другой пептидной связи. Конкретная последовательность аминокислот в более длинной цепи называется аминокислотной последовательностью. По соглашению аминокислотная последовательность перечисляется в таком порядке, чтобы свободная аминогруппа находилась на левом конце молекулы, а свободная карбоксильная группа — на правом конце молекулы.Например, предположим, что последовательность аминокислот глицина, триптофана и аланина образована со свободной аминогруппой как часть глицина и свободной карбоксильной группой как частью аланина. Аминокислотная последовательность может быть легко записана с использованием сокращений Gly-Trp-Ala. Эта последовательность отличается от последовательности Ala-Trp-Gly, потому что в этом случае свободные амино- и карбоксильные группы будут находиться на разных аминокислотах.
Сводка
- Пептид определен.
- Описана пептидная связь.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http://www.sciencedaily.com/articles/p/peptide_bond.htm
- Какой класс реакции приводит к образованию пептидной связи?
- Какая молекула удаляется в этой реакции?
- Какой класс органических соединений является продуктом этой реакции?
Обзор
Вопросы
- Что такое пептидная связь?
- Чем он отличается от сложного эфира?
- Вы смешиваете две аминокислоты: glu и ser.Если вы отреагируете на них, сколько разных дипептидов вы ожидаете получить? Перечислите их.
- пептид: Комбинация аминокислот, в которой аминогруппа одной аминокислоты вступила в реакцию с карбоксильной группой другой аминокислоты.
- пептидная связь: Амидная связь, которая возникает между азотом аминогруппы одной аминокислоты и углеродом карбоксильной группы другой аминокислоты.
- Определите полипептид.
- Определите белок.
- Перечислите и опишите четыре уровня структуры белка.
Серьезный сдвиг
Гемоглобин — сложный белок, имеющий четвертичную структуру и содержащий железо. В молекуле гемоглобина четыре субъединицы — две альфа-субъединицы и две бета-субъединицы. Каждая субъединица содержит один ион железа, степень окисления которого изменяется от +2 до +3 и обратно, в зависимости от окружающей среды вокруг железа. Когда кислород связывается с железом, трехмерная форма молекулы изменяется.При выделении кислорода клеткам форма снова меняется.
При нормальном строении гемоглобина такое изменение конформации не вызывает никаких проблем. Однако люди с гемоглобином S действительно испытывают серьезные осложнения. Этот гемоглобин имеет одну аминокислоту в двух бета-цепях, которая отличается от аминокислоты в этой точке в первичной структуре нормального гемоглобина. Результатом этого единственного структурного изменения является агрегация отдельных белковых молекул при высвобождении кислорода.Соседние молекулы гемоглобина контактируют друг с другом и слипаются, вызывая деформацию и разрушение эритроцитов.
Эта аномалия, известная как серповидноклеток, имеет генетическую природу. Человек может унаследовать ген от одного из родителей и иметь серповидно-клеточную характеристику (только часть гемоглобина представляет собой гемоглобин S), что обычно не опасно для жизни. Наследование гена от обоих родителей приведет к серповидно-клеточной анемии, очень серьезному заболеванию.
Белки
Полипептид представляет собой последовательность аминокислот длиной от десяти до ста.Белок представляет собой пептид, длина которого превышает сто аминокислот. Белки очень распространены в живых организмах. Волосы, кожа, ногти, мышцы и гемоглобин в красных кровяных тельцах — это некоторые из важных частей вашего тела, которые состоят из разных белков. Широкий спектр химических и физиологических свойств белков зависит от их аминокислотных последовательностей. Поскольку белки обычно состоят из ста или более аминокислот, количество возможных аминокислотных последовательностей практически безгранично.
Трехмерная структура белка очень важна для его функции. Эту структуру можно разбить на четыре уровня. Первичная структура представляет собой аминокислотную последовательность белка. Аминокислотная последовательность данного белка уникальна и определяет функцию этого белка. Вторичная структура представляет собой очень регулярную субструктуру белка. Двумя наиболее распространенными типами вторичной структуры белка являются альфа-спираль и бета-лист.Альфа-спираль состоит из аминокислот, которые принимают спиралевидную форму. Бета-лист — это чередующиеся ряды аминокислот, которые выстраиваются бок о бок. В обоих случаях вторичные структуры стабилизируются за счет обширных водородных связей между боковыми цепями. Взаимодействие различных боковых цепей в аминокислоте, в частности водородная связь, приводит к принятию конкретной вторичной структуры.
Рисунок 26.14
Альфа-спираль и бета-лист.
Третичная структура — это общая трехмерная структура белка. Типичный белок состоит из нескольких участков определенной вторичной структуры (альфа-спираль или бета-лист), а также других областей, в которых встречается более случайная структура. Эти области объединяются, чтобы создать третичную структуру.
Некоторые белковые молекулы состоят из нескольких белковых субъединиц. Четвертичная структура белка относится к специфическому взаимодействию и ориентации субъединиц этого белка. Гемоглобин — очень большой белок, обнаруженный в красных кровяных тельцах, функция которого заключается в связывании и переносе кислорода по кровотоку.Гемоглобин состоит из четырех субъединиц — двух субъединиц α (желтый) и двух субъединиц β (серый), которые затем соединяются определенным и определенным образом посредством взаимодействия боковых цепей (см. Рисунок ниже). Гемоглобин также содержит четыре атома железа, расположенных в середине каждой из четырех субъединиц. Атомы железа являются частью структуры, называемой порфирином, показанной на рисунке красным цветом.
Рисунок 26.15
Гемоглобин
Некоторые белки состоят только из одной субъединицы и, следовательно, не имеют четвертичной структуры. Рисунок ниже показывает взаимодействие четырех уровней структуры белка.
Рисунок 26.16
Четыре уровня структуры белка.
Сводка
- Определены пептиды и белки.
- Перечислены и определены четыре уровня белковой структуры.
Практика
Вопросы
Посмотрите видео по ссылке ниже и ответьте на следующие вопросы:
Нажмите на изображение выше, чтобы увидеть больше
http: // www.youtube.com/watch?v=Q7dxi4ob2O4
- Что является частью того, что определяет, как белок сворачивается?
- Что скрепляет вторичную структуру?
- Что скрепляет третичную структуру?
Обзор
Вопросы
- Белок имеет следующую последовательность: ser-his-thr-tyr. Что это за компонент белковой структуры?
- Как мы называем общую трехмерную форму белка?
- Белок состоит из одной субъединицы.Будет ли у него четвертичная структура?
- полипептид: Последовательность аминокислот длиной от десяти до ста.
- первичная структура: Аминокислотная последовательность белка.
- белок: Пептид, длина которого превышает сто аминокислот.
- Четвертичная структура: Специфическое взаимодействие и ориентация субъединиц этого белка.
- вторичная структура: Очень регулярная субструктура белка.
- третичная структура: Общая трехмерная структура белка.
- Определите фермент.
- Определите активный сайт.
- Опишите процесс ферментативной реакции.
- Опишите процесс, с помощью которого конкурентный ингибитор изменяет скорость ферментативной реакции.
- Опишите процесс, с помощью которого неконкурентный ингибитор изменяет скорость ферментативной реакции.
- Объясните роль кофакторов в ферментативных реакциях.
Что он обнаружил?
Первый выделенный фермент был открыт в 1926 году американским химиком Джеймсом Самнером, который кристаллизовал белок. Фермент представлял собой уреазу, которая катализирует гидролитическое разложение мочевины, компонента мочи, на аммиак и диоксид углерода.
Сначала его открытие высмеяли, потому что никто не верил, что ферменты будут вести себя так же, как другие химические вещества. В конечном итоге Самнер оказался прав и получил Нобелевскую премию по химии в 1946 году.
Ферменты
Фермент — это белок, который действует как биологический катализатор. Напомним, что катализатор — это вещество, которое увеличивает скорость химической реакции, но не расходуется в ней. Клеточные процессы состоят из множества химических реакций, которые должны происходить быстро, чтобы клетка функционировала должным образом. Ферменты катализируют большинство химических реакций, происходящих в клетке. Субстрат — это молекула или молекулы, на которые действует фермент.В приведенной выше реакции, катализируемой уреазой, субстратом является мочевина. Рисунок ниже изображает типичную ферментативную реакцию.
Рисунок 26.17
Последовательность шагов для связывания субстрата с ферментом в его активном центре, реакции и последующего высвобождения в виде продуктов.
Первым этапом реакции является связывание субстрата с определенной частью молекулы фермента. Связывание субстрата определяется формой каждой молекулы.Боковые цепи фермента определенным образом взаимодействуют с субстратом, что приводит к образованию и разрыву связей. Активный центр — это место на ферменте, где связывается субстрат. Фермент сворачивается таким образом, что обычно имеет один активный сайт, обычно карман или щель, образованную структурой сворачивания белка. Поскольку активный центр фермента имеет такую уникальную форму, только один конкретный субстрат способен связываться с этим ферментом. Другими словами, каждый фермент катализирует только одну химическую реакцию только с одним субстратом.После образования комплекса фермент / субстрат происходит реакция, и субстрат превращается в продукты. Наконец, молекула или молекулы продукта высвобождаются из активного центра. Обратите внимание, что на фермент реакция не влияет, и теперь он способен катализировать реакцию другой молекулы субстрата.
Ингибиторы
Ингибитор — это молекула, которая нарушает функцию фермента, замедляя или останавливая химическую реакцию.Ингибиторы могут работать по-разному, но один из наиболее распространенных показан на Рис. ниже.
Рисунок 26.18
Конкурентный ингибитор — это молекула, которая связывается с активным центром фермента, не вступая в реакцию, тем самым предотвращая связывание субстрата.
Ингибитор конкурентно связывается в активном центре и блокирует связывание субстрата. Поскольку с ингибитором реакции не происходит, фермент не может катализировать реакцию.Цианид — сильный яд, который действует как конкурентный ингибитор. Он связывается с активным центром фермента цитохром с оксидазы и прерывает клеточное дыхание. Связывание цианида с ферментом необратимо, и пораженный организм быстро умирает.
Неконкурентное ингибирование
Неконкурентный ингибитор не связывается в активном центре. Он прикрепляется к другому участку фермента и изменяет форму белка. Этот сдвиг в трехмерной структуре изменяет форму активного сайта, так что субстрат больше не будет подходить к сайту должным образом (см. Рис. ниже).
Рисунок 26.19
Неконкурентное торможение
Кофакторы
Некоторым ферментам для правильного функционирования требуется присутствие небелковой молекулы, называемой кофактором. Кофакторами могут быть ионы неорганических металлов или небольшие органические молекулы. Многие витамины, например витамины группы B, действуют как кофакторы. Некоторые ионы металлов, которые действуют как кофакторы различных ферментов, включают цинк, магний, калий и железо.
Сводка
- Фермент определен.
- Проиллюстрирован обзор процесса ферментативной реакции.
- Описаны конкурентные и неконкурентные ингибиторы.
- Описана роль кофактора.
Практика
Посмотрите анимацию на сайте ниже и пройдите викторину:
http://highered.mcgraw-hill.com/sites/0072495855/student_view0/chapter2/animation__how_enzymes_work.html
Обзор
Вопросы
- Что такое подложка?
- Как действует конкурентный ингибитор?
- Как действует неконкурентный ингибитор?
- Активный центр: Место на ферменте, где связывается субстрат.
- фермент: Белок, который действует как биологический катализатор.
- ингибитор: Молекула, которая нарушает функцию фермента, замедляя или останавливая химическую реакцию.
- субстрат: Молекула или молекулы, на которые действует фермент.
- Опишите строение насыщенных и ненасыщенных жирных кислот.
- Опишите структуру триглицерида.
- Опишите роль триглицеридов в диете.
Правильно питаться или принимать добавки?
В наши дни есть большой интерес к здоровому питанию, а также проблемы с сердцем. Существует также сильный рынок для продажи жирных кислот омега-3, которые, как говорят, помогают снизить уровень жира в крови. Но слишком многие люди полагаются на добавки, чтобы помочь своему сердцу, и не понимают, что за всем этим стоит химия. Да, прием жирных кислот омега-3 даст вам часть жирных кислот, необходимых вашему организму.Нет, это не замена здоровому питанию и физическим упражнениям. Вы не можете сидеть перед телевизором, съедая большую пиццу, и ожидать, что эти таблетки сохранят ваше здоровье. Вы должны поступать нелегко — есть овощи и заниматься спортом. Да, мама.
Триглицериды
Липид относится к классу нерастворимых в воде соединений, который включает масла, жиры и воски. Масла и жиры имеют одну и ту же общую структуру, но жиры являются твердыми веществами при комнатной температуре, а масла — жидкостями.Сливочное масло является примером жира, полученного от животных. Некоторые масла включают оливковое масло и масло канолы, которые получают из растений. Липиды являются неотъемлемой частью здорового питания, хотя избыток пищевых жиров может быть вредным. Липиды хранят энергию в организме, а также необходимы для поддержания здоровья клеточных мембран.
Один тип липидов называется триглицеридом , сложным эфиром, полученным из глицерина в сочетании с тремя молекулами жирных кислот.
Рисунок 26.20
Триглицеридные компоненты
Глицерин — это триол, спирт, содержащий три гидроксильные функциональные группы. Жирная кислота представляет собой длинную углеродную цепь, обычно от 12 до 24 атомов углерода, с присоединенной карбоксильной группой. Каждая из трех молекул жирных кислот подвергается этерификации с одной из гидроксильных групп молекулы глицерина. В результате получается большая молекула триэфира, называемая триглицеридом.
Триглицериды функционируют как форма длительного хранения энергии в организме человека.Из-за длинных углеродных цепей триглицериды являются почти неполярными молекулами и поэтому не растворяются легко в полярных растворителях, таких как вода. Вместо этого масла и жиры растворимы в неполярных органических растворителях, таких как гексан и простые эфиры.
Жиры могут быть насыщенными или ненасыщенными. Насыщенный жир — это жир, состоящий из триглицеридов, углеродные цепи которых полностью состоят из одинарных углерод-углеродных связей. Следовательно, углеродные цепи насыщены максимально возможным числом атомов водорода.Ненасыщенный жир представляет собой жир, состоящий из триглицеридов, углеродные цепи которых содержат одну или несколько двойных углерод-углеродных связей . Жир с одной двойной связью называется мононенасыщенным, а жир с несколькими двойными связями — полиненасыщенным (см. Рисунок ниже).
Рисунок 26.21
Насыщенные и ненасыщенные жирные кислоты
Ненасыщенные жиры обычно считаются более полезными для здоровья, поскольку они содержат меньше калорий, чем эквивалентное количество насыщенных жиров.Кроме того, высокое потребление насыщенных жиров связано с повышенным риском сердечно-сосудистых заболеваний. Некоторые примеры продуктов с высоким содержанием насыщенных жиров включают масло, сыр, сало и некоторые жирные сорта мяса. Продукты с более высокой концентрацией ненасыщенных жиров включают орехи, авокадо и растительные масла, такие как масло канолы и оливковое масло. Рисунок ниже показывает процентное содержание жиров в некоторых распространенных продуктах питания.
Рисунок 26.22
Некоторые распространенные продукты и масла с указанием процентного содержания насыщенных, мононенасыщенных и полиненасыщенных жиров.
Сводка
- Приведена структура триглицерида.
- Описывается роль триглицеридов в нашем рационе.
- Приведен состав насыщенных и ненасыщенных жирных кислот.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http://www.heart.org/HEARTORG/GettingHealthy/NutritionCenter/Triglycerides_UCM_306029_Article.jsp
- Каков нормальный уровень триглицеридов в крови?
- Какие уровни упражнений рекомендуются для снижения уровня триглицеридов в крови?
- Какие виды растительных масел самые полезные?
Обзор
Вопросы
- Что такое жирная кислота?
- Что такое триглицерид?
- Почему важны ненасыщенные жирные кислоты?
- липид: Член класса нерастворимых в воде соединений, который включает масла, жиры и воски.
- насыщенный жир: Жир, состоящий из триглицеридов, углеродные цепи которых полностью состоят из одинарных углерод-углеродных связей.
- триглицерид: Сложный эфир, полученный из глицерина в сочетании с тремя молекулами жирных кислот.
- ненасыщенный жир: Жир, состоящий из триглицеридов, углеродные цепи которых содержат одну или несколько двойных углерод-углеродных связей.
- Опишите структуру фосфолипида.
- Опишите структуру мембраны.
Вы что-нибудь чувствуете сейчас?
Когда вы идете к стоматологу, чтобы удалить зуб, вы действительно не хотите чувствовать никакой боли. Дантист вводит анестетик в вашу десну, и в конечном итоге она немеет. Одна из теорий о том, почему работают анестетики, связана с движением ионов через клеточную мембрану. Анестетик проникает в структуру мембраны и вызывает сдвиг в том, как ионы перемещаются через мембрану. Если движение ионов нарушено, нервные импульсы не будут передаваться, и вы не почувствуете боли — по крайней мере, до тех пор, пока действие анестетика не пройдет.
Фосфолипиды
Фосфолипид представляет собой липид, который содержит фосфатную группу и является основным компонентом клеточных мембран. Фосфолипид состоит из гидрофильной (водолюбивой) головки и гидрофобного (водобоязненного) хвоста (см. , рисунок ниже). Фосфолипид по существу представляет собой триглицерид, в котором жирная кислота заменена какой-либо фосфатной группой.
Рисунок 26.23
Фосфолипид состоит из головы и хвоста.«Голова» молекулы содержит фосфатную группу и является гидрофильной, что означает, что она растворяется в воде. «Хвост» молекулы состоит из двух жирных кислот, которые являются гидрофобными и не растворяются в воде.
Согласно правилу «подобное растворяется в подобном», гидрофильная головка молекулы фосфолипида легко растворяется в воде. Длинные цепи жирных кислот фосфолипидов неполярны и поэтому избегают использования воды из-за их нерастворимости. В воде фосфолипиды спонтанно образуют двойной слой, называемый липидным бислоем, в котором гидрофобные хвосты молекул фосфолипидов зажаты между двумя слоями гидрофильных головок (см. Рисунок ниже).Таким образом, только головы молекул подвергаются воздействию воды, в то время как гидрофобные хвосты взаимодействуют только друг с другом.
Рисунок 26.24
В водном растворе фосфолипиды образуют бислой, где гидрофобные хвосты обращены друг к другу внутри, и только гидрофильные головки подвергаются воздействию воды.
Фосфолипидные бислои являются критическими компонентами клеточных мембран. Липидный бислой действует как барьер для прохождения молекул и ионов внутрь и из клетки.Однако важной функцией клеточной мембраны является обеспечение избирательного проникновения определенных веществ в клетки и из них. Это достигается за счет встраивания различных белковых молекул в липидный бислой и через него (см. Рисунок ниже). Эти белки образуют каналы, по которым могут перемещаться определенные ионы и молекулы. Многие мембранные белки также содержат присоединенные углеводы за пределами липидного бислоя, что позволяет ему образовывать водородные связи с водой.
Рисунок 26.25
Фосфолипидный бислой клеточной мембраны содержит встроенные белковые молекулы, которые обеспечивают избирательный проход ионов и молекул через мембрану.
Сводка
- Описано строение фосфолипидов.
- Описано строение клеточной мембраны.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http: // гиперфизика.phy-astr.gsu.edu/hbase/organic/phoslip.html
- Что такое фосфолипидный остов?
- Какова консистенция двухслойной фосфолипидной мембраны?
- Мембрана жесткая или жидкая?
Обзор
Вопросы
- Что такое фосфолипид?
- Какая часть молекулы фосфолипида растворима в воде?
- Какая часть не растворяется в воде?
- фосфолипид: Липид, который содержит фосфатную группу и является основным компонентом клеточных мембран.
- Определить воск.
- Опишите свойства восков.
- Перечислите распространенные воски.
Тар она дует!
С 1700-х до конца 1900-х китобои искали в океане кашалота. Китобойный промысел был опасным занятием — добыча в среднем составляла около пятидесяти футов в длину. Но в случае успеха поиск того стоил. Один большой кит может производить до 500 галлонов масла, ценного для изготовления свечей, мазей, косметических кремов и промышленных смазок.В 1988 году кашалоты (и другие виды китов) были помещены под международную защиту, поскольку их численность быстро сокращалась. Сегодня вместо китового жира используются различные растительные масла.
Воски
Другая категория липидных молекул — воски. Воски представляют собой сложные эфиры длинноцепочечных жирных кислот и длинноцепочечных спиртов. Воски представляют собой мягкие твердые вещества с обычно низкой температурой плавления и нерастворимы в воде. Рисунок ниже показывает структуру цетилпальмитата, натурального воска, присутствующего в кашалотах.
Рисунок 26.26
Цетилпальмитат относится к категории соединений, называемых восками. Он получен из жирной кислоты с 15 атомами углерода и спирта с 16 атомами углерода.
Один из самых известных натуральных восков — пчелиный воск, хотя многие другие животные и растения синтезируют воск естественным путем. Воск можно найти на листьях растений, а также на коже, волосах или перьях животных, где они служат для сохранения эластичности и водонепроницаемости этих структур.Люди используют защитные свойства натуральных и синтетических восков в таких применениях, как полироль для полов и автомобильный воск.
Сводка
- Показан состав восков.
- Описаны свойства восков.
- Перечислены обычные воски.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http://lipidlibrary.aocs.org/lipids/waxes/index.htm
- Какие еще органические компоненты можно найти в восках, помимо эфиров воска?
- Как еще называют шерстяной воск?
- Какие три основных неполярных липида на поверхности кожи человека?
Обзор
Вопросы
- Что такое воск?
- Назовите два свойства восков.
- Назовите воск, обнаруженный у кашалотов.
- воск: Сложный эфир длинноцепочечных жирных кислот и длинноцепочечных спиртов.
- Определите нуклеиновую кислоту.
- Определите нуклеотид.
- Опишите структуру общих нуклеотидов.
Лечение рака с помощью химии
Лечение рака — это сложная задача. Раковые клетки растут без обычных средств контроля, которые действуют на нормальные клетки. Один из подходов к лечению рака — изменить структуру ДНК, чтобы замедлить или остановить рост аномальных клеток.Было показано, что соединения, которые структурно напоминают обычные строительные блоки ДНК, очень эффективны в предотвращении распространения некоторых форм рака по организму.
Нуклеиновые кислоты
Швейцарский биохимик Фридрих Мишер впервые обнаружил азотсодержащие соединения в ядрах клеток в 1869 году. Термин нуклеиновая кислота использовался для описания этих молекул из-за их открытия в ядре клетки и из-за наличия фосфатных групп и их связи с фосфорная кислота.Нуклеиновая кислота представляет собой большой биополимер, состоящий из множества нуклеотидов. Двумя первичными нуклеиновыми кислотами, которые обнаруживаются в клетках, являются дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК). ДНК является носителем генетической информации и в конечном итоге отвечает за то, как клетки производят белки, чтобы выполнять все функции, необходимые для жизни. РНК — это родственная молекула, которая участвует в механизме преобразования информации, хранящейся в ДНК, в молекулы белка.
Основными компонентами нуклеиновых кислот являются нуклеотиды. Нуклеотид — это молекула, которая содержит пятиуглеродный сахар, фосфатную группу и азотсодержащее основание. Пятиуглеродный сахар представляет собой рибозу в случае РНК или дезоксирибозу в случае ДНК. Единственное различие между двумя молекулами — это наличие гидроксильной группы, присоединенной к одному члену углеродного кольца в РНК. В ДНК тот же атом углерода присоединен только к атому водорода (см. рис. ниже).Обратите внимание, что на чертеже структуры органических молекул отдельные атомы водорода не показаны в структуре, но подразумеваются присоединенными к каждой углеродной точке, если не показана другая молекула.
Рисунок 26.27
Сахара рибоза и дезоксирибоза являются компонентами РНК и ДНК соответственно.
Нуклеотиды составляют основу РНК и ДНК. Каждый нуклеотид состоит из основания, пентозы (рибоза или дезоксирибоза) и фосфатных групп (см. Рисунок ниже).Три основания в РНК и ДНК идентичны (аденин, цитозин и гуанин). Тимин содержится в ДНК, а урацил — в РНК.
Рисунок 26.28
Нуклеотиды
Сводка
- Дано определение нуклеиновой кислоты.
- Дается определение нуклеотида и структуры пяти нуклеотидов.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http: // www.ncbi.nlm.nih.gov/pubmed/17
2
- Что Мишер изучал в 1868-1869 гг.?
- Что было интересного в химическом составе выделенного им материала?
- Как он это назвал и почему?
Обзор
Вопросы
- Что такое нуклеиновая кислота?
- Что такое нуклеотид?
- Какая пентоза содержится в ДНК, а какая в РНК?
- нуклеиновая кислота: Большой биополимер, состоящий из множества нуклеотидов.
- нуклеотид: Молекула, содержащая пятиуглеродный сахар, фосфатную группу и азотсодержащее основание.
- Опишите структуру нуклеотида.
- Перечислите основания, обнаруженные в ДНК.
- Перечислите основания, обнаруженные в РНК.
- Опишите двойную спиральную структуру ДНК.
Их всех не выиграть.
Линус Полинг был одним из величайших ученых двадцатого века.Двукратный лауреат Нобелевской премии (по химии в 1954 г. и премии мира в 1962 г.). Однако не всегда он был первым. В 1950-х годах был большой интерес к структуре ДНК. Полинг потратил некоторое время на разгадку этой головоломки, хотя в первую очередь его интересовали белки. Недостаточный объем информации, которую он получил, заставил его предложить структуру ДНК, в которой основания были бы снаружи, а фосфатные группы — внутри. Оказывается, он ошибался в этой идее, но это, конечно, не повлияло на его выдающуюся научную репутацию.
ДНК и РНК
Три части нуклеотида ДНК собраны, как показано на Рис. ниже.
Рисунок 26.29
Нуклеотиды состоят из фосфатной группы, сахара и одного из пяти различных азотистых оснований.
Каждый полимер ДНК и РНК состоит из множества нуклеотидов, соединенных вместе в чрезвычайно длинные цепи. Единственная вариация в каждом нуклеотиде — это азотистое основание.На рисунке выше показан один пример азотистого основания, называемого аденином. Во всех нуклеиновых кислотах есть только пять различных азотистых оснований. Четыре основания ДНК — это аденин, тимин, цитозин и гуанин, сокращенно A, T, C и G соответственно. В РНК, основание тимин не обнаружено и вместо этого заменено другим основанием, называемым урацилом, сокращенно U. Остальные три основания присутствуют как в ДНК, так и в РНК.
Специфическая структура ДНК была недостижимой для ученых в течение многих лет.В 1953 году Джеймс Уотсон и Фрэнсис Крик предположили, что структура ДНК состоит из двух расположенных бок о бок полинуклеотидных цепей, свернутых в форму двойной спирали . Одним из аспектов этой структуры является то, что каждое азотистое основание на одной из цепей ДНК должно быть спарено с другим основанием на противоположной цепи. Рисунок ниже иллюстрирует пару оснований. Каждое адениновое основание всегда связано с тимином, а каждый цитозин — с гуанином. Основания идеально подходят друг к другу от одной нити к другой, а также удерживаются вместе водородными связями.Пара A-T содержит две водородные связи, а пара C-G содержит три водородные связи. Концы каждой нити помечены 3 ’или 5’ в зависимости от нумерации сахарного кольца дезоксирибозы.
Рисунок 26,30
Спаривание оснований в ДНК
Двойная спиральная структура ДНК показана на Рисунке ниже.
Рисунок 26.31
Двойная спираль ДНК
Сводка
- Описаны нуклеотидные структуры ДНК и РНК.
- оснований в ДНК.
- Показана двойная спираль ДНК.
Проиллюстрировано спаривание
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
www.accessexcellence.org/RC/AB/BC/Rosalind_Franklin.php
- Где Розалинда Франклин проводила свои исследования?
- Какие важные данные о структуре ДНК у нее были?
- Знала ли она, что Ватсон и Крик видели данные ее исследования?
Обзор
Вопросы
- Какие четыре основания составляют цепочку ДНК?
- Как держатся вместе эти базы?
- Как называется получившаяся структура?
- двойная спираль: Трехмерная структура ДНК.
- Определить ген.
- Опишите коды триплетов ДНК для аминокислот.
Все еще работает
Проект «Геном человека» стартовал в 1990 году с благородной цели — секвенировать полный набор ДНК человека. Этот проект был завершен в апреле 2003 года с опережением графика и в рамках установленного бюджета (редкость для государственного проекта). Обладая этими знаниями, теперь мы можем быстро выявлять генетические нарушения и индивидуализировать лечение многих заболеваний.Однако предстоит еще много работы, чтобы полностью понять связи между конкретными последовательностями ДНК и конкретными заболеваниями.
Генетический код
Каждый конкретный организм содержит множество белковых молекул, специфичных для этого организма. Конкретная последовательность оснований ДНК отвечает за производство всех различных белков, которые присутствуют в каждом живом существе, когда-либо населявшем Землю. Как это работает? Клетки используют уникальную последовательность оснований ДНК, чтобы решить, какие белки синтезировать.Ген — это сегмент ДНК, который несет код для создания конкретной полипептидной цепи. Клетка, по сути, декодирует ДНК, чтобы производить пептиды и белки, необходимые этому организму.
Генетический код работает как серия трехбуквенных кодов. Каждая последовательность из трех букв, называемая триплетом, соответствует одной из двадцати общих аминокислот. Тройки считываются клеткой один за другим в процессе синтеза белка.Ниже перечислены все возможные триплеты и аминокислоты, полученные в результате каждого трехбуквенного кода.
| 1-я база: A | 1-я база: G | 1-я база: T | 1-я база: C |
|---|---|---|---|
| AAA Lys | GAA Glu | TAA Стоп | CAA Gln |
| AAG Lys | GAG Glu | TAG Stop | CAG Val |
| AAT Asn | GAT Leu | ТАТ Тир | CAT Его |
| AAC Asn | GAC Asp | TAC Tyr | CAC His |
| AGA Arg | GGA Gly | Стоп TGA | CGA Arg |
| AGG Arg | GGG Gly | ТГГ Трп | CGG Arg |
| AGT Ser | GGT Gly | TGT Cys | CGT Arg |
| AGC Ser | GGC Gly | ТГК Цис | CGC Arg |
| ATA Иль | GTA Val | TTA Leu | CTA Leu |
| ATG Met | ГТГ Вал | TTG Leu | CTG Leu |
| ATT Ile | GTT Val | TTT Phe | CTT Leu |
| ATC Ile | GTC Val | TTC Phe | CTC Leu |
| ACA Thr | GCA Ala | TCA Сер | CCA Pro |
| ACG Thr | GCG Ала | TCG Ser | CCG Pro |
| ACT Thr | GCT Ala | TCT Сер | CCT Pro |
| ACC Thr | GCC Ala | TCC Ser | CCC Pro |
В приведенной выше таблице указано, что кодовое слово ДНК GCA соответствует аминокислоте аланину, а кодовое слово ДНК TCG соответствует аминокислоте серину.Большинство аминокислот представлено более чем одним возможным триплетным кодом, но каждый триплетный код дает только одну аминокислоту. Три кодовых слова ДНК (TAA, TAG и TGA) являются конечными или конечными кодовыми словами. Когда достигается один из этих кодонов, цепь аминокислот высвобождается и больше не добавляется. Напомним, что белки состоят из сотни и более аминокислот. Белок, содержащий 120 аминокислот, будет кодироваться геном, содержащим 363 пары оснований ДНК (по 3 для каждой аминокислоты, плюс стоп-кодовое слово).
Даже с четырьмя различными основаниями количество возможных нуклеотидных последовательностей в цепи ДНК практически безгранично. Последовательность ДНК конкретного организма составляет генетический план этого организма. Этот генетический план находится в ядре каждой клетки организма и передается от родителей к потомству. Невероятное разнообразие жизни на Земле проистекает из различий в генетическом коде каждого живого существа.
Сводка
- Определен ген.
- Описан генетический код.
Практика
Вопросы
Ознакомьтесь с материалом по ссылке ниже и ответьте на следующие вопросы:
http://nihrecord.od.nih.gov/newsletters/2010/02_05_2010/story3.htm
- Что сделал Маршалл Ниренберг?
- Когда он впервые сообщил о своих результатах?
- Что он выиграл за свое открытие?
Обзор
Вопросы
- Что такое ген?
- Что делает генетический код?
- Какой нуклеотидный код у фенилаланина?
- ген: Сегмент ДНК, который несет код для создания определенной полипептидной цепи.
- генетический код: Трехосновный набор нуклеотидов, который определяет конкретную аминокислоту в последовательности белка.
- Опишите последовательность процессов, происходящих при синтезе белка.
Очень организованный процесс
Сборочная линия — это американское изобретение, которое было разработано примерно в 1901 году для серийного производства автомобилей. До этого бригады рабочих вместе строили машины. С появлением сборочной линии автомобили можно было производить намного быстрее и с меньшими затратами.Идея сборочной линии быстро распространилась на другие продукты, такие как лампочки, показанные выше. Возможность выстраивать детали по порядку и плавный процесс сборки этих деталей означает, что изделие можно производить быстро и воспроизводимо, получая каждый раз одним и тем же способом.
Синтез белка
Процесс синтеза белка представлен на диаграмме ниже. ДНК производит матрицу РНК, которая затем направляет аминокислоты, которые должны быть введены в растущую белковую цепь в надлежащей последовательности.Специфическая РНК-переносчик (тРНК) присоединяется к каждой конкретной аминокислоте и переносит амионную кислоту в РНК для включения.
Рисунок 26.32
Обзор синтеза белка
Первым шагом в этом процессе является транскрипция — развертывание ДНК и производство цепи информационной РНК (мРНК). Этот шаг происходит в ядре клетки.
Рисунок 26.33
Образование РНК из ДНК
ДНК разматывается и обеспечивает образец для образования единой цепи мРНК.После образования РНК ДНК снова складывается в исходную двойную спираль. МРНК экспортируется в цитоплазму (вне ядра) для дальнейшей обработки.
Аминокислоты будут связываться со специфическими молекулами тРНК для правильного размещения в белковой цепи. ТРНК представляет собой небольшую спиралевидную молекулу, которая принимает аминокислоту на одном конце и соответствует определенной трехосновной части мРНК на другом конце. ТРНК взаимодействует с мРНК, чтобы расположить аминокислоту в правильной последовательности для развивающегося белка.После добавления аминокислоты к последовательности тРНК затем отщепляется от аминокислоты и рециркулируется для дальнейшего использования в процессе.
В рибосоме происходит процесс сборки аминокислот. Эта структура состоит из двух субъединиц, содержащих рибосомную РНК, которые включают мРНК и катализируют образование амидных связей в растущем белке в процессе, известном как трансляция . Когда синтез белка завершен, две субъединицы диссоциируют и высвобождают завершенную белковую цепь.
Процесс синтеза белка идет довольно быстро. Аминокислоты добавляются к растущей пептидной цепи со скоростью примерно 3-5 аминокислот в секунду. Небольшой белок (100-200 аминокислот) может быть произведен за минуту или меньше.
Рисунок 26.34
Роль рибосомы в синтезе белка
Сводка
- Описаны этапы синтеза белка.
Практика
Вопросы
Посмотрите видео по ссылке ниже и ответьте на следующие вопросы:
http: // www.biostudio.com/demo_freeman_protein_synthesis.htm
- Что такое инициирующая аминокислота?
- Как движется рибосома, когда входит новая аминокислота?
- Что происходит с каждой тРНК после того, как она доставляет свою аминокислоту?
Обзор
Вопросы
- Что такое транскрипция?
- Что такое перевод?
- Какая молекула получает аминокислоту в последовательности в нужное время?
- транскрипция: Производство цепи мРНК из ДНК.
- перевод: Производство белков рибосомами.
Показать ссылки
Список литературы
- Предоставлено Национальным институтом здравоохранения. http://commons.wikimedia.org/wiki/File:Human_brain_NIH.png.
- Правообладатель иллюстрации Elena Schweitzer, 2014. http://www.shutterstock.com.
- Фонд CK-12 — Джой Шэн. .
- Фонд CK-12 — Кристофер Ауён. .
- Рибоза: Пользователь: NEUROtiker / Wikimedia Commons; Дезоксирибоза: Пользователь: Yikrazuul / Wikimedia Commons.Рибоза: http://commons.wikimedia.org/wiki/File:Beta-D-Ribofuranose.svg; Дезоксирибоза: http://commons.wikimedia.org/wiki/File:Deoxyribose_structure.svg.
- Пользователь: Бостон / Википедия. http://commons.wikimedia.org/wiki/File:Hood_Milk_Bottle.jpg.
- Фонд CK-12 — Кристофер Ауён и Джой Шэн. .
- Пользователь: Wobble / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Lactose%28lac%29.png.
- Пользователь: NEUROtiker / Wikimedia Commons. http: //commons.wikimedia.org / wiki / Файл: Maltose_Haworth.svg.
- Томас Нетч. https://commons.wikimedia.org/wiki/File:Marathon-Munich-2005-10-09-10-01.jpg.
- Пользователь: NEUROtiker / Wikimedia Commons. Амилоза: http://commons.wikimedia.org/wiki/File:Amylose2.svg, Амилопектин: http://commons.wikimedia.org/wiki/File:Amylopektin_Sessel.svg.
- Пользователь: NEUROtiker / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Glykogen.svg.
- Пользователь: CeresVesta / Википедия. http: //en.wikipedia.org / wiki / Файл: Cellulose_spacefilling_model.jpg.
- Flickr: nathanmac87. http://www.flickr.com/photos/nathanmac87/4377056429/.
- Пользователь: NEUROtiker / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Aminos%C3%A4ure_allgemein.svg.
- Пользователь: Sponk / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Overview_proteinogenic_amino_acids-DE.svg.
- Авторское право на изображениеolekuul.be, 2014. http://www.shutterstock.com.
- Пользователь: YassineMrabet / Wikimedia Commons.http://commons.wikimedia.org/wiki/File:Peptidformationball.svg.
- Национальный институт сердца, легких и крови (NHLBI). http://commons.wikimedia.org/wiki/File:Sickle_cell_01.jpg.
- Alpha: Пользователь: Ayacop / Wikimedia Commons; Бета: Пользователь: Dcrjsr / Wikimedia Commons. Альфа: https://commons.wikimedia.org/wiki/File:CALC1_2GLH.png; Бета: http://commons.wikimedia.org/wiki/File:1gwe_antipar_betaSheet_both.png.
- Предоставлено Тоддом Л. Молланом, CBER, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.http://blogs.fda.gov/fdavoice/index.php/tag/blood-substitutes/.
- Мариана Руис Вильярреал (Викимедиа: LadyofHats). http://commons.wikimedia.org/wiki/File:Main_protein_structure_levels_en.svg.
- Нобелевский фонд. http://commons.wikimedia.org/wiki/File:James_Batcheller_Sumner.jpg.
- Пользователь: TimVickers / Wikimedia Commons и пользователь: Fvasconcellos / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Induced_fit_diagram.svg.
- Джерри Кримсон Манн (Викимедиа: Mcy jerry), пользователь: TimVickers / Wikimedia Commons и пользователь: Fvasconcellos / Wikimedia Commons.http://commons.wikimedia.org/wiki/File:Competitive_inhibition.svg.
- Джерри Кримсон Манн (Викимедиа: Мси Джерри). http://commons.wikimedia.org/wiki/File:Allosteric_competitive_inhibition_3.svg.
- Flickr: Sam_Catch. http://www.flickr.com/photos/samcatchesides/5419724548/.
- Фонд CK-12 — Джой Шэн. .
- Вольфганг Шефер (Викимедиа: WS62). Пальмитовый: http://commons.wikimedia.org/wiki/File:Palmitic_acid_shorthand_formula.PNG; Олейк: http: // commons.wikimedia.org/wiki/File:Oleic_acid_shorthand_formula.PNG; Линолевая: http://commons.wikimedia.org/wiki/File:Linoleic_acid_shorthand_formula.PNG.
- CK-12 Foundation с использованием данных Министерства сельского хозяйства США и Национальной базы данных по питательным веществам для стандартной справки. Данные: http://ndb.nal.usda.gov/.
- Пользователь: Акузнецова / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Lipid_bilayer_expansion_hypothesis_of_anesthetic_effect.png.
- Фонд CK-12 — Джой Шэн..
- Мариана Руис Вильярреал (Викимедиа: LadyofHats), модифицировано фондом CK-12. http://commons.wikimedia.org/wiki/File:Phospholipids_a Water_solution_structures.svg.
- Мариана Руис Вильярреал (Викимедиа: LadyofHats), модифицировано фондом CK-12. http://commons.wikimedia.org/wiki/File:Cell_membrane_detailed_diagram_en.svg.
- Предоставлено Таттлом Стивеном, Служба охраны рыболовства и дикой природы США. http://commons.wikimedia.org/wiki/File:Sperm_whale_swimming_in_water_close_up_physeter_catodon.jpg.
- Пользователь: Smokefoot / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Cetyl_palmitate.png.
- Предоставлено Рода Баер, Национальный институт рака. http://commons.wikimedia.org/wiki/File:Catheter_for_chemotherapy.jpg.
- Рибоза: Пользователь: NEUROtiker / Wikimedia Commons; Дезоксирибоза: Пользователь: Yikrazuul / Wikimedia Commons. Рибоза: http://commons.wikimedia.org/wiki/File:Beta-D-Ribofuranose.svg; Дезоксирибоза: http://commons.wikimedia.org/wiki/File:Deoxyribose_structure.svg.
- Пользователь: BorisTM / Wikimedia Commons и Пользователь: Sjef Boris / Wikimedia Commons. http://commons.wikimedia.org/wiki/File:Nucleotides_1.svg.
- Нобелевский фонд. http://commons.wikimedia.org/wiki/File:Linus_Pauling_1962.jpg.
- Фонд CK-12 — Джой Шэн, структура пользователя: NEUROtiker / Wikimedia Commons. Структура: http://commons.wikimedia.org/wiki/File:Desoxyadenosinmonophosphat_protoniert.svg.
- Мариана Руис Вильярреал (LadyofHats) для фонда CK-12..
- Правообладатель иллюстрации ermess, 2014. http://www.shutterstock.com.
- Предоставлено Линдой Бартлетт, Национальный институт рака. http://commons.wikimedia.org/wiki/File:DNA_sequencing.jpg.
- Правообладатель иллюстрации Михеев Виктор, 2014. http://www.shutterstock.com.
- Предоставлено Национальным институтом здравоохранения. http://commons.wikimedia.org/wiki/File:MRNA-interaction.png.
- Пользователь: Calibuon / En.Wikibooks. http://commons.wikimedia.org/wiki/File:Transcription.jpg.
- Мариана Руис Вильярреал (Викимедиа: LadyofHats). http://commons.wikimedia.org/wiki/File:TRNA_ribosomes_diagram_en.svg.
Adm ксантановая камедь MSDS Sheet
ADM Австралия и ADM Новая Зеландия предлагают следующие полиолы и камеди по всему региону Океании для пищевой и промышленной промышленности: Ксантановая камедь Ксантановая камедь — это полисахарид, выделяемый бактерией Xanthomonas campestris, используемый в качестве пищевой добавки и модификатор реологии, обычно используемый в качестве пищевого загустителя (например, в салатах) и стабилизатора (в косметических продуктах, например, для предотвращения разделения ингредиентов).
26.07.2018 · ксантановая камедь 11138-66-2 0,1 — 1. 4. Меры первой помощи: вдыхание: вывести на свежий воздух. … лист был написан на основе лучших знаний и опыта на данный момент … 【Название продукта】. Ксантановая камедь. 【Синонимы】. Контейнеры из этого материала могут быть опасными при опорожнении. Поскольку в опорожненных контейнерах остаются остатки продукта (пар, жидкость и / или твердое вещество), необходимо соблюдать все меры предосторожности, указанные в техническом паспорте.
Часто задаваемые вопросы: доступна ли органическая ксантановая камедь? Большинство камедей имеют тенденцию образовывать комки при добавлении в воду, и ксантановая камедь может быть особенно трудной для диспергирования и растворения.биополимер xb- 23 ксантановая камедь biozan r enorflo x flocon 1035 galaxy xb kelflo keltrol (камедь) kelzan kentrol полисахарид b 1459 родопол 23 xanflood xanthomonas gum ксантановая камедь 11138-66-2 0 — 0,3 3/23 название материала: сенсодиновая зубная паста диоксид) 135494 номер версии: 23 дата редакции: 11-10-2015 дата выпуска: 28.06.2013 sds us
Паспорт безопасности материала (MSDS). РАЗДЕЛ 1: Идентификация вещества / смеси и компании / предприятия. РАЗДЕЛ 3: Состав / информация о компонентах.3.1. Название вещества Номер CAS: ксантановая камедь, чистый пищевой: 11138-66-2.XANTHAN GUM 11138-66-2> 20% TRIETHANOLAMINE 102-71-6> 1% CI DIRECT BLACK 168 85631-88-5> 10% Магазин в прохладном месте. Хранить вдали от солнечных лучей. Надевайте полностью защитный костюм. Устройство защиты органов дыхания во рту. Не вдыхать взрывоопасные или горючие газы. Нет информации Нет информации
Поиск заменителя ксантановой камеди может стать вашим новым кето-дружественным секретным оружием. Ксантановая камедь — популярная пищевая добавка, которую обычно добавляют в качестве загустителя или стабилизатора.Многие приправы, соусы и немолочные заменители молока, например, полагаются на эти свойства для предотвращения разделения и … ПАСПОРТ БЕЗОПАСНОСТИ Stokoderm Protect PURE 1. Идентификация Идентификатор продукта Название продукта Stokoderm Protect PURE Номер продукта UPW150ML-CAN, UPW1L- CAN, UPW30ML-CAN, UPW100ML-CAN Синонимы; Торговые наименования Deb Universal PROTECT Размер контейнера 150 мл, 1 л, 30 мл, 100 мл Рекомендуемое использование химического вещества и ограничения по применению Применение Предваряющая защита .
